- Arthropathies à dépôts de cristaux
La prévalence de l’ hyperuricémie et de la goutte a augmenté régulièrement dans tous les pays industrialisés ces dernières années. L’ hyperuricémie entraîne non seulement des dépôts d’ urates dans les articulations, les structures proches des articulations (par ex. gaines tendineuses, bourses séreuses) et, plus rarement, dans les organes internes, mais elle est également en association avec une augmentation du risque cardiovasculaire, probablement une détérioration de la fonction rénale et éventuellement une augmentation de la tension artérielle. Dans cet article, les mesures actuelles de diagnostic et de traitement sont compilées et le diagnostic différentiel de la pseudo-goutte est également expliqué.
Au cours de l’ évolution – dans la transition de la vie dans l’ eau à la vie sur terre – des taux d’ acide urique plus élevés ont dû apporter des avantages. Par conséquent, certains reptiles de grade supérieur et tous les primates sont dépourvus de l’ enzyme uricase, qui décompose l’ acide urique en allantoïne dans tous les autres organismes. Simultanément, 90 % de l’ acide urique filtré est réabsorbé dans nos reins.
Cependant, les changements dans les habitudes alimentaires, l’ augmentation de l’ espérance de vie (diminution de la fonction rénale) et d’ autres facteurs font qu’ aujourd’ hui nous sommes principalement confrontés aux conséquences négatives de l’ hyperuricémie. La plupart des laboratoires définissent l’ hyper-uricémie comme un taux d’ acide urique supérieur à 420 µmol/l. Le produit de solubilité, en revanche, se situe à 360 µmol/l, c’ est-à-dire que l’ acide urique commence à précipiter à des valeurs plus élevées. Pour cette raison une valeur inférieure à 360 µmol/l est visée pour le traitement d’ abaissement de l’ acide urique.
Clinique et diagnostic
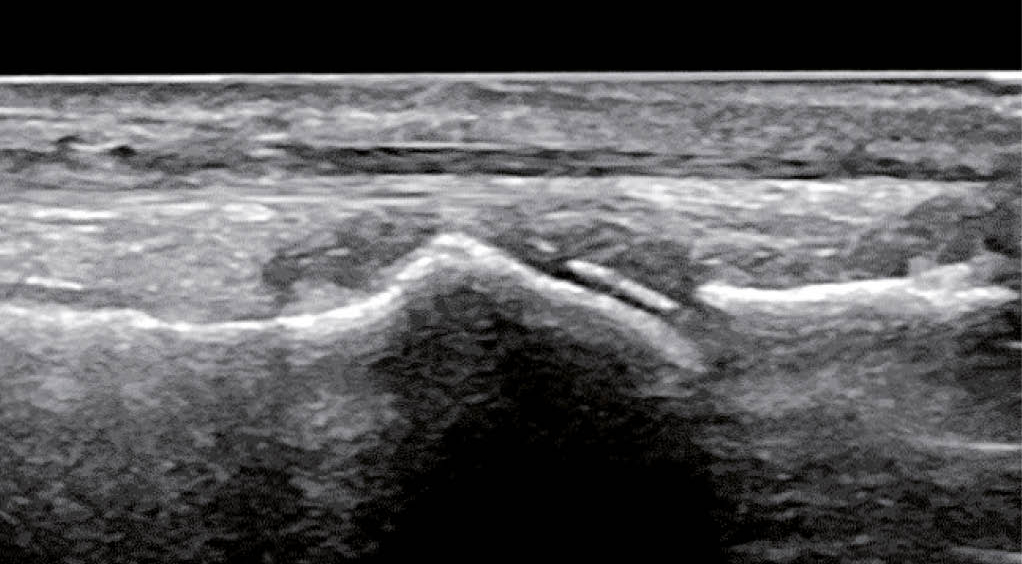
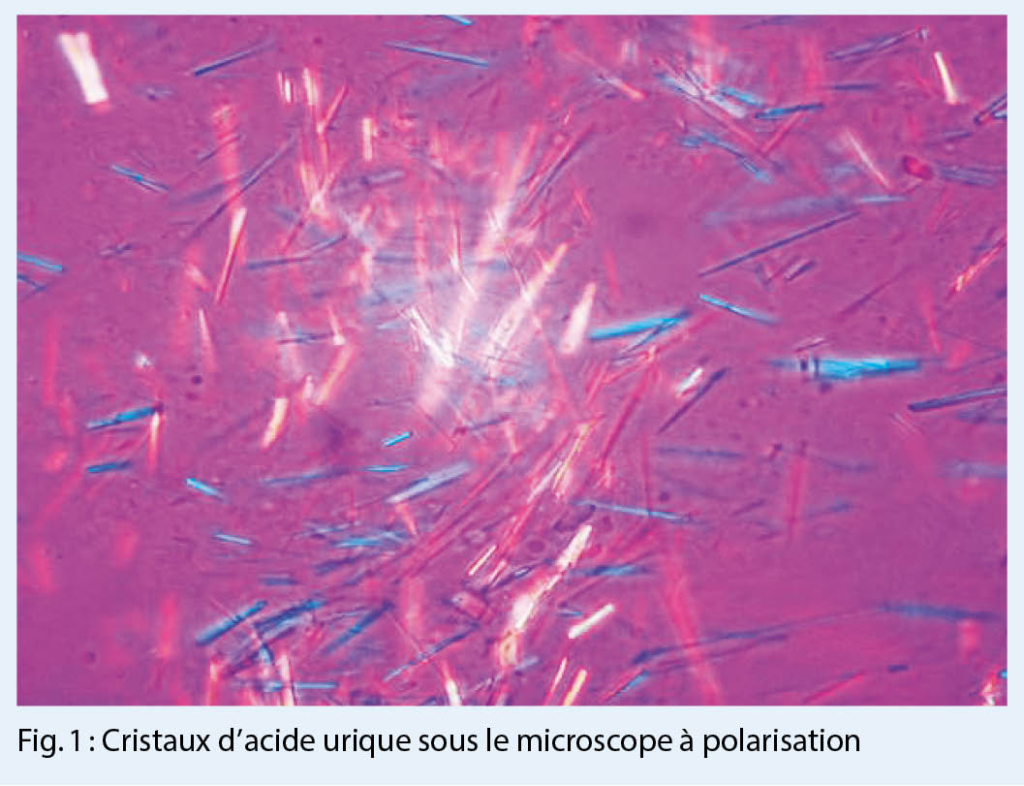
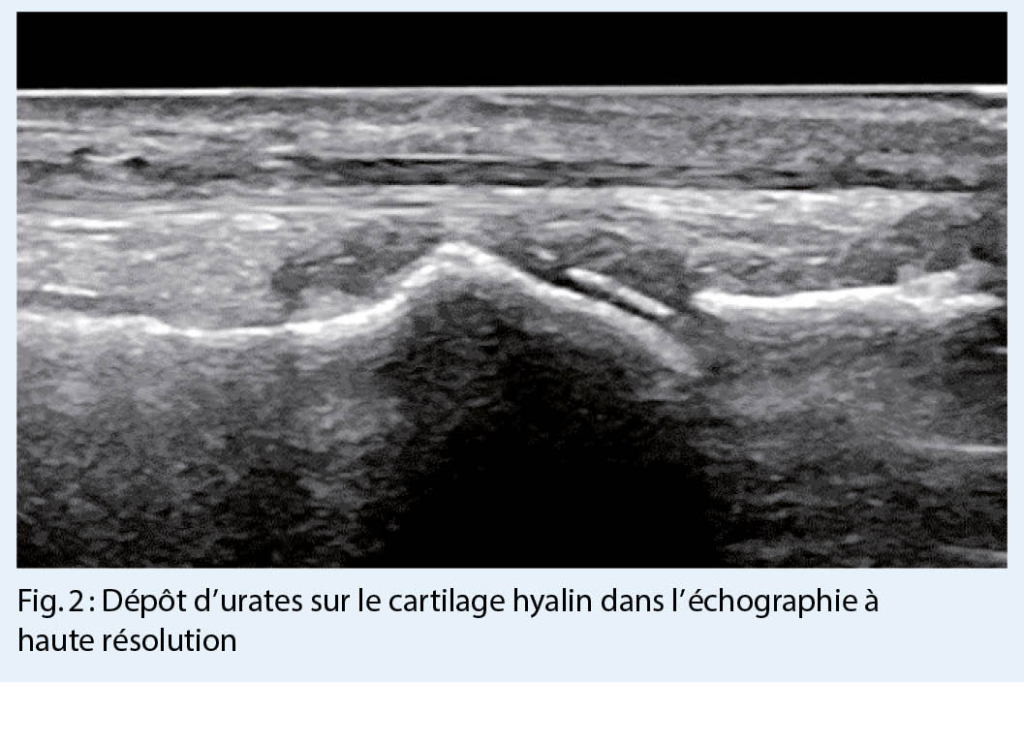
L’ arthrite goutteuse aiguë est généralement une monoarthrite qui se manifeste de façon suraiguë (avec des douleurs, des rougeurs et des gonflements importants) et affecte de préférence les membres inférieurs. Plus la clinique est typique, plus le diagnostic est probable. Cependant, le diagnostic différentiel doit toujours considérer une infection ou une pseudo-goutte (chondrocalcinose). Le gold-standard pour un diagnostic fiable reste la détection microscopique de cristaux d’ urates dans le prélèvement de l’ articulation affectée (fig. 1.) (ou celui du tissu) ou d’ identifier des dépôts d’ urates par échographie à haute résolution (fig. 2.) ou, à la rigueur, par tomodensitométrie à double énergie (les deux méthodes d’ imagerie sont très spécifiques, mais nécessitent un certain dépôt d’ urates pour être détectées et peuvent donc être faussement négatives, surtout dans les premiers stades).
La détermination de l’ acide urique sérique est moins utile au diagnostic lors d’ une crise (il peut même être plus faible qu’ en dehors d’ une crise), mais elle est importante pour le contrôle de la thérapie de base visant la réduction de l’ acide urique. Les signes accrus d’ inflammation (CRP, VS) et une leucocytose vont bien ensemble avec l’ inflammation aiguë de la goutte, mais ne sont bien sûr pas spécifiques à celle-ci.
Traitement
Traitement de la goutte aiguë
En plus du refroidissement local, il faut administrer des anti-inflammatoires puissants, c’ est-à-dire des anti-inflammatoires non stéroïdiens (s’ il n’ y a pas de contre-indication) ou des stéroïdes soit systémiques soit (mieux) administrés par voie intra-articulaire (si’ il n’ y a pas d’ infection suspectée) ou de la colchicine (bien qu’ elle ne soit pas officiellement approuvée en Suisse). Dans des cas particuliers, un inhibiteur de l’ interleukine-1 peut être administré par voie sous-cutanée en collaboration avec un rhumatologue en utilisation « off label ».
Traitement de base de l’ hyperuricémie
Des mesures non médicamenteuses (mode de vie) doivent être recommandées pour chaque patient. En ce qui concerne la nutrition, un régime alimentaire réduit est très utile en cas de surpoids (le risque d’ acide urique et de goutte augmente de façon linéaire avec l’ IMC). En outre, tous les patients doivent limiter la consommation de protéines animales au profit de protéines laitières et, si possible, éviter les boissons sucrées contenant du fructose, les jus de fruits et la bière. La prise en charge générale d’ un patient atteint d’ hyperuricémie comprend également l’ attention portée aux facteurs de risque cardiovasculaire les plus couramment associés.
Selon la situation, un traitement de base avec des médicaments (qui réduisent l’ acide urique) doit être envisagé après la première crise de goutte, mais est certainement indiqué en cas de plusieurs crises par an, en cas d’ insuffisance rénale simultanée ou si des calculs rénaux, tophi ou calculs d’urates existent déjà. Le traitement est initié après la disparition de la crise aiguë et doit conduire à une réduction fiable de l’ acide urique < 360µmol/l (en présence de tophi, de destruction articulaire ou de crises fréquentes < 300 µmol/l). En conséquence, la dose est progressivement augmentée et l’ acide urique est contrôlé régulièrement jusqu’ à ce que la valeur cible soit atteinte (« treat to target »). Il faut noter et expliquer au patient que, d’ une part, des crises aiguës de goutte peuvent se reproduire au début de la réduction du taux d’ acide urique (et que par conséquent il faut prescrire une prophylaxie d’ AINS à faible dose, de stéroïdes, par exemple 5 mg de Spiricort, ou 0,5 mg de colchicine pendant les premières semaines, soit au moins réserver des médicaments pour le traitement des crises !), et il faut lui expliquer que d’ autre part, même avec un traitement de base correct, on ne peut s’ attendre à une absence totale de crises qu’ après de nombreux mois. Le risque d’ effets secondaires est plus faible si les inhibiteurs de l’ acide urique sont dosés progressivement et augmenté progressivement (« start slow and go slow »).
Les inhibiteurs de la xanthine oxydase allopurinol ou fébuxostat restent le premier choix de médicament. Ce dernier n’ est pris en charge par les caisses maladies en Suisse que si des effets secondaires se produisent sous l’ allopurinol, s’ il y a une contre-indication ou si l’ effet est insuffisant. En cas de fonction rénale normale, il est recommandé de commencer par une dose de 100 mg d’ allopurinol, puis d’ augmenter progressivement la dose de 100 mg, par ex. toutes les 4 semaines, jusqu’ à ce que le niveau cible d’ acide urique soit atteint. Si nécessaire, l’ allopurinol peut être dosé sans problème jusqu’ à 600 mg/jour. En cas de fonction rénale limitée, la dose de départ doit être adaptée à la clairance de la créatinine. Souvent, ces patients ne reçoivent aucun traitement ou un traitement insuffisant pour réduire l’ acide urique par crainte des effets secondaires ; cependant, tant l’ expérience clinique que les données scientifiques de plus en plus nombreuses montrent qu’ une réduction adéquate de l’ acide urique améliore fréquemment la fonction rénale ou ralentit la progression de l’ insuffisance rénale.
Si l’ allopurinol entraîne des effets secondaires ou si son effet est insuffisant, le fébuxostat peut être utilisé, également en augmentant peu à peu les doses, commençant par 40 mg/j et augmentant jusqu’ à 80 mg/j. Contrairement à l’ allopurinol, aucun ajustement de dose n’ est nécessaire en cas d’ insuffisance rénale. Cependant, le fébuxo-stat doit être utilisé avec prudence chez les patients souffrant de cardiopathie ischémique.
Une troisième possibilité est l’ administration d’ uricosuriques (uniquement en cas de fonction rénale normale !), soit le probénécide (attention aux interactions !), soit le lésinurad (uniquement en combinaison avec l’ allopurinol).
Comme pour tous les traitements médicamenteux à long terme, une bonne information du patient et des contrôles réguliers sont tout aussi importants pour une adhérence optimale à la thérapie. Idéalement, le patient souffrant de la goutte connaît son taux d’ acide urique (et le taux cible) tout comme chaque patient diabétique connaît son taux d’ HbA1c.
Arthropathie à dépôts de pyrophosphate de calcium (« chondrocalcinose », « pseudo-goutte »)
Avec l’ âge, la prévalence des dépôts de cristaux de pyrophosphate de calcium dans les cartilages hyalins et fibreux augmente (ce qu’ on appelle la chondrocalcinose). Les causes et les mécanismes exacts de ce type de chondrocalcinose, dite primaire, sont encore inconnus. Sur le plan épidémiologique, les femmes sont un peu plus fréquemment touchées ; les groupes familiaux sont également décrits. Chez les patients plus jeunes (c’ est-à-dire avant l’ âge de 50 ans), un dépôt de cristaux de pyrophosphate de calcium peut déjà se produire dans certaines maladies métaboliques (par ex. l’ hémochromatose, l’ hypomagnésémie, l’ hyperparathyroïdie – on parle alors de chondrocalcinose secondaire).
Clinique et diagnostic
Cette maladie de dépôt de cristaux est également considérée comme le « caméléon » de la rhumatologie, car elle peut se manifester de nombreuses façons :
- résultats radiographiques asymptomatiques (« chondrocalcinose »)
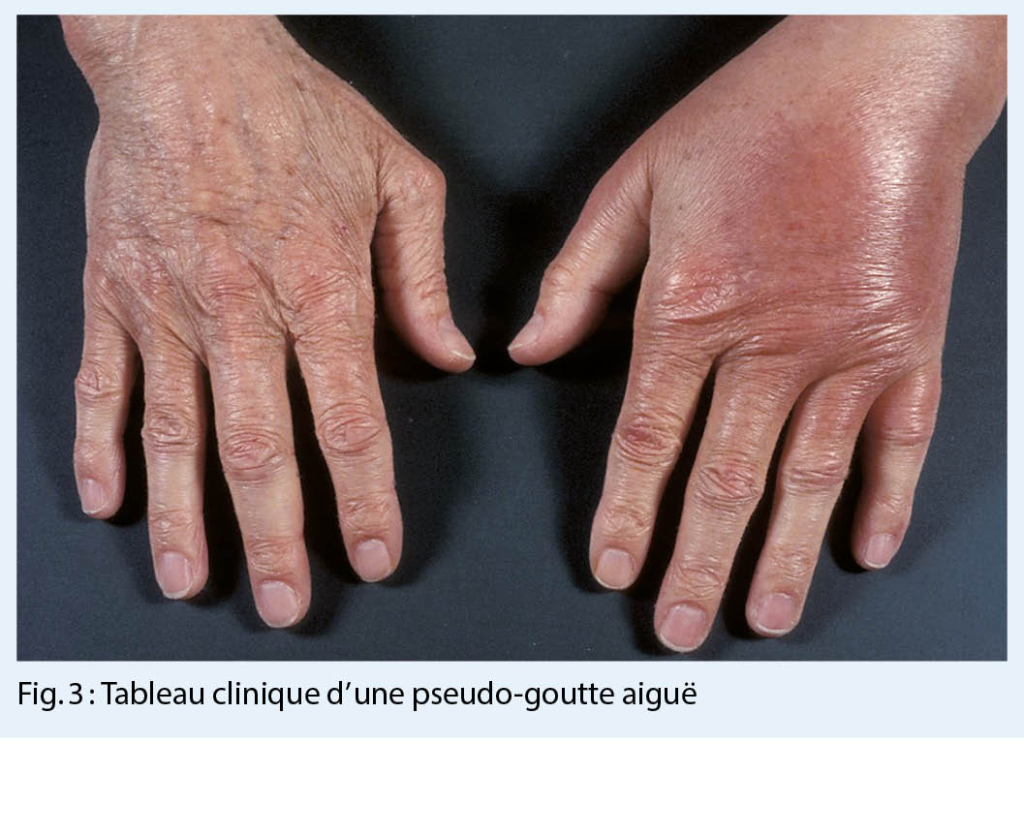
- arthrite aiguë (« pseudo-goutte ») (fig. 3)
- arthrose progressive dans les articulations qui ne sont pas principalement touchées par l’ arthrose (typiquement : carpe, articulations MCP, épaule, genou, hanche) ; lésions méniscales
- arthropathie destructive à évolution rapidement progressive (en particulier l’ articulation de la hanche, l’ articulation de l’ épaule)
- oligo-/ polyarthrite chronique (arthrite « pseudo-rhumatoïde »)
- ressemblant à la polymyalgie
- syndrome de la « dent couronnée » (angl. crowned dens syndrome – CDS) (« pseudoméningite » due à des dépôts de calcium dans les ligaments atlanto-axiales)
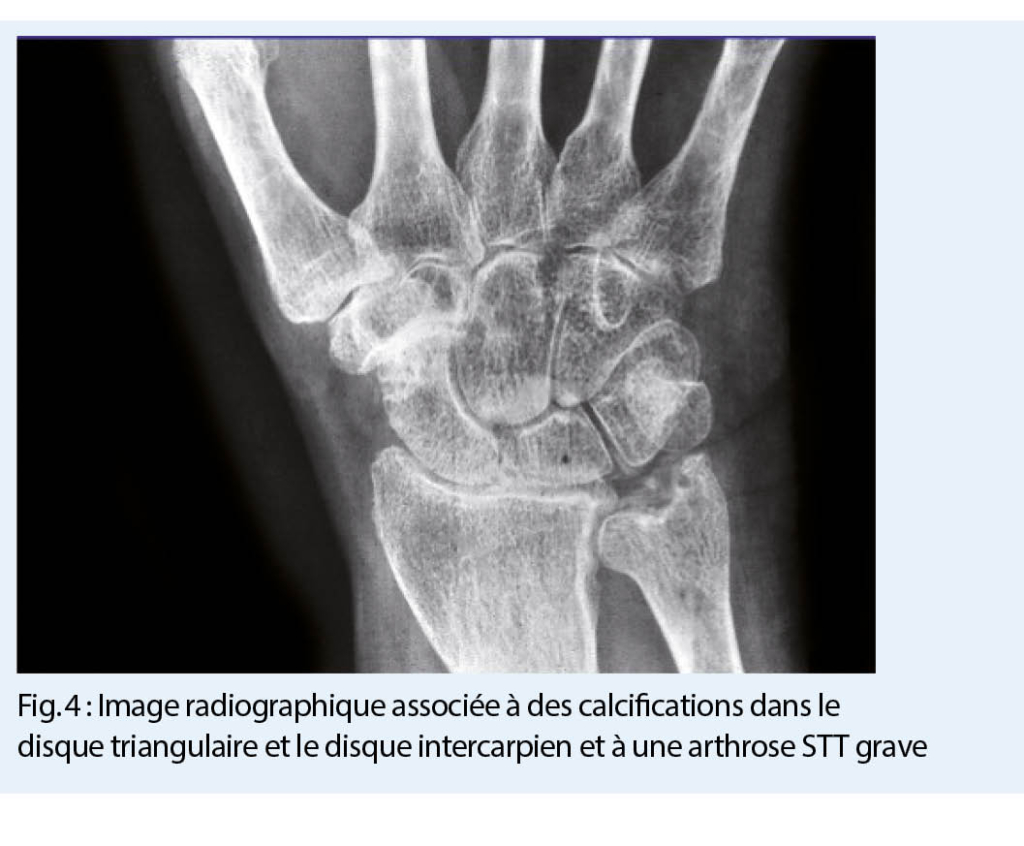
En plus du tableau clinique respectif, le diagnostic comprend également la détection microscopique de cristaux de pyrophosphate de calcium dans le liquide synovial ou de calcifications pathognomoniques du cartilage dans la radiographie conventionnelle (fig. 4.) ainsi que dans l’ échographie à haute résolution (ou dans la tomodensitométrie en cas d’ un syndrome de la dent couronnée).
Traitement
Les mêmes principes s’ appliquent au traitement de l’ arthrite aiguë (« pseudo-goutte ») qu’ à celui de l’ arthrite goutteuse. Il n’ existe cependant pas de véritable thérapie de base (ou traitement causal). Si les crises sont fréquentes, on peut essayer la colchicine ou, au mieux, une supplémentation en magnésium. En cas d’ oligo- à polyarthrite avec une évolution plutôt chronique, il faut essayer un traitement de base avec le méthotrexate.
Cet article est une traduction de « der informierte arzt » 03_2020
Rheuma- und Osteoporose-Zentrum Kloten
Kalchengasse 7
8302 Kloten
andreaskrebs@hin.ch
L’ auteur n’ a déclaré aucun conflit d’ intérêts en rapport avec cet article.
- La détection microscopique des cristaux reste le gold-standard du
diagnostic. L’ imagerie moderne peut aider, car elle est très spécifique, mais sa sensibilité est limitée. - Traitement de base de l’ acide urique par allopurinol ou (en cas d’ effets secondaires ou de contre-indications) par fébuxostat. Commencer
par de faibles doses, augmentation graduelle et cohérente de la dose jusqu’ à ce que la valeur cible de l’ acide urique de 360µmol/l ou 300µmol/l soit atteinte (« treat to target »). - Penser aux mesures non médicamenteuses et aux comorbidités.
- La chondrocalcinose est une cause fréquente de monarthrite aiguë chez les personnes âgées. Une radiographie conventionnelle contribue souvent au diagnostic.
la gazette médicale
- Vol. 9
- Ausgabe 2
- April 2020