- «ASCO-GI Symposium 2020» San Francisco
Zwischen dem 22. und 24. Januar 2020 fand das jährliche Symposium der ASCO zu den gastrointestinalen Tumoren statt. Kongressthema war «Accelerating Personalized Care». Das Symposium wurde durch 3500 internationale Teilnehmer in San Francisco besucht. Wie auch in den letzten Jahren wurden parallel dazu die Virtual Meeting Präsentationen in persönlicher Atmosphäre auf dem Uetliberg über Zürich verfolgt und interdisziplinär diskutiert. Die nachfolgende Zusammenfassung der wichtigsten Abstracts basiert auf der Einschätzung ihrer klinischen Relevanz und folgt in der Listung gemäss der Einteilung des Symposiums:
Tumore des Oesophagus und des Magens
Die Rolle einer Erhaltungstherapie mit einem Checkpoint Inhibitor bei Karzinomen des Magens und des gastroösophagealen Übergangs wurde in der Javelin Gastric 100-Studie untersucht. In dieser internationalen Phase III-Studie wurden bislang unbehandelte, lokal inoperable oder metastasierte Her-2-negative Magenkarzinome bzw. Karzinome des gastroösophagealen Übergangs mit einer mindestens stabilen Tumorsituation nach einer 12-wöchigen Induktionsphase mit einem FOLFOX/XELOX-Regime randomisiert zw. einer Erhaltungstherapie mit Avelumab bzw. Fortführung des bisherigen Chemotherapie-Regimes. Primärer Endpunkt dieser Studie war das Gesamtüberleben für die Gesamtpopulation sowie für die PD-L1-positive Subgruppe. Eine Verbesserung des Gesamtüberlebens durch eine Erhaltungstherapie mit Avelumab konnte nicht gezeigt werden (medianes OS mit Avelumab 10.4 Monate vs. 10.9 Monate mit Chemotherapie, HR 0.91; 2 Jahres OS: Avelumab 22.1% vs 15.5% mit Chemotherapie). Auch in der Subgruppe der PD-L1 positiven (cutoff ≥ 1% der Tumorzellen), die ca. 12% der Studienpopulation umfasste, fand sich keine Verbesserung des Gesamtüberlebens durch eine Erhaltungstherapie mit Avelumab. In den sekundären Endpunkten PFS und ORR zeigte sich ebenso keine sign. Verbesserung, jedoch eine längere duration of response durch Avelumab.
In der EXPEL-Studie wurde der Nutzen einer extensiven, peritonealen Lavage mit 10 Liter Kochsalzlösung gegenüber dem Standard einer Lavage mit < 2 Liter nach kurativ intendierter Gastrektomie beim Magenkarzinom untersucht. Der primäre Endpunkt dieser Phase III- Studie war das Gesamtüberleben. Hierbei zeigte sich im Gesamtüberleben nach 3 Jahren kein Unterschied (3 J OS: Lavage 23.1%, Standard 23.3%, HR 1.09). Auch die sekundären Endpunkte DFS und peritoneale Rezidivrate waren nicht unterschiedlich. Dieses rein mechanistische Vorgehen einer ausgiebigen Lavage nach Gastrektomie hat sich nicht als nützlich erwiesen und kann somit nicht empfohlen werden.
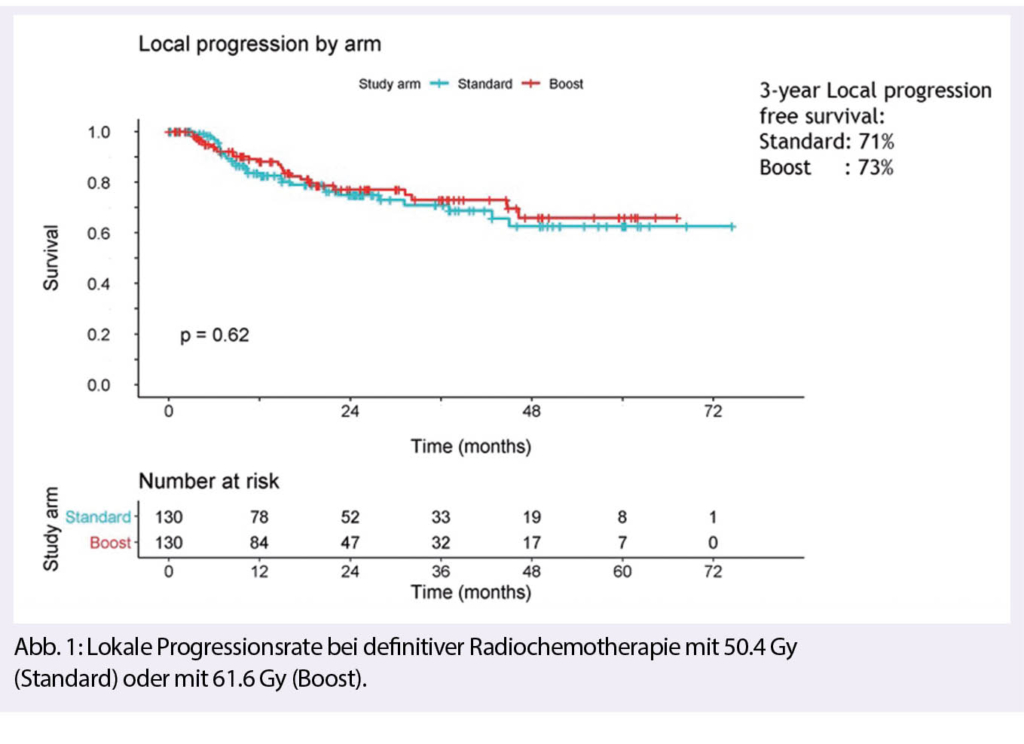
Eine Phase III-Studie untersuchte die Wirksamkeit einer Eskalation der Strahlendosis bei der definitiven kombinierten Radio-/Chemotherapie des Oesophaguskarzinoms. Die 2002 publizierte INT 0123 RTOG-Studie, welche eine Standarddosis von 50.4 Gy gegenüber einer höheren Strahlendosis von 64.8 Gy untersuchte, konnte keine Verbesserung der lokalen Kontrolle oder des Gesamtüberlebens zeigen. In der holländischen ARTDECO-Studie wurde die Frage erneut untersucht. Lokal fortgeschrittene Oesophaguskarzinome (T2-4a, N0-3, M0) wurden entweder mit der Standarddosis von 50.4 Gy oder im experimentellen Arm mit 61.6 Gy bestrahlt. Es erfolgte eine 3D-konformale Bestrahlungstechnik, hauptsächlich IMRT/VMAT, radiosensibilisierend wurden 6 Gaben einer wöchentlichen Chemotherapie mit Carboplatin und Paclitaxel verabreicht. Primäres Studienziel war die Verbesserung der lokalen Kontrolle. Die lokale Tumorkontrolle nach 3 Jahren betrug 71% im Standardarm und 73% im experimentellen Arm und war somit nicht signifikant unterschiedlich. Auch nach Aufschlüsselung gemäss histologischem Subtyp ergab sich kein Benefit durch die höhere Strahlendosis. Im Therapiearm mit 61.6 Gy waren die G3 und G4 Toxizitäten leicht erhöht (75% vs. 66%), ebenso fand man eine leicht erhöhte therapieassoziierte Mortalität. Somit bleibt die empfohlene Standarddosis der definitiven Radio-/Chemotherapie des inoperablen Oesophaguskarzinoms 50.4 Gy.
Tumore der Bauchspeicheldrüse, Gallenwege und Leber
In einer randomisierten Phase II-Studie wurden 50 nicht vorbehandelte Patienten mit BRCA 1/2 oder mit PALB2-mutierten Pankreaskarzinom in eine wöchentliche Chemotherapie mit Cisplatin (25 mg/m2) und Gemcitabin (600 mg/m2) alleine oder mit dem PARP-Inhibitor Veliparib randomisiert. 47 Patienten hatten eine BRCA-Keimbahnmutation, die meisten davon eine BRCA-2-Mutation. Die RECIST-Remissionsraten lagen bei 65% und 74%, das mPFS bei 10.1 bzw. und bzw. 9.7 Monaten. Die mediane Überlebenszeit betrug 16 Monaten. Die Erkenntnis aus dieser relativ kleinen Studie ist folgende: Der Einsatz einer platinhaltigen Chemotherapie bei frühzeitiger Diagnose einer BRCA 1/2-, oder einer PALB2-Mutation ist wirksam. Der ergänzende Nutzen eines PARP-Inhibitors erscheint gesamthaft klein zu sein. Die geringe Zahl an BRCA1/2-Mutationen rechtfertigt jedoch eine routinemässige Untersuchung aller Patienten mit metastasiertem Pankreaskarzinom nicht.
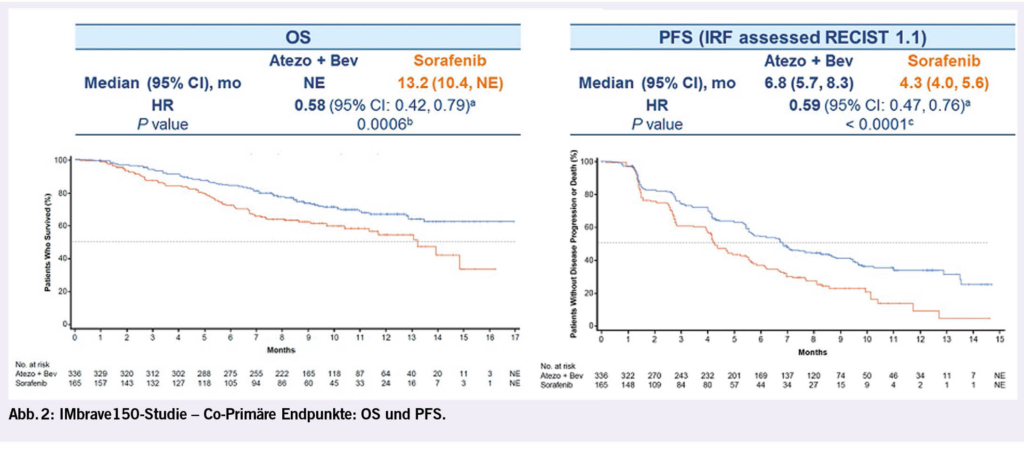
Die IMbrave150-Studie ist eine internationale Phase III-Studie bei Patienten mit fortgeschrittenem HCC und erhaltener Leberfunktion (Child A). Randomisiert wurde in Sorafenib oder in eine Kombinationstherapie mit Atezolizumab und Bevacizumab. Erste Resultate dieser Studie wurden bereits am ESMO Asia Meeting im Herbst 2019 vorgestellt. In dieser Studie konnte erstmalig eine Überlegenheit einer Immun-Kombinationstherapie gegenüber Sorafenib festgestellt werden. Obgleich die Ergebnisse noch früh sind (mediane Nachbeobachtungszeit 8 Monate), zeigt sich eine stat. Überlegenheit beim gesamt- als auch beim progressionsfreien Überleben. Ergänzt wurden die Ergebnisse durch umfangreiche PRO- und Lebensqualitätsanalysen, die die klinische Überlegenheit der Kombinationstherapien weiter unterstützen.
Tumore von Kolon und Rektum
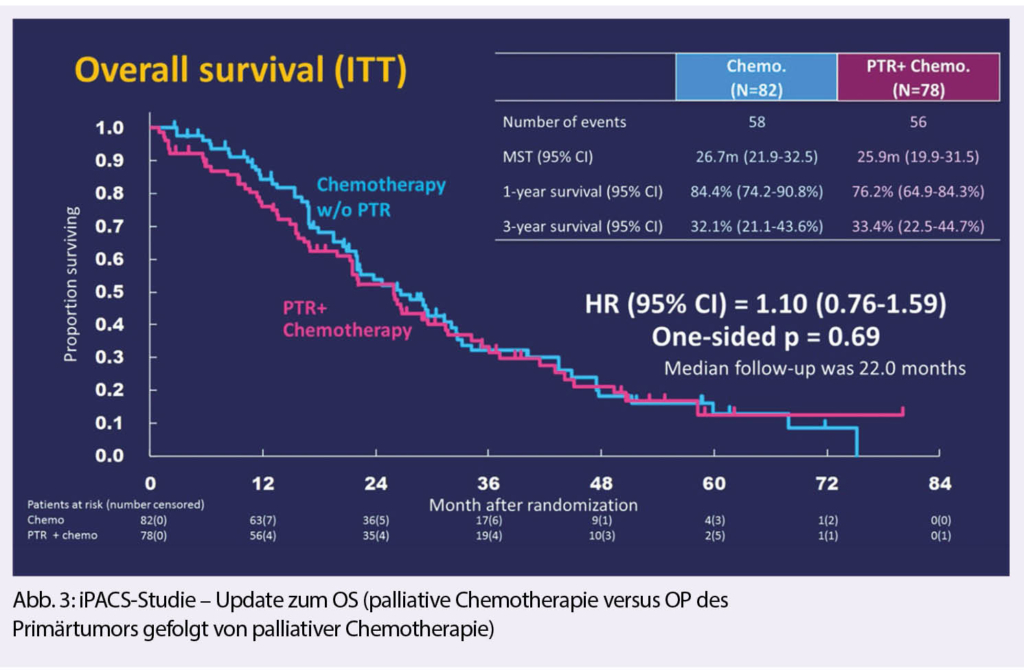
In der vorzeitig abgebrochenen Phase III-Studie JCOG1007 study (iPACS) wurde erstmals randomisiert untersucht, ob Patienten mit synchron aufgetretenen nicht resezierbaren Metastasen eines kolorektalen Karzinoms von einer Resektion des Primarius, vor Einleitung einer palliativen Chemotherapie, profitieren. Bisher gab es dazu retrospektive Analysen, die eine Prognoseverbesserung nach einer Resektion des Primärtumors suggerierten. Das mediane OS lag in beiden Gruppen bei 26 Monate. Es kam zu drei Todesfällen aufgrund von postoperativen Komplikationen. In dieser Studie konnte klar gezeigt werden, dass bei Patienten mit metastasiertem Kolorektalkarzinom, die bezüglich des Primärtumors asymptomatisch sind, die primäre Tumorresektion kein Vorteil bringt. Weitere Resultate zu diesem Thema werden aus einer deutschen Phase III-Studie erwartet.
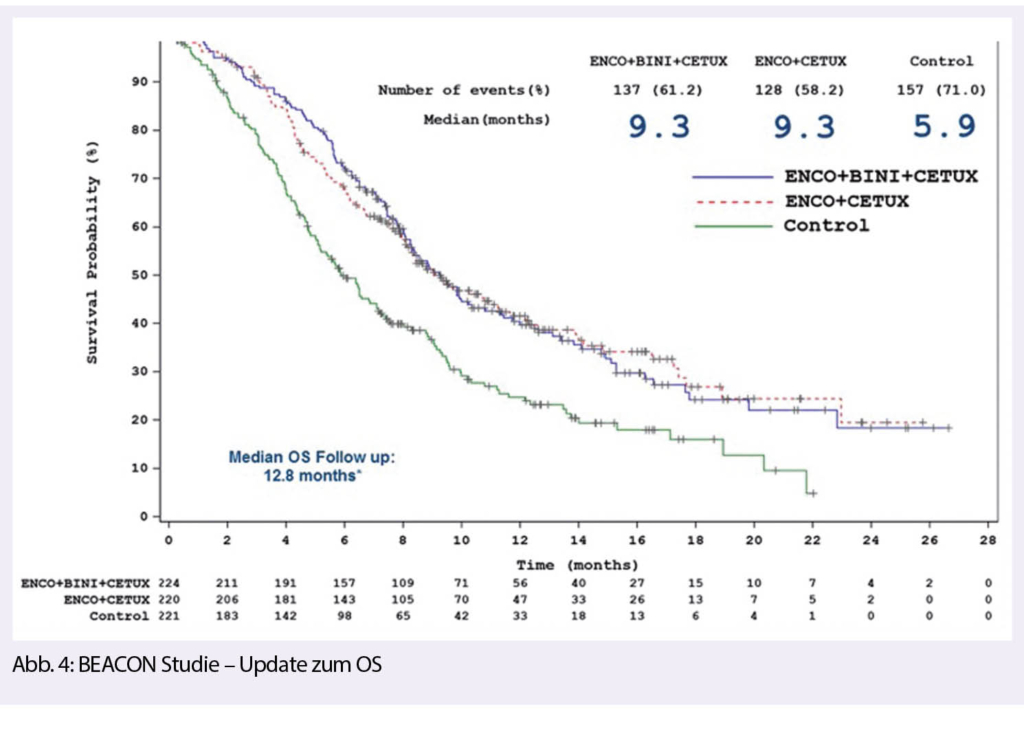
Die BEACON CRC-Studie war eine randomisierte, dreiarmige Phase III-Studie (vgl. Vollpublikation Kopetz S et al. N Engl J Med 2019; 381:1632-43), welche bei Patienten mit BRAF V600E-Mutationen in der Zweitlinienbehandlung eine zielgerichtete Therapie mit einem Triplet (Encorafenib+Binimetinib + Cetuximab) oder die Doublette (Encorafenib + Cetuximab) gegenüber einer Chemotherapie mit Irinotecan oder FOLFIRI-Schema + Cetuximab untersuchte.
Es konnte zusammengefasst gezeigt werden, dass die beiden zielgerichteten Therapien zu einer signifikanten Verbesserung des OS und des Tumoransprechens führt.
Neben einem Update der Studienhauptresultate wurden Ergebnisse zur Lebensqualität vorgestellt.
Die Lebensqualität wurde in verschiedenen Messungen untersucht. Hierbei zeigte sich eine signifikant längere Zeit bis zur Verschlechterung in den beiden Armen mit zielgerichteter Therapie – ein weiteres wichtiges Argument für den Einsatz von Präzisionsmedizin bei Patienten mit BRAF-mutiertem Kolorektalkarzinom.
Ein Update zur Phase 2 CheckMate 142-Studie wurde bei Patienten mit metastasiertem mikrosatelliteninstabilem (MSI) Kolorektalkarzinom vorgestellt. In der Erstlinientherapie wurde Nivolumab (3 mg/kg) und Ipilimumab (1 mg/kg) eingesetzt. Die ORR lag bei 60%. Die Remissionen waren lange anhaltend. 16% der Patienten hatten Grad 3-4 Nebenwirkungen. Eindrucksvolle Resultate für eine Immunkombinationstherapie in der Erstlinie.
St. Claraspital
Kleinriehenstrasse 30
4058 Basel
St. Claraspital
Kleinriehenstrasse 30
4058 Basel
St. Claraspital AG
Tumorzentrum
Kleinriehenstrasse 30
4058 Basel
tumorzentrum@claraspital.ch
info@onco-suisse
- Vol. 10
- Ausgabe 2
- April 2020