- Welchen Stellenwert hat das MRI?
Lage- und Funktionsveränderungen von Beckenorganen sind ein häufiges Problem und betreffen fast jede zweite Frau im Verlauf ihres Lebens. In der westlichen Welt wird sich jede fünfte Frau bis zum Alter von 80 Jahren einer Prolaps- oder Kontinenzoperation unterziehen (lifetime risk 19 %) (1). Bei bis zu 30 % der operierten Patientinnen ist wiederum eine Rezidiv-Deszensusoperation erforderlich.
Les altérations de position et de fonction des organes du petit bassin sont un problème fréquent et touchent presque une femme sur deux au courant de sa vie. Dans le monde occidental, une femme sur 5 aura subi jusqu’à ses 80 ans une intervention pour prolapsus ou incontinence (lifetime risk 19 %) (1). Et jusqu’à 30 % de ces femmes devront se faire réopérer pour récidive de prolapsus.
Eine statistische Auswertung der Daten der Arbeitsgemeinschaft Schweizerischer Frauenkliniken (ASF), die die stationären gynäkologischen Operationen erfassen, zeigte, dass die Anzahl urogynäkologischer Operationen zwischen 1998 und 2013 um 57% zugenommen hat.
Doch welche anatomische Läsion Ursache für die Beckenbodenpathologie ist, bleibt im Einzelfall meist ungeklärt. Diese Wissenslücke könnte mitunter ein Grund für die relativ hohe Rezidivrate sein.
Dank Magnet-Resonanz-Tomographie (2) können wir anatomische Supportstrukturen wie die Subdivisionen des Levator ani Muskels, den urethralen Sphinkterkomplex und ligamentäre Strukturen visualisieren (3, 4). Dies sind wichtige Strukturen in der Pathogenese von urogynäkologischen Erkrankungen.
Technik der Magnetresonanztomographie des Beckenbodens
Die Magnetresonanztomographie ist ein diagnostisches Verfahren, das keine Röntgenstrahlung zur Bilderstellung verwendet, sondern mit Magnetfeldern und Radiowellen arbeitet. Nach derzeitigem Erkenntnisstand (seit 1984 in der Patientenanwendung) hat die MRT keinen schädigenden Einfluss auf den menschlichen Organismus. Im Gegensatz zur Tumordiagnostik kann die MRT Untersuchung für die urogynäkologischen Untersuchungen kontrastmittelfrei durchgeführt werden. Nachteilig gegenüber anderen Bildgebungen wie dem Ultraschall sind die höheren Kosten.
Die Untersuchungsparameter werden organ- und untersuchungsspezifisch (T1, T2, Protonendichte-Wichtung) gewählt. Die T2-gewichteten multiplanaren Schichten eignen sich besonders gut für die Darstellung der feinen anatomischen Schichten und Strukturen, was z.B. die Beurteilung der Schichtung der Vagina (Mukosa, Muskulatur und Adventitia), Urethra und ihrer Sphinkter, Uterus, aber auch zur Beurteilung der Faserverläufe des Levator ani erlaubt (3). Die T1 gewichteten Sequenzen sind ideal für die Detektion von Fett und Blut (Hämatokolpos/-metra bei Fehlbildungen). Mit dem technischen Fortschritt können dynamische Untersuchungen von 14 bis 16 Sekunden lang dauernden Pressmanövern abgebildet werden, was für die Patientin zeitlich zumutbar ist. Damit könnte in Zukunft die MRT für die Funktionsabklärung an Bedeutung gewinnen, insbesondere durch den Fortschritt der Technik und der sinkenden Preise der MRT-Untersuchung. Kontraindikationen für den Einsatz der MRT sind nicht-MRT-taugliche Herzschrittmacher und Implantate sowie eine schwere Klaustrophobie. Bei anamnestisch angegebenen Hirn- oder Herzoperationen ist wegen der Verwendung potentiell nicht-MRT-tauglicher Clips oder Prothesen Vorsicht geboten.
Was können wir mit MRT visualisieren?
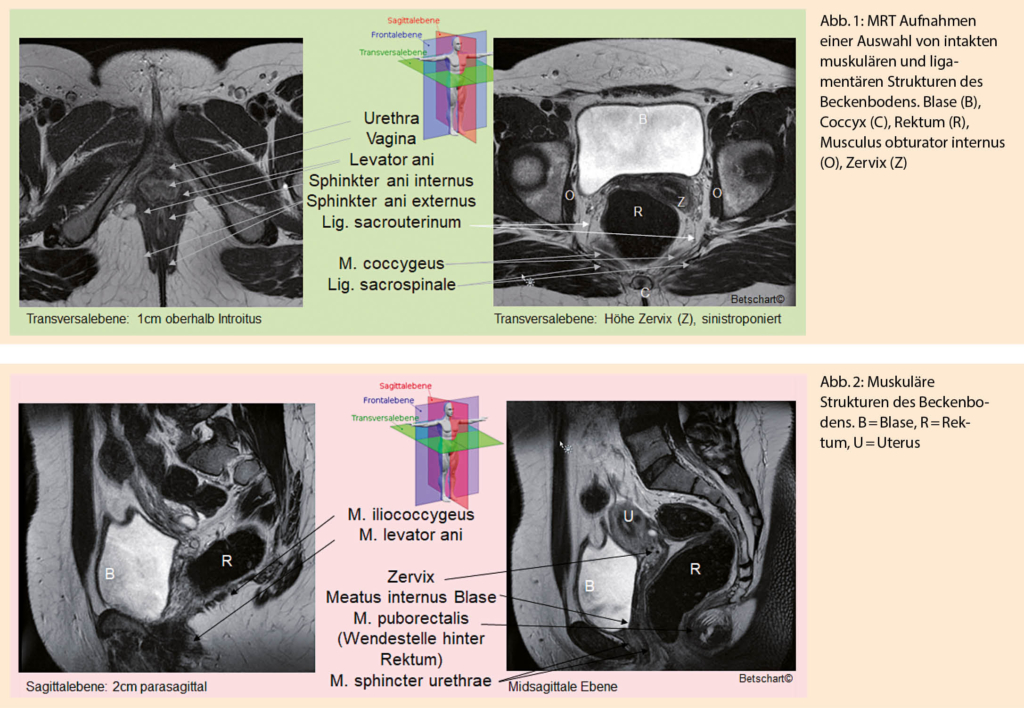
Mit der MRT können anatomische Strukturen mit einer hohen Detailtreue abgebildet werden (5, 6). Durch die hohe Bildauflösung der Weichteile gelingt die Darstellung der Morphologie von Harnblase, Urethra (7), Rektum, Anus inklusive Analsphinkterkomplex, Vagina, Musculus levator ani und benachbarter Faszien- und Bandkomplexe (Abb. 1 und 2) (8, 9). Die meisten Beckenbodenstrukturen verlaufen nicht exakt in einer der multiplanaren Schichten, weshalb auf jedem Schnittbild nur ein Teil der Struktur abgebildet wird. Die Identifikation intakter Strukturen, z. B. bei jungen, nulliparen Frauen, ist wichtig, um weiteres Wissen über die Morphologie und Funktion des Beckenbodens zu gewinnen (Tab. 1). Denn basierend auf dem Wissen über die intakten Strukturen können Insuffizienzen in einem späteren, präsymptomatischen Stadium detektiert werden, was für das Verständnis der Pathomechanismen, die später im Leben zum symptomatischen Prolaps führen, von Bedeutung ist (10). Auch ein wichtiger Stellenwert der MRT liegt in der Abklärung von urogenitalen Malformationen. Nicht selten liegen hierbei komplexe Fehlbildungen vor, die verschiedene Organe wie Vagina, Uterus, Wirbelsäule und Nieren betreffen können. Aus Platzgründen kann diese Problematik in diesem Artikel nicht vertieft dargestellt werden.
Die MRT beantwortet auch wissenschaftliche Fragestellungen zur Pathomorphologie der Belastungsharninkontinenz (11), der Analinkontinenz und des Descensus urogenitalis (12), sowie zu qualitativen und quantitativen Fragestellungen schwangerschafts- und altersbedingter Veränderungen der Beckenbodenstrukturen.
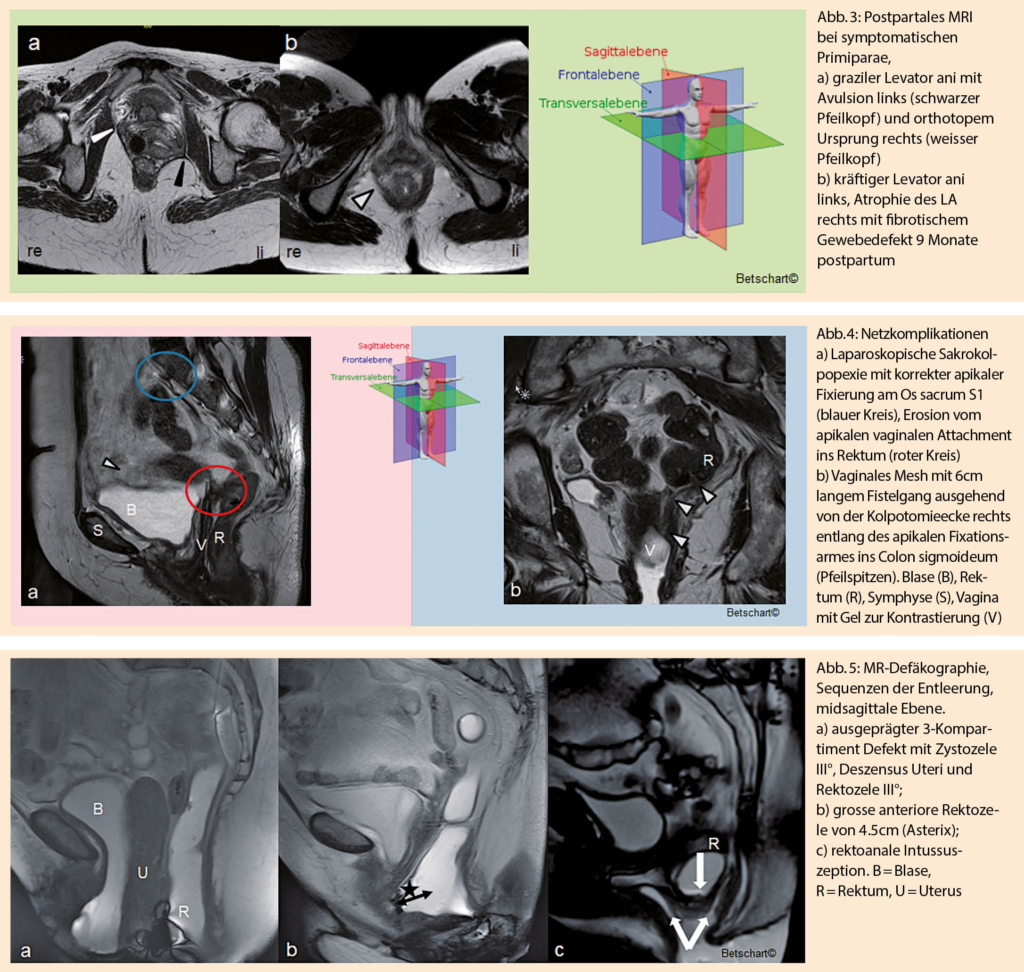
Abbildung 3 zeigt postpartale Defekte. Intrapartal kann es zum Ausriss des Levator ani (genauer gesagt des M. pubovisceralis-Anteils symphyhysennahe am Os pubis) kommen. Ein solcher Levatorabbriss (im englischen Sprachgebrauch auch «Levator avulsion» genannt) ist in Abb. 3a dargestellt. Solche Muskeldefekte können im vorderen Kompartiment eine Zystozele und im mittleren Kompartiment einen Deszensus uteri oder Scheidenstumpfprolaps zur Folge haben. In der Abbildung 3b ist eine Muskelschädigung durch eine intrapartale Kompression dargestellt: Durch die kindliche Kopfkompression können neurologische Traumata und Ischämien resultieren, worauf der geschädigte Muskel durch fibrotisches Gewebe (helle Struktur) ersetzt wird. Eindrücklich ist in diesem Bildvergleich auch die interindividuelle Variation der Muskeldicke des Levator ani zwischen den beiden Primiparae.
Die MRT hat weitere Kenntnisse zur in-vivo Anatomie der Beckenbodenmuskulatur und endopelvinen Faszie ermöglicht: Bei Nulliparae liegen 2- bis 3-fache interindividuelle Volumenschwankungen der Beckenbodenmuskulatur vor, und in 10% fehlt der Nachweis der Insertion des M. levator ani am Os pubis und der muskulofaszialen Verschmelzung zwischen seitlicher Vaginalwand und Levatormuskulatur, was ein konstitutionelles Risiko für die Harninkontinenz-Entstehung bedeuten könnte (13).
Folgende Zeichen in der MRT sind Hinweise für pathomorphologische Veränderungen der Beckenbodenmuskulatur und der endopelvinen Faszie:
1. eine in T2-gewichteten Bildern erhöhte Signalintensität des M. levator ani, bedingt durch Verlust quer gestreifter Muskelfasern und vermehrter Fett- und Bindegewebseinlagerung (Abb. 3),
2. der Verlust der symphysenwärts konkaven Scheidenkonfiguration und das Fehlen der muskulofaszialen Verschmelzung zwischen seitlicher Vaginalwand und Levatormuskulatur weisen auf laterale Defekte der endopelvinen Faszie hin,
3. der Verlust der Faszienstruktur der vorderen Vaginalwand weist auf zentrale Defekte der endopelvinen Faszie (11).
MRT Indikationen im Alltag
Im klinischen Alltag begegnen uns Patientinnen mit unterschiedlichen Beckenbodenbeschwerden. Die wohl am schwierigsten fassbaren Beschwerden sind die prolongierten postpartalen Schmerzen, die chronischen Unterbauchschmerzen (chronic pelvic pain syndrome, CPP) oder Schmerzen nach Operationen, wo die klinische gynäkologische Untersuchung an ihre Grenzen stösst (14, 15). Hierzu hat sich die MRT als gutes Diagnostikum zur Abklärung von Infektionen, Abszessen, Ödemen oder Fisteln gezeigt. Netzkomplikationen resp. netzverursachte Erosionen in Blase oder Darm können mit MR sichtbar gemacht werden (Abb. 4). Diese Diagnostik ist auch wichtig für den interdisziplinären Einbezug von Kollegen in der Operationsplanung.
Eine neuere Studie zu Netz-assoziierten Beschwerden zeigte, dass die MRT-Untersuchung bei 42,1% der Frauen ein Versagen des Netzes oder der OP-Technik (Netzausriss vaginal oder am Promontorium, Netzlaxität oder Netzbruch), bei 12,6% eine Infektion (Abszedierung, Spondylodiszitis), bei 12,6% eine Netzerosion in benachbarte Organe, bei 11,5% eine Umgebungsentzündung, bei 2,3% eine Kompression von Organen und bei 2,3% eine Darmextrusion detektierte. Die Übereinstimmung zwischen dem MRT-Bericht und der chirurgischen Diagnose war bei Netzversagen, Infektion und Kompression nahezu perfekt, während die Übereinstimmung bei Netzerosion und Entzündungszeichen mässig war (15).
Der Stellenwert der MRT bei CPP lässt dagegen zu wünschen übrig. Auch eine oberflächliche peritoneale Endometriose, Adhäsionen, aber auch die Diagnose des idiopathischen Schmerzsyndroms können nicht zuverlässig gestellt werden (14). Hier zeigte sich in einer neueren Studie die Laparoskopie der MRT in der CPP-Diagnostik überlegen. Trotzdem können bei CPP in der MRT Periostitiden, Symphysitis oder neurologische Pathologien entdeckt werden, welche wiederum laparoskopisch nicht erfasst werden können. Somit sind MRT und Laparoskopie je nach Fragestellung komplementäre Untersuchungen.
Junge Frauen mit urogenitalen Fehlbildungen können verschiedene Fehlbildungen in Kombination aufweisen. Die MRT erfasst diese einseitig, was für die Aufklärung und die Operationsplanung von Bedeutung ist. Auf der Grundlage der Bildgebung können Fragen zur Reproduktion, Entartungsrisiken und zur nephrologischen Vorsorge beantwortet werden.
MR-Defäkographie
Bei einer Diskrepanz zwischen der geschilderten Darmfunktionsstörung (Obstipation, Nachschmieren, Stuhldrang oder manuell unterstützte Darmentleerung) und der klinischen Ausprägung einer Rektozele sollte die Defäkographie indiziert werden. Sie ermöglicht eine objektive Beurteilung der Lageveränderung des Rektums (anteriore Rektozele, Intussuszeption, siehe Abb. 5), eines Anal- bzw. Rektumprolapses bzw. die Kompression des Rektums durch eine durchhängende Sigmaschleife (Cul-de-sac-Phänomen). Die aufgezeichneten Sequenzen erlauben weiter eine Beurteilung der Motorik der Beckenbodenmuskulatur und können Hinweise auf eine dyssynerge Defäkation geben.
Bei der MR-Defäkographie wird der Patientin peranal ein Gel appliziert. Es werden dynamische sagittale Sequenzen aufgezeichnet: Ruhe, Kneif-, Press-, und Entleerungsphase, während denen die Bewegung der Beckenorgane und schliesslich der Defäkationsvorgang abgebildet werden. Die Deszensusqualität, im Speziellen beim Scheidenstumpfprolaps, lässt sich zuverlässig diagnostizieren: Darstellung von Enterozele (Defekt-Level I), Urethrozysto- und Rektozele (Defekt-Level II und III) (16). Ganz wichtig und nicht durch eine andere Bildgebung ersetzbar ist die Diagnostik der Intussuszeption (17), was therapeutische Konsequenzen hat, da sie durch eine klassische Kolpoperineoplastik nicht behoben werden kann.
Wie werden Beckenbodendefekte quantifiziert?
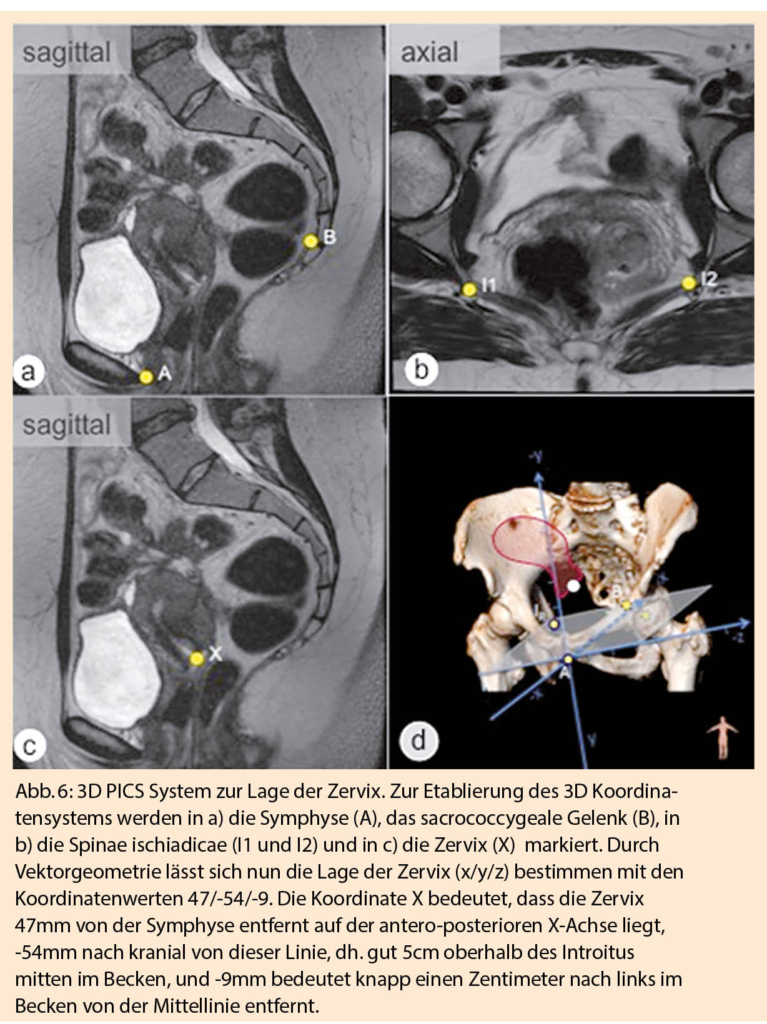
Die Beckenbodeninsuffizienz ist ein Phänomen, das der Schwerkraft unterliegt. Bis anhin fand die Klassifizierung semiquantitativ mittels der Baden-Walker oder POP-Q Klassifikation statt. MRT dagegen ermöglicht eine millimetergenaue und untersuchungsabhängige Lokalisierung im Raum: Mit vier Fixpunkten in zwei Ebenen lässt sich ein Koordinatensystem aufstellen, worin jedes Organ, Ligament oder Muskel mit einer oder – wenn es sich um einen Verlauf oder wie bei Muskeln um Ursprung und Ansatz handelt – mehreren Koordinaten versehen werden kann. Ein solches System ist das 3D Pelvic Inclination Correction System (3D PICS) (18). Das 3D PICS definiert sich über die knöchernen Fixpunkte der Symphyse, des Promontorium und den Spinae ischiadicae (Abb. 6). Organe oder Strukturen, die sich im Lauf des Lebens senken können, werden mit einer Koordinate im 3D Raum (x/y/z) versehen. Die Koordinate lässt sich unabhängig von der Lage der Patientin im Scanner und unabhängig vom Senkungs- und Füllungszustand der Organe rekonstruieren und erlaubt, Studienkollektive und operative Outcomes zu vergleichen. Im Gegensatz zu den MR-Referenzlinien, welche sich nur in einer Ebene, nämlich der midsagittalen Ebene anwenden lassen, kann mit dem 3D PICS System jede Struktur im Raum in jeder der drei MRT Ebenen quantifiziert werden. Dieses System findet zunehmend Verbreitung und die Autoren*innen werden bald ein user-freundliches Online System vorstellen können.
PD Dr. med. Cornelia Betschart
Dr. med. Ioannis Dedes
Dr. med. David Scheiner
PD Dr. med. Cäcilia Reiner
Klinik für Gynäkologie, Universitätsspital Zürich
Frauenklinikstrasse 10, 8091 Zürich
Wir bedanken uns beim Schweizerischer Nationalfonds zur Förderung der wissenschaftlichen Forschung für die Projektunterstützung «Beckenbodenanatomie in der Bildgebung» (SNF Project PBBEP3_139382).
Copyright bei Aerzteverlag medinfo AG
Stellvertretende Klinikdirektorin
Klinik für Gynäkologie, USZ
Frauenklinikstrasse 10
8006 Zürich
cornelia.betschart@usz.ch
Klinik für Gynäkologie
Universitätsspital Zürich
Frauenklinikstrasse 10
8091 Zürich
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Beitrag deklariert.
- Klinische Indikationen für eine Becken-MRT sind Beschwerden nach Operationen, nach Netzeinlagen, komplexe Urethraldivertikel, v.a. vesikovaginale oder rektovaginale Fisteln, sowie urogenitale Fehlbildungen. Bei urogenitalen Fehlbildungen empfiehlt sich, die MRT bis zu den Nieren zu fahren.
- MRT und Laparoskopie beim Chronic Pelvic Pain Syndrome sind je nach Fragestellung und Anamnese differenziert zu indizieren und komplementär zu betrachten.
- Die dynamische MR-Defäkographie ermöglicht die Differenzierung zwischen anteriorer Rektozele und Intussuszeption. Diese Unterscheidung ist wichtig für die Wahl des chirurgischen Verfahrens.
- Spezielle MR-Protokolle dienen der Wissenschaft zur Erforschung der Krankheitsmechanismen von Prolaps und dessen Haltestrukturen sowie der Inkontinenz.
Messages à retenir
- Les indications cliniques pour une résonance magnétique (IRM) du petit bassin sont les troubles après opération ou pose de mesh, des diverticules urétraux complexes, la suspicion de fistule vésico- ou rectovaginale et les malformations urogénitales. Dans ces derniers cas, il convient de monter avec l’imagerie jusqu’aux reins.
- En cas de douleurs pelviennes chroniques (Chronic Pelvic Pain Syndrome), l’IRM et la laparoscopie ont leurs indications différenciées selon l’anamnèse et les questions précises à résoudre. Ce sont des examens complémentaires.
- La défécographie dynamique par IRM permet de différencier la rectocèle antérieure de l’intussusception. Cette distinction est importante pour le choix de la procédure opératoire.
- Des protocoles IRM scientifiques étudient les mécanismes du prolapsus, les structures de soutien du plancher pelvien et la génèse de l’incontinence.
1. Smith FJ, Holman CD, Moorin RE, Tsokos N. Lifetime risk of undergoing surgery for pelvic organ prolapse. Obstetrics and gynecology. 2010;116(5):1096-100.
2. Lim K, Small W, Jr., Portelance L, Creutzberg C, Jurgenliemk-Schulz IM, Mundt A, et al. Consensus guidelines for delineation of clinical target volume for intensity-modulated pelvic radiotherapy for the definitive treatment of cervix cancer. Int J Radiat Oncol Biol Phys. 2011;79(2):348-55.
3. Betschart C, Kim J, Miller JM, Ashton-Miller JA, DeLancey JOL. Comparison of muscle fiber directions between different levator ani muscle subdivisions: in vivo MRI measurements in women. International urogynecology journal. 2014;25(9):1263-8.
4. Luo JJ, Betschart C, Chen LY, Ashton-Miller JA, DeLancey JOL. Using stress MRI to analyze the 3D changes in apical ligament geometry from rest to maximal Valsalva: a pilot study. International urogynecology journal. 2014;25(2):197-203.
5. Lockhart ME, Bates GW, Morgan DE, Beasley TM, Richter HE. Dynamic 3T pelvic floor magnetic resonance imaging in women progressing from the nulligravid to the primiparous state. International urogynecology journal. 2018;29(5):735-44.
6. Khatri G, de Leon AD, Lockhart ME. MR Imaging of the Pelvic Floor. Magn Reson Imaging Clin N Am. 2017;25(3):457-80.
7. Clobes A, DeLancey JO, Morgan DM. Urethral circular smooth muscle in young and old women. American journal of obstetrics and gynecology. 2008;198(5):587 e1-5.
8. Margulies RU, Hsu Y, Kearney R, Stein T, Umek WH, DeLancey JO. Appearance of the levator ani muscle subdivisions in magnetic resonance images. Obstetrics and gynecology. 2006;107(5):1064-9.
9. Umek WH, Morgan DM, Ashton-Miller JA, DeLancey JO. Quantitative analysis of uterosacral ligament origin and insertion points by magnetic resonance imaging. Obstetrics and gynecology. 2004;103(3):447-51.
10. Thomas V, Shek KL, Guzman Rojas R, Dietz HP. Temporal latency between pelvic floor trauma and presentation for prolapse surgery: a retrospective observational study. International urogynecology journal. 2015;26(8):1185-9.
11. Tunn R, Goldammer K, Neymeyer J, Gauruder-Burmester A, Hamm B, Beyersdorff D. MRI morphology of the levator ani muscle, endopelvic fascia, and urethra in women with stress urinary incontinence. European journal of obstetrics, gynecology, and reproductive biology. 2006;126(2):239-45.
12. DeLancey JO, Morgan DM, Fenner DE, Kearney R, Guire K, Miller JM, et al. Comparison of levator ani muscle defects and function in women with and without pelvic organ prolapse. Obstetrics and gynecology. 2007;109(2 Pt 1):295-302.
13. Tunn R, Delancey JO, Howard D, Ashton-Miller JA, Quint LE. Anatomic variations in the levator ani muscle, endopelvic fascia, and urethra in nulliparas evaluated by magnetic resonance imaging. American journal of obstetrics and gynecology. 2003;188(1):116-21.
14. Khan KS, Tryposkiadis K, Tirlapur SA, Middleton LJ, Sutton AJ, Priest L, et al. MRI versus laparoscopy to diagnose the main causes of chronic pelvic pain in women: a test-accuracy study and economic evaluation. Health Technol Assess. 2018;22(40):1-92.
15. Mahoney C, Hindle A, Rajashanker B, Kearney R. MR scan evaluation of pelvic organ prolapse mesh complications and agreement with intra-operative findings. International urogynecology journal. 2019.
info@gynäkologie
- Vol. 10
- Ausgabe 3
- Juni 2020