- Kongressausgabe der info@onkologie
 Hier finden Sie das PDF der Kongresszeitung
Hier finden Sie das PDF der Kongresszeitung
EDITORIAL
ASCO 2020: Zukunftsweisende virtuelle Konferenz oder «Geisterspiel»?
Der «ASCO Chicago 2020» trotzte der Corona Pandemie mit einer hervorragend geplanten und durchgeführten virtuellen globalen Konferenz: Der Wissenstransfer hat prima geklappt, die Präsentationen – auch von zuhause aus – waren von hoher Qualität und es könnte durchaus der Anfang einer neuen Form von solchen globalen Riesenkongressen werden. Auch die Zeitverschiebung war problemlos und hat es allen erlaubt, die Konferenz in ihrer Zeitzone tageskonform zu erleben.
Das «ASCO in the Mountains», vielmehr diesmal «in the clouds», der SAKK hat etwas davon vorweggenommen, auch wenn es hier bereits um eine Selektion und Einordnung der wichtigsten Studienergebnisse geht und nicht primär nur um eine Abbildung des ASCO per se.

Allein schon die Einsparung an Zeit, an Flug-, Reise und Hotel-Kosten und die viel geringeren Abwesenheiten zuhause in den Praxen und in den Spitälern ist gewaltig. Ebenso die CO2-Einsparungen sind gross. Auch konnte die Gefahr von einem internationalen «Corona-Spreading» zweifellos vermindert werden.
Man kann sich somit fragen: Warum haben wir dies nicht schon früher so gemacht? Es geht doch in erster Linie ums neue Wissen für unsere Patienten und nicht primär um ein Reiseerlebnis und Marketingevent.
Vermisst haben wir jedoch das persönliche Treffen mit Kollegen, mit alten Weggefährten von hüben und drüben, die direkte Diskussion mit ihnen über die neuen Daten und ihre Relevanz für uns in der Schweiz und zusätzlich das USA-Feeling und Chicago als architektonisch spektakuläre Grossstadt mit vielfältigster Kultur geniessen zu können.
Wir freuen uns trotz der durch die Covid-19 verursachten Kollateralschäden, die uns vermutlich noch länger beschäftigen werden, in unserer alljährlichen Kongresszeitung der info@onkologie auch dieses Jahr über die wichtigsten Studien und deren interessante Ergebnisse zu berichten. Es gab deren viele und viele Patienten werden davon profitieren können!
Pädiatrische Onkologie
Kinder mit refraktären Malignomen profitieren von personalisierter Medizin
Bei pädiatrischen Hochrisiko-Malignomen, welche nicht primär kurativ behandelt werden konnten, ist die Prognose mit einem medianen OS von 9.5 Monaten und einer sekundären Heilungschance von weniger als 20% schlecht. Viele dieser Tumore weisen aber onkogene Mutationen und Fusionen wie zB NTRK1/2/3, ROS1und ALK auf, dies besonders bei hochgradigen Gliomen, infantilen Fibrosarkomen und inflammatorischen myelofibroblastischen Tumoren.
Entrectinib ist ein oraler TRK/ROS1/ALK-Tyrosinkinaseinhibitor, der auch im ZNS wirksam ist und in der Dosis von 550mg/Tag in einer Studie mit bisher 34 Kindern (median 7 Jahre alt , 4,9 M – 20 J) untersucht wurde.
Die Ansprechsrate der Patienten mit Fusions-positiver Erkrankung wurde durch ein verblindetes unabhängiges zentrales Review-Kommittee ermittelt :
Die OR (vollständiges+partielles Ansprechen insgesamt) betrug 86% bei Fusions-positiver Erkrankung vs 5% bei Fusions-negativer Erkrankung. Das PFS war 17,5 Monate bei Fusions-positiver Erkrankung vs.1,9 Monate bei Fusions-negativer Erkrankung. Die am häufigsten dokumentierten unerwünschten Wirkungen waren Gewichtszunahme (n = 14), erhöhtes Kreatinin (n = 13), Anämie (n = 13), Übelkeit (n = 11), erhöhte Alanin-Aminotransferase (n = 10), erhöhte Aspartat-Aminotransferase (n = 10), reduzierte Neutrophilenzahl (n = 9) und Knochenfrakturen (n = 7, von denen 4 behandlungsbedingt waren). 8,8% der Patienten brachen die Behandlung wegen unerwünschter Ereignisse ab, und 32,4% hatten aus dem gleichen Grund eine Dosisreduktion. Die Nutzen-Risiko Bewertung bei noch kleiner Fallzahl war besonders eindrücklich für Patienten mit hochgradigen Gliomen.
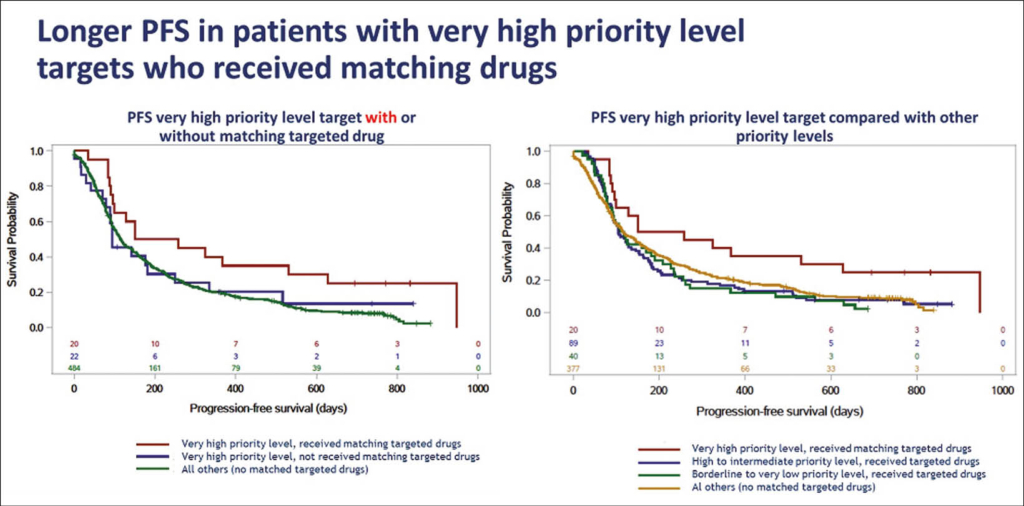
In einer weiteren Studie («Inform Study») basierend auf Daten aus dem INFORM (Individualized Therapy For Relapsed Malignancies in Childhood) Register, einer europäisch multinationalen, pädiatrisch-onkologischen Plattform mit Schweizer Beteiligung, konnte gezeigt werden, dass eine Stratifizierung der Patienten zu einer zielgerichteten Off-Label-Therapie auf Basis molekularer Signaturen (DNA- und RNA-Analysen) in der Praxis machbar ist und eine rationale Basis für Therapieverbesserungen auch bei seltenen Malignomen darstellt. Erhalten nun diese Kinder, bei denen molekulare Signaturen für bekannte zugelassene zielgerichtete Therapien identifiziert wurden, rasch die entsprechende Therapie, so haben sie ein deutlich längeres progressionsfreies Überleben als alle übrigen Patienten. Es wurden 526 pädiatrischen Patienten dokumentiert, von denen 149 eine zielgerichtete Therapie erhielten. Bei 377 Patienten fand sich keine solche molekulare Signatur. Bei 20 dieser 149 behandelten Patienten wurde eine Zielstruktur mit der Priorität «sehr hoch» (13,4 %) identifiziert. Diese Patienten überlebten median 204,5 Tage ohne Progress, alle übrigen Patienten überlebten median 114 Tage ohne Progression (p = 0,0093).
Die ASCO hat diese repräsentative Analyse der INFORM-Plattform für ein Late Breaking Abstract (LBA10503) ausgewählt: das INFORM-Konsortium repräsentiert 72 pädiatrisch-onkologische Zentren aus 8 europäischen Ländern. Targets mit hoher Priorität waren ALK-, BRAF- und NRAS-Mutationen sowie MET- und NTRK-Fusionen. Die Kinder hatten zB eine Hoch-Risiko (HR) akute lymphatische Leukämie (ALL), ein ALL-Rezidiv nach Stammzelltransplantation, ein frühes Rezidiv einer akuten myeloischen Leukämie (AML), Hoch-Risiko-ZNS-Tumore, rhabdoide Tumoren, Ependymome, Medulloblastome, Ewing-Sarkome oder Hepatoblastom. Ausserdem wurden durch die umfangreichen Genomanalysen bei einem Teil der Kinder (7,6 %) genetische Prädispositionen für Malignome entdeckt, die zuvor unbekannt waren. Diese bilden die Basis für genetische Beratungen betroffener Familien. Es wird erwartet, dass diese Datenbasis und der weitere Einschluss von zukünftigen Kindern in eine solche «Umbrella-Type-Study» einen «practice changing» Effekt haben wird und den Zugang pädiatrischer Patienten zur personalisierten Medizin erleichtern wird.
Abstract 107: Desaj AV et al. Updated entrectinib data in children and adolescents with recurrent or refractory solid tumors, including primary CNS tumors.
ThC
Quelle: van Tilburg CM et al. The pediatric precision oncology study INFORM: clinical outcome and benefit for molecular Subgroups. ASCO virtual Scientific Meeting 2020, Abstract LBA 10503 (Inform study)
Ältere Patienten > 70J mit RAS-BRAF-wt mCRC profitieren von FOLFOX-Panitumumab
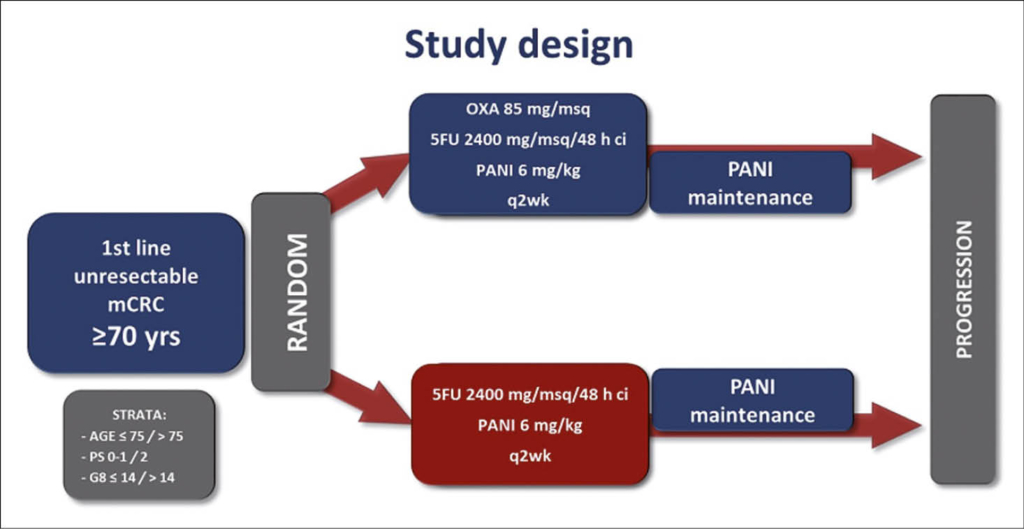
Patienten ≥70 Jahre mit nicht resezierbarem und zuvor unbehandeltem RAS-BRAF-wt mCRC wurden in dieser multizentrischen, randomisierten Phase 2-Studie (PANDA-Studie) eingeschlossen. Sie wurden 1:1 randomisiert in FOLFOX-Panitumumab (Gruppe A, n=92) oder 5FU/LV-Panitumumab (Gruppe B, n=93) für bis zu 12 Zyklen, gefolgt von einer Panitumumab-Erhaltungstherapie bis zur Progression, zugeteilt. Der primäre Endpunkt war das progressionsfreie Überleben (PFS) und sekundäre Endpunkte waren die Ansprechrate (ORR) und das Sicherheitsprofil. Zwischen den Gruppen war kein direkter Vergleich geplant.
Der primäre Endpunkt nach einem medianen Follow-up von 20.5 Monaten wurde in beiden Gruppen erreicht: das mediane PFS betrug 9,6 Monate in Gruppe A und 9,1 Monate in Gruppe B. Die ORR (Gruppe A: 65%, Gruppe B: 57%) und Krankheitskontrollrate (Gruppe A: 88%, Gruppe B: 86%) waren in beiden Gruppen ähnlich.
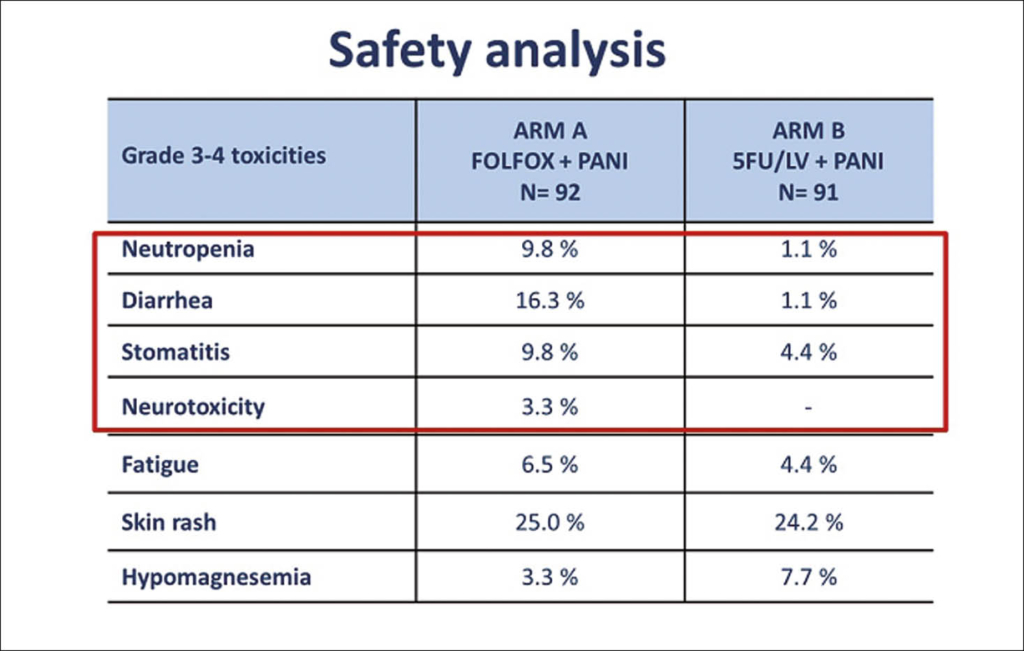
Unter Monotherapie ohne Oxaliplatin wurden weniger Nebenwirkungen beobachtet. Die Kombínation aus 5-Fluorouracil und Leucovorin (5FU/LV)-Monochemotherapie plus Pantumumab ist somit eine attraktive wenig toxische palliative Therapie Option bei älteren Patienten mit RAS-BRAF-wt mCRC. Nun werden Phase 3 Studien folgen müssen, um diese Daten für > 70 jährige Patienten mit dieser molekularen Signatur zu bestätigen.
ThC
Quelle: Lonardi S et al. First-line FOLFOX plus panitumumab versus 5FU plus panitumumab in RAS-BRAF wild-type metastatic colorectal cancer elderly patients: The PANDA study. ASCO 2020, Abstract #4002
PROSPER-Studie
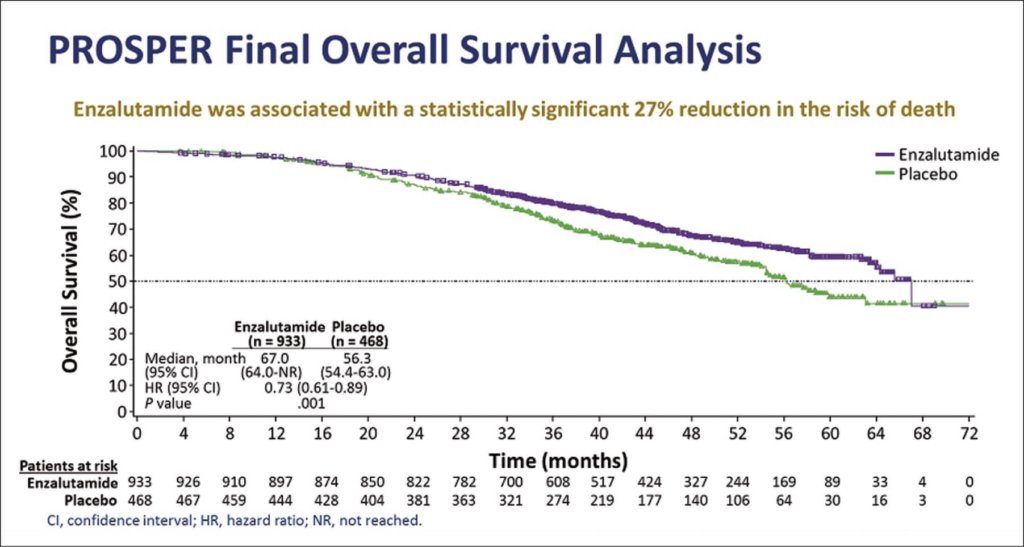
Enzalutamid verbessert auch das Gesamtüberleben
Im Rahmen der PROSPER-Studie konnte bei Patienten mit einem nichtmetastasierten, kastrationsresistenten Prostatakarzinom durch die Gabe von Enzalutamid (Xtandi™) zusätzlich zu einer Androgendeprivationstherapie das PFS signifikant verbessert werden. Neue Daten zeigen, dass dies auch zu einer Verbesserung des Gesamtüberlebens führt.
Es handelt sich dabei um eine multinationale, 2:1 randomisierte, doppelblinde, placebokontrollierte Phase-III-Studie, in die 1.401 Männer mit einem nichtmetastasierten kastrationsresistenten Prostatakarzinom, d. h. einer PSA-Verdopplungszeit von ≤ 10 Monate aufgenommen wurden. Primärer Endpunkt war das metastasenfreie Überleben, genauer gesagt die Zeit von der Randomisierung bis zu einem radiologisch nachweisbaren Krankheitsprogress oder Tod. Diese Zeit wurde durch Enzalutamid um 71% verlängert (36,6 Monate vs. 14,7 Monate; HR = 0,29).
Jetzt wurden erstmals Daten zum OS publiziert. Bei einem medianen Follow up von 48 Monaten traten insgesamt 466 Todesfälle auf, davon 288 (30,9%) in der Enzalutamid-Gruppe und 178 (38%) in der Placebo-Gruppe. Somit wurde durch Enzalutamid das OS signifikant um 27% vebessert. Das mediane OS betrug unter Enzalutamid 67,0 Monate vs. 56,3 Monate unter Placebo. Eine nachfolgende Therapie benötigten unter Enzalutamid 33%, unter Placebo 65%.Die mediane Dauer der Enzalutamid-Therapie lag bei 33,9 Monate, bei Placebo waren es nur 14,2 Monate.
Das Sicherheitsprofil von Enzalutamid entsprach dem aus früheren Studien bekannten. Grad ≥ 3- Nebenwirkungen traten unter Enzalutamid bei 48%, unter Placebo bei 27% der Patienten auf. Am häufigsten waren Stürze, Fatigue und Hypertonie. «Die Ergebnisse sprechen dafür, dass eine frühe Behandlung mit Enzalutamid für Männer von Vorteil ist, deren PSA-Wert nach einer Salvage-Behandlung und anschliessender Androgendeprivationstherapie weiter ansteigt», so Professorin Cora N. Sternberg, New York).
PS
Quelle: ASCO 2020, Abstract #5515
Metastasiertes hormonsensitives Prostatakarzinom
Enzalutamid verbessert das rPFS unabhängig vom Metastasenverteilungsmuster
Im Rahmen der ARCHES-Studie konnte gezeigt werden, dass Enzalutamid das radiografische progressionsfreie Überleben bei Männern mit einem metastasierten, aber noch hormonsensitiven Prostatakarzinom signifikant verbessert. Neue Daten zeigen, dass dieser Benefit unabhängig von der Lokalisation der Metastasen besteht.
Es handelt sich um eine randomisierte doppelblinde, placebokontrollierte Phase-III-Studie, welche die Wirksamkeit und Sicherheit von Enzalutamid (XtandiTM) plus Androgendeprivationstherapie (ADT) bei 1.150 Patienten mit einem metastasierten hormonsensitiven Prostatakarzinom (mHSPC) im Vergleich zur alleinigen ADT untersuchte. Der primäre Endpunkt war das radiografische progressionsfreie Überleben (rPFS). Enzalutamid plus ADT reduzierte das Risiko für rPFS oder Tod um 61% (HR = 0,39; p < 0,0001) im Vergleich mit ADT allein. Die mediane Zeit für ein rPFS-Ereignis war im Verum-Arm noch nicht erreicht und lag im Kontroll-Arm bei 19,4 Monaten.
Signifikante Verbesserungen fanden sich in allen Subgruppen (Erkrankungsmuster zu Studienbeginn, Lokalisation der Metastasen, vorherige Docetaxel-Therapie). So profitierten alle Patienten unabhängig davon, welches Metastasenmuster vorlag: Knochenmetastasen und/oder Weichteilmetastasen und/oder viszerale Metastasen. Bei Patienten ohne viszeraler Metastasierung war der Benefit etwas ausgeprägter Auch das Risiko für einen PSA-Anstieg war ebenso vermindert wie die Notwendigkeit für eine neue antineoplastische Therapie.
PS
Quelle: ASCO 2020, Abstract #5547
Ex-Raucher mit Lungenkrebs haben eine bessere Prognose: Je früher desto besser
Patienten mit Lungenkrebs und häufig auch ihre Ärzte vertreten die Meinung, dass Patienten mit Lungenkrebs von einem Rauchstopp nicht profitieren. Gerade auch im Hinblick auf ein Lungenkrebsscreening ist es relevant gute Argumente zu haben, um begleitend zum Lungenkrebs Screening Raucher möglichst früh zum Rauchstopp zu motivieren. Diese Daten liefern gute Hinweise, dass ein Rauchstopp sich immer lohnt, ganz abgesehen davon, dass auch die verminderte Lungenfunktion und die kardiovaskulären Belastungen sich zurückbilden.
Ein internationales Lungenkrebs Konsortium (ILCCO) auf drei Kontinenten hat aus 17 Studien im Zeitraum 1994-2017 insgesamt 35 428 Patienten mit Lungenkrebs bezüglich ihrer Raucheranamnese und Prognose untersucht. Davon waren je 41% zum Zeitpunkt der Diagnose Raucher und Exraucher und 18% waren Nichtraucher. Das mediane Alter betrug 66 Jahre (20-93), 52% waren Männer, 78% Kaukasier, 58% hatten ein Adenokarzinom, 55% hatten ein Stadium 3 oder 4.
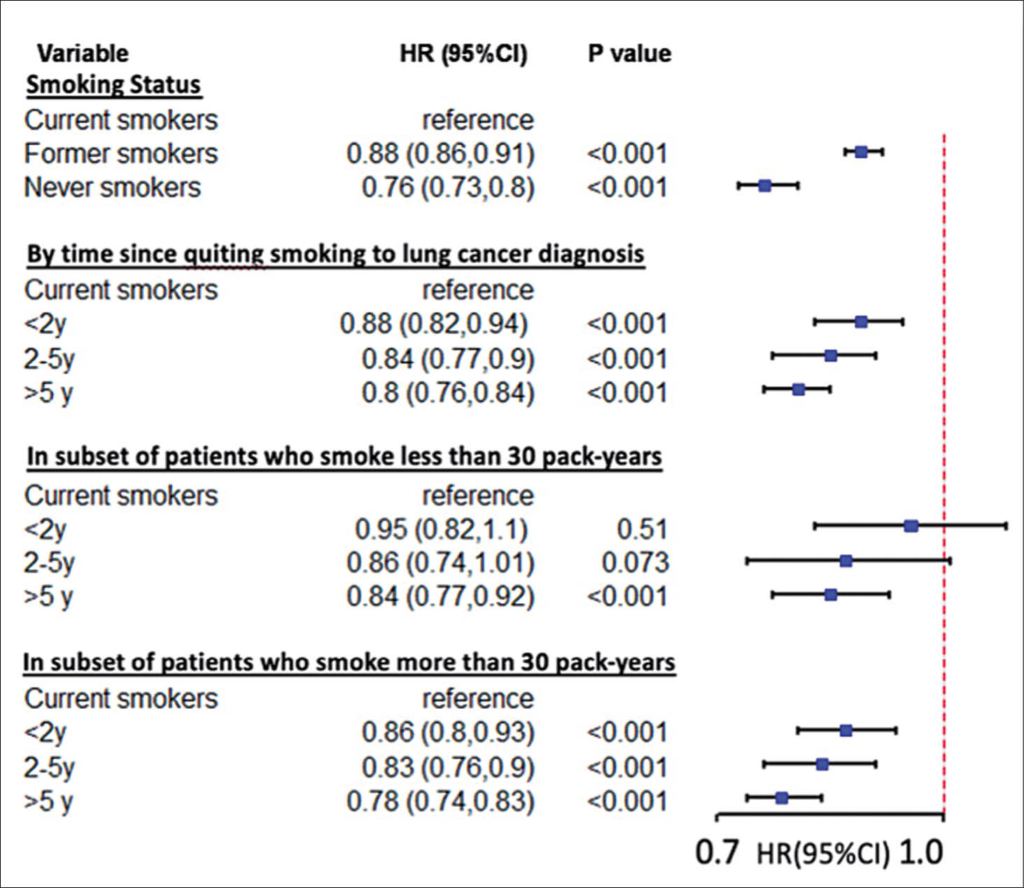
Auch Patienten mit Lungenkrebs, die sogar weniger als 2 Jahre vor ihrer Diagnose das Rauchen beendet hatten, hatten ein signifikant besseres OS als aktuelle Raucher. Die Ergebnisse waren unabhängig von «pack years», Alter, Krankheitsstadium und weiteren Variablen. Bei Raucherstopp < 2 Jahre vor Diagnose war das OS +12%, Rauchstopp vor 2-5 Jahren +20% OS verbessert. Das Lungenkrebs spezifische Überleben per se war erst bei einem Raucherstopp von >5 Jahren signifikant reduziert. Insgesamt waren bei Patienten mit >30 PY (Pack Years) die Resultate am eindrücklichsten. Diese Daten legen auch den Schluss nahe, dass die Gesamtmortalität der Raucher auch wesentlich durch andere Ursachen verursacht wird als Lungenkrebs.
ThC
Quelle: Fares AF et al. Smoking cessation (SC) and lung cancer (LC) outcomes: A survival benefit for recent-quitters? A pooled analysis of 34 649 International Lung Cancer Consortium (ILCCO) patients. ASCO 2020, Abstract #1512
Hohes Ansprechen von Prembrolizumab beim Missmatch repair defizienten Kolorektalen Karzinom
Nur etwa 5% der mCRC-Patienten haben eine Mikrosatelliteninstabilität und eine Mismatch-Repair-Defizienz (MSI-H/dMMR). In dieser internationalen randomisierten Phase 3 Studie wurden 307 Patienten mit MSI-H/dMMR mCRC, die einen guten Performance Status aufwiesen, randomisiert zu einer Behandlung mit bis zu 35 Zyklen Pembrolizumab (200 mg alle 3 Wochen), oder einer Chemotherapie nach Wahl des behandelnden Arztes (z.B. modifiziertes FOLFOX mit oder ohne Bevacizumab oder Cetuximab oder FOLFIRI mit oder ohne Bevacizumab oder Cetuximab (KENOTE-177).
Die Pembrolizumab-Gruppe zeigte gegenüber der Chemotherapie-Gruppe ein längeres medianes PFS (16,5 Monate vs. 8,2 Monate; HR 0,60; P=0,0002) und höhere PFS-Raten über 12 Monate (55% vs. 37%) und 24 Monate (48% vs. 19%). Zudem hatte die Pembrolizumab-Gruppe auch eine höhere RR (43,8%; davon 11,1% komplett und 32,7% partiell) als die Chemotherapie-Gruppe (33,1%; davon 3,9% komplett und 29,2% partiell). Allerdings war die Rate stabiler Erkrankungen niedriger in der Pembrolizumab-Gruppe (20,9% vs. 42,2%) und 29,4% der Pembrolizumab-Gruppe hatte eine progressive Erkrankung verglichen mit 12,3% der Chemotherapie-Gruppe. Nach 2 Jahren lag die anhaltende Responserate bei hohen 83% in der Pembrolizumab-Gruppe vs. 35% in der Chemotherapie-Gruppe.
Unerwünschte behandlungsbedingte Ereignisse in der Pembrolizumab-Gruppe versus der Chemotherapie-Gruppe waren: ≥ Grad 3: 22% zu 66% (Kontrollgruppe) , immunologische unerwünschte Ereignisse und Infusionsreaktionen: 31% zu 13% (Kontrollgruppe). Für die OS Analyse ist es noch zu früh. 36% der Patienten aus dem Kontrollarm bekamen sekundär Pembrolizumab (cross-over). Die Verbesserung des PFS um ca. das Doppelte ist grösser als bei jeder der bisherigen mCRC-Therapien beobachteten Verbesserung und dürfte damit einen neuen Standard darstellen für Patienten, welche fit für eine Pembrolizumab Therapie sind.
ThC
Quelle: Andre T et al. Pembrolizumab versus chemotherapy for microsatellite instability-high/mismatch repair deficient metastatic colorectal cancer: The phase 3 KENOTE-177 study. ASCO 2020, Abstract #LBA4.
Muskel-invasives Blasenkarzinom
Adjuvante Gabe von Atezolizumab verbessert nicht das DFS
Der bisherige Standard beim Muskel-invasiven Blasenkarzinom ist die neoadjuvante Cisplatin-basierte Chemotherapie gefolgt von der radikalen Zystektomie. Doch die 5-Jahresrezidivrate bei diesem Vorgehen liegt bei 50-60%. Somit stellt sich die Frage, ob durch eine adjuvante Immuntherapie die Rezidivrate gesenkt werden kann.
Im Rahmen der IMvigor 010-Studie wurde die zusätzliche postoperative adjuvante Gabe des PD-L1-Inhibitors Atezolizumab untersucht, nachdem sich diese Substanz bereits bei Patienten im metastasierten Stadium des Blasenkarzinoms bewährt hat.
Aufgenommen in diese Studie wurden insgesamt 809 Patienten mit einem Muskel-invasiven Blasenkarzinom. Sie erhielten nach der neoadjuvanten Chemotherapie und anschliessender Zystektomie entweder adjuvant Atezolizumab in einer Dosierung von 1200 mg alle 3 Wochen, insgesamt also 16 Zyklen über ein Jahr, oder sie wurden nur nachverfolgt ohne adjuvante Medikation.
Die Auswertung nach einem Jahr ergab beim DFS keinen signifikanten Unterschied zwischen den beiden Strategien. Unter Atezolizumab traten bei 52% Tumor-bedingte Ereignisse auf, ebenso viele wie bei den nur unter Beobachtung stehenden Patienten. Beim medianen DFS standen 19,4 Monate unter Atezo 16,6 Monate bei ausschliesslicher Beobachtung gegenüber, der Unterschied war nicht signifikant. Die DFS-Rate nach 18 Monaten lag unter Atezo bei 56% vs. 54% bei Beobachtung. Bei PD-L1-positiven Patienten war das DFS insgesamt günstiger und zwar unabhängig davon, ob eine adjuvante Therapie durchgeführt wurde oder nicht. Auch weitere Subgruppenanalysen ergaben keinen Benefit für die adjuvante Therapie.
Was die Sicherheit betrifft, so gab es keine neuen Gesichtspunkte. 16% entwickelten in der Atezo-Gruppe eine Therapie-induzierte Nebenwirkung Grad 3-4. Die dermatologische und gastrointestinale Toxizität waren die häufigsten Ursachen für eine Unterbrechung der Therapie.
PS
Quelle: ASCO 2020, Abstract #5000
Fortgeschrittenes hepatozelluläres Karzinom
Cabozantinib ist auch in der real world wirksam und sicher
Nachdem der Multikinase-Inhibitor Cabozantinib (Cabometyx®) bereits beim metastasierten Nierenzellkarzinom und fortgeschrittenen Leberzellkarzinom (HCC) in randomisierten klinischen Studien seine gute Wirksamkeit und Sicherheit unter Beweis stellen konnte, gibt es neue überzeugende Daten einer Kohortenstudie, die eine gute Wirksamkeit und Sicherheit dieser Substanz beim fortgeschrittenen hepatozellulären Karzinom auch in der real world bestätigen.
Offiziell zugelassen ist Cabozantinib beim fortgeschrittenen HCC als second line-Therapie nach einer Vortherapie mit Sorafenib, nachdem die Substanz in einer randomisierten Studie (CELESTIAL-Studie) überzeugen konnte. Doch lässt sich dies auch auf den praktischen Alltag, also die real world, übertragen?
Um diese Frage beantworten zu können, wurde eine retrospektive internationale Kohortenstudie durchgeführt. Ausgewertet wurden die Daten von 74 Patienten mit einem fortgeschrittenen HCC, die in der second oder third line nach Sorafenib mit Cabozantinib behandelt wurden. Die häufigsten Ursachen des HCC waren Hepatitis C und B, alkoholische Leberzirrhose und nicht-alkoholische Fettleber.
Bei 5% konnte mit Cabozantinib eine partielle Remission und bei 30% eine Stabilisierung erreicht werden. Bei 32% kam es zu einer Progression und der Rest konnte nicht ausgewertet werden. Die durchschnittliche Dauer der Cabozantinib-Therapie betrug 4,4 Monate. 47% der Patienten waren bis zum Tage der Auswertung verstorben. Das mediane OS betrug 7,7 Monate. Die häufigsten Nebenwirkungen waren Fatigue und Diarrhöen. Zusammenfassend bestätigen diese Daten die Ergebnisse der Phase-III-Zulassungsstudie CELESTIAL.
PS
Quelle: ASCO 2020, Abstract #e16668
Kurz und knapp
«Borderline-resectable» Pankreaskarzinom
Abstract 9004:
Second line Mesotheliom: in der italienischen randomisierten «Rames» Phase 2 Studie (n: 164) ist die Kombination Ramucirumab/Gemcitabine der Gemcitabine Monotherapie überlegen mit einem medianen OS von 13.8 versus 7.5 Monate (HR 0.7) und nach einem Jahr waren 56.5% versus 33.9%, der Patienten am Leben.
Abstract 4505: Beim neudiagnostizierten «borderline-resectable» Pankreaskarzinom ist in dieser europäischen randomisierten ESPAC-5F Studie (n: 90) in der 1.Linien Therapie das neoadjuvante Vorgehen (2xGEMCAP oder 4xFOLFIRINOX oder 54Gy mit Capecitabine Chemoradiotherapy (CRT)) gegenüber der sofortigen Operation klar überlegen mit einem 1 Jahres OS von 77% [95%CI, 66% – 89%] für die neoadjuvante Therapie und 40% [95% CI, 26% – 62%] für sofortige Operation gefolgt von adjuvanter Therapie (HR=0.27 [95% CI, 0.13 – 0.55]).
Abstract LBA6008: In dieser französischen kleinen Phase 2 TROPHIMMUN Studie wurde Avelumab (median 8x 10 mg/kg Q2W) bei der sehr seltenen Gruppe der 15 chemoresistenten (nach Methotrexat und in einem Fall auch Actinomycin) Patientinnen mit einem gestationsbedingten Trophoblastentumor (dieser exprimierte PD-L1 in allen Fällen) eingesetzt und die Hälfte dieser Patienten konnte dadurch schliesslich geheilt werden.
Abstract 4004: Im IDEA Trial (n:12,835 Patienten aus 6 grossen Phase 3 Studien) konnte gezeigt werden, dass 3x versus 6x adjuvante Oxaliplatin/Fluoropyrimidine-basierte Therapie für die grosse Mehrheit der Patienten mit operiertem Stadium III Kolonkarzinom mit 5 Jahres OS und DFS mit viel weniger Toxizität und Kosten als ebenbürtig betrachtet werden kann.
Abstract 5001: Der neue orale GnRG-Rezptor Antagonist Relugolix (n:622) wurde in dieser grossen Phase 3 HERO Studie bei 930 Patienten mit fortgeschrittenem Prostatakarzinom mit Leuprolide (n:308) verglichen und zeigte eine Überlegenheit: bei 96,7 Prozent der mit Relugolix bzw. 88,8 Prozent der mit Leuprolid behandelten Männer wurde die Kastrationswerte über 48 Wochen aufrechterhalten und die Häufigkeit relevanter unerwünschter kardiovaskulärer Ereignisse war 2,9% in der Relugolix-Gruppe und 6,2% in der Leuprolid-Gruppe (Hazard Ratio 0,46; 95% CI, 0,24 bis 0,88).
ThC
Cabozantinib in Kombination mit dualer Immuntherapie
COSMIC-313: Neue Studie beim fortgeschrittenen Nierenzellkarzinom
Beim fortgeschrittenen Nierenzellkarzinom sind sowohl Multikinase-Inhibitoren wie Cabozantinib (Carbometyx®) als auch Checkpoint-Inhibitoren wie Nivolumab und Ipilimumab wirksam. Experimentelle Daten sprechen dafür, dass die Kombination beider Wirkprinzipien noch wirksamer sein könnte.
Im Rahmen einer Phase-III-Studie (COSMIC-313-Studie) wird deshalb jetzt die Kombination beider Wirkprinzipien im Rahmen der first line-Therapie untersucht und zwar bei Patienten mit einem niedrigen oder intermediären Risiko.
Verglichen wird in einem randomisierten Design die Triple-Therapie mit Cabozantinib + Nivo + Ipi mit einer alleinigen kombinierten Immuntherapie mit Nivo + Ipi und auch die kombinierte Immuntherapie Nivo + Ipi mit einer Mono-Immunmonotherapie nämlich Nivo. Endpunkte der Studie sind Wirksamkeit (PFS) und Sicherheit. Das Follow up beträgt 1 Jahr. Die ersten Patienten für diese Studie wurden im Juni 2019 rekrutiert.
PS
Quelle: ASCO 2020, Abstract #TPS5102
Fortgeschrittenes NSCLC
Immunkombinationstherapie ist alleiniger Chemotherapie überlegen
In der CheckMate-9LA-Studie wurde in der First line die Kombination Chemotherapie plus duale Immuntherapie mit Nivolumab (nivo) + Ipilimumab (ipi) mit einer alleinigen Chemotherapie verglichen. Dabei zeigte sich in einer Interimsanalyse ein signifikanter OS-, PFS- und ORR-Vorteil für die Immunkombinationstherapie.
In der CheckMate-227-Studie wurde in der Erstlinientherapie bei einem fortgeschrittenen NSCLC ein OS-Vorteil bei der kombinierten Immuntherapie nivo + ipi unabhängig vom PD-L1-Status gegenüber der alleinigen Chemotherapie gezeigt. Die Hypothese, dass eine zeitlich begrenzte Chemotherapie zusätzlich zu dieser erfolgreichen Immunkombinationstherapie zu einer besseren und schnelleren Krankheitskontrolle führen könnte, wurde im Rahmen der CheckMate-9LA-Studie evaluiert.
Eingeschlossen in diese Studie wurden 719 therapienaive Patienten mit einem fortgeschrittenen metastasierten bzw. rezidivierten therapienaiven NSCLC. Eine Zwischenanalyse nach einer Mindestnachbeobachtungzeit von 12, 7 Monaten bestätigte diese Hypothese. Durch die Zugabe der Chemotherapie ( 2 Zyklen) zusätzlich zur kombinierten Immuntherapie verlängerte sich im Vergleich zur alleinigen Chemotherapie (4 Zyklen) das mediane Überleben von 10,9 Monate auf 15,6 Monate (HR = 0,66). Die Ein-Jahres-Überlebensrate stieg von 47% auf 63%. Das PFS nach einem Jahr konnte durch die Immunkombinationstherapie von 18% auf 33% angehoben werden. Das mediane PFS stieg von 5,0 auf 6,7 Monate (HR = 0.68). Auch die mediane Ansprechdauer (DOR) stieg von 5,6 auf 11,3 Monate und die Gesamtansprechrate von 25 auf 38%.
Insgesamt wurden bei 38% im Chemotherapie-Arm und bei 47% unter der Kombinationstherapie schwerwiegende therapieassoziierte unerwünschte Ereignisse dokumentiert (Schweregrad ≥ 3) dokumentiert. Dazu gehörten insbesondere Übelkeit, Anämie, Asthenie und Diarrhoe. Zusammenfassend lässt sich sagen: CheckMate-9LA hat bei der Interimsanalyse eine signifikante Überlegenheit für die Immunkombinationstherapie gezeigt und den primären Endpunkt nämlich eine Verbesserung des OS erreicht. «Die frühzeitige Trennung der beiden OS-Kurven und die niedrigen Krankheitsprogressionsdaten als beste Response haben die Hypothese dieses Studiendesigns validiert» so das Fazit des Studienautors Dr. Martin Reck, Grosshansdorf.
PS
Quelle: ASCO 2020, Abstract #9501
Fortgeschrittenes NSCLC
Auch nach drei Jahren deutliche Überlegenheit der kombinierten Immuntherapie
In der Check-Mate-227-Studie erwies sich bei Patienten mit einem fortgeschrittenen PD-L1-positiven NSCLC die kombinierte Immuntherapie Nivolumab (nivo) plus Ipilimumab (ipi) in der Erstlinientherapie einer Chemotherapie signifikant überlegen und gut verträglich. Jetzt wurden die 3-Jahresergebnisse vorgestellt.
Eingeschlossen in diese Phase-3-Studie wurden 1189 NSCLC-Patienten in einem fortgeschrittenen Stadium. Sie erhielten entweder die kombinierte Immuntherapie mit nivo + ipi oder nivo alleine oder eine Chemotherapie mit einer Platin-Douplette. 68% der Patienten waren PD-L1-positiv.
Die Auswertung nach einem medianen Follow up von 43,1 Monaten ergab ein medianes OS in der kombiniert therapierten Gruppe von 17,1 Monate im Vergleich zu nur 14.9 Monate unter der Chemotherapie (HR = 0.79). Das mediane OS bei Patienten mit einer PD-L1-Expresson von < 1% lag bei 17,2 Monate, bei PD-L1-Expression von > 1% bei 17,1 Monate. Nach 3 Jahren waren 18% der kombiniert behandelten Patienten mit einer PD-L1-Expression > 1% Progressions-frei, unter nivo allein waren es nur 12% und nur 4% unter der Chemotherapie. Schwere Nebenwirkungen (Grad 3 und 4) traten bei 36% der Patienten mit der kombinierten Immuntherapie und bei 36% der Patienten unter der Chemotherapie auf. Bei Patienten mit einer PD-L1-Expression war die Inzidenz schwerer Nebenwirkungen mit 20% niedriger als bei Patienten mit einer PD-L1-Expressin < 1%, bei denen die Rate an schwerwiegenden Komplikationen bei 56% lag. «Diese Daten zeigen, dass die Überlegenheit der kombinierten Immuntherapie unabhängig vom PD-L1-Status auch längerfristig und anhaltend besteht», so der Studienautor Suresh S Ramalingam, Atlanta.
PS
Quelle: ASCO 2020, Abstract #9500
Pembrolizumab bei Frauen mit unbehandeltem trippel negativem fortgeschrittenem Mammakarzinom (TNBC)
Pembrolizumab als Monotherapie ist aktiv bei Patientinnen mit TNBC. Diese randomisierte Phase 3 Studie KEYNOTE-355 untersuchte nun die Kombination mit gebräuchlichen Chemotherapien. Patientinnen mit einem de-novo TNBC, welche nach Diagnose mindestens 6 Monate krankheitsfrei waren, wurden 2:1 randomisiert: im Verumarm erhielten 566 Patientinnen Pembrolizuma (Pembro) + Chemo (Nab-paclitaxel; Paclitaxel; oder Gemcitabine/cCrboplatin) und im Kontrollarm 266 Patientinnen Placebo + Chemo, insgesamt bis zu 35 Pembro/Placebo Gaben bis zur Progression oder intolerablen Toxizität. Eine Stratifikation erfolgte nach der Art der Chemotherapie (Taxane vs Gemcitabine/Carboplatin), vorgängiger neoadjuvanter oder adjuvanter Therapie und PD-L1 Status (CPS ≥1 vs <1). Die beiden primären Endpunkte waren PFS und OS entsprechend gesondert für die beiden Gruppen PD-L1 Expression (CPS ≥10 und ≥1) und für alle Patientinnen. Nach einem medianen Beobachtungszeit von 17.5. Monaten für die Verum-Gruppe und 15.5. Monate für die Placebo-Gruppe war das mediane PFS für die Verum-Gruppe signifikant verbessert: für die Gruppe CPS ≥10 (Abb 1): auf 9.7 versus 5.6 Monate (HR: CI-95%, 0.65 (0.49-0.86)), für die Gruppe CPS >1 (Abb 2): 7.6 versus 5.6 Monate ( HR: 0.74 (0.61-0.90)) und für die ganze ITT Gruppe: 7.5 versus 5.6. Monate. Insgesamt spielt also der Expressionsgrad von PD-L1 eine wichtige Rolle für das Ausmass des Ansprechens.
Reife Daten für OS werden erst im deutlichen längeren Verlauf erwartet werden können. Grade 3-5 behandlungsassoziierte AE’s traten in 68.1% im Verum-Arm (2 Todesfälle) und in 66.9% im Placebo-Arm (0 Todesfälle) auf und die Rate an immunologischen AE’s Grade 3-4 war 5.5% versus 0%. Neue Sicherheitssignale traten nicht auf. Somit bestehen für die 15-20% der Patientinnen mit einem prognostisch weiterhin ungünstigen TNBC Hoffnung auf neue wirksamere Therapien.
ThC
Quelle: ASCO 2020, Abstract #1000
Clinical Trial Registry Number: NCT02819518 Citation: J Clin Oncol 38: 2020 (suppl; abstr 1000)
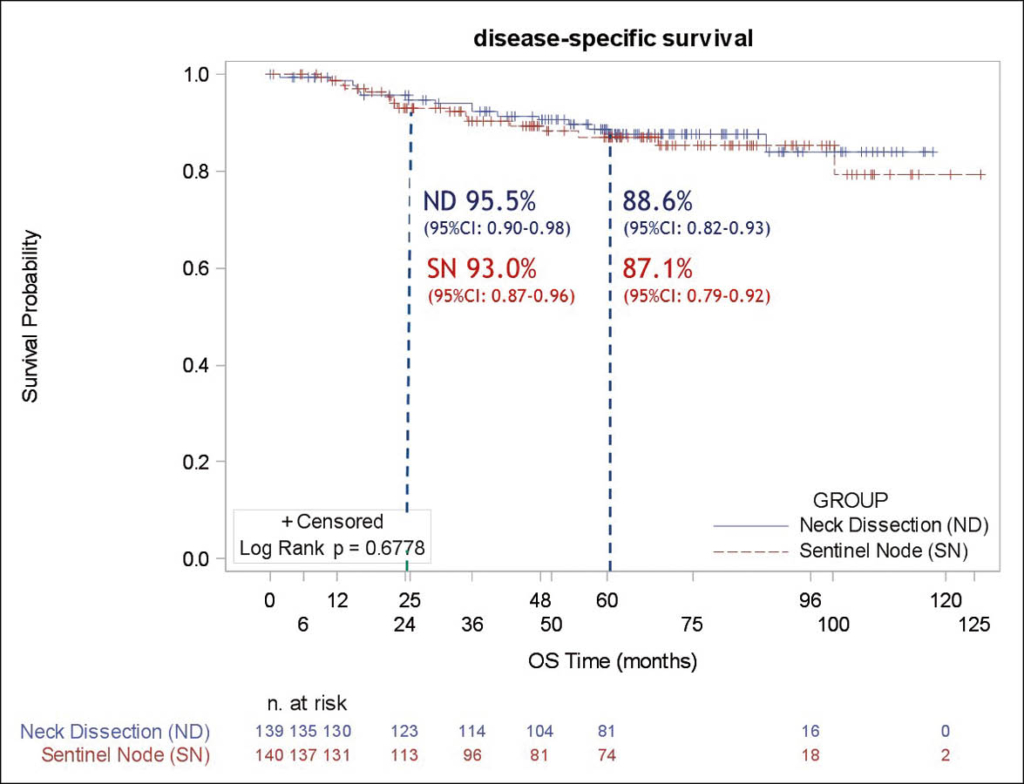
HNO-Karzinom T1-T2N0: Sentinel oder Neckdissektion?
Diese französische nationale Studie untersuchte die Frage ob bei operablen Patienten mit T1-T2N0 oralen oder oropharyngealen Plattenepithelkarzinomen eine weniger mutilierende Sentinel-Op (SN) basierte Therapie gegenüber einer Neckdissektion (ND) gleich wirksam ist. In der prospektiven randomisierte Multizenterstudie (inklusive einer ökonomischen Begleitstudie) wurden die neu diagnostizierten Patienten entweder in den ND-Kontrollarm oder SN-Verumarm (nur SN Biopsie wenn SN-negativ oder dann ND wenn bei SN-positiv) randomisiert. Der primäre Endpunkt war das rückfallfreie Überleben (RFS) nach 2 und 5 Jahren. Sekundär wurden funktionale Aspekte im HNO und Schulterbereich, Hospitalisationsdauer und Anzahl physiotherapeutischer Interventionen währen den ersten 24 Monaten untersucht. Es wurden an 10 Zentren insgesamt 307 Patienten eingeschlossen. Nach 2 Jahren und 5 Jahren waren 279 der 307 Patienten Rückfall frei: im ND-Arm traten 14 Rückfälle bei 139 Patienten auf und im SN-Arm 13 Rückfälle bei 140 Patienten auf. Eine OS Differenz (10%) bestand nicht und die Aequivalenz war hochsignifikant (p = 0.008) bestätigt.
Die Hospitalisationsdauer betrug 8 Tage im ND- und 7 Tage im SN-Arm. Bezüglich der funktionalen Aspekte war der ND-Arm nach 2, 4 und 6 Monaten schlechter als der SNArm und diese Differenz war nach 12 Monaten nicht mehr nachweisbar. Die Autoren schliessen daraus, dass ein Sentinel-basiertes Vorgehen gegenüber einer primären Neck-Dissektion heute das Vorgehen der Wahl darstellt.
ThC
Quelle: ASCO 2020, abstract #6501
Fortgeschrittenes Blasenkarzinom
Kosteneffektivität der kombinierten Immun-Chemotherapie
Im Rahmen der IMvigor130-Studie wurde bei Patienten mit einem metastasierten bzw. fortgeschrittenen muskelinvasiven Blasenkarzinom die alleinige Chemotherapie mit der Kombination platinbasierte Chemotherapie plus Immuntherapie (Atezolizumab) verglichen. Die Ergebnisse sprechen für die Kombination mit dem Checkpoint-Inhibitor. Doch ist die kombinierte Therapie auch Kosten-effektiv?
Aufgenommen in diese Studie wurden bisher unbehandelte Patienten mit einem fortgeschrittenen bzw. metastasierten Blasenkarzinom und zwar unabhängig davon, ob sie für eine Cisplatin-Chemotherapie geeignet waren oder nicht. Die PFS-Event-Rate lag unter der Kombination bei 74%, unter der alleinigen Chemotherapie bei 82%. Beim PFS standen 6,3 Monate unter der Chemotherapie 8,2 Monate unter der Kombination gegenüber (HR 0.82; p = 0,007). Bei der intention-to-treat-Interims-Analyse zeigte sich auch eine Verbesserung des OS, allerdings ohne statistische Signifikanz (HR 0,83; medianes OS 16,0 Monate vs. 13,4 Monate). Die Response-Rate betrug bei der Kombination 47,4% im Vergleich zu 43,8% bei der Chemotherapie. Eine komplette Remission erreichten 12,5% in der Kombi-Gruppe und 6,8% in der Chemotherapie-Gruppe Dies ist die erste Studie, die einen Vorteil der Immuntherapie in Kombination mit einer Chemotherapie bei Patienten mit einem fortgeschrittenen bzw. metastasierten Blasenkarzinom nachgewiesen hat.
Eine Analyse bzgl. Kosteneffektivität kommt zu dem Ergebnis, dass die kombinierte Therapie in der First line nicht kosteneffektiv ist, da für ein zusätzliches Lebensjahr ca. 630.000 $ aufgewendet werden müssen. Doch bei einem Preisrabatt von 33% wäre die Kosteneffektivität gegeben.
PS
Quelle: ASCO 2020, Abstract #5031
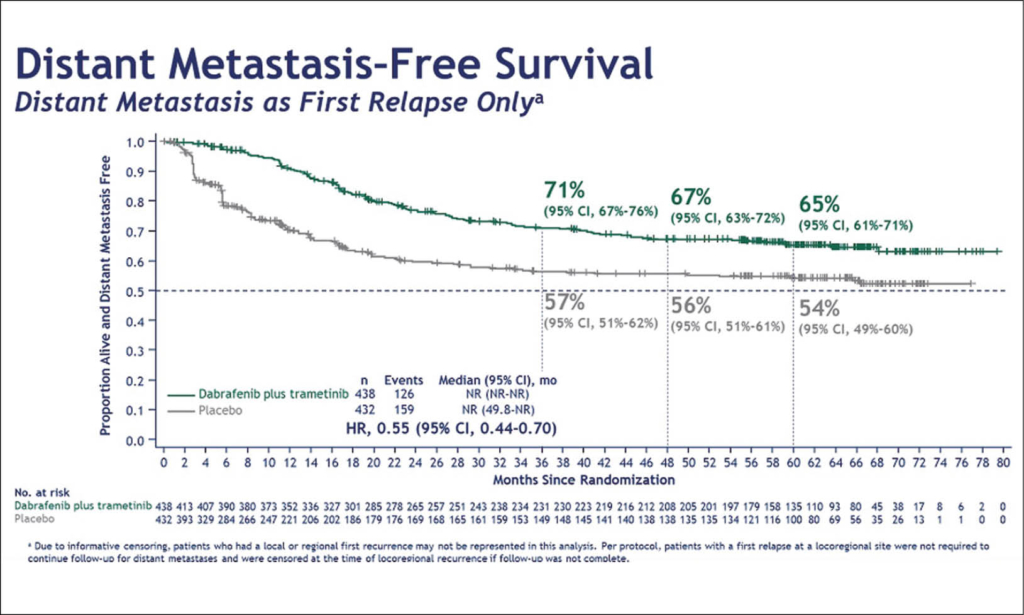
Reseziertes BRAF-mutiertes Melanom im Stadium III: Klarer Nutzen durch adjuvant Dabrafenib/Trametinib
Dieser bisher längste follow-up einer Phase 3 Adjuvanten Melanom Studie mit Dabrafenib (D) plus Trametinib (T) über 12 Monate bei Patienten mit BRAF-mutiertem Melanom im Stadium III schloss 870 Patienten mit komplett reseziertem V600E/K-mutiertem Melanom ein. Die Patienten wurden 1:1 randomisiert zu 12 Monaten D+T oder Placebo. Der Primäre Endpunkt war rezidivfreies Überleben (RFS) und sekundäre Endpunkte waren OS und fernmetastasenfreies Überleben (DMFS). Das kürzeste Follow-up der Studie betrug 60 Monate (D+T-Gruppe) und 59 Monate (Placebo-Kontrollgruppe) .
190/438 Patienten in der D+T-Gruppe und 262/432 Patienten in der Placebogruppe waren zu diesem Zeitpunkt rezidivfrei. Das mediane RFS wurde in der D+T-Gruppe noch nicht erreicht und betrug 16,6 Monate mit Placebo (HR 0,51; 95% KI 0,42-0,61). Die RFS-Raten nach 5 Jahren waren:
52% (95% KI 48%-58%) unter D+T und 36% (95% KI 32%-41%) unter Placebo. Die RFS-Kurven für beide Gruppen zeigen ein Plateau. Der RFS-Benefit unter D+T fand sich in allen Untergruppen des American Joint Committee on Cancer (AJCC) 7 und ebenso unter den Untergruppen IIIB, IIIC und IIID des AJCC 8. Das mittlere DMFS wurde in keinem Arm erreicht, war jedoch günstiger unter D+T (HR 0,55%; 95% KI 0,44-0,70). Das OS wurde nicht neu erhoben, da die vorbestimmte Anzahl an Ereignissen bisher noch nicht eingetreten ist. Diese Studie schloss auch Schweizer Patienten ein.
ThC
Quelle: Hauschild A et al. Long-term benefit of adjuvant dabrafenib + trametinib (D+T) in patients (pts) with resected stage III BRAF V600-mutant melanoma: Five-year analysis of COMBI-AD ASCO 2010, Abstract #10001.
Neue Daten zu Sicherheit und Verträglichkeit
NSCLC: Atezolizumab ist der Chemotherapie überlegen
Im Rahmen der IMpower 110-Studie wird der PD-L1-Inhibitor Atezolizumab (Tecentriq®) in der First line mit einer platinbasierten Chemotherapie bei Patienten mit einem fortgeschrittenen NSCLC verglichen. Dabei zeigte sich eine Überlegenheit der Immuntherapie. Dies gilt nicht nur für die Wirksamkeit resp. das OS, sondern auch im Hinblick auf Sicherheit und Verträglichkeit.
Ausgewertet wurden die Daten von 572 Patienten. Sie erhielten randomisiert Cisplatin/Carboplatin + Pemetrexed oder 1200 mg Atezolizumab (Tecentriq®) alle 3 Wochen. Der primäre Endpunkt ist das OS in der wild-type-Population (WT), also bei Patienten ohne ALK- oder EGFR-Mutation. Eine Auswertung nach 6 Monaten ergab eine Verbesserung des OS um 7,1 Monate (medianes OS unter Atezolizumab 20,2 Monate vs. 13,1 Monate unter der Chemotherapie (HR 0,595; p = 0,0106)) und zwar bei Patienten mit einer hohen PD-L1-Expression. Unter Atezolizumab betrug das OS nach 6 Monate 76,3% im Vergleich zu 64,9% unter der Chemotherapie. Bei den Ansprechraten standen 38,3% unter Atezolizumab 28,6% unter der Chemotherapie gegenüber Dieser überlegene Effekt des PD-L1-Inhibitors war auch bei Patienten mit einem mittleren PD-L1-Spiegel nachweisbar, aber ohne statistische Signifikanz (18,2 Monate vs. 14,9 Monate; HR 0,717; p = 0,0416). In dieser Gruppe lag das 12-Monatsüberleben unter Atezolizumab bei 60,7% im Vergleich zu nur 56% unter der Chemotherapie.
Verbesserung der Lebensqualität
Im Rahmen dieser Studie wurden auch die Patient Related Outcomes (PROs) mit ausgewertet. Sie waren ein präspezifizierter Endpunkt. PROs-Daten sind wichtig; denn sie geben einen Einblick in die Verträglichkeit bzw. Lebensqualität aus Patientensicht unter der Therapie. Zu Beginn der Studie waren die entsprechenden Scores für die Lebensqualität (QLQ-C30 und QLQ-LC13) in beiden Gruppen vergleichbar hoch (90% in der Atezo- vs. 86% in der Chemo-Gruppe). Unter der Therapie blieb der Score in beiden Gruppen meist über 80%. Auch bei der Zeit bis zur Verschlechterung der Lebensqualität zeigte sich kein signifikanter Unterschied. Dies gilt auch für die Verbesserung der Tumor-Symptome Husten, Dyspnoe und Thoraxschmerz. Die mediane Verbesserung in Bezug auf den Global Health Status (GHS) war aber bei Woche 42 unter Atezo etwas stärker als unter der Chemotherapie. Dieser günstige Effekt auf die Tumor-Symptome war am Anfang der Studie am stärksten und hielt dann an. Auch die Symptome Fatigue und Nausea verbesserten sich sehr rasch unter Atezo und dieser günstige Effekt hielt ebenfalls bis Woche 48 an.
Günstiges Sicherheitsprofil
Auch das Sicherheitsprofil von Atezo war günstiger als bei der Chemotherapie. Dies zeigt schon die Dauer der Therapie. Während die Patienten im Durchschnitt 5,3 Monate unter Atezo blieben, lag die Therapiedauer unter der Chemotherapie nur bei 3.5 Monate. Bei einem medianen Follow up von 13,7 Monaten waren bei der Interimsanalyse noch 31,6% unter Atezo, aber nur 8,7% unter der Chemotherapie. Auch was die Nebenwirkungen der Therapie betrifft, so sprechen die Daten für Atezo. Grad 3-4 Nebenwirkungen wurden in der Atezo-Gruppe bei 30,1%, in der Chemotherapie-Gruppe bei 52,5% der Patienten dokumentiert. Dabei stehen immunvermittelte Komplikationen bei Atezo im Vordergrund. Die Rate an immuninduzierten Nebenwirkungen lag unter Atezo bei 40,2%, unter der Chemotherapie bei 16,7%. Während unter Atezo 6,3% die Therapie wegen Nebenwirkungen unterbrechen mussten, war dies unter der Chemotherapie bei 16,3% der Fall. «Insgesamt entsprach das Sicherheitsprofil von Atezo dem von bisherigen Studien bekannten», so Prof. Jacek Jassem, Gdansk.
PS
Quelle: ASCO 2020, Abstract #9594 + Abstract #e21623
Olaparib beim seltenen BRCA+ Pankreas-und Prostatakarzinom
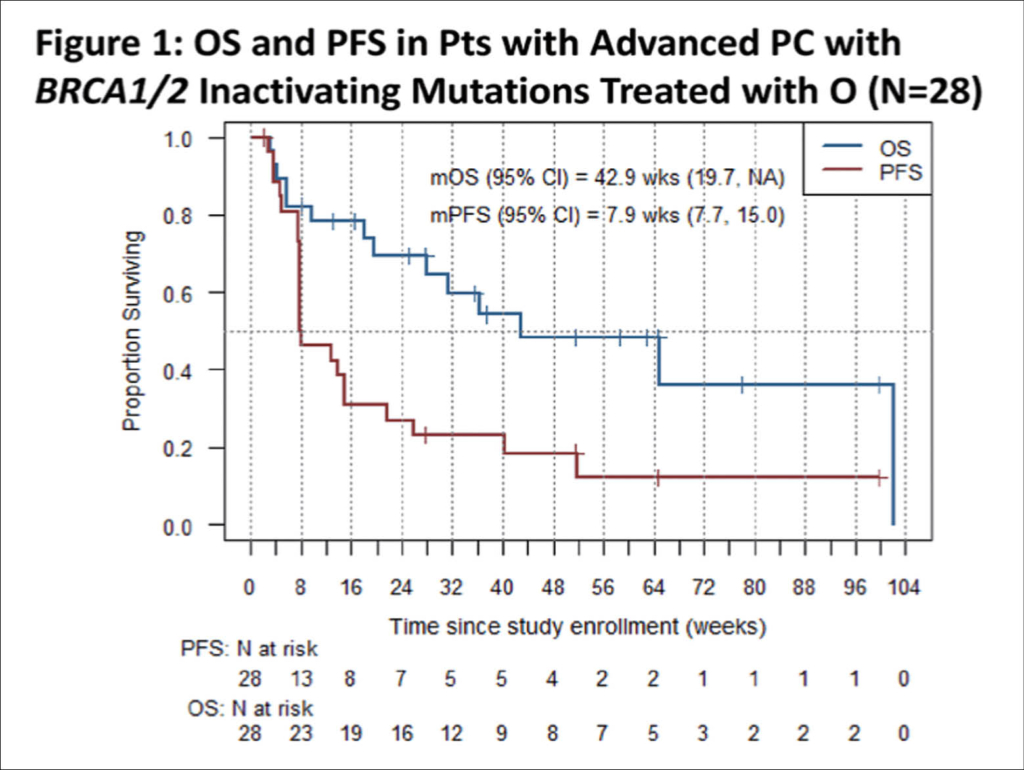
Im Rahmen der TAPUR Phase II Basket Studie wurden zwei Kohorten von Patienten mit refraktärem Pankreasekarzinom bez. Prostatakarzinom mit Keimbahn- oder somatischen BRCA1/2 inaktivierenden Mutationen ohne sonstige Therapieoptionen Olaparib eingesetzt. Nur je einige wenige Prozent aller Patienten mit diesen Diagnosen haben diese DNA-Reparatur Defizienz.
1. In der Kohorte der Pankreaskarzinom Patienten musste der ECOG Performance Status (PS) 0-2, die Organfunktionen intakt sein und alle mussten messbare Tumormanifestationen aufweisen. Das mediane Alter betrug 60 Jahre (44-79) und 63% waren Männer. Der primäre Endpunkt war die Ansprechrate (OR) und sekundäre Endpunkte waren das PFS (eingeschlossen «stable disease» nach +16 Wochen), OS und die Verträglichkeit. Die Olaparib Dosis betrug 300 mg (n=27) oder 400 mg (n=3) zweimal täglich bis zur Progression. 20 Patienten von insgesamt 30 eingeschlossenen Patienten waren mit Platin vorbehandelt. 2 Patienten konnten nicht ausgewertet werden. Die Krankheitskontrolle (2PR und 6 SD16+) ergaben eine OR von 31% (90% CI: 18% – 40%). Grade 3 AE’s oder SAE ‘s fanden sich bei 7 Patienten (Anämie, Diarrhoe, erhöhte Transaminasen, Enterokolitis, erhöhtes Bilirubin und orale Mukositis). Das mediane PFS betrug 7.9 Wochen, das mediane OS betrug 42.9 Wochen und das 1-Jahres OS betrug 47.2 Wochen (95%CI: 19.7.-70.7.).
Angesichts der vielen Vorbehandlungen sind dies ermutigende Resultate für die kleine Gruppe der BRCA1/2 positiven Pankreaskarzinom Patienten.
2. In der Kohorte der Prostatakarzinom Patienten wurden die gleichen Einschlusskriterien und die gleiche Olaparibtherapie angewendet. Es konnten 29 Patienten eingeschlossen werden wobei 4 wegen alleinigen nicht messbaren Knochenmetastasen ausgeschlossen werden mussten. Das mediane Alter betrug 65 Jahre (40-90). Der Allgemeinzustand PS war in 44% ECOG 0 und in 56% ECOG 1. 60% der Patienten hatten mindestens 3 Vorbehandlungen erhalten. Die Krankeitskontrolle (DC) betrug 68% (53-77), die OR 36% (18-57), das mediane PFS 41 Wochen (16.3.-53.1), das mediane OS 75.4 Wochen (49.4.-noch nicht erreicht) und das Gesamtüberleben 79.4 Wochen (47.6-93.1). Somit konnte auch hier bei schwer vorbehandelten Patienten eine längerdauernde Krankheitskontrolle erreicht werden.
ThC
Quellen:
Eugene R Ahn, Olaparib (O) in patients (pts) with pancreatic cancer with BRCA1/2 inactivating mutations: Results from the Targeted Agent and Profiling Utilization Registry (TAPUR) study. Abstract #4367
Evan P. Pisick, Olaparib (O) in patients (pts) with prostate cancer with BRCA1/2 inactivating mutations: Results from the Targeted Agent and Profiling Utilization Registry (TAPUR) study. Abstract #5564
Platinsensitives Ovarialkarzinom: Erhaltungstherapie mit PARP-I verlängert das OS um mindestens ein Jahr
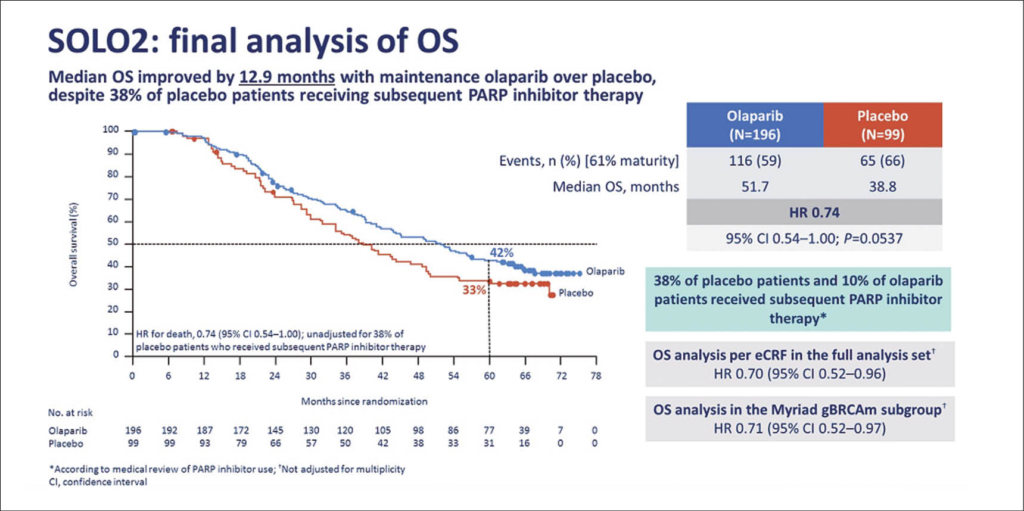
Olaparib ist ein bereits zugelassener oraler Poly (ADP-Ribose)-Polymerase (PARP)-Inhibitor. Dies ist die erste randomisierte Phase 3-Studie, die über reife OS Daten unter einem PARP-Inhibitor als Erhaltungstherapie bei Patientinnen mit einem rezidivierten, noch platinsensitiven Ovarialkarzinom mit einer BRCA-Mutation berichtet. Die finalen OS-Ergebnisse der randomisierten kontrollierten Studie SOLO2 zu Olaparib (300 mg zweimal täglich; n=196) vs. Placebo (n=99) zeigen bei einem mediane Follow-up für beide Gruppen von 65 Monate:
l Olaparib verlängerte das mittlere OS gegenüber Placebo um 12,9 Monate : 51,7 Monate unter Olaparib vs. 38,8 Monate unter Placebo (HR 0,74; 95% KI 0,54-1,00).
lNach 5 Jahren waren 42,1% der Olaparib-Empfänger am Leben vs. 33,2% der Placebo Empfänger.
Es wurden keine neuen unerwünschten Ereignisse (AEs) entdeckt und die häufigsten AEs waren Übelkeit, Fatigue/Asthenie und Anämie. AEs, die zu einer Dosisunterbrechung führten, traten bei 50% der Olaparib- vs. 19% der Placebo-Empfänger auf, und AEs, die zu einer Dosisreduktion führten, bei 28% der Olaparib- vs. 3% der Placebo-Empfänger.
Diese finalen Ergebnisse zeigen, dass eine Erhaltungstherapie mit Olaparib bei Frauen mit platinsensitivem rezidiviertem Eierstockkrebs mit einer BRCA-Mutation das Gesamtüberleben (OS) um beinahe 13 Monate verlängert. Ein so eindrücklicher OS-Vorteil konnte bisher noch in keiner Studie bei Patientinnen mit rezidiviertem Ovarialkarzinom erzielt werden. Olaparib als Erhaltungstherapie setzt damit einen neuen hochwillkommen Standard.
ThC
Quelle: Poveda A et al. Final overall survival (OS) results from SOLO2/ENGOT-ov21: A phase III trial assessing maintenance olaparib in patients (pts) with platinum-sensitive, relapsed ovarian cancer and a BRCA mutation. ASCO 2020, Abstract #6002 .
Tuctinib auch im ZNS wirksam bei HER2+ Mamma-Karzinom Patientinnen
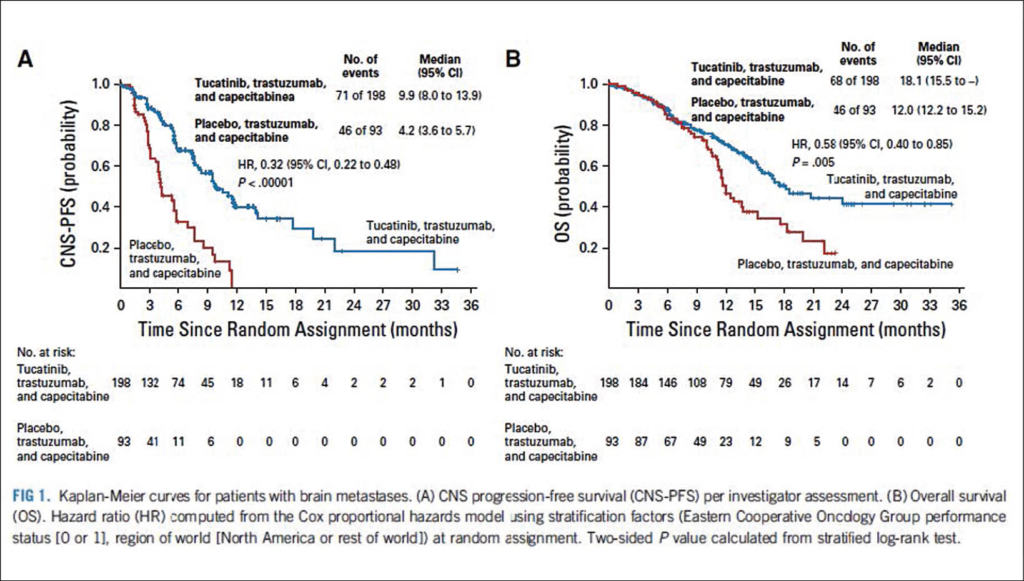
Tucatinib ist ein neu von Swissmedic zugelassener hochselektiver HER2 TKI. Als Zulassungsstudie, welche parallel zum ASCO im JCO bereits als Vollpublikation erschien, diente die doppelblinde, placebo-kontrollierte, 2:1 randomisiertenPhase 2-Studie HER2CLIMB (NCT02614794). Tucatinib oder Placebo wurden als Kombination mit Trastuzumab und Capecitabine eingesetzt. Von initial total 612 eingeschlossenen Patientinnen mit HER“+ lokale fortgeschrittenem oder metastasiertem Brustkrebs nach Vorbehandlung (Herceptin, Perjeta und/oder TDM1. 410 im Verumarm und 202 im Kontrolarm) ) wurden für diese Publikation alle 291 Patientinnen mit Hirnmetastasen (46% der eingeschlossenen Patientinnen) als geplante explorative Subgruppenanalyse ausgewertet. Davon waren 48% im Tucatinib Arm und 46% im Kontrollarm mit Placebo. Die mediane Dauer von der Diagnose bis zum Auftreten von Hirnmetastasen betrug 15.8 Monate (1.1 – 169.2 Monate ) und 14.5 Monate ( 0.5 -99.3 Monate) im Kontrollarm. Bei 47,3% der Patienten sprachen die Hirnmetastasen auf Tucatinib an, komplett (5,5%) oder partiell (41,8%) an. Im Placebo-Arm der Studie gab es nur bei 20% der Patienten ein partielles Ansprechen. Die Dauer des Ansprechens betrug mit Tucatinib 6,8 Monate, mit Placebo 3 Monate. Bei 30 Patienten (21 im Tucatinib- und 9 im Placeboarm) wurde bei einem ZNS Progress eine Lokaltherapie durchgeführt und danach die Studienmedikation wieder aufgenommen.Ddas Risiko für eine erneute Progression mit Tucatinib war deutlich geringer als in der Placebogruppe (HR 0,33; 95% KI 0,11–1,02; p = 0,02). Im Median vergingen vom ersten bis zur erneuten Progress ionmit Tucatinib 7,6 Monate und mit Placebo 3,1 Monate. In der Tucatinib-Gruppe war somit das Risiko einer ZNS-Progression gegenüber Placebo um 68% verringert (HR 0,32; 95% KI 0,22–0,48; p < 0,00001). 40,2% der Patienten dieser Gruppe waren nach einem Jahr weiterhin ohne ZNS-Progression, in der Kontrollgruppe keine Patientin. Das mediane ZNS-PFS lag mit Tucatinib bei 9,9 Monaten, mit Placebo bei 4,2 Monaten (Lin, JCO 2020).
Die Analyse aller eingeschlossenen Patientinnen (N 612) ergab ein mediane PFS mit Tucatinib von 7.8 Monaten (95% confidence interval [CI] 7.5, 9.6) verglichen zu 5.6 Monaten (95% CI 4.2, 7.1) für Patientinnen im Placeboarm (hazard ratio [HR] 0.54; 95% CI 0.42, 0.71; p < 0.00001). Auch das mediane Gesamtüberleben (OS) für alle eingeschlossenen Patientinnen war in der Tucatinib-Gruppe signifikant verlängert mit 20,7 Monaten (11,6 Monate in der Kontrollgruppe), die Ein-Jahres-OS-Rate betrug 71,7% und für Placebo: 41,1% (HR 0,49; 95% KI 0,30–0,80). Bei Patienten mit stabilen Hirnmetastasen bei Studienbeginn gab es dagegen keinen signifikanten Unterschied im OS. Tucatinib hat somit das Potential als neuer Standard bei Patientinnen mit vorbehandeltem metastasiertem HER2+Mammakarzinom in Kombination mit Trastuzumab und Capecitabin für Patientinnen insbesondere mit Hirnmetastasen.
ThC
Quelle: Lin NU, Borges V, Anders C et al. (2020) Intracranial Efficacy and Survival With Tucatinib Plus Trastuzumab and Capecitabine for Previously Treated HER2-Positive Breast Cancer With Brain Metastases in the HER2CLIMB Trial. ASCO 2020, Abstract #1005 Journal of Clinical Oncology DOI: 10.1200/JCO.20.00775
Codebreak 100: Neuartiger niedermolekularer Inhibitor von KRASG12C
AMG 510 bei Patienten mit fortgeschrittenem Kolorektalkarzinom
Die KRASG12C-Mutation des viralen Onkogenhomologen (KRAS) ist mit einer schlechten Prognose bei Darmkrebs (CRC) assoziiert. AMG 510 ist ein neuartiger niedermolekularer Inhibitor, der KRASG12C spezifisch und irreversibel hemmt, indem er im inaktiven Guanosindiphosphat-gebundenen Zustand festgehalten wird. In einer früheren Zwischenanalyse der Phase 1 der ersten am Menschen durchgeführten Studie mit AMG 510 wurde ein günstiges Sicherheitsprofil und eine vorläufige Antitumoraktivität bei Patienten mit fortgeschrittenen soliden Tumoren, die KRASG12C aufwiesen, festgestellt.
Experimentelles
Die wichtigsten Einschlusskriterien waren die durch molekulare Tests identifizierte KRASG12C-Mutation, die messbare Erkrankung und die Progression unter Standardtherapie. Primärer Endpunkt war die Sicherheit. Sekundäre Endpunkte waren die objektive Ansprechrate (ORR), die Krankheitskontrollrate (DCR), das progressionsfreie Überleben (PFS) gemäss RECIST 1.1 und die Gesamtüberlebenszeit (OS). In der Dosis-Eskalationsphase wurden orale Tagesdosen von 180, 360, 720 und 960 mg getestet. Für die Expansionsphase wurde eine Dosis von 960 mg gewählt.
Resultate
Bis zum 8. Januar 2020 wurden 42 Patienten mit CRC (21 weiblich [50%], mittleres Alter: 57,5 Jahre; Bereich: 33-82) erfasst und von 25 auf 960 mg dosiert. Alle Patienten erhielten vorherige systemische Therapien; 19 Patienten (45,2%) erhielten > 3 vorherige Linien. Die mediane Nachbeobachtungszeit betrug 7,9 Monate (Bereich: 4,2-15,9). 13 Patienten (31,0%) starben, und 8 Patienten (19,0%) blieben in Behandlung. 22 (52,4%) und 8 (19,0%) Patienten waren länger als 3 bzw. 6 Monate in Behandlung geblieben. Progressive Krankheit war der häufigste Grund für das Absetzen der Behandlung. 20 Patienten(47,6%) hatten behandlungsbezogene unerwünschte Ereignisse (TRAEs): 18 (42,9%) hatten TRAEs des Grades 2 oder niedriger; 2 (4,8%) hatten TRAEs des Grades 3, bei denen es sich um Durchfall (2,4%) und Anämie (2,4%) handelte. Es gab keine dosisbegrenzenden Toxizitäten, tödliche TRAEs oder TRAEs, die zum Abbruch der Behandlung führten. Insgesamt lagen ORR und DCR bei 7,1% (3 von 42) bzw. 76,2% (32 von 42). Mit der Dosis 960 mg lagen ORR und DCR bei 12,0% (3/25) bzw. 80,0% (20/25). 3 Patienten mit PR hatten eine Ansprechdauer von 1,5, 4,2 bzw. 4,3 Monaten, und ihr Ansprechen war zum Zeitpunkt des Datenschlusses noch nicht abgeschlossen. Bei den Patienten, die mit allen Dosierungen behandelt wurden, betrug die mediane Dauer der stabilen Erkrankung 4,2 Monate (Bereich: 2,5 ±11,0).
Schlussfolgerungen
Bei Patienten mit stark vorbehandelter KRASG12C-CRC-Mutation wurde die Monotherapie mit AMG 510 gut vertragen, wobei die Mehrheit der Patienten die Krankheit unter Kontrolle brachte. Die Studie ist noch nicht abgeschlossen.
red.
Quelle: Fakih M et al. CodeBreak 100: Activity of AMG 510, a novel small molecule inhibitor of KRASG12C, in patients with advanced colorectal cancer. ASCO Virtual Meeting 2020, abstract 4018
Ewing Sarkom: Verbessertes Überleben mit modifizierter Chemotherapie: VDC/IE statt VIDE
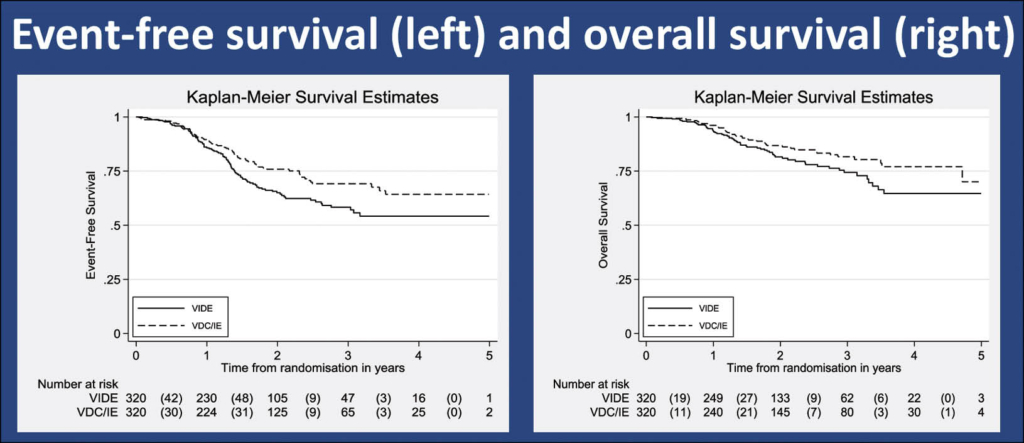
Das Euro Ewing Konsortium ist seit Jahrzehnten erfolgreich daran die Therapien und Prognose dieser sehr jungen Menschen mit Ewing Sarkom (ES) zu verbessern. Also im 2010 zwei Standardtherapien in Europa und den USA für die Primärtherapie zur Verfügung standen und ein direkter Vergleich fehlte, und zudem keine neuen wirksamen Medikamente zur Verfügung standen, wurde ein randomisierter Vergleich vom Europäischen Standard (Arm A) von VIDE (vincristine [V], ifosfamide [I], doxorubicin [D] and etoposide [E]) Induktion und VAI or VAC (V, actinomycin D and I or cyclophosphamide [C]) Konsolidation oder der USA-Standad Arm B) mit kompimiertem VDC/IE Induktion und IE/VC Konsolidation. Es wurden 640 Patienten UAlter 5-50Jahre) mit neudiagnostiziertem lokalisiertem oder metastasiertem ES in die Studie von 2013-2019 in 10 europäischen Ländern incl Schweiz aufgenommen und 1:1 randomisiert in Arm A oder B.
Der primäre Endpunkt war das ereignisfreie Überleben EFS und der sekundäre Endpunkt das Gesamtüberleben OS. Es wurde stratifiziert nach Geschlecht, Alter, Stadium und Metastasierunsmuster, Tumorvolumen und Land. Der mediane Followup betrug 1.7 Jahre. Der Arm B war dem Arm A überlegen: HRs (95% CI) waren 0.70 (0.51, 0.95) für das EFS und 0.64 (0.42, 0.96) für das OS mit eine nachträglichen Wahrscheinlichkeit von 98% für Es und OS, das Arm B besser war. Der Unterschied war in allen Subgruppen vorhanden. Auch waren die Toxizitäten vergleichbar mit 68% AE’s in Arm A und 67% in Arm B. Zusammenfassend erwies sich der amerikanische Standard VDC/IE als klar besser gegenüber tVIDE sowohl für EFS wie OS ohne zusätzliche Toxizität und dürfte damit den neuen Standard darstellen.
ThC
Quelle: ASCO 2020, abstract #11500
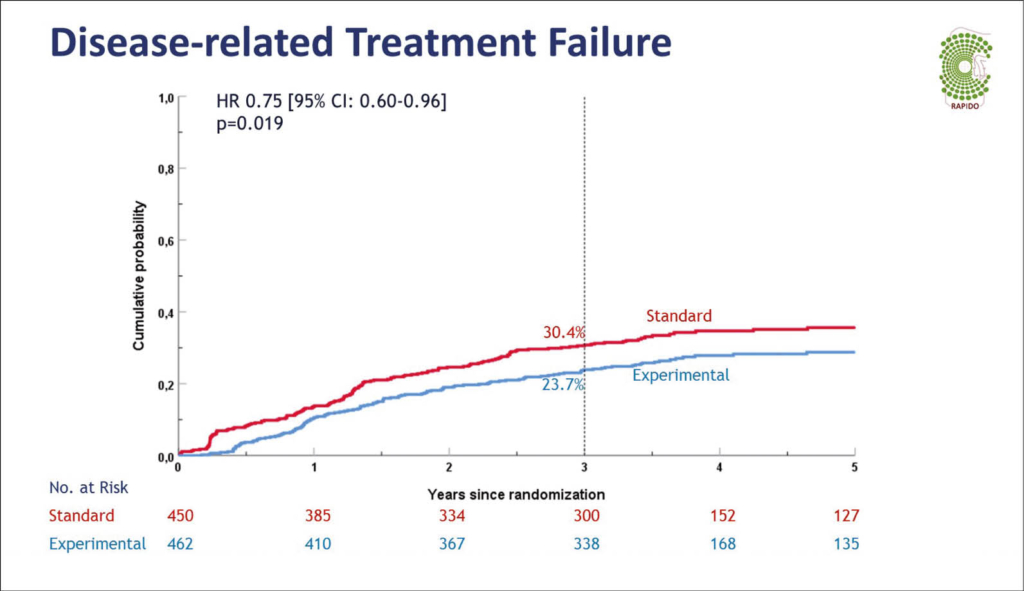
Bessere Resultate durch «short course» neoadjuvante Radiotherapie bei lokal fortgeschrittenem Rektumkarzinom
Eine Kurzzeit Bestrahlung vor Chemotherapie und Operation könnte die Compliance verbessern und damit sowohl die lokale Kontrolle sichern als auch das Risiko für Fernmetastasen vermindern. Das krankheitsfreie Überleben beim lokal fortgeschrittenen Rektumkarzinom ist bisher <75%, weil Fernmetastasen noch häufig auftreten. Die europäischen von Holland geführte RAPIDO Phase 3 Mulitizenterstudie testet 2011-2016 dieses neue Konzept der 5-tägigen Kurzzeitbestrahlung vor präoperativer Chemotherapie und totaler Mesorektumexzision. Es wurden 920 Patienten mit MRI dokumentiertem lokal fortgeschrittenem Rektumkarzinom eingeschlossen (Stadium T4a oder T4b und N2, extramuraler Gefässinvasion und befallener mesorektaler Faszie oder vergrösserter lateraler Lymphknoten, welche als Metastasen beurteilt wurden): 468 wurden in die Kurzzeit Bestrahlung und 452 in den Kontrollarm mit Standard Therapie randomisiert.
Die Kurzzeit-Radiotherapie bestand aus 5 x 5 Gy, gefolgt von Chemotherapie (6 x CAPOX [oder 9 x FOLFOX4) und dann der totalen Mesorektumexzision. Der Kontrollarm bestand aus seiner capecitabinbasierten Standard Chemoradiotherapy (25–28 x 2.0–1.8 Gy) gefolgt von totaler Mesorektumexzision, optional konnte entsprechend lokaler institutioneller Gepflogenheit postoperative noch 8 x CAPOX oder 12 x oder FOLFOX4 angeschlossen werden. Insgesamt wurden 901 Patienten nach Protokoll behandelt, 460 im Verum- und 441 im Kontrollarm. 426 Patienten im Verum- und 400 im Kontrollarm erhielten eine totale Mesorektumexzision. Ein vollständiges pathologische Staging erfolgte bei 423 Patienten im Verum- und 398 im Kontrollarm. Ein komplettes pathologisches Ansprechen wurde bei 27.7% im Verum- und 13.8% im Kontrollarm erreicht (OR 2.40 (95% CI 1.70–3.39; P < .001). Nach 3 Jahren war die Wahrscheinlichkeit des Behandlungsversagens 23.7.% im Verum- und 30.4% im Kontrollarm (HR: 0.75 (95% CI: 0.60–0.96; P = .02). Die Wahrscheinlichkeit für Fernmetastasen nach 3 Jahren war 20% für die Verum- und 26.6% für die Kontrollgruppe (HR 0.69, 95% CI 0.54–0.90; P = .005). Zu diesem Zeitpunkt war die Wahrscheinlichkeit für ein lokales Rezidiv bei 6% im Verum- und 8.7% im Kontrollarm und damit statistisch nicht signifikant verschieden (HR 1.45, 95% CI 0.93–2.26; P = .09). Alle Lebensqualitäts Erfassungen waren vergleichbar ebenso die Verträglichkeit und es fanden sich keine signifikanten Zentrums-
unterschiede auch nicht bei optionaler zusätzlicher adjuvanter Behandlung (P = .37). Lediglich währen der präoperativen Kurzzeitbestrahlung wurden vermehrt > Grade 3 neurologische AES (4.3% vs 0.2%), vaskuläre AES (8.5% vs 4.1%), und Durchfall (17.6% vs 9.3%) im Vergleich zur Kontrollgruppe festgestellt. Es gab in beiden Gruppen keine Unterschiede bezüglich postoperativer Komplikationen.
Dieses neue neoadjuvante Konzept mit Kurzzeitbestrahlung, gefolgt von Chemotherapie und Operation reduziert somit das Therapieversagern um 7%, inklusive dem Risiko von Fernmetastasen und kann der neue Standard in der Therapie von Patienten mit lokal fortgeschrittenem Rektumkarzinom werden.
ThC
Quelle: ASCO 2020, abstract #4006 Citation: J Clin Oncol 38: 2020 (Suppl; abstr 4006) DOI: 10.1200/JCO.2020.38.15_suppl.4006
SCLC limited disease (LD):
Höhere konsolidierende Strahlendosis verbessert das Überleben
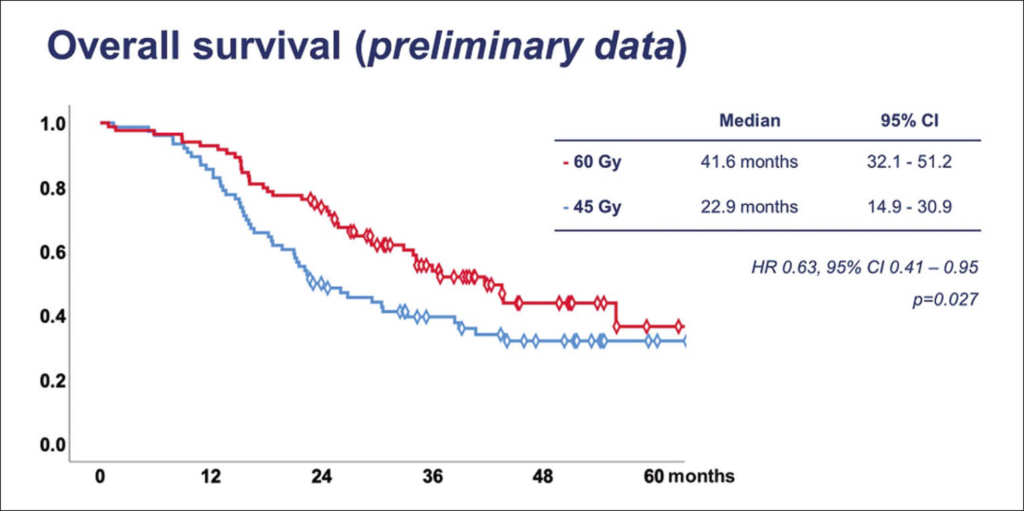
Diese nationale Studie aus Norwegen (22 skandinavische Zentren) untersucht eine alte Frage: was ist die beste konsolidierende Radiotherapie beim lokalisierten kleinzelligen Lungenkarzinom (SCLC)? Bisher war 45 Gy in 30 Fraktionen (2xtäglich) die am meisten angewendete konsolidierende Radiotherapie nach erfolgreicher Chemotherapie. Ob eine höhere Dosis das Überleben verlängert ist eine Hypothese, welche in einer prospektiv randomisierten Studie noch nicht untersucht ist. So wurde in dieser randomisierten Phase 2 Studie untersucht, ob 60 Gy in 40 Fraktionen gegenüber 45Gy in 30 Fraktionen (beide 2xtäglich) für die meisten Patienten machbar, tolerierbar und mit besserem Überleben einhergeht.
Es wurden 2014-2018 176 Patienten (>18 Jahre, PS 0-2) nach erfolgreicher Chemotherapie mit 4 Zyklen Platin-Etoposid randomisert 1:1 zu
60 oder 45 Gy konsolidierender Bestrahlung. Eine prophylaktische Hirnbestrahlung (PCI) von 25-30 Gy wurde allen Patienten angeboten. Der Primäre Endpunkt war das 2-Jahresüberleben, sekundäre Endpunkte waren PFS, Toxizität und gesamtes OS.
160 von 176 Patienten erhielten die ganze Radiotherapie wie geplant : 60 Gy: n = 84, 45 Gy:
n = 76. Das mediane Alter war 65 (58% Frauen, 90% PS 0-1). Keine signifikanten Unterschiede fanden sich in G 3–4 Ösophagitis (60 Gy: 19%, 45 Gy: 18%, p = .92) oder G 3–4 Pneumonitis (60 Gy: 4%, 45 Gy: 0%, p = .10). Ein Trend zu mehr Neutropenie fand sich im 45 Gy Arm
(60 Gy: 21%, 45 Gy: 36%, p = .05). Weiter fanden sich keine G3-4 Toxizitätsunterschiede. Insgesamt starben 3 Patienten in der Bestrahlungsphase (60 Gy: neutropener Infekt, Aortendissektion; 45 Gy: Blutung in Thrombopenie).
Die Ansprechraten waren statistisch nicht unterscheidlich:
60 Gy: 88% [95% CI 81-95], 45 Gy: 85% [95% CI 76-93], p = .52) ebenso das mediane PFS für 60 Gy: 20 Monate [95% CI 11-29], 45 Gy: 14 Monate [95% CI 10-19], p = .31). Nach 2 Jahren waren jedoch signifikant mehr Patienten im 60 Gy arm am Leben: 60 Gy: 73% [95% CI 63-83], 45 Gy: 46% [95% CI 36-60], p = .001), und hatten auch ein signifikant längeres medianes OS: 60 Gy: 42 months [95% CI 32-51], 45 Gy: 23 months [95% CI 17-28], HR .63 [95% CI .41-.96], p = .031).
Zusammenfassend ist die höher dosierte konsolidierende Radiotherapie beim LD SCLC wirksamer mit einem überraschend deutlich verbesserten Gesamtüberleben von 19 Monaten bei vergleichbarer Toxizität. Zu bemerken ist hier auch, dass die Frauen die Mehrheit in dieser Studie darstellten.
ThC
Quelle: ASCO 2020, abstract #9007
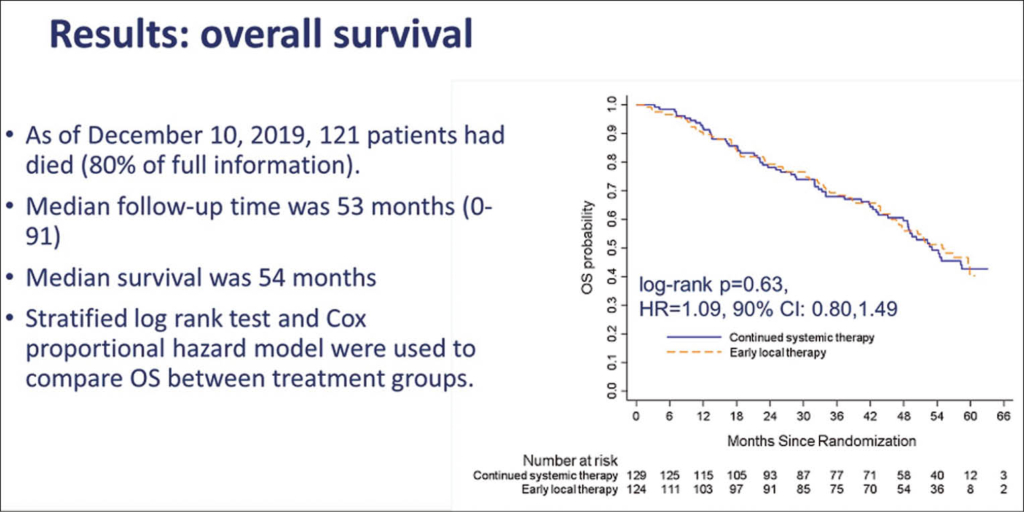
Mammakarzinom Stadium IV: Eine lokale Therapie zur Systemtherapie verbessert die Prognose nicht LBA2
Mit nun reifen Daten nach einer medianen Beobachtungszeit von 59 Monaten wurden die finalen Ergebnisse der ECOG Studie E2108 (ECOG-ACRIN) vorgestellt: 390 Frauen mit neu diagnostiziertem Mammakarzinom im Stadium IV wurden untersucht mit der Frage ob eine zusätzliche lokale Therapie zur Systemtherapie die Ergebnisse verbessert. Alle Patientinnen bekamen die optimale systemische Behandlung entsprechend ihrem Tumor-Biomarker-Status und ihrem Metastasen-Profil. Von den Teilnehmerinnen, welche auf die Systemtherapie ansprachen, wurden 256 Frauen 1:1 randomisiert: die Kontrollgruppe setzte die systemische Behandlung direkt fort und Verumgruppe erhielt vor der Systemtherapie eine lokale Therapie. Nach 5 Jahren zeigte sich kein Überlebensvorteil durch die zusätzliche lokale Therapie gegenüber der alleinigen systemischen Therapie (68,4% vs. 67,9%; HR 1,09; 90 % KI 0,80-1,49; P=0,63). Zudem verbesserte die lokale Therapie das 3-jährige progressionsfreie Überleben nicht (P=0,40).
Ein Unterschied zeigte sich jedoch für das Rückfall- und Progressionsrisiko: bei alleiniger Systemtherapie war das Risiko dafür signifikant höher (25,6% vs. 10,2%; P=0,003). Die Lebensqualität, gemessen am FACT-B Trial Outcome Index, zeigte indessen keinen Vorteil für die zusätzliche Lokaltherapie. Somit muss festgehalten werden, dass im Stadium IV Mammakarzinom die Patientinnen mit einer adäquaten Systemtherapie weder von einer zusätzlichen Operation noch einer Bestrahlung profitierten.
ThC
Quelle. Khan SA, et al. A randomized phase III trial of systemic therapy plus early local therapy versus systemic therapy alone in women with de novo stage IV breast cancer: A trial of the ECOG-ACRIN Research Group (E2108). ASCO Virtual Meeting, 29-31 May 2020, Abstract LBA2.
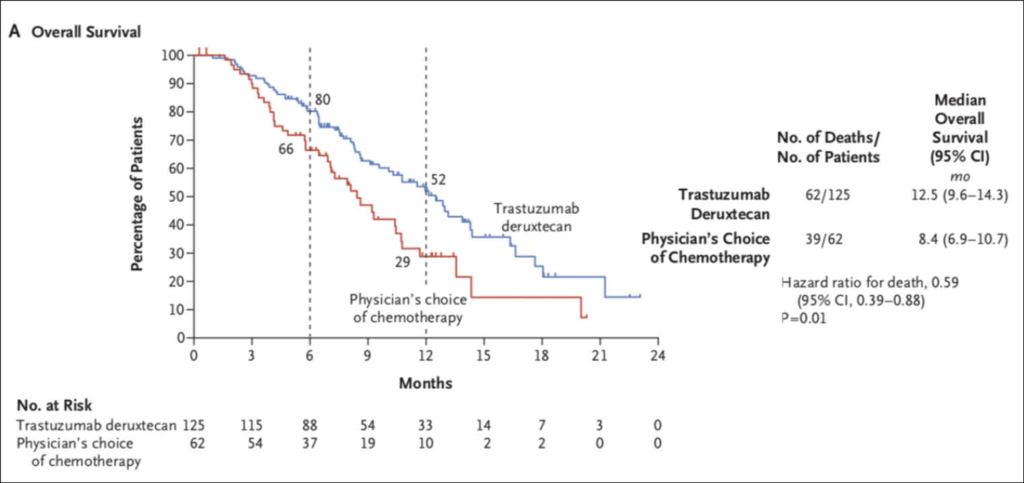
HER+ Magen- und Gastroösophageales Übergangskarzinom (GEJ) profitieren von Trastuzumab Deruxtecan
Trastuzumab Deruxtecan (T-DXd) ist ein Antikörper-Drug-Konjugat aus Anti-HER2-mAb Trastuzumab und einem Topoisomerase-Inhibitor. In Japan und den USA ist es für die Therapie des HER2-positiven Mammakarzinoms bereits zugelassen. In DESTINY-Gastric01 wurde die Wirksamkeit beim HER2-positiven Adenokarzinom des Magens getestet mit primärem Endpunkt Remissionsrate. Die Frage dieser randomisierten offenen multizentrischen Phase 2 Studie war, ob eine Therapie mit dem Antikörper-Drug-Konjugat Trastuzumab Deruxtecan bei Patienten mit HER2- positivem Adenokarzinom des Magens oder des gastroösophagealen Übergangs (mit >2 Vortherapien) zu einer höheren Remissionsrate im Vergleich zu Irinotecan oder Paclitaxel führt. 187 Patienten aus Asien erhielten T-DXd (n = 125) or PC (n = 62 [55 irinotecan; 7 paclitaxel]); 79.7% waren aus Japan, 20.3% aus Korea. Von allen Patienten hatten 44.4% ≥ 3 Vorbehandlungen, die anderen Im Nov 2019 (data cutoff) waren 22.4% mit T-DXd und 4.8% der PC Patienten noch im Behandlungsarm. Die OR war 51.3% (61/119; 11 CR and 50 PR) für T-DXd und 14.3% (8/56; all PR) für PC (P< .0001); Die mediane Dauer des Ansprechsens (mDOR) betrug 11.3 vs 3.9 Monate; das mediane PFS, war 5.6 vs 3.5 Monate (HR, 0.47 [95% CI, 0.31-0.71]; P = .0003). Auch das mediane OS war signifikant länger für T-DXd mit 12.5 vs 8.4 Monaten (HR, 0.59 [95% CI, 0.39-0.88]; P = .0097; Grade ≥ 3 AEs traten in 85.6% der Patienten with T-DXd vs 56.5% with PC; auf. Am häufigsten wurde eine Neutropenie dokumentiert: 51.2%; 24.2%, Anämie 37.6%; 22.6%, und Leukopenie 20.8%; 11.3%. 12 Patienten (9.6%) hatten im T-DXd–rArm eine interstitielle Pneumopathie (ILD; 2 Grade 3, 1 Grade 4, keine Grad 5) vs 0 im PC-Arm. Ein Todesfall durch Penumonie trat im T-DXd arm auf.
T-DXd verbesserte in dieser asiatischen Studie die ORR sowie das OS gegenüber Paclitaxel oder Irinotecan signifikant für Patienten mit HER2+ fortgeschrittenem Magen oder GEJ Adenokarzinom. Inwieweit diese Daten direkt auf andere ethnische Gruppen zu übertragen sind werden weitere Studien zeigen müssen. Auch ist die Lungentoxizität weiter untersuchen. Die Daten wurden zeitgleich im NEJM (Shitara, NEJM 2020) publiziert, https://www.nejm.org/doi/full/10.1056/NEJMoa2004413?query=featured_home.
ThC
Quelle: ASCO 2020, abstract #4513
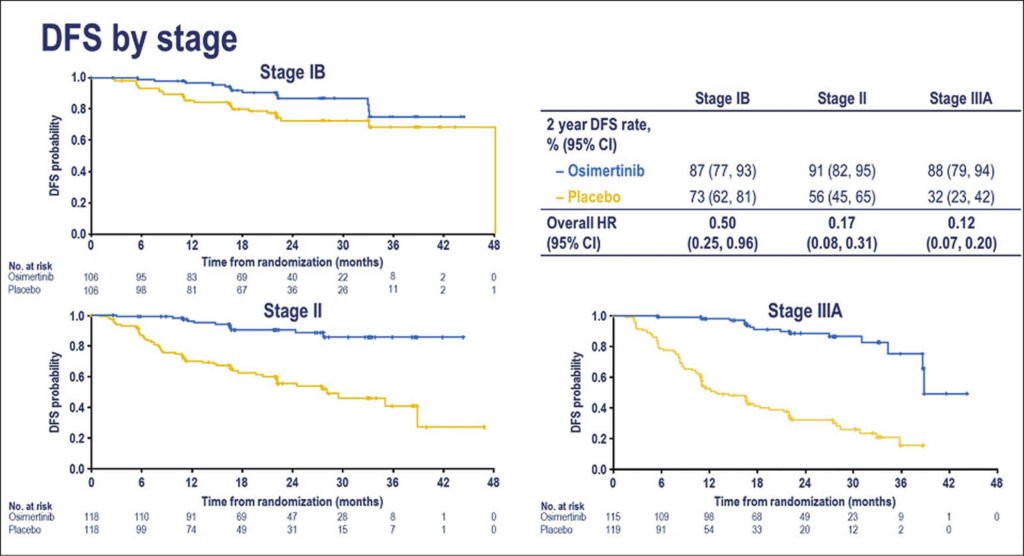
NSCLC adjuvant: Osimertinib neuer Stadard für EGF-R+ Patienten
Osimertinib, ein bereits gut etablierter 3.Generations EGF-R Inhibitor, mit guter ZNS- Aktivität und gegenüber Gefitinib und Erlotinib besserer Wirksamkeit bei unbehandeten EGF-R+Patienten mit NSCLC, ist ein guter Kandidat für eine adjuvante Therapie der erfolgreich operierten Patienten nach erfolgreicher Erstbehandlung bei Stadien I-IIIA. Eine adjuvante Therapie ist heute Standard bei Stadien II und III sowie ausgewählten Patienten mit Stadium IB, allerdings ist die Rückfallrate immer noch hoch. Diese doppelblinde randomiserte globale Phase 3 Studie (ADAURA) untersuchte, ob nach erfolgter kompletter kurativ intendierter Therapie Osimertinib versus Placebo bei 683 EGFR mutierten Patienten die Resultate weiter verbessern konnte. Gemäss dem unabhängigen Review Kommittee musste die Studie frühzeitig entblindet werden, da der Verumarm sich bereits früh als überlegen erwies. Patienten erhielten nach einer 1:1 Randomisation Osimertinib 80 mg täglich oral oder Placebo für maximal 3 Jahre. Der primäre Endpunkt war DFS und sekundäre Endpunkte waren OS und Sicherheit. Die Patientengruppen war in allen Belangen gut ausgeglichen: 339 Patienten erhielten Osimertinib und 343 Placebo. Im Stadium II und III war in dieser früher ungeplanten Interimsanalyse das DFS hochsignifikant besser mit DFS HR von 0.17 (95% CI 0.12, 0.23); p<0.0001 (156/470 events): das 2-Jahres DFS war 90% für Osimertinib und 44% für Placebo. Für die Gesamtpopulation war das DFS HR 0.21 (0.16, 0.28); p<0.0001 (196/682 events): 2-Jahres DFS betrug 89% für Osimertinib und 53% für Placebo.
Das Gesamt-OS mit 29/682 Todesfällen (Osimertinib n=9, PBO n=20) noch nicht ersichtlich. Bezüglich Sicherheit gab es keine neuen unerwarteten Signale für Osimertinib adjuvant. Diese neuen Daten zeigen eindrücklich, dass diese zielspezifische adjuvante Therapie mit Osimertinib hocheffizient ist und die Prognose in den Stadien II und III in relevantem Ausmass verbessern dürfte. Diese Studienresultate wurden zeitgleich zum ASCO im NEJM publiziert (Herbst, NEJM 2020) .
ThC
ASCO 2020, abstract LBA5
Mammakarzinom HER2+ neoadjuvant: es geht auch ohne Anthrazyklin
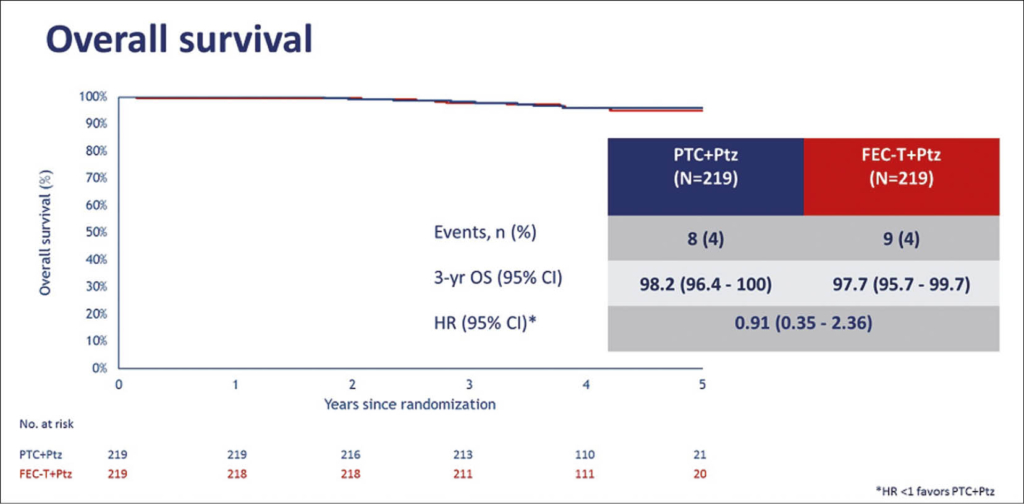
In dieser Phase 3-Studie TRAIN-2 wurden 438 Patientinnen von 37 niederländischen Spitälern eingeschlossen und randomisiert (1:1) zu 3 Zyklen 5-Fluoruoracil, Epirubicin-Cyclophosphamid-Trastuzumab (FEC-T) + Pertuzumab (Ptz), gefolgt von 6 Zyklen Paclitaxel-Trastuzumab-Carboplatin (PTC) + Ptz oder zu einer Behandlung mit 9 Zyklen PTC + Ptz. Primärer Endpunkt ist die Rate an pathologischen CR’s. Sekundäre Endpunkte sind ereignisfreies Überleben (EFS), Gesamtüberleben (OS) und krankheitsfreies Überleben (DFS).
Das 3-Jahres EFS betrug 93,5% ohne und 92,7% mit Anthrazyklinen, wobei kein Unterschied zu Gunsten von Anthrazyklinen in irgendeiner der folgenden Subgruppe beobachtet werden konnte: HR-Status, Alter, Grösse, Nodalstatus, histologischer Grad. Nach 3 Jahren betrug das OS 98,2% ohne und 97.7% mit Anthrazyklinen (nicht statistisch signifikant). Patienten, die nach neoadjuvanter Therapie eine pCR erreichten, waren häufiger krankheitsfrei: DFS 94,1% mit pCR und 85,1% ohne pCR (HR 0,42). Wie erwartet war die Kardiotoxizität höher in der Anthrazyklin-Gruppe, und die Abnahme der linksventrikulären Ejektionsfraktion (LVEF) erholte sich in der Folge bei etwa 1/3 der Patienten nicht mehr auf Normalniveau. Weitere neue Sicherheitsbedenken wurden nicht gefunden.
Somit ist die bisherige Praxis bei HER2+ Mammakarzinom Patientinnen <Stadium II und III Anthrazykline neoadjuvant einzusetzen in Frage gestellt und eine neoadjuvante Anthrazyklin-freie duale HER2-Blockade ist eine vergleichbare aber weniger toxische Alternative. Es wird wichtig sein, dass diese Daten auch in der längerfristigen Beobachtung bestätigt werden können.
ThC
Quelle: van der Voort A et al. Three-year follow-up of neoadjuvant chemotherapy with or without anthracyclines in the presence of dual HER2-blockade for HER2-positive breast cancer (TRAIN-2): A randomized phase III trial. ASCO 2020, Abstract #501
Prostatakarzinom (nmCRPC): Aramis-Studie
Die ARAMIS-Studie ist eine randomisierte, multizentrische, doppelt verblindete, placebo-kontrollierte klinische Phase 3-Studie zur Untersuchung der Wirksamkeit und Sicherheit von oralem Darolutamid, einem weiteren Androgenrezeptor Antagonist, bei Patienten mit nmCRPC, die mit ADT behandelt werden und bei denen ein hohes Risiko für die Entwicklung einer metastasierenden Erkrankung vorliegt. Sie ist damit analog angelegt zur PROSPER-Studie mit Enzalutamid. Es wurden 1.509 Patienten im Verhältnis 2:1 randomisiert und erhielten 600 mg Darolutamid oder Placebo zweimal täglich oral, jeweils zusammen mit der ADT. Krampfanfälle in der Vorgeschichte waren kein Ausschlusskriterium.
Früher veröffentlichte Ergebnisse der ARAMIS-Studie zeigten eine hoch signifikante Verbesserung des primären Endpunkts, des metastasenfreien Überlebens (MFS) mit median 40,4 Monaten für Darolutamid plus ADT im Vergleich zu 18,4 Monaten für Plazebo plus ADT (p < 0,001). Nun liegen die Daten für das Gesamtüberleben (overall survival [OS]) nach einer mittleren Beobachtungszeit von 29.1 Monaten vor. Männer, die Darolutamid plus ADT erhielten, zeigten eine signifikante Verbesserung des OS im Vergleich zu Placebo plus ADT mit einer Reduktion des Sterberisikos um 31% (HR = 0,69, 95%-KI 0,53-0,88; p = 0,003). Zudem war das Auftreten von krebsspezifischen Symptomen, die Schmerzprogression, die erste Folgebehandlung mit zytotoxischer Chemotherapie und das erste Auftreten von symptomatischen Skelettereignissen signifikant verzögert. Auch war die Inzidenz unerwünschter Ereignisse wie Stürze, ZNS-Nebenwirkungen und Hypertonie unter Darolutamid vergleichbar mit der unter Placebo.
Darolutamid scheint somit auch ein gutes Sicherheitsprofil zu haben und ist eine weitere Therapie Option für diese Patienten. Auch diese Studie wurde parallel im NEJM bereits publiziert.
ThC
Quelle: Karim Fizazi, Overall survival (OS) results of phase III ARAMIS study of darolutamide (DARO) added to androgen deprivation therapy (ADT) for nonmetastatic castration-resistant prostate cancer (nmCRPC). ASCO 2020, Abstract #5514 Citation: J Clin Oncol 38: 2020 (suppl; abstr #5514) DOI: 10.1200/JCO.2020.38.15_suppl.5514
SCLC: Pembrolizumab mit EP etwas besser als EP alleine in der 1.line
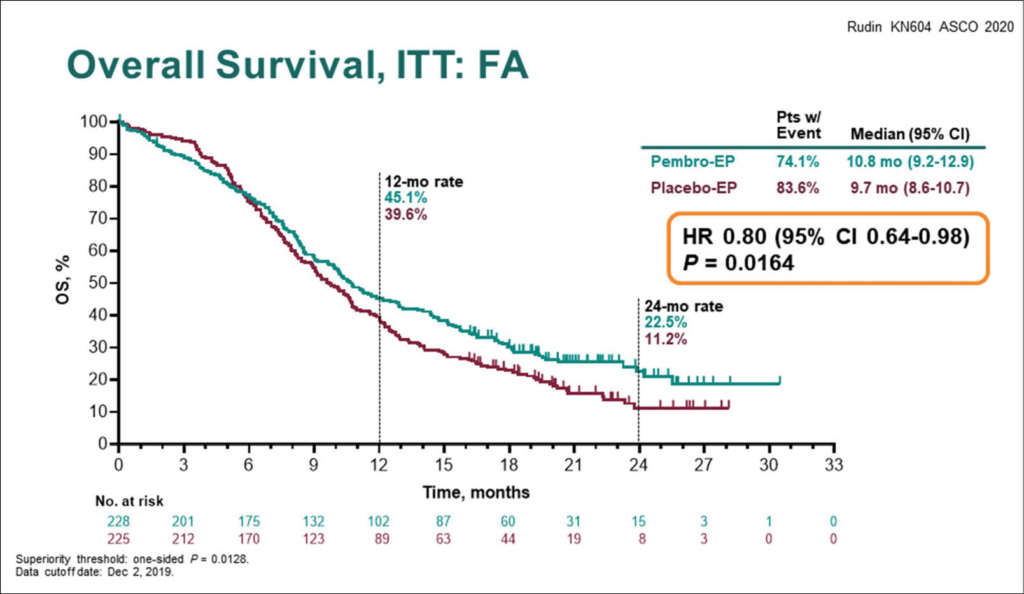
Pembrolizumab als Monotherapie ist wirksam bei vorbehandelten Patienten mit SCLC. Die Studie KEYNOTE-604, eine placebo-kontrollierte, doppelblinde Phase 3 Studie, untersuchte pembro + EP vs Placebo + EP als 1.linien Therapie beim Extensive-stage -SCLC. Insgesamt wurden 453 unbehandelte Patienten 1:1 randomisiert; sie durften ZNS-Metastasen haben, wenn diese lokale behandelt wurden. Pembrolizumab wurde in der Dosis von iv 200mg alle 3 Wochen für maximal 35 Zyklen verabreicht, EP (Cis oder Carbo) wurden in Standard Dosierungen 4x verabreicht. Der Primäre Endpunkt war das OS und PFS, sekundäre Endpunkte waren ORR, DOR, und Sicherheit. Das mediane Alter betrug 65Jahre, 14% im Pembroarm hatten ZNS -Metastasen, im Kontrollarm waren es 10%. Eine PCI erhielten 12% im Pembroarm und 14% im Kontrollarm. Nach einem medianen follow-up von 21 Monaten waren noch 9% der Patienten im Verumarm versus 1% im Placeboarm unter der Studienbehandlung. Bei der zweiten Interimsanalyse nach median 13,5 Monaten war Pembrolizumab beim PFS nummerisch signifikant besser mit median 4,5 versus 4,3 Monaten, und einer HR von 0,74 (p = 0,0023). Zum Zeitpunkt der finalen Analyse nach median 21,6 Monaten war auch das Gesamtüberleben besser mit median 10,8 versus 9,7 Monaten (HR 0,80), dies aber erreichte mit einem p-Wert von 0,0164 den festgelegten Wert für statistische Signifikanz (p = 0,0128) noch nicht.
Der Kurvenverlauf ist typisch für Checkpoint-Inhibitoren: initial zeigt sich kaum ein Unterschied, aber längerfristig separieren sich die Kurven, sodass nach zwei Jahren die Überlebensrate im Pembrolizumab-Arm doppelt sich hoch ist wie im Kontrollarm (23,0% vs. 11,3%). Alle untersuchten Subgruppen konnten von der Immuntherapie zu profitieren – mit Ausnahme der Patienten mit Hirnmetastasen zu Studienbeginn, wo kein Unterschied zwischen den beiden Therapieregimes zu erkennen war. Auch bei den Ansprechraten (letzter Analysezeitpunkt) war Pembrolizumab mit 71% versus 62% dem Placeboarm überlegen, die mediane Dauer des Ansprechens war 4,2 versus 3,7 Monaten. Das Nebenwirkungsprofil war wie erwartet: Grad-3–4- Toxizitäten traten bei 77% versus 75% der Patienten auf, Grad-5-Nebenwirkungen bei 6% versus 5%, und 15% bzw. 6% der Patienten mussten die Therapie wegen Nebenwirkungen abbrechen.
Die Kombination Pembrolizumab und Etoposid und Platin verlängert beim fortgeschrittenen noch unbehandelten SCLC das PFS und absehbar wohl auch das Gesamtüberleben.
ThC
Quelle: Rudin. ASCO 2020, Abtract #9001. J Clin Concol 2020, may 29 DOI:10.1200/JCO.20.00793
Seröses hochgradiges Ovarialkarzinom
Aussichtsreiche Updates zum Einsatz des PARP-Inhibitors Niraparib
Die Einführung von PARP-Inhibitoren, wie Niraparib und Olaparib, hat das Behandlungsrepertoire bei serösem hochgradigem Ovarialkarzinom massgeblich bereichert (1). Dabei kann Niraparib in der Schweiz unabhängig vom BRCA-Mutationsstatus zur Behandlung von Patientinnen mit rezidivierendem Platin-sensitivem Ovarialkarzinom eingesetzt werden (2).
Bereits in der randomisierten, Phase-III-NOVA-Studie verbesserte die Erhaltungstherapie mit Niraparib im Anschluss an eine platinbasierte Chemotherapie das mediane progressionsfreie Überleben (mPFS) gegenüber einer Behandlung mit Placebo signifikant (3).
Nun zeigen aktuelle Ergebnisse der randomisierten Phase-II-Studie AVANOVA2 nach einem medianen Follow-Up von 24.7 Monaten, dass eine Chemotherapie-freie Kombinationstherapie aus dem PARP-Inhibitor Niraparib und dem Angiogenesehemmer Bevacizumab das mPFS gegenüber einer Niraparib-Monotherapie bei rezidivierendem Ovarialkarzinom signifikant verlängern kann (12.5 Monate vs. 5.5 Monate; HR 0.34, p < 0.0001). Zudem war die Zeit bis zur ersten Nachfolgetherapie unter Niraparib und Bevacizumab mit median 14.3 Monaten knapp doppelt so lang wie unter Niraparib allein (7.2 Monate; HR 0.45; p = 0.0004). Das mediane Gesamtüberleben (mOS) betrug unter der Kombinationstherapie 29.4 Monate und unter der Monotherapie 27.8 Monate (HR 0.75; p = 0.30). Insgesamt konnte der kombinierte Einsatz von Niraparib und Bevacizumab das klinische Outcome bei Patientinnen mit rezidivierendem Ovarialkarzinom signifikant verbessern. Gleichzeitig wurde die Therapie gut toleriert und es konnte kein negativer Einfluss auf die Lebensqualität beobachtet werden (4).
Die Lebensqualität zu bewahren, spielt zusätzlich zur Wirksamkeit besonders im Erhaltungstherapie-Setting eine wichtige Rolle. Entscheidend ist in diesem Zusammenhang ein gutes Nebenwirkungsmanagement (5]. In Bezug auf Niraparib hat eine Post-hoc-Analyse der NOVA-Studie das Ausgangskörpergewicht sowie die Thrombozytenzahl als prädiktive Faktoren für die Entwicklung einer hochgradigen Thrombozytopenie identifiziert. Dosismodifikationen konnten der Thrombozytopenie, sowie dem Auftreten von Nebenwirkungen generell, entgegenwirken, hatten jedoch keinen Einfluss auf die Wirksamkeit (6). Basierend auf diesen Beobachtungen wurde Niraparib in der Schweiz erstmalig mit einer verringerten Startdosis von 200 mg bei der Behandlung des rezidivierenden Ovarialkarzinoms zugelassen. Bei einem Körpergewicht ≥ 77 kg und einer normalen Thrombozytenzahl (≥ 150’000/ µl) ist eine Startdosis von 300 mg indiziert (2).
In der randomisierten, doppelblinden, Phase-III-PRIMA-Studie konnte diese individualisierte Startdosierung (ISD) in Hinblick auf Wirksamkeit und Sicherheit beim Einsatz von Niraparib in der ersten Therapielinie bei fortgeschrittenem Ovarialkarzinom validiert werden. Hierfür erhielten die Patientinnen entweder eine auf 300 mg Niraparib fixierte Startdosis (FSD) oder eine basierend auf Gewicht und Thrombozytenzahl individualisierte Startdosis (ISD) von 200 oder 300 mg. Dosisunterbrechungen (FSD 84.1% vs. ISD 71.0%) und -reduktionen (FSD 79.7% vs. ISD 65.7%) kamen in der ISD-Gruppe deutlich seltener vor, was auf eine verbesserte Verträglichkeit bei einer ISD hindeutet. Auch behandlungsbedingte Nebenwirkungen Grad ≥ 3, u.a. Thrombozytopenie, Anämie und Neutropenie, traten in der ISD-Patientengruppe seltener auf (FSD 75.9% vs. ISD 60.4%). Dabei war die klinische Wirksamkeit von Niraparib unter beiden Behandlungsregimen ähnlich (7).
Zusammenfassend unterstützen diese Ergebnisse den Einsatz von Niraparib mit individualisierter Startdosis in der ersten Therapielinie, wie er sich bereits bei der Behandlung des rezidivierenden Ovarialkarzinoms bewährt (6, 7).
red.
Literatur:
1. Madariaga A et al. Manage wisely: poly (ADP-ribose) polymerase inhibitor (PARPi) treatment and adverse events. Int J Gynecol Cancer, 2020. 30(7): p. 903-915.
2. Product Information Zejula (Niraparib). www.swissmedicinfo.ch. Last Access 06.08.2020.
3. Mirza MR et al. Niraparib Maintenance Therapy in Platinum-Sensitive, Recurrent Ovarian Cancer. N Engl J Med, 2016. 375(22): p. 2154-2164.
4. Mirza MR et al. Survival analysis of NSGO-AVANOVA2/ENGOT-OV24: Combination of niraparib and bevacizumab versus niraparib alone as treatment of recurrent platinum-sensitive ovarian cancer. A randomized controlled chemotherapy-free study. Presented at the ASCO Annual Meeting 2020; May 29-31, 2020.
5. DiSilvestro P et al. Maintenance treatment of recurrent ovarian cancer: Is it ready for prime time? Cancer Treat Rev, 2018. 69: p. 53-65.
6. Berek JS et al. Safety and dose modification for patients receiving niraparib. Ann Oncol, 2018.
7. Mirza MR et al. Evaluation of an individualized starting-dose of niraparib in the PRIMA/ENGOT-OV26/GOG-3012 study. Presented at the ASCO Annual Meeting 2020; May 29-31, 2020.
Editorial zum EHA 2020
Europäischer Hämatologie-Kongress:
Liebe Kolleginnen und Kollegen
Auch wenn der diesjährige EHA Kongress nur virtuell stattfinden konnte, so wurden doch einige Studien von hoher wissenschaftlicher Relevanz und auch mit direktem Einfluss auf die tägliche Praxis vorgestellt. Ich möchte Ihnen daher im Folgenden kurz einige practice changing Studien vorstellen.
In der Lymphombehandlung sind sicherlich zwei Studien zur Behandlung des klassischen Hodgkin Lymphoms (cHL) hervorzuheben. So wurden im Rahmender HD17 Studie mehr als 1100 neue diagnostizierte cHL Patienten im early unfavorable Stadium mit dem Standardregimen der GHSG Studiengruppe (2 Zyklen BEACOPPesc. gefolgt von 2 Zyklen ABVD) behandelt und die Frage gestellt, ob bei neg. Abschluss PET-CT (sog. PET4) die bisher obligate Radiotherapie mit 30 GY IF noch erfolgen muss. Bei einer medianen Beobachtungszeit von 46 Monaten ergab sich kein signifikanter Unterschied in Bezug auf das 5-Jahres PFS (95% vs. 97%). Damit sollten entsprechende cHL Patienten mit einem Deauville Socre < 3 im PET4 keine konsolidierende Radiotherapie mehr erhalten.
Die optimale Therapie des fortgeschrittenen cHL wird weiterhin intensiv studiert und die Immuntherapie mit PD1 blockierenden Antikörpern stellt sicherlich einen zunehmend bedeutsameren Bestandteil dar. Offen ist die Frage, ob bei rezidivierten bzw. refraktären cHL Patienten primär eine Immuntherapie mit Brentuximab vedotin oder PD1 blockierenden Antikörper erfolgen soll. Diese Fragestellung wurde nun in der KEYNOTE-204 Studie an 300 Patienten randomisiert getestet. Dabei zeigte sich im direkten Vergleich eine signifikante Überlegenheit des PD1 Antikörpers Pembrolizumab mit einem PFS von 13.2 vs. 8.3 Monaten. Auch aufgrund des Toxizitätsprofils sollten daher PD1 blockierende Antikörper frühzeitig im Rezidiv eingesetzt werden.
Bei den indolenten Lymphomen setzt sich der Siegeszug sog. targeted therapies fort und in verschiedenen Studien konnten insbesondere Daten zur BTK-Inhibitor (BTKi) Therapie vorgestellt werden. Aus meiner Sicht bedeutsam ist die ASPEN Studie, die den neuen BTKi Zanubrutinib vs. den bisher verfügbaren und klinisch etablierten BTKi Ibrutinib in der Erstlinientherapie von Morbus Waldenström Patienten getestet hat. Beide BTKi zeigten eine hohe Wirksamkeit mit einem nahezu identischen 12-Monats PFS von 87% (Ibrutinib) vs. 89 % (Zanubrutinib).
Klinisch auffallend war jedoch eine deutlich geringere Toxizität von Zanubrutinib und es traten insbesondere weniger kardiale Nebenwirkungen (Vorhofflimmern nur 2% für Zanubrutinib vs. 15% für Ibrutinib) und klinisch relevante Blutungsereignisse auf. Es ist zu hoffen, dass uns Zanubrutinib bald im klinischen Alltag zur Verfügung stehen wird.
Auf dem Gebiet des Multiplen Myeloms wurden verschiedene Kombinationstherapien, u.a. auch mit der Phase III ANDRMOMEDA zur Behandlung der AL Amyloidose vorgestellt. Dabei wurde randomisiert geprüft, ob die Hinzunahme von Daratumumab zur Standardtherapie CyBorDex (Cyclophosphamid, Bortezomib, Dexamethason) die Ansprechraten und insbesondere die AL-typischen Organtoxizitäten reduzieren kann. Erfreulicherweise liess sich diese Annahme bestätigen und es zeigte sich neben einer höheren hämatologischen CR Rate (53% vs. 18%) auch eine höhere Organansprechrate nach 6 Monaten (kardiologisches Ansprechen 42% vs. 22% und renales Ansprechen 54% vs. 27%). Da der Erhalt der Organfunktion wesentlich den Verlauf der AL-Amyloidose bestimmt, sollte die Dara-CyBorDex Kombination rasch Standard werden.
Als letztes noch ein paar Worte zur Behandlung des älteren Menschen mit AML, da auf diesem Gebiet wirksame Substanzen bisher fehlen und intensive Therapien nicht eingesetzt werden können. Einzig hypomethylierende Substanzen wie Azacytidine oder Decitabine erzielen marginale Erfolge. In der nun vorliegenden VIALE-A Studie wurde Azacytidine (AZA) mit Placebo respektive dem BCL2 Inhibitor Venetoclax (VEN) kombiniert und in der de-novo Therapie älterer AML Patienten getestet. Dabei zeigte sich für die AZA + VEN Kombination eine signifikante Verlängerung des medianen Überlebens mit 14,7 vs. 9,6 Monaten.
Neben dem längeren Überleben konnte zudem eine Reduktion der Supportivtherapien und hier insbesondere der Bluttransfusionen erreicht werden. Damit ist zu hoffen, dass diese Therapie möglichst rasch unseren älteren AML Patienten zur Verfügung stehen wird.
Ich hoffe, mit den kurz skizzierten Studien Ihr Interesse geweckt zu haben und verbleibe mit freundlichen Grüssen,
Prof. Dr. med. Christoph Renner
Chronische lymphatische Leukämie
Obinutuzumab als Backbone der Erstlinientherapie
Bei In der HOVON139/GIVe konnte bei therapienaiven, FCR-unfitten Patienten durch zwei Zyklen Obinutuzumab (Obi) als Prä-Induktionstherapie vor der Kombination mit Venetoclax (Ven) das Risiko für ein Tumor-Lyse-Syndrom reduziert und hohe Ansprechraten (Gesamtansprechrate nach 12 Zyklen Obi-Ven: 97%) mit einer hohen Rate an Patienten mit einer nicht mehr nachweisbaren Residualerkrankung (uMRD, 88% im Knochenmark) erreicht werden (1).
Die CLL2-GIVe Studie schloss 41 bisher unbehandelte Hochrisikopatienten [TP53-Mutation und/oder del(17p)] unabhängig von Alter und Komorbiditäten ein (2). Sie erhielten während 6 Monaten Obi, Ibrutinib (Ibr) und Ven. Beim finalen Re-Staging (Zyklus 15) zeigte sich eine beachtliche Ansprechrate und hohe Raten einer uMRD im peripheren Blut und Knochenmark.
Die multizentrische offene Phase-3-Studie CLL14 schloss 432 bisher unbehandelte Patienten mit Komorbiditäten ein. Sie erhielten entweder 6 Zyklen Ven-Obi gefolgt von 6 Zyklen Ven oder 6 Zyklen Chlorambucil-Obi (Clb-Obi) gefolgt von 6 Zyklen Clb (3). Bei einer medianen Nachbeobachtungszeit von 39,6 Monaten ergab sich für Ven-Obi ein signifikant besseres medianes progressionsfreies Überleben (PFS) im Vergleich zu Clb-Obi (nicht erreicht vs. 35,6 Monate, HR 0.31 [0.22-0.44], p < 0.001). Im peripheren Blut wiesen 18 Monate nach Behandlungsende 47,2% der Ven-Obi Patienten und 7,4% der Patienten im Vergleichsarm eine nicht mehr nachweisbare minimale Residualerkrankung (uMRD, < 10-4) auf. Die Sicherheitsanalyse ergab eine tiefe Rate an Nebenwirkungen mit einem leichten Anstieg an sekundären Primärtumoren in der Post-Therapie-Phase (6,4% nach Ven-Obi und 1,9% nach Clb-Obi). Eine zusätzliche Analyse zeigte, dass Patienten mit einem partiellen Ansprechen und einer uMRD ein vergleichbar gutes PFS erreichten wie Patienten mit komplettem Ansprechen und uMRD (4).
red.
1. Levin MD et al. Obinutuzumab and venetoclax in untreated unfit patients with chronic lymphocytic leukemia. EP688
2. Huber H et al. CLL2-GIVE, a prospective, open-label, multicenter phase-II trial of obinutuzumab, ibrutinib, plus venetoclax in untreated patients with CLL with 17p deletion / TP53 mutation. S157.
3. Al-Sawaf O et al. Fixed-duration venetoclax-obinutuzumab for previously untreated chronic lymphocytic leukemia: follow-up of efficacy and safety results from the multicenter, open-label, randomized phase 3 CLL14 trial. S155.
4. Al-Sawaf O et al. Characteristics and outcome of patients with chronic lymphocytic leukaemia and partial response to venetoclax-obinutuzumab. EP699
Rezidiviertes/refraktäres Hodgkin-Lymphom
Pembrolizumab ist ein neuer Behandlungsstandard
Patienten mit einem rezidivierten bzw. refraktären klassischen Hodgkin-Lymphom (r/r cHL) haben eine schlechte Prognose, wenn sie aufgrund von Komorbiditäten oder Alter nicht für eine autologe Stammzelltransplantation in Frage kommen oder nach einer Transplantation ein Rezidiv entwickeln. Im Rahmen der Phase-3-KEYNOTE-204-Studie wurde der PD-1-Inhibitor Pembrolizumab bzgl. Wirksamkeit und Sicherheit mit Brentuximab Vedotin bei Patienten r/r cHL verglichen.
Die Patienten erhielten randomisiert entweder 200 mg Pembrolizumab oder 1.8 mg/kg Brentuximab Vedotin. Diese Patienten hatten entweder vor dem Rezidiv eine autologe SCT erhalten oder waren für eine solche nicht geeignet. Primäre Endpunkte der Studien waren PFS und Gesamtüberleben.
Die Monotherapie mit Pembrolizumab führte im Verglich zu Brentuximab Vedotin zu einer statistisch signifikanten Verlängerung des PFS (13,2 vs. 8,3 Monate; HR: 0,65). Neue Gesichtspunkte zum Sicherheitsprofil ergaben sich nicht. Die Überlegenheit von Pembrolizumab fand sich in allen Subgruppen auch bei Patienten mit einem primär refraktären Verlauf bzw. bei Patienten ohne vorangegangene SCT. «Pembrolizumab stellt eine bevorzugte Behandlungsoption, ja sogar einen neuen Behandlungsstandard für Patienten mit einem r/r cHL dar, die nach einer SCT ein Rezidiv entwickeln oder für die autologe SCT nicht in Frage kommen», so der Studienautor Dr. Pier Luigi Zinzani, Bologna.
PS
Akute lymphoblastische Leukämie
Chemotherapie plus Bestrahlung vor der Stammzelltransplantation
Die Behandlung der ALL im Kindesalter ist eine grosse Erfolgsgeschichte, d.h. über 90% werden durch eine moderne Chemotherapie geheilt. Doch bei 10% verläuft die Erkrankung resistent oder es kommt zu einem Rezidiv. Dann kommt die Transplantation hämatopoetischer Stammzellen von einem Spender (allogene HSZT) zum Einsatz. Dadurch können 50 – 80% der Transplantierten geheilt werden.
Der Goldstandard für die Konditionierung vor der Transplantation ist die Kombination aus Ganzkörperbestrahlung (TBI) plus Hochdosischemotherapie. Doch damit sind eine Reihe von Risiken im späteren Leben assoziiert: Sterilität, Wachstumsverzögerung, Lungenprobleme und sekundäre Malignome. Deshalb wurde im Rahmen einer Studie (FORUM-Studie) der Frage nachgegangen, ob auf eine TBI verzichtet werden kann. Doch die alleinige Chemotherapie zeigte deutlich schlechtere Ergebnisse, so dass die Studie aus ethischen Gründen vorzeitig abgebrochen wurde.
Kurz und knapp
COVID-19-Infektion
Die Sichelzellkrankheit ist ein Risikofaktor für einen schweren Verlauf
Im Rahmen der COVID-19-Pandemie wurde in England ein neues Versorgungsnetzwerk geschaffen. Damit sollen nationale Daten und Verläufe einer COVID-19-Infektion bei Patienten mit einer Hämoglobinopathie insbesondere der Sichelzellanämie erfasst und ausgewertet werden.
Die Analyse bis Anfang Juni ergab, dass auch bei Patienten mit einer Sichelzellanämie die Mehrheit der Fälle einen milden Verlauf zeigt und auch Kinder keinem erhöhten Risiko zu unterliegen scheinen. Doch bei Erwachsenen mit einer Sichelzellanämie scheinen schwerere Verläufe etwas häufiger zu sein, so dass solche als Risikopatienten angesehen werden sollten.
PS
Follikuläres Lymphom
In In der laufenden Phase-IV-Studie GAZELLE wird untersucht, ob Obinutuzumab bei therapienaiven Patienten mit einem follikulären Lymphom ab dem 2. Zyklus rascher (über 90 Minuten) infundiert werden kann, ohne dass es zu einer erhöhten Rate an infusionsassoziierten Nebenwirkungen (IRR) > Grad 3 kommt (1). Die eingeschlossenen Patienten (bisher 69 von 112) müssen den ersten Zyklus ohne IRR Grad 3 oder 4 toleriert haben.
In einer Phase Ib/II-Studie wird bei rezidivierten/refraktären Patienten die Kombination aus Polatuzumab vedotin – ein gegen CD79b gerichtetes Antikörper-Wirkstoff-Konjugat – mit Obinutuzumab (Obi) und Venetoclax (Ven) als Induktionstherapie gefolgt von einer Obi-Ven-Erhaltungstherapie untersucht (2). Eine erste Interimsanalyse mit 15 hinsichtlich Wirksamkeit auswertbaren Patienten ergab am Ende der Induktionstherapie eine Gesamtansprechrate von 87%, bei 60% Komplettremissionen.
red.
1. Hübel K et al. Obinutuzumab short duration infusion in previously untreated advanced follicular lymphoma: an ongoing study. PB2191.
2. Yuen S et al. Polatuzumab vedotin + obinutuzumab + venetoclax in patients with relapsed/refractory follicular lymphoma: interim analysis of a phase Ib/I trial. EP1162.
CLL
Ein neues Erstlinien-Therapieschema bewährt sich
Die Prognose der CLL bei Hochrisikopatienten ist weiterhin trotz grosser Fortschritte ernst. Im Rahmen der CLL2GIVe-Studie wurde ein neues Erstlinienschema bei Patienten mit hohem Risiko, d.h. einer 17p-Deletion und/oder TP53-Mutation untersucht.
Bei diesem Therapieschema erhalten die Patienten in den ersten sechs Monaten die drei Wirkstoffe Obinutuzumab, Venetoclax und Ibrutinib gefolgt von der Zweier-Kombination Venetoclax und Ibrutinib über weitere sechs Monate. Anschliessend wird eine Erhaltungstherapie mit Ibrutinib dann durchgeführt, wenn bis dahin keine nicht mehr nachweisbare Resterkrankung (MRD) oder keine vollständige Remission nach IWCLL-Kriterien erreicht ist.
Das Behandlungsschema ist eine dem Ansprechen angepasste limitierte Therapie. Die Rate an vollständigen Remissionen betrug 58,5%. Bei 80,5% der Patienten war nach 15 Zyklen im peripheren Blut keine MRD mehr nachweisbar. Das Sicherheitsprofil war akzeptabel. „Demnach ist das GIVe-Schema eine vielversprechende Erstlinientherapie für CLL-Patienten mit einem hohen Risiko“, so die Studienautorin Dr. Henriette Huber, Ulm.
PS
Darutumumab
Eine neue vielversprechende Therapieoption bei der Amyloidose
Im Rahmen der ANDROMEDA-Studie wurde die Wirksamkeit des AntiCD38-Antikörpers Darutumumab bei der Leichtketten-Amyloidose untersucht. Die Ergebnisse sind vielversprechend.
Die Leichtkettenamyloidose ist eine seltene und potenziell tödliche Systemerkrankung. Sie entsteht, wenn abnorme Plasmazellen im Knochenmark abnorme Antikörperstücke, sogenannte Leichtketten, bilden, die zu Amyloid verklumpen. Dieses kann in allen Organen abgelagert werden. Besonders betroffen sind Herz, Nieren und Nervensystem.
Bisher gibt es keine zugelassenen Behandlungsmöglichkeiten. Oft werden Chemo-basierte Kombinationen eingesetzt, die aber nur eine begrenzte Wirksamkeit zeigen. Daratumumab ist der erste und einzige subkutan applizierbare AntiDC38-Antikörper, der weltweit zur Behandlung des Multiplen Myeloms zugelassen ist. Im Rahmen einer Phase-III-Studie (ANDROMEDA-Studie) wurde dieser Antikörper zusammen mit Cyclophosphamid (Cy), Bortezomib (Bor) und Dexamethason (D) bei Patienten mit einer Leichtkettenamyloidose eingesetzt und mit der Kombination CyBorD verglichen. Als primärer Endpunkt wurde Gesamtansprechrate festgelegt. Diese lag nach sechs Monaten bei der Kombination D-CyBorD bei 53% im Vergleich zu nur 18% unter CyBorD allein. Bei kardialer Amyloidose lagen die Ansprechraten bei 42% vs. 22% und bzgl. der renalen Manifestation bei 54% vs. 27%. Das Sicherheitsprofil der Kombination D-CyBorD war akzeptabel und entsprach dem in früheren Studien mit D dokumentierten. „Die ANDROMEDA-Studie ist eine neue vielversprechende Behandlungsoption für Patienten mit einer neu entdeckten Leichtketteamyloidose, die dringend neue Behandlungsmöglichkeiten benötigen“, so die Studienautorin Dr. Efstathios Kastritis, Athen.
PS
Myelodysplastisches Syndrom
Vielversprechende Behandlungsergebnisse mit Imetelstat
Im Rahmen der IMerge-Studie wurde die Wirksamkeit und Sicherheit des neuartigen Telomerase-Hemmers Imetelstat bei Patienten mit einem myelodysplastischen Syndrom (MDS) mit geringem Risiko evaluiert.
Eingeschlossen in diese Phase-II-Studie wurden 38 Patienten mit einem MDS, die nicht-del(5q) sind, auf eine Erythrozytentransfusion angewiesen sind oder nach einer Therapie mit Erythropoese-stimulierenden Substanzen einen Rückfall erreichen oder auf eine solche nicht ansprechen. Als primärer Wirksamkeitsendpunkt der Studie war die Rate an Patienten, die in den ersten 8 Wochen nach Beginn der Studie keine Erythrozytentransfusionen benötigten., definiert. Ein Follow up nach 24 Monaten ergab folgendes:
l 16 Patienten (42%) erreichten eine 8-wöchige Freiheit von Erythrozytentransfusionen, 12 dieser Responder (75%) zeigten einen Hb-Anstieg von > 3 g/dL im Vergleich zur Vorbehandlung.
- 12 Patienten (32%) erreichten eine 24-wöchige Freiheit von Erythrozytentransfusionen.
- 11 Patienten (29%) waren mehr als 1 Jahre lang transfusionsfrei, wobei das längste transfusionsfreie Intervall 2,7 Jahre betrug.
- Die mediane Dauer der Transfusionsfreiheit betrug 88 Wochen, die längste bisher beobachtete Dauer bei einem Non-del(q5) LR-MDS.
- Eine erythroide hämatologische Verbesserung wurde bei 26 Patienten (68%) nach einer medianen Dauer von 93 Wochen erreicht.
- Die Dauerhaftigkeit der Tranfusionsfreiheit sowie die zytogenetische und die molekularbiologisch nachweisbare Reduktion maligner Klone bei einigen Patienten könnten auf eine mögliche krankheitsmodifizierende Wirkung von Imetelstat hinweisen.
- Die am häufigsten beobachteten unerwünschten Ereignisse waren reversible Grad > 3 –Zytopenien.
PS