- Das idiopathische Parkinsonsyndrom
Das idiopathische Parkinsonsyndrom (iPS) zählt mit rund zehn Millionen Betroffenen zu den häufigsten neurodegenerativen Erkrankungen weltweit. Alleine in der Schweiz leiden mehr als 15 000 Menschen unter den fortschreitenden Symptomen, die unter anderem auf eine Degeneration der Dopamin-produzierenden Zellen der Substantia nigra zurückzuführen sind. Die frühe Diagnosestellung und der frühe Beginn der medikamentösen und nicht-medikamentösen Therapien führen zu einer signifikanten Steigerung der Lebensqualität und längerfristig zu einer Verlängerung der Selbstständigkeit.
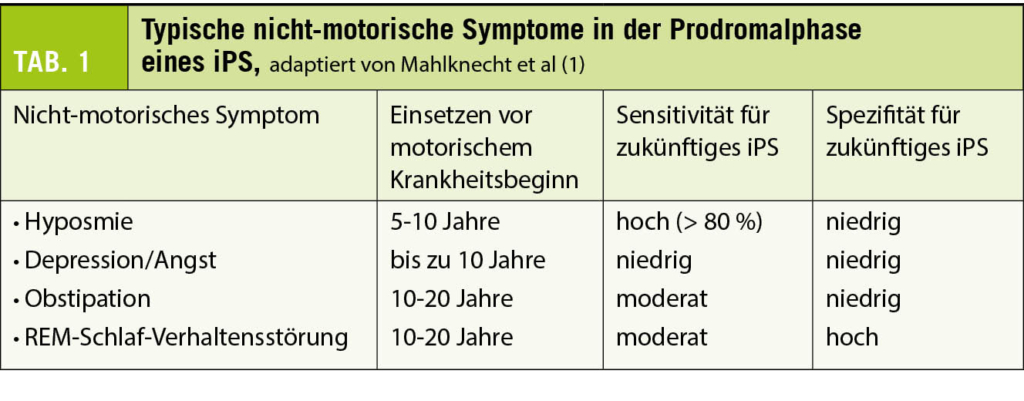
Der degenerative Prozess beginnt bereits Jahre bis Jahrzehnte vor dem krankheitsdefinierenden motorischen Symptombeginn. Diese Phase mit dezenten vor allem nicht-motorischen Symptomen wird auch Prodromalphase genannt. Aufgrund der fehlenden motorischen Symptomatik werden diese sehr unspezifischen Beschwerden meist nicht mit einem beginnenden Parkinson-Syndrom in Verbindung gebracht. Beim Vorliegen erster motorischer Symptome erweist sich die Prodromalphase retrospektiv jedoch als hilfreich. Durch eine gezielte Anamnese und Fremdanamnese der häufigsten nicht-motorischen Symptome (Tab. 1) lässt sich der Verdacht eines Parkinson-Syndroms oft bereits früh erhärten.
Erste motorische Symptome
Erst ab einem Zellverlust der Substantia nigra pars compacta von über 60% manifestieren sich motorische Symptome (2). Die Patienten stellen sich häufig mit unspezifischen Beschwerden vor. So berichten sie beispielsweise von allgemeiner Schwäche, kleiner und unleserlichen Handschrift, Schulter-Armschmerzen oder neu aufgetretenem Zittern. Den Angehörigen können eine leisere Sprache, eine Hypomimie oder eine Änderung des Gangbildes auffallen. Die Diagnose des idiopathischen Parkinsons wird klinisch gestellt. Obligat benötigt es verlangsamte Bewegungen – Bradykinese. Zusätzlich ist ein weiteres «Kardinal-Symptom» wie 4-6Hz Ruhetremor und/oder Rigor für die Diagnosestellung gefordert. In der Regel beginnen die beschriebenen Beschwerden einseitig an einem Arm, breiten sich auf das gleichseitige Bein aus und gehen im Verlauf auch nach kontralateral über. Die Asymmetrie bleibt zumeist auch in fortgeschrittenen Stadien bestehen.
Die Bradykinese macht sich in den repetitiven Bewegungen der Hände und Füsse (Finger-/Foot-tapping) durch ein Frequenz-/Amplitudendekrement bemerkbar. In der weiteren klinischen Untersuchung sollte besonders auf das Gangbild des Patienten geachtet werden. Der meist einseitig reduzierte Mitschwung des Armes in Verbindung mit einer verkürzten Schrittlänge und einer nach vorne übergebeugten Haltung fallen oft als frühe motorische Symptome auf. Ein weiterer hilfreicher Teil der Untersuchung ist es, den Patienten mehrere Sätze schreiben zu lassen. Hierbei lässt sich häufig eine undeutliche Schrift, welche gegen Ende des Satzes kleiner wird, objektivieren. Die Mikrographie bemerken die Patienten meist schon lange vor dem Arztbesuch selber. Des Weiteren können auch anamnestisch Hinweise auf eine Bradykinese erfragt werden. Viele Parkinsonpatienten leiden bereits früh unter diskreten Feinmotorikstörungen. Häufig bejahen sie beispielsweise Probleme beim Zuknöpfen von Hemden. Falls möglich sollte immer eine Fremdanamnese eingeholt werden. Die Angehörigen können zu Symptomen, welche den Patienten selber nicht auffallen, meist bessere Auskunft geben. So lässt sich auf Nachfrage eine Veränderung der Stimme und der Mimik bestätigen.
Bei Bewegungen einzelner Gelenke durch den Untersucher macht sich der Rigor häufig durch das Zahnradphänomen bemerkbar. Ein subklinischer Rigor kann durch Bewegungen der kontralateralen Extremität demaskiert werden. Das Zittern ist ausgeprägter in ruhender Position (Ruhetremor) und nimmt üblicherweise bei Gebrauch der Hand ab, im Gegensatz zu anderen Tremorformen.
Medikamentöse Behandlungs-möglichkeiten motorischer Symptome
Die medikamentöse Therapie sollte begonnen werden, sobald der Patient einen negativen Einfluss der motorischen Symptome auf seine Lebensqualität beklagt. Lange Zeit galt es, bei frühem Krankheitsbeginn ein möglichst Dopamin-sparendes Therapieregime zu führen, um die gefürchteten L-Dopa-induzierten Dyskinesien hinauszuzögern. Deshalb wurde für die initiale Behandlung eine Therapie mit Dopaminagonisten bevorzugt. Neuere Studien konnten jedoch zeigen, dass eine frühe Behandlung mit L-Dopa im Gegensatz zu einer L-Dopa-sparenden Therapie keinen relevanten Einfluss auf die Ausbildung von motorischen Fluktuationen hat, gleichzeitig aber zu einer Verbesserung der Lebensqualität führt (3 - 5). Zusätzlich wird das positive. Ansprechen der motorischen Symptome auf L-Dopa als unterstützendes Kriterium in der Diagnosestellung angesehen (6). Die Behandlung mit L-Dopa kann durch andere Substanzgruppen bei Bedarf ergänzt werden. Bei Auftreten von Fluktuationen kann mit Zugabe von Dopaminagonisten, COMT-Hemmern oder MAO-B-Hemmern eine Stabilisierung erreicht werden. Hierbei sollte je nach Komorbiditäten und nicht-motorischen Symptomen des Patienten auf das Nebenwirkungsspektrum der einzelnen Substanzen geachtet werden. Im Falle von störenden Dyskinesien kann eine Therapie mit Amantadin erwogen werden.
Die subkutane Apomorphin-Injektion und die duodenale L-Dopa-Infusion mit Hilfe von Pumpen bieten aufgrund der kontinuierlichen Medikamentenapplikation gute Alternativen zur oralen medikamentösen Therapie beim fortgeschrittenen Parkinsonpatienten mit schweren Fluktuationen.
Wichtigste Nicht-Motorische Symptome
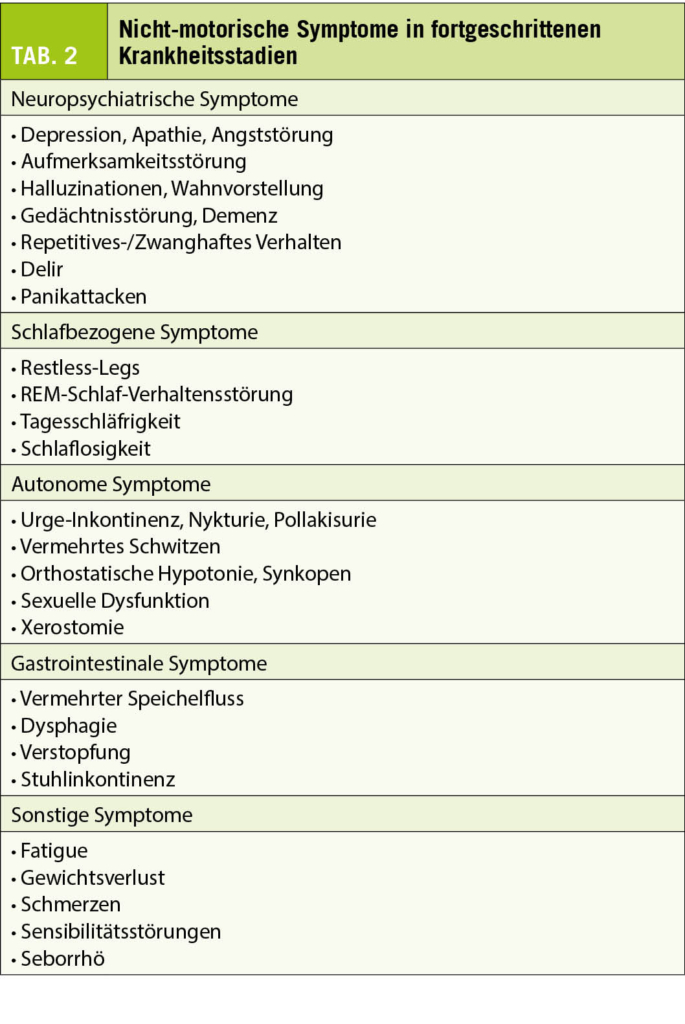
Im fortgeschrittenen Krankheitsstadium kommt es zu einer stetigen Zunahme der nicht-motorischen Symptome. Sie führen zur eingeschränkten Lebensqualität, Invalidität und verkürzten Lebenserwartung der Patienten. Darum ist es wichtig, diese Symptome zu erkennen und zu behandeln (Tab. 2).
Medikamentöse Therapie nicht-motorischer Symptome
Da die meisten nicht-motorischen Symptome zumindest teilweise auf die dopaminerge Therapie ansprechen (u.a. Schmerzen, Depression…), steht eine möglichst gute Einstellung der motorischen Parkinsonsymptome immer am Anfang. Auch das Wissen und die Evaluation nicht-motorischer Fluktuationen sind hier von entscheidender Bedeutung (z.B. ängstlich depressive Zustände in Off Phasen). Bleibt auch bei optimaler Behandlung der motorischen Parkinsonsymptome eine Depression manifest, empfiehlt sich der Einsatz eines selektiven Serotonin-Wiederaufnahmehemmers.
Die Therapie mit Rivastigmin, als Pflaster oder Kapsel, zeigt einen positiven Effekt auf kognitive Beeinträchtigungen bzw. Parkinsondemenz. Psychosen und Delir beim Parkinsonpatienten sollten primär mit Clozapin behandelt werden. Alternativ kann auf Quetiapin zurückgegriffen werden.
Eine orthostatische Hypotonie kann neben allgemeinen Massnahmen wie Flüssigkeits-/Salzzufuhr und Stützstrümpfen medikamentös versuchsweise mit Fludrocortison behandelt werden. Wichtig ist hierbei, ein Blutdruckprotokoll zu führen, um die medikamentöse Therapie gut zu überwachen. Obstipation sollte mit den gängigen Pro- und Präbiotika therapiert werden. Bedarfsweise können zusätzlich Laxantien wie Macrogol zum Einsatz kommen. Bei Übelkeit und Erbrechen ist Domperidon das Medikament erster Wahl (7).
Invasive Behandlungsmethoden – Tiefe Hirnstimulation (Deep Brain Stimulation – DBS)
Bei Patienten mit medikamentös nicht mehr ausreichend beherrschbaren Wirkfluktuationen sollte eine operative Behandlung mittels tiefer Hirnstimulation in Betracht gezogen werden. Die tiefe Hirnstimulation führt zu einer eindrücklichen Stabilisierung motorischer und teilweise auch nicht-motorischer Symptome und einer damit verbundenen Verbesserung der Lebensqualität.
Copyright bei Aerzteverlag medinfo AG
Klinik für Neurologie, Kantonsspital St. Gallen
Rorschacher Strasse 95
9007 St. Gallen
patrick.dorin@kssg.ch
Klinik für Neurologie, Kantonsspital St. Gallen
Rorschacher Strasse 95
9007 St. Gallen
Die Autoren haben im Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
- Das idiopathische Parkinsonsyndrom zählt zu den häufigsten neurodegenerativen Erkrankungen.
- Die nicht-motorischen Symptome gehen den motorischen Beschwerden häufig um Jahre voraus.
- Die Diagnose wird primär klinisch gestellt. In der klinischen Untersuchung sollte vor allem nach einer Bradykinese gesucht werden, denn ohne diese lässt sich die Diagnose nicht stellen.
- Der frühzeitige Einsatz von L-Dopa führt zu einer optimalen Symptomkontrolle und zum Erhalt der Lebensqualität. Bei fehlendem Ansprechen auf L-Dopa muss die Diagnose in Frage gestellt werden und ggf. die Zuweisung an einen spezialisierten Neurologen erfolgen.
- Für fortgeschrittene Krankheitsstadien stehen mit den Pumpensystemen und der tiefen Hirnstimulation gute Alternativen zur oralen Therapie zur Verfügung.
- Regelmässige Physio-, Ergo- und Logotherapie sollten je nach Bedarf grosszügig in Anspruch genommen werden.
1. P Mahlknecht et al. / The Concept of Prodromal Parkinson’s Disease. Journal of Parkinson’s Disease 5 (2015) 681–697
2. MB Stern et al. / Toward a redefinition of Parkinson’s disease. Mov Disord (2012), 27, 54-60.
3. R Cilia et al. / The modern pre-levodopa era of Parkinson’s disease: insights into motor complications from sub-Saharan Africa. Brain (2014): 137; 2731–2742
4. CVM Verschuur et al. / Randomized Delayed-Start Trial of Levodopa in Parkinson’s Disease. N Engl J Med (2019);380:315-24.
5. RMA de Bie et al. / Initiation of pharmacological therapy in Parkinson’s disease: when, why, and how. Lancet Neurol 2020
6. G Deuschl, W Oertel, H Reichmann et al. / DGN-Leitlinien Idiopathisches Parkinson-Syndrom (2016)
7. K Seppi et al. / Update on Treatments for Nonmotor Symptoms of Parkinson’s Disease—An Evidence-Based Medicine Review (2019)
der informierte @rzt
- Vol. 10
- Ausgabe 11
- November 2020