- Ektope Schwangerschaft
Die ektope Schwangerschaft, auch Extrauteringravidität (EUG) genannt, ist eine Schwangerschaft ausserhalb der Gebärmutterhöhle. Geschätzt 2% aller festgestellten Schwangerschaften (1) sind EUGs und somit ein häufiges Krankheitsbild im klinischen Alltag. Eine sichere Diagnose ist nicht immer evident und die differentialdiagnostische Abtrennung zur gestörten oder noch nicht nachweisbaren intrauterinen Frühschwangerschaft kann schwierig sein. Wegen der potentiell lebensbedrohlichen intra-abdominellen Blutung im Falle einer Ruptur der hochvaskularisierten Struktur gehören die ektopen Schwangerschaften zu den herausforderndsten gynäkologischen Notfällen.
La grossesse extra-utérine (GEU, ou grossesse ectopique) est une grossesse implantée à l’extérieur de la cavité utérine. On estime que 2 % de toutes les grossesses diagnostiquées sont ectopiques (1) ce qui en fait un tableau clinique fréquent dans le quotidien du gynécologue. De poser le diagnostic correct n’est pas toujours évident et la distinction avec une grossesse intrautérine à évolution perturbée voire intrautérine précoce pas encore cliniquement visible peut s’avérer difficile. En raison du risque de rupture de ces structures hautement vascularisées avec hémorragie intra-abdominale menaçant la vie, la GEU fait partie des urgences gynécologiques les plus exigeantes.
Klinik und Diagnostik der EUG
Klinik
Die häufigste Lokalisation der ektopen Schwangerschaft ist der Eileiter (ca. 96%), selten befindet sie sich in der Zervix, interstitiell/cornual, im Bereich einer Sectionarbe, ovariell oder intraabdominell; eine extreme Rarität stellen die intramuralen-in der Uteruswand (nur 50 Fälle in der Literatur) und die heterotopen (gleichzeitiges Bestehen einer intrauterinen und einer ektopen Schwangerschaft) Schwangerschaften dar.
Die zwei Kardinalsymptome der EUG sind Unterbauchschmerzen und vaginale Blutung in der Frühschwangerschaft bzw. nach einer Amenorrhoe (2). Typischer Weise beginnen die Beschwerden ca. 6-8 Wochen nach der letzten Periode, bei den selteneren, nicht-tubaren EUGs kann diese Symptomatik auch etwas später auftreten.
Bezüglich der Unterbauchschmerzen gibt es kein spezifisches Schmerzmuster für die EUG, häufig befinden sich die Schmerzen diffus im Unterbauch, gelegentlich zu einer Seite lokalisiert. Sowohl das zeitliche Auftreten, die Stärke als auch der Schmerzcharakter können sehr unterschiedlich sein. Beim perakuten, starken Schmerz und kreislauf-instabiler Patientin mit positivem Schwangerschaftstest muss an eine rupturierte EUG gedacht werden.
Auch die vaginale Blutung folgt keinem für die EUG spezifischem Blutungsmuster. Sie kann schwach im Sinne eines Spottings sein oder einer übermensstarken Blutung entsprechen. Die Blutung ist häufiger intermittierend als kontinuierlich.
Die allgemeinen Schwangerschaftsbeschwerden (wie z.B. Übelkeit und Brustspannen) treten häufig später als erwartet auf; dies liegt an den tieferen Hormonwerten im Vergleich zu vitalen intrauterinen Schwangerschaften (gilt sowohl für bHCG als auch für Progesteron und Östrogen) (3).
Selten sind Patientinnen auch oligo- bis asymptomatisch.
Diagnostik
Die zwei Säulen der Diagnostik der EUG sind der transvaginale Ultraschall und die serielle Messung des Schwangerschaftshormons bHCG im Serum.
Ultraschall
Die Ultraschalluntersuchung bei potentiell schwangeren Patientinnen ist die Untersuchungsmethode der ersten Wahl, da dieses Verfahren (ohne Anwendung ionisierender Strahlen wie z.B. beim CT) problemlos für die Patientin und die Schwangerschaft angewendet werden kann. Für eine rasche Übersicht des ganzen Abdomens kann der transabdominelle Ultraschall verwendet werden, insbesondere dient diese Ultraschalluntersuchung dazu grössere Mengen freier Flüssigkeit im Rahmen einer Ruptur und Blutung in die freie Bauchhöhle zu entdecken. Für die detaillierte Untersuchung zur Diagnose und genaueren Lokalisation einer EUG verwendet man die transvaginale Sonografie.
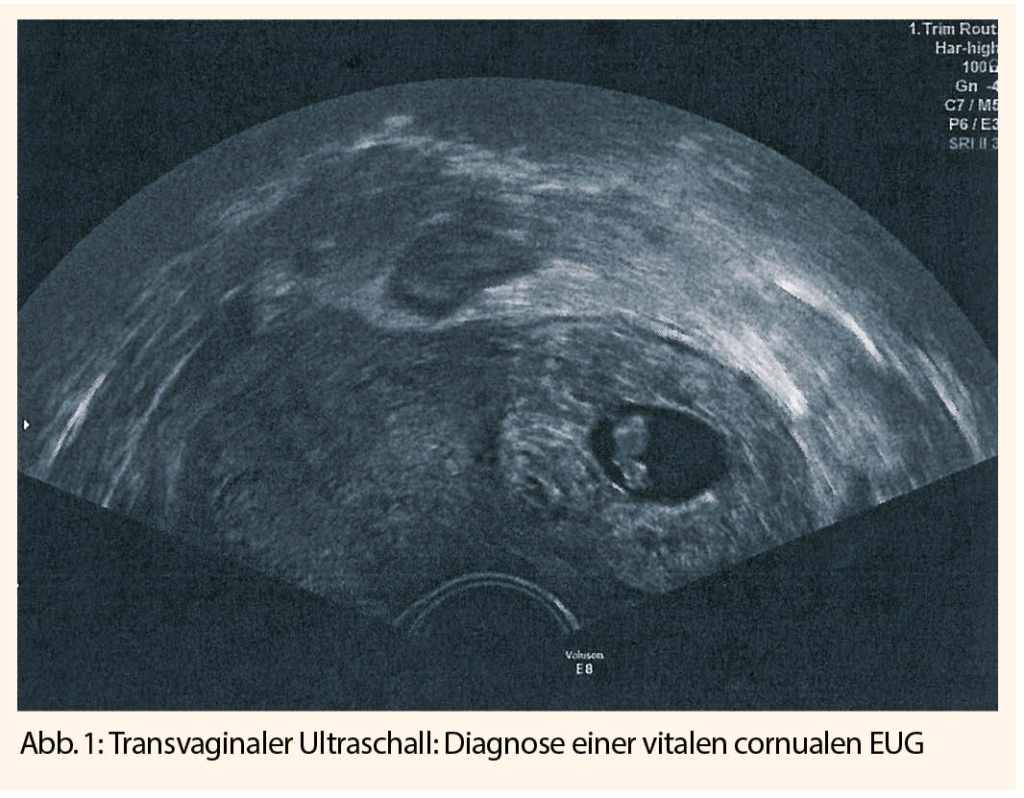
Eine EUG gilt als sonografisch gesichert, wenn man einen extrauterinen, inhomogenen Adnexbefund mit Gestationssack und Embryonalstruktur mit messbarer Schädel-Steiss-Länge darstellen kann. Die Darstellung einer positiven embryonalen Herzaktion untermauert die sonografische Diagnose (4).
Eine EUG gilt sonografisch als wahrscheinlich, wenn man einen extrauterinen, inhomogenen Adnexbefund (sogenanntes «blob sign») sieht, welcher sich klar vom ipsilateralen Ovar abgrenzen lässt. Ebenso gilt die EUG als wahrscheinlich, wenn man einen inhomogenen Adnexbefund darstellt, der einen leeren Gestationssack enthält («bagel sign»). Die Sensitivität und Spezifität dieser Untersuchungen sind hoch (5). Gleichzeitig ist die Absenz einer intrauterinen Schwangerschaft bei positivem Schwangerschaftstest suggestiv für das Vorliegen einer EUG. Je nach Amenorrhoedauer sollte normalerweise zwischen der 4. – 6. SSW eine intrauterine Doppelringstruktur zu sehen sein, ab ca. 5+3 SSW ein Dottersack nachgewiesen werden und zwischen 6+0 und 6+3 SSW eine
beginnende Embryonalanlage im Uteruscavum zu sehen sein (6).
Die Doppler-Ultraschalluntersuchung kann bei der Visualisierung einer EUG hilfreich sein, da Trophoblastgewebe einen hohen systolischen Fluss anzeigt. Gelegentlich kann man das Flusssignal als sog. «ring of fire» um einen inhomogenen Adnexbefund darstellen.
Leider schliesst die Abwesenheit dieses Dopplerphänomens eine EUG nicht aus und gleichzeitig kann eine Corpus luteum des Ovars das «ring of fire» Phänomen imitieren (7).
Serielle bHCG-Messungen
Das schwangerschaftsspezifische Hormon «humanes Choriongonadotropin» beschreibt in der Frühschwangerschaft einen charakteristisch exponentiell verlaufenden Anstieg. Beim Vorliegen einer intakten intrauterinen Schwangerschaft kann man als Faustregel von mindestens einer Verdoppelung innerhalb von 48 Stunden ausgehen. Dieser exponentielle Anstieg ist in der Regel bis zum 41. Schwangerschaftstag nachweisbar, danach steigt das Hormon langsamer an.
Um zwischen beginnendem Abortgeschehen, intakter intrauteriner Frühschwangerschaft und ektoper Schwangerschaft zu unterscheiden, benötigt man in der Regel serielle Messungen des bHCGs, falls zum Untersuchungsdatum sonografisch keine intrauterine Schwangerschaft gesehen werden kann und Zeichen einer EUG nicht gesichert werden können (sowohl klinisch als auch sonografisch).
Eine Studie aus dem Jahr 2004 von Barnhart et al. hat gezeigt, dass aber auch bei einem langsameren, nicht exponentiellen Anstieg in der seriellen Messung, eine intakte intrauterine Schwangerschaft nachgewiesen werden konnte. Der niedrigste Anstieg betrug 53% innerhalb von 48h in dieser Studie (8). Eine Plateaubildung oder ein Abfall des Hormons spricht für eine ektope Schwangerschaft oder ein Abortgeschehen.
Ein häufig diskutierter Begriff ist die sogenannte «discriminatory zone» des bHCG. Dieser Begriff beschreibt den Hormonwert, ab dem beim Vorliegen einer intrauterinen Schwangerschaft in der sonografischen Untersuchung ein Gestationssack gesehen werden sollte (9).
Bei Verwendung der transvaginalen Sonografie liegt dieser Wert zwischen 1500 und 2000mU/ml. Wenn man bei der Diagnostik höhere Werte ansetzt, erhöht sich das Risiko einer unentdeckten ektopen Schwangerschaft, bei niedrigen cut-off Werten erhöht sich das Risiko mit einer evtl. eingeleiteten Abort-Therapie eine entstehende intrauterine Schwangerschaft zu unterbrechen.
Therapie der EUG
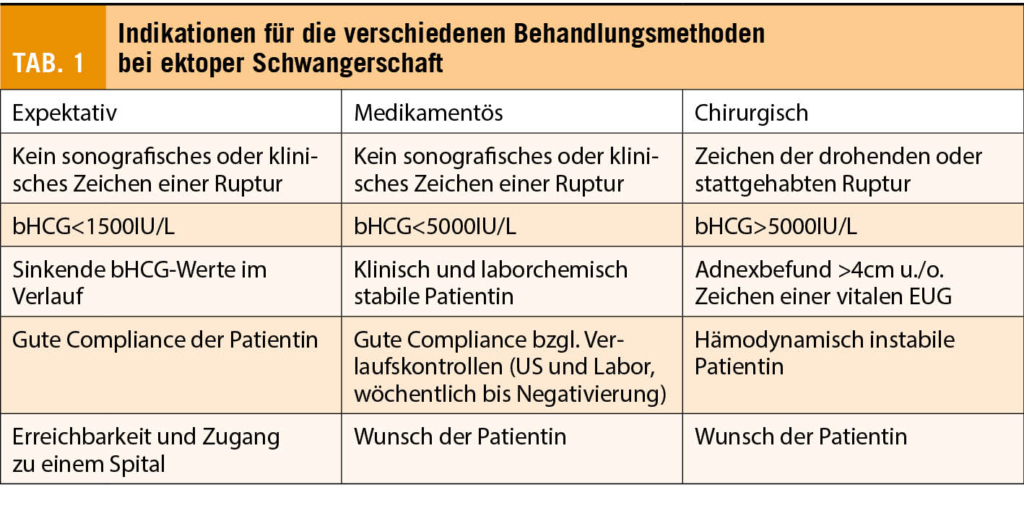
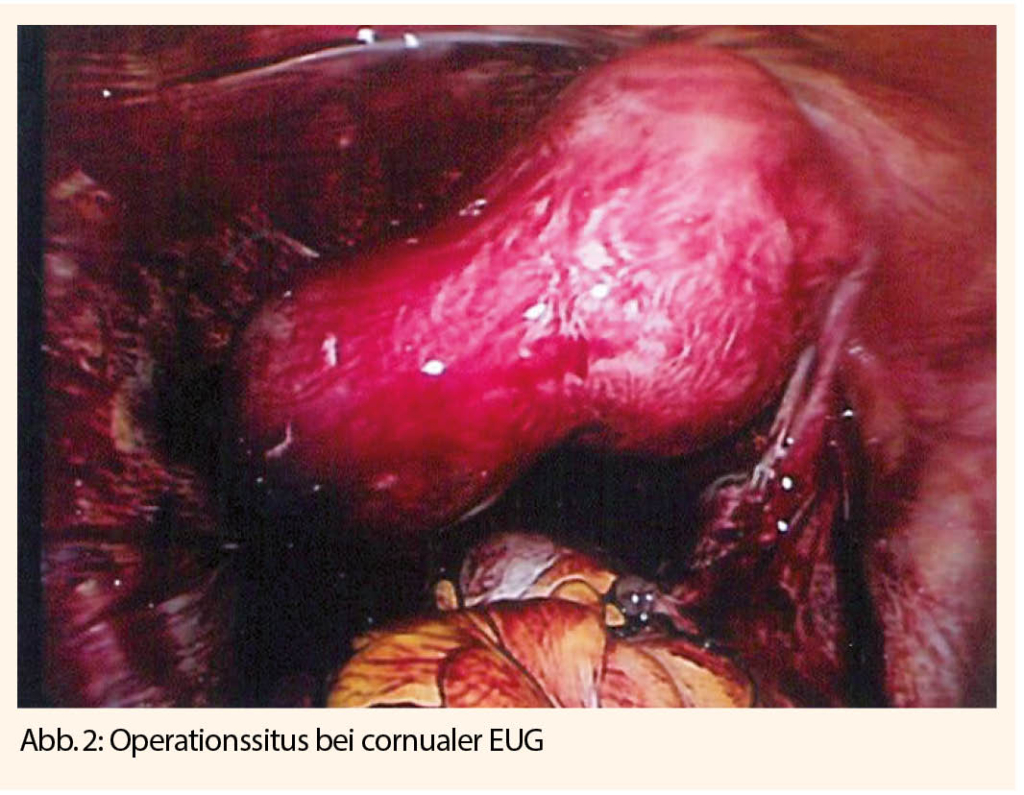
Bei der Therapie der EUG kann prinzipiell zwischen chirurgischer Therapie, medikamentöser Therapie und expektativem Verhalten unterschieden werden (10). Die chirurgische Therapie, meist im Sinne einer minimal-invasiven Laparoskopie ist bei der klinisch und sonografisch diagnostizierten EUG sicher und effektiv.
Je nach klinischer Situation der Patientin, intraoperativem Situs und Wunsch nach maximalem Fertilitätserhalt wird entweder eine Salpingotomie oder eine Salpingektomie durchgeführt. Mehrere Untersuchungen haben jedoch keinen sicheren Vorteil für die zukünftige Fertilität bei Salpingotomie vs. Salpingektomie gezeigt, insbesondere, wenn die kontralaterale Tube makroskopisch unauffällig aussieht. Jedoch besteht ein leicht erhöhtes Risiko der persistierenden ektopen Schwangerschaft nach Salpingotomie (4-15%) (11). Aus diesem Grund sind nach Operation die histologische Aufarbeitung des Präparates und serielle bHCG Kontrollen bis zur Negativität empfohlen.
Im Falle einer hämodynamisch instabilen Patientin sollte die operative Therapie mittels Lapartomie in Erwägung gezogen werden.
Die medikamentöse Behandlung der EUG besteht aus der systemischen Gabe von Methotrexat, entweder als i.m. Einmaldosis (i.d.R.50mg/m2) oder als wiederholte i.m. Gabe über 7 Tage (i.d.R.1mg/kg KG an Tag 1,3,5,7) (12). Methotrexat ist ein Folsäureantagonist, welcher auch als potentes Chemotherapeutikum eingesetzt wird und das Wachstum von schnell proliferierenden Zellen hemmt. Seit 1982 wird Methotrexat zur Behandlung der ektopen Schwangerschaft eingesetzt (13).
Die Bedingungen für eine medikamentöse Therapie sind: Keine klinischen Zeichen für Ruptur (Hämatoperitoneum, Abdominal-
schmerzen, Kreislaufinstabilität), bHCG <5000mlU/ml, keine fetale Herzaktion, Wunsch und Compliance der Patientin bzgl. Follow-up Untersuchungen.
Eine belgische single-center Studie von C. Beguin untersuchte 2019 die Erfolgsraten von Methotrexat bei der Behandlung der ektopen Schwangerschaften in Abhängigkeit vom prätherapeutischen bHCG Wert (14). Es konnte gezeigt werden, dass die Wirksamkeit für die Behandlung mit MTX ab einem gewissen bHCG-Wert (in der Studie war der cut-off Wert 2439IU/L), deutlich sinkt.
In der Studie war die Therapie bei einem prätherapeutischen Wert von < 2000 IU/L in 93% erfolgreich und in 7% erfolglos (sekundäre Operation notwendig). Bei den Werten zwischen 2000 und 3000 IU/L waren es 71% Erfolg und 29% Misserfolg, lag der Wert jedoch über 3000 IU/L führte die Behandlung nur noch in 12,5% zum Erfolg, 87,5% waren erfolglos.
Selbstverständlich können Frauen auch bei Werten über 3000 IU/L mit MTX behandelt werden, wenn sie vorgängig über diese Zahlen informiert werden.
In den letzten Jahren wurde versucht, die medikamentöse Therapie mit weiteren Medikamenten zu ergänzen. Das erfolgversprechendste Medikament ist der bekannte Progesteron-Rezeptorantagonist Mifepriston. Im Vergleich mit der alleinigen Therapie mit Methotrexat ergab die Kombination mit oralem Mifepriston in zwei randomisierten Studien eine leicht erhöhte Erfolgsrate für die kombinierte Therapie. Jedoch ergaben sich keine Daten bzgl. der zukünftigen Fertilität und die Patientinnenzahlen waren sehr klein (15,16). Hier werden weitere Studien erwartet, momentan ist die zusätzliche Gabe von Mifepriston kein etablierter Standard.
Das expektative Vorgehen kann bei Patientinnen angewendet werden, bei denen der bHCG Wert sehr niedig ist (< 1500lU/l) und im Verlauf nach 48 Stunden abfällt und welche klinisch und sonografisch kein Anhaltspunkt für eine Ruptur zeigen (17). Auch bei diesen Patientinnen ist eine genaue Aufklärung über die Risiken (z.B. Persistenz der EUG mit Gefahr der Ruptur und Schädigung der Tube) und eine gute Compliance für die wichtigen Nachkontrollen essentiell.
Psychische Folgen nach Diagnose und Behandlung der EUG
Die ektope Schwangerschaft kann eine lebensbedrohliche Erkrankung der Frau im fertilen Alter darstellen, gleichzeitig endet eine ektope Schwangerschaft praktisch nie mit der Geburt eines lebensfähigen Kindes. Die Diagnose aber auch die Therapie sind komplex und zum Teil sehr langwierig. Dies ruft bei den betroffenen Frauen eine extreme Stressreaktion hervor. Gefühle wie Traurigkeit über den Verlust der Schwangerschaft, Schock, Unverständnis, Schuld und Angst bezüglich der zukünftigen Fertilität sind häufig (18). In einer qualitativen Studie aus Irland wurden Frauen nach durchgemachter Diagnose und Therapie einer EUG (mit chirurgisch, medikamentösem und abwartendem Verhalten) interviewt.
Es zeigte sich, wie extrem die Enttäuschung bei Diagnosestellung ist (Verlust aller Hoffnung auf eine normale Schwangerschaft und ein gesundes Kind) und wie gross der Einfluss der ärztlichen Betreuung bei Diagnose und Therapie auf den Heilungs- und Verarbeitungsprozess ist.
Es ist von essentieller Bedeutung, die Verarbeitungsstrategien der einzelnen Patientinnen zu erkennen und zu bestärken. Nicht nur die Anerkennung des Verlustes der Schwangerschaft, sondern auch die Nachuntersuchungen und die Besprechung der zukünftigen Familienplanung mit Eingehen auf Risiko der erneuten EUG und evtl. reduzierter Fertilität, beeinflussen den Verlauf der Genesung und die Zufriedenheit der Frauen (19, 20).
Copyright bei Aerzteverlag medinfo AG
Stadtspital Waid und Triemli
Frauenklinik
Birmensdorferstrasse 497
8063 Zürich
nina.manz@triemli.zuerich.ch
Die Autoren haben im Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
- Die ektope Schwangerschaft ist ein potentiell lebensbedrohliches Krankheitsbild, welches uns im Klinikalltag mit einer relativ hohen Häufigkeit begegnet.
- Die Diagnose kann sehr schwierig und herausfordernd sein.
- Frauen sind durch langwierige Diagnoseprozesse und Therapie psychisch stark belastet.
- Die ärztliche Behandlung sollte ein follow-up Gespräch mit Erläuterung der nachfolgenden Fertilität und Besprechung des Risikos einer erneuten EUG beinhalten.
Messages à retenir
- La grossesse extra-utérine (ou ectopique) est un tableau clinique potentiellement mortel que nous rencontrons relativement souvent dans notre activité clinique.
- Le diagnostic est un défi qui peut s’avérer très difficile.
- A cause de processus diagnostiques fastidieux et longs la femme peut vivre une souffrance psychique importante.
- Dans le suivi, la prise en charge médicale devrait comporter un entretien de conseil au sujet de la fertilité ultérieure et du risque de récidive.
1. Centers for Disease Control and Prevention (CDC). Ectopic pregnancy–United States, 1990-1992. MMWR Morb Mortal Wkly Rep. 1995;44(3):46-48.
2. Alkatout I. Honemeyer U., Strauss A, etal. Clinical diagnosis and treatment of ectopic pregnancy, Obstet Gynecol Surv 2013;68:571
3. Zou S, Li X, Feng Y., et al. Comparison of the diagnostic values of circulating steroid hormones, VEGF-A, PIGF, and ADAM12 in women with ectopic pregnancy, J Transl Med 2013;11:44
4. Webster K, Eadon H, FishburnS, Kumar G, Guideline Committee
5. Ectopic pregnancy and miscarriage: diagnosis and initial management: summary of updated NICE guidance, BMJ.2019;367:I6283. Epub 2019 Nov 13
6. Nadim B, Infante F et al Morphological ultrasound types known as “blob” and “bagel” signs should be reclassified from suggesting probable to indicating definite ectopic pregnancy, Ultrasound Obstet Gynecol 2018;51:543-549
7. Goldstein SR, Snyder JR, Watson C, Danon M. Very early pregnancy detection with endovaginal ultrasound. Obstet Gynecol. 1988;72(2):200-204.
8. Kurjak A, Zalud I, Schulman H. Ectopic pregnancy: transvaginal color Doppler of trophoblastic flow in questionable adnexa. J Ultrasound Med. 1991;10(12):685-689. doi:10.7863/jum.1991.10.12.685
9. Barnhart KT, Sammel MD, Rinaudo PF, Zhou L, Hummel AC, Guo W. Symptomatic patients with an early viable intrauterine pregnancy: HCG curves redefined. Obstet Gynecol. 2004;104(1):50-55. doi:10.1097/01.AOG.0000128174.48843.12
10. Connolly A, Ryan DH, Stuebe AM, Wolfe HM. Reevaluation of discriminatory and threshold levels for serum β-hCG in early pregnancy. Obstet Gynecol. 2013;121(1):65-70. doi:10.1097/aog.0b013e318278f421
11. Capmas P, Bouyer J, Fernandez H. Treatment of ectopic pregnancies in 2014: new answers to some old questions. Fertil Steril. 2014;101(3):615-620. doi:10.1016/j.fertnstert.2014.01.029
12. Farquhar CM. Ectopic pregnancy. Lancet. 2005;366(9485):583-591. doi:10.1016/S0140-6736(05)67103-6
13. Lipscomb GH. Medical therapy for ectopic pregnancy. Semin Reprod Med. 2007;25(2):93-98. doi:10.1055/s-2007-970048
14. Beguin C, Brichant G, De Landsheere L, Tebache L, Karampelas S, Seidel L, Nisolle M. Use of methotrexate in the treatment of ectopic pregnancies: a retrospective single center study. Facts Views Vis Obgyn. 2020 Mar 27;11(4):329-335.
PMID: 32322829; PMCID: PMC7162662.
15. Tanaka T, Hayashi H, Kutsuzawa T, Fujimoto S, Ichinoe K. Treatment of interstitial ectopic pregnancy with methotrexate: report of a successful case. Fertil Steril. 1982;37(6):851-852. doi:10.1016/s0015-0282(16)46349-1
16. Hajenius PJ, Mol F, Mol BW, Bossuyt PM, Ankum WM, van der Veen F. Interventions for tubal ectopic pregnancy. Cochrane Database Syst Rev. 2007;2007(1):CD000324. Published 2007 Jan 24. doi:10.1002/14651858.CD000324.pub2
17. Gómez García MT, Aguarón Benitez G, Barberá Belda B, Callejón Rodríguez C, González Merlo G. Medical therapy (methotrexate and mifepristone) alone or in combination with another type of therapy for the management of cervical or inter-
stitial ectopic pregnancy. Eur J Obstet Gynecol Reprod Biol. 2012;165(1):77-81. doi:10.1016/j.ejogrb.2012.06.024
18. Banerjee S, Aslam N, Zosmer N, Woelfer B, Jurkovic D. The expectant management of women with early pregnancy of unknown location. Ultrasound Obstet Gynecol. 1999;14(4):231-236. doi:10.1046/j.1469-0705.1999.14040231.x
19. Bansen SS, Stevens HA. Women’s experiences of miscarriage in early pregnancy. J Nurse Midwifery. 1992;37(2):84-90. doi:10.1016/0091-2182(92)90142-p
20. Spillane N, Meaney S, O’ Donoghue K. Irish women’s experience of Ectopic pregnancy. Sex Reprod Healthc. 2018;16:154-159. doi:10.1016/j.srhc.2018.04.002
21. Svirsky R, Rozovski U, Vaknin Z, Pansky M, Schneider D, Halperin R. The safety of conception occurring shortly after methotrexate treatment of an ectopic pregnancy. Reprod Toxicol. 2009 Jan;27(1):85-7. doi: 10.1016/j.repro-
tox.2008.11.055. Epub 2008 Dec 3. PMID: 19103279
info@gynäkologie
- Vol. 10
- Ausgabe 6
- Dezember 2020