- Genitourinary syndrome of the menopause (GSM)
Rund 50% aller Frauen in der Peri- und Postmenopause haben Symptome des «Genitourinary syndrome of the menopause» (GSM). Dieses Syndrom umfasst, ergänzend zur vulvovaginalen Atrophie (VVA), zusätzlich die durch absinkende Hormonspiegel entstehenden Symptome der ableitenden Harnwege. Die Lebensqualität der betroffenen Frauen kann als Folge der Gewebeveränderungen stark eingeschränkt sein. Ziel dieser Übersicht ist die Darstellung der aktuellen Therapiemöglichkeiten und deren stufenweiser Einsatz.
Env. 50% de toutes les femmes autour et après la ménopause présentent des symptômes du « syndrome génito-urinaire de la ménopause » (GSM). Ce syndrome comprend, en plus de l’atrophie vulvo-vaginale (VVA), des symptômes des voies urinaires provoqués par les taux hormonaux qui baissent. La qualité de vie des femmes touchées peut en être fortement affectée en raison de l’altération des tissus dans la sphère uro-génitale. La présente revue décrit les modalités thérapeutiques actuelles et leur utilisation séquentielle.
Zu den typischen Symptomen des GSM gehören genitale Trockenheit, Dyspareunie, Irritation des Gewebes, Brennen und Juckreiz an der Vulva und Vagina sowie Dysurie, vermehrter Harndrang und Urge-Symptomatik. Die gängigen Behandlungsmethoden sind nur bei einem Teil der Patientinnen erfolgreich. Daher hat die Entwicklung neuer Methoden eine besondere Bedeutung.
Terminologie: VVA und GSM
Das «Genitourinary syndrome of the menopause» (GSM) ist ein Komplex von Symptomen der Vulva, der Vagina und der ableitenden Harnwege, welche bei postmenopausalen Frauen auftritt (1). Der neue Begriff wurde 2014 eingeführt. Die neue Terminologie GSM beinhaltet alle urogenitalen Symptome, die in der Menopause durch den Hormonabfall hervorgerufen werden können und sich an den Labien, am Introitus, an der Vagina, der Urethra und der Blase manifestieren. Ergänzend zu den Symptomen der VVA sind Belastungsinkontinenz, Dranginkontinenz und Bakteriurie typische Symptome des GSM. Sowohl die VVA als auch das GSM sind häufig unterdiagnostiziert und auch untertherapiert. Deshalb soll im ärztlichen Gespräch gezielt nach Beschwerden des GSM gefragt werden, zumal diese von vielen Frauen nicht offen kommuniziert werden (2).
Veränderungen des Gewebes und Konzepte zur Behandlung
Infolge der menopausal absinkenden Östrogenspiegel entwickelt sich eine progrediente, chronische Involution des vaginalen Gewebes. Die daraus entstehenden Symptome sind Ausdruck der morphologischen und funktionellen Veränderungen. Die Haut der Vagina wird dünner und weniger elastisch. Die Vagina wird insgesamt enger und kürzer. Die Oberfläche der Vagina erscheint trocken und es können Blutungen nach minimalem Trauma entstehen. Die Vulva wird atrophisch und leichter vulnerabel, insbesondere im Bereich der Klitoris. Die Atrophie der Vagina kann mit der Zeit zunehmen und die Lebensqualität deutlich negativ beeinflussen. Etwa 50 % der postmenopausalen Frauen entwickeln eine VVA (3). Da die Lebenserwartung immer mehr zunimmt, können die Beschwerden für die Dauer von mehr als einem Drittel der Lebenszeit bestehen.
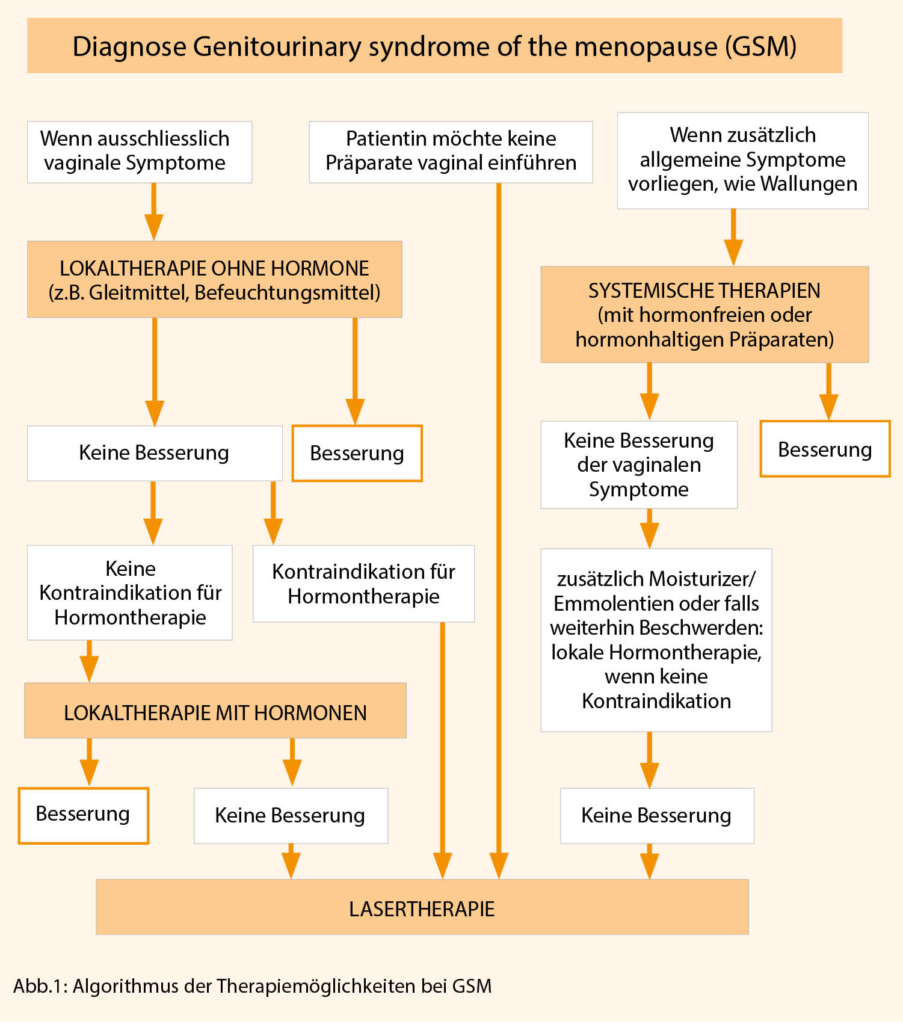
Zur Behandlung der Symptome der VVA werden meist folgende lokale Behandlungsoptionen genutzt (Abb. 1):
a) hormonfreie Produkte zur Lokaltherapie in Form von Gleitmitteln oder Befeuchtungsmitteln
b) lokale Hormontherapie.
Als weiteres Konzept etabliert sich momentan zunehmend die Lasertherapie der Vagina und der Vulva. Mit DHEA gibt es zudem ein neues, weiteres Konzept zur lokalen Behandlung.
Gleitmittel und Befeuchtungsmittel
Internationalen Leitlinien entsprechend sind Gleitmittel und Befeuchtungsmittel die Therapie der ersten Wahl zur Therapie der VVA. Der Hauptunterschied zwischen vaginalen Gleitmitteln und Befeuchtungsmitteln ist der Zeitpunkt der Anwendung.
Vaginale Gleitmittel sind indiziert bei Frauen, deren Hauptsorge die vaginale Trockenheit beim Geschlechtsverkehr ist. Gleitmittel können die Trockenheit kurzfristig lindern und die Dyspareunie lindern. Vaginale Befeuchtungsmittel sind nicht-lösliche hydrophile Polymere mit der Eigenschaft der Bioadhäsivität. Sie können häufiger verwendet werden als allein in Zusammenhang mit sexueller Aktivität, sind länger wirksam, verbessern die Feuchtigkeit der Vaginalhaut und reduzieren den pH-Wert.
Die initiale Dosierung besteht in der lokalen Anwendung am Abend, vor dem Schlafengehen, an 7 bis 10 aufeinanderfolgenden Tagen. Anschliessend erfolgt meist eine Erhaltungstherapie durch zwei Applikationen pro Woche. Die am häufigsten verwendeten Befeuchtungsmittel basieren auf Hyaluronsäure. Bei bestimmungsgemässer Anwendung können die auf Hyaluronsäure basierenden Produkte die Symptome der vaginalen Trockenheit lindern.
Hormonelle Behandlungen
Internationale Leitlinien empfehlen zur Behandlung der VVA, einschliesslich Dyspareunie, die lokale Hormontherapie als zweiten Schritt für den Fall, dass vaginal applizierte Gleit- und Befeuchtungsmittel nicht die gewünschte Wirkung haben (4).
Für die lokale Therapie stehen Estriol und Estradiol zur Verfügung, die Applikation erfolgt in Form von Gels, Cremes, Ovula, Tabletten, oder Ringen. Vaginal applizierte Estrogene zeigten sich in Studien mit 6- bis 12-monatiger Dauer wirksamer als Gleit- und Befeuchtungsmittel.
Die häufigste Empfehlung zur Dosierung ist die tägliche einmalige Applikation vaginal für die Dauer von 2 Wochen und anschliessend eine Erhaltungstherapie durch die Anwendung zweimal pro Woche (5).
Bei Anwendung in niedriger Dosierung innerhalb der Empfehlung für das verwendete Präparat ist es nicht erforderlich, zusätzlich ein Progesteronpräparat zur Endometriumprotektion einzusetzen. In grossen Observationsstudien zeigte sich kein erhöhtes Risiko für ein Endometriumkarzinom bei Frauen, die Estrogene vaginal verwendeten.
Bei erhöhtem Risiko für ein Endometriumkarzinom oder bei höher dosierter vaginaler Oestrogengabe werden Kontrollen mittels Transvaginalsonographie oder der intermittierende Einsatz von Progesteron empfohlen. Vaginale Blutungen oder Spotting bei postmenopausalen Frauen unter lokaler Hormontherapie müssen unbedingt abgeklärt werden mit Ultraschall und/oder einer Histologie. Ein bestehendes oder früheres Mammakarzinom bzw. entsprechender Verdacht gelten als Kontraindikation. 12-13% der Frauen zeigen trotz lokaler Hormontherapie weiterhin Beschwerden eines GSM.
DHEA
Die Wirksamkeit von DHEA (Dehydroepiandrosteron) als Lokaltherapie ist durch mehrere Studien belegt, unter anderem durch eine prospektive randomisierte Placebo-kontrollierte Phase III-Studie (9). DHEA führt nicht zu Veränderungen am Endometrium, weder sonographisch noch histologisch. DHEA führt nicht zur Erhöhung der Estrogenspiegel. Jedoch ist auch DHEA für Frauen mit Mammakarzinom kontraindiziert. DHEA ist in der Schweiz zur Lokalbehandlung seit September 2020 zugelassen.
Vaginale Lasertherapie
Die Lasertherapie ist ein neues Konzept bei Patientinnen mit VVA, sie hat eine wachsende Akzeptanz und Verbreitung. Der grundsätzliche Mechanismus des Lasereffekts basiert auf der Bildung supraphysiologischer Hitze mit nachfolgender lokaler Hitzeschockreaktion. Zur vaginalen Lasertherapie wurden verschiedene Systeme eingesetzt. Die meisten wissenschaftlichen Daten basieren auf der CO2-Lasertechnologie. Dieser Laser besteht aus infraroten Strahlen, die Hitze erzeugen und das Wasser in den Zellen des behandelten Gewebes vaporisieren.
Die CO2-Lasertechnologie wird in der vaginalen Therapie eingesetzt, um eine Regeneration mit minimalem Aufwand zu erreichen. So werden die Elastizität und die Hydratation der Vaginalwand verbessert, was zu einer Linderung der Beschwerden führt.
Das fraktionierte Lasersystem kann in tieferen Schichten der Haut der Vagina wirken und sowohl die extrazelluläre Matrix reaktivieren als auch die Bildung von Kollagen, was zu Veränderungen des vaginalen Gewebes führt, mit nur minimalem Trauma der oberflächlichen Schicht.
Studienergebnisse zur vaginalen Lasertherapie
Salvatore et al. veröffentlichten eine Studie zur Behandlung der VVA bei postmenopausalen Frauen (6). Die Linderung der Symptome der vaginalen Trockenheit, des vaginalen Brennens und des vaginalen Juckens, der Dyspareunie und der Dysurie war statistisch signifikant (p< 0,001).
Weitere Studien zeigten ebenfalls positive Ergebnisse zur Praktikabilität und Wirksamkeit. Dies konnte durch eigene Resultate mit dem für diese Indikation zugelassenen CO2-Laser MonaLisa Touch (Fa. Lasermed AG, Roggwil) bestätigt werden (7).
Aktuell wurde die grösste Studie zur Wirksamkeit der CO2-Lasertherapie bei VVA veröffentlicht, eine Multicenterstudie mit den Daten von 645 Patientinnen. Bei allen Patientinnen fand sich nach der Laserapplikation im Vergleich zu der Situation vor der Therapie eine signifikante Verbesserung der Symptome Dyspareunie, Schmerzen im Introitus vaginae, vaginale Trockenheit, Jucken, Brennen und pH-Wert-Veränderung bei gleichzeitig guter Toleranz der Behandlung (8).
Randomisierte kontrollierte Studien mit Langzeitdaten zur Sicherheit und Wirksamkeit der Lasertherapie liegen noch nicht vor und dementsprechend machte die amerikanische FDA 2018 darauf aufmerksam, dass die Lasertherapie des GSM nicht freigegeben oder genehmigt sei (11). Dieser Hinweis war wichtig, um einer Ausweitung von Indikationen jenseits der Zulassung entgegenzuwirken. Jedoch ist er nicht sehr präzise – es gibt unterschiedliche Lasergeräte mit unterschiedlicher FDA-Zulassung. Heute wird die Warnung aufgrund von Sicherheitsdaten als fraglich begründet diskutiert (12).
Praktische Aspekte der Lasertherapie
Die Laserbehandlung wird gut toleriert. Nebenwirkungen sind selten. Die meisten Patienten erleben die vaginale Anwendung nicht als schmerzhaft. Es ist keine Vorbehandlung und keine Nachbehandlung erforderlich. Zumeist werden 3 Lasertherapien im Abstand von 4 Wochen durchgeführt, gefolgt von einer Auffrischung nach Ablauf eines Jahres in Form von einer Sitzung.
Die Lasertherapie der Vulva wird im Vergleich zu vaginaler Lasertherapie mit einem anderen Applikator durchgeführt. Um auch die Lasertherapie der Vulva schmerzfrei durchführen zu können hat sich die Vorbehandlung mit Emla® Creme 5% unmittelbar vor der Laserbehandlung bewährt. Die Lasertherapie ist aktuell noch keine Pflichtleistung der Krankenkassen, dies muss den Patientinnen unbedingt mitgeteilt werden.
Zum Schluss sei erwähnt, dass weitere nichtpharmakologische Therapieoptionen zur Verfügung stehen, wie insbesondere Sexualtherapie und Becken-Bodentherapie, welche gemäss amerikanischer Konsensusempfehlungen bei durch GSM verursachten sexuellen Beschwerden zum Einsatz kommen können (10).
Bei diesem Artikel handelt es sich um einen Zweitabdruck des in «der informierte arzt» 11-2020 erschienen Originalartikels.
Copyright bei Aerzteverlag medinfo AG
Spezialarzt Gynäkologie und Geburtshilfe FMH
Praxis am Bahnhof Rüti
Dorfstrasse 43, 8630 Rüti
meden@praxisambahnhof.ch
Der Autor hat deklariert, dass in Zusammenhang mit diesem Artikel keine Interessenskonflikte bestehen.
- Ziel der Lokaltherapie bei Frauen mit vulvovaginaler Atrophie ist die Optimierung der Lebensqualität.
- Therapie der ersten Wahl sind Gleit- und Befeuchtungsmittel.
- Therapie der zweiten Wahl sind Hormonpräparate.
- DHEA als Lokaltherapie ist eine neue lokale Behandlungsmöglichkeit.
- Die Lasertherapie ist eine weitere Option, insbesondere für Frauen,
bei denen eine Hormonersatztherapie kontraindiziert ist oder nicht gewünscht wird.
Messages à retenir
- L’ objectif d’un traitement local pour la femme souffrant d’atrophie vulvo-vaginale est l’optimisation de la qualité de vie.
- Le premier choix thérapeutique sont les lubrifiants et les préparations hydratantes.
- Le deuxième choix thérapeutique sont les préparations hormonales.
- Le DHEA, en application locale, représente une nouvelle possibilité de traitement. .
- Le traitement au Laser (CO2 fractionné) est une option supplémentaire, notamment pour les femmes présentant des contre-indications ou ne souhaitant pas de thérapie hormonale (systémique).
1. Portman DJ et al.: Genitourinary syndrome of menopause: new terminology for
vulvovaginal atrophy from the International Society for the Study of Women’s Sexual
Health and the North American Menopause Society. J Sex Med. 2014
Dec;11(12):2865-72.
2. Kingsberg S, Wysocki S, Magnus L, Krychman M. J. Sex Med. 2013 Jul;10(7)
1790-9
3. Nappi RE, Kokot-Kierepa M. Women’s voices in the menopause: results from an
international survey on vaginal atrophy. Maturitas 2010;67:233–8.
4. The NAMS 2017 Hormone Therapy Position Statement Advisory Panel. The 2017
hormone therapy position statement of the North American Menopause Society.
Menopause 2017, 24, 728–753
5. Salwowska, NM et al.: Physiochemical properties and application of hyaluronic
acid: A systematic review. J. Cosmet. Dermatol. 2016, 15, 520–526
6. Salvatore S et al.: A 12-week treatment with fractional CO2 laser for vulvovaginal
atrophy: a pilot study. Climacteric 2014;17:363–9.
7. Meden H, Zeller C.: Vulvovaginale Atrophie (VVA): CO2-Lasertherapie als neues
Konzept. In: Rabe T (Hrsg.). Seminar in Gynäkologischer Endokrinologie – Band
6: Update, Trends & Fallberichte. Ein Praxisleitfaden, Baier Digitaldruck Heidelberg
2017, S. 300-304, ISBN 978-3-00-053173-6.
8. Filippini M et al.: Efficacy of fractional CO2 laser treatment in postmenopausal
women with genitourinary syndrome: a multicenter study. Menopause. 2020
Jan;27(1):43-49.
9. Labrie, F et al. Efficacy of intravaginal dehydroepiandrosterone (DHEA) on moderate
to severe dyspareunia and vaginal dryness, symptoms of vulvovaginal atrophy,
and of the genitourinary syndrome of menopause. Menopause 2018, 25,
1339–1353
10. Faubion St. S et al: Consensus Recommendations: Management of genitourinary
syndrome of menopause in women with or at high risk for breast cancer:
consensus recommendations from The North American Menopause Society and
The International Society for the Study of Women’s Sexual Health. Menopause:
June 2018;25:596-608
11. https://www.fda.gov/medical-devices/safety-communications/fda-warns-againstuse-
energy-based-devices-perform-vaginal-rejuvenation-or-vaginal-cosmetic.
12. Guo J. et al.: Vaginal laser treatment of genitourinary syndrome of menopause:
does the evidence support the FDA safety communication? Menopause 2020;27:
1177-1184
info@gynäkologie
- Vol. 11
- Ausgabe 1
- März 2021