- Moderne bildgestützte Radiotherapie – Techniken und Perspektiven
In der modernen Radioonkologie ist die bildgestützte Einstellung inzwischen ein fester Bestandteil der Therapie. Die neueste Entwicklung in diesem Bereich ist die Zusammenführung der MRI-Bildgebung mit einem Linearbeschleuniger zu einem sogenannten MRI-LINAC. Dieser Beitrag beleuchtet die aktuelle Entwicklung und Vorteile der modernen bildgeführten Radiotherapie inklusive der neuesten Technologie des MRI-LINAC.
Dans la radio-oncologie moderne, le guidage par l’ image fait désormais partie intégrante de la thérapie. Le dernier développement dans ce domaine est la combinaison de l’ imagerie IRM avec un accélérateur linéaire pour former ce qu’ on appelle un IRM-LINAC. Cet article met en lumière le développement actuel et les avantages de la radiothérapie moderne guidée par l’ image, y compris la toute dernière technologie de l’ IRM-LINAC.
In der modernen Radioonkologie ist heutzutage die sogenannte bildgestützte Einstellung, also die Nutzung diagnostischer Verfahren zur Lokalisation des Zielvolumens, ein fester Bestandteil der Therapie. Mit dem Einsatz intensitätsmodulierter Techniken und Fortschritten bei Geräten und Software wurden die Bereiche, die «unbeabsichtigt» mitbehandelt werden, immer kleiner.
Eine weitere Reduktion der Dosisbelastung für Normalgewebe konnte nur noch mit einer Erhöhung der Präzision bei der Applikation weiter reduziert werden. In den letzten 15 Jahren wurden somit stetig neue Techniken entwickelt, mit denen mittels verschiedenster Bildgebung die erforderlichen Sicherheitsabstände zwischen klinischem Zielbereich (Clinical target volume, CTV) und tatsächlichem Planungsvolumen (Planning target volume, PTV), weiter reduziert werden konnten. Hinzu kamen neue Techniken zur Kontrolle der Atembeweglichkeit, diese werden als Gating bzw. Tracking bezeichnet.
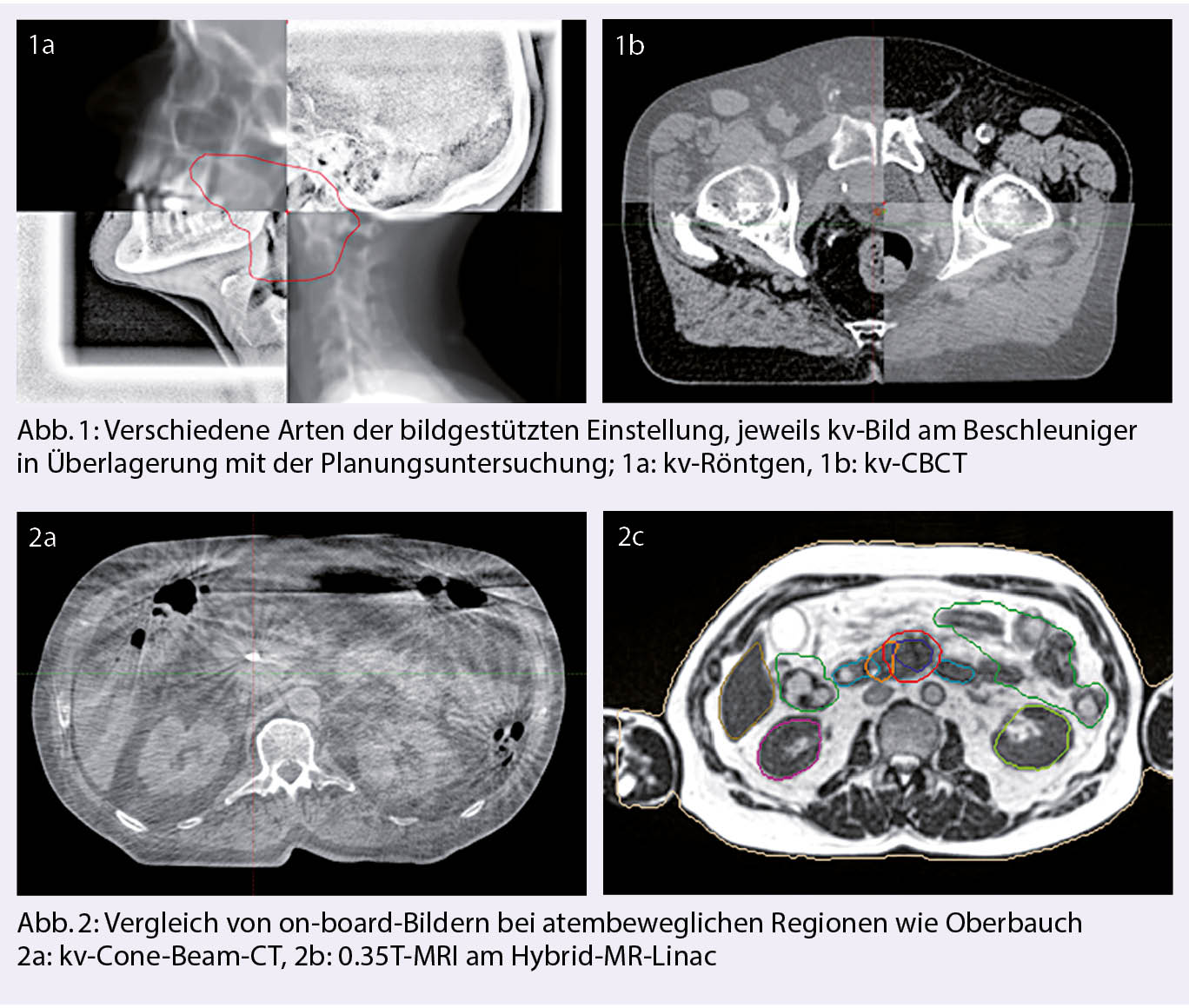
Ursprünglich erfolgte die Bildgebung mit Röntgenbildern, indem die knöchernen Strukturen in Übereinkunft gebracht wurden. Im 21. Jahrhundert kam die Entwicklung des heutzutage zum Standard gehörenden kv-Cone-Beam-CT (CBCT), bei dem mit einer Rotation einer an den Linearbeschleuniger angebrachten kv-Röhre ein CT generiert wird (Abb. 1). Dieses lässt neben der knöchernen Übereinstimmung auch bis zu einem gewissen Grad die Beurteilung der Weichteile und damit auch z.B. der inneren Organe wie Blase oder Darm zu. Diese sogenannte «Image Guided Radiotherapy» (IGRT) konnte sich in klinisch merkbar reduzierter Toxizität niederschlagen und legte den Grundstein für die Einführung von stereotaktischen Techniken (1).
Zusätzlich zur Einstellungs-Bildgebung wurden auch Techniken entwickelt, um Bewegungen des Ziels während der Bestrahlung zu überwachen. Dazu gehören implantierte Goldmarker oder Transponder mit elektromagnetischem Signal, Oberflächenscanner, sowie externe Aufnahme der Atemkurven. Diese Methoden lassen sich alle mit der Radiotherapie koppeln, so dass ausserhalb der prädefinierten Toleranz diese automatisiert gestoppt wird. Diese Techniken haben nochmals die Präzision bei beweglichen Organen deutlich erhöht (2).
Mit der zunehmenden Entwicklung der Radiotherapie hin zu stereotaktischen hypofraktionierten Verfahren, d.h. Applikation einer ablativen Dosis in wenigen Fraktionen, nimmt die Bedeutung dieser intrafraktionellen Überwachung, sowie Techniken zur Verringerung der Sicherheitsabstände stetig zu. Dies brachte die Hybrid-Kombination aus MRI und Beschleuniger, die 2014 erstmals klinisch beschrieben wurde (3).
In der Schweiz wurde diese Technik erstmals im April 2019 am USZ eingeführt. Bis heute wurden hier über 200 Patienten damit behandelt. Anfang 2020 nahm das Hôpital Riviera-Chablais in Rennaz den zweiten MRI LINAC in der Schweiz in Betrieb. Aktuell gibt es zwei kommerzielle Anbieter von MRI LINAC Geräten: der «MRIDIAN» von ViewRay (ViewRay Technologies Inc, Oakwood Village, Ohio) und «Unity» von Elekta (Elekta AB, Stockholm, Sweden).
Anwendungsgebiete der IGRT
Stereotaktische Strahlentherapie
Die intensitätsmodulierte Strahlentherapie, welche hoch-konformale Bestrahlung insbesondere von irregulär konfigurierten Zielvolumina erlaubt, hat sich in der kurativen Behandlung von Tumoren der Lunge, der Kopf-Hals- und Becken-Region mit Nutzung der IGRT mittels CCBCT als Standard etabliert.
Neben dieser Technik gewinnen stereotaktische Hochpräzisionsverfahren zunehmend an Bedeutung. Diese Techniken ermöglichen die Applikation einer hohen, biologisch aktiven Einzeldosis im Tumor, mit steilem Dosisabfall in der Umgebung, und somit die Schonung des umliegenden gesunden Gewebes.
Stereotaktische Radiochirurgie von Hirnmetastasen
Für intakte Hirnmetastasen hat sich die Radiochirurgie, bei der eine sehr hohe Strahlendosis in nur einer Sitzung appliziert wird, als Standardbehandlung etabliert. Für dieses Verfahren wird je nach Technik CBCT und/oder kv-Röntgenbilder in Serie zur Einstellung genutzt. Zunehmend wir die Radiochirurgie inzwischen nicht nur bei solitären Metastasen, sondern auch bei 4-10 Hirnmetastasen durchgeführt, nachdem erste Studien keine Einbusse im Gesamtüberleben zeigen konnten (4).
Extrakranielle stereotaktische Strahlentherapie (SBRT)
Aktuell ist die SBRT für Tumore der Lunge im Frühstadium als Alternative zur Operation, sowie bei Lungen-, Leber- und Knochenmetastasen fest etabliert. Es können dabei lokale Kontrollraten von 80-90% nach 3 Jahren erreicht werden, sofern aufgrund von Grösse und Lage der Metastasen eine ablative Strahlendosis appliziert werden kann (5). Je nach Lokalisation reicht die Einstellung mittels CBCT aus, jedoch sind bei abdominellen Zielen auch Techniken zur Atemkontrolle und –Überwachung nötig. (Abb. 2)
Adaptive Strahlentherapie
Technologische Weiterentwicklungen im Bereich der automatisierten Konturanpassung und Bestrahlungsplanung erlaubten die Einführung der adaptiven Bestrahlungsplanung.
Die Rationale für die adaptive Radiotherapie ist, geometrische oder biologische Veränderungen des Tumors oder von Risikoorganen während einer Strahlenbehandlung zu detektieren und eine Anpassung des Bestrahlungsplans durchzuführen. Dies erhöht die Präzision und Wirksamkeit der Therapie im Tumor, bei gleichzeitig besserer Schonung von Normalgewebe.
Grundsätzlich wird die adaptive Planung bereits in der klinischen Routine gelebt, indem bei relevanten systematischen Veränderungen der Anatomie eine Planadaptation durchgeführt wird (z.B. Verkleinerung eines Bronchialkarzinoms im Laufe der Behandlung). Tagesaktuelle Veränderungen (z.B. täglich wechselnde anatomische Lage von Risikoorganen) oder Reaktionen des Tumors bleiben hierbei bisher unberücksichtigt.
Idealvorstellung einer adaptiven Strahlentherapie ist jedoch Änderungen am Bestrahlungsplan gemäss der aktuellen Anatomie kurz vor der tatsächlichen Strahlenbehandlung durchführen zu können, mit anschliessend sofortiger Applikation der Dosis gemäss den aktuellen Gegebenheiten. Hierfür existieren bereits diverse technische und technologische Ansätze, von denen die Erfahrungen mittels MRI-Linac im Moment am weitesten fortgeschritten ist. Auf die technischen Herausforderungen und klinischen Möglichkeit soll im Folgenden eingegangen werden.
MRT-geführte Radiotherapie (MRgRT)
Wie bereits ausgeführt haben in der Vergangenheit beträchtliche technologische Entwicklungen zu einer Verbesserung der Präzision in der Radiotherapie geführt. Am (vorläufigen) Ende der Entwicklung der IGRT steht die Einführung der MRgRT. Bestrebungen die MRI-Bildgebung mit ihrem besseren Weichteilkontrast in die Bestrahlung zu integrieren, bestehen bereits seit Jahrzenten. Eine der grossen Herausforderungen in der Entwicklung lag in der Wechselwirkung zwischen dem Magnetfeld des MRIs, welches permanent wirkt, und dessen Auswirkungen auf die Bahn der durch die Photonenstrahlung erzeugten Sekundärelektronen. Dies muss in den Berechnungen während des Planungs-Prozesses berücksichtigt werden.
Die Gefahr der geometrisch verzerrten Darstellung der Anatomie im MRI («geometrical distortion») ist in der Radio-Onkologie äusserst relevant, insbesondere bei der Stereotaxie, in welcher eine Präzision bis auf wenige Millimeter gefordert ist. Diese «geometrical distortion» nimmt zu, je weiter weg sich die darzustellende Struktur vom Zielpunkt befindet. Zudem führen Unterschiede in der Magnetisierbarkeit von Eigen- oder Fremdgewebe im Patienten – z.B. Metallimplantate, Clips oder Lufthöhlen – auch zu geometrischen Verzerrungen. Dies muss bei der Selektion von Patienten für die Behandlung am MRI-LINAC bedacht werden.
Von dem unter Versuchsbedingungen erfolgreichen «proof of concept» der Anwendung dieser Hybrid-Technik bis zur ersten klinischen Behandlung an einem MRI-LINAC 2014 vergingen einige Jahre (3). Seither hat die Verfügbarkeit der MRI-LINAC Geräte kontinuierlich zugenommen, mit zuletzt weltweit insgesamt 60 verfügbaren Geräten der zwei oben genannten Firmen (6, 7). Eine weitere Zunahme ist in nächster Zeit zu erwarten. Denn nebst dem verbesserten Weichteilkontrast bietet sich mit den neuen Hybridgeräten auch das erste Mal die Möglichkeit die Anatomie live unter Bestrahlung abzubilden. Damit ist ein «Live-Tracking» des Behandlungsziels möglich. Dies ist insbesondere bei atemvariablen Tumoren von Vorteil, da damit das zu bestrahlende Volumen kleiner gehalten werden kann: indem in Atemanhaltetechnik in einer vordefinierten Atemphase bestrahlt wird, muss die Läsion nicht mit Ihrer ganzen Amplitude erfasst werden. Ein weiterer Vorteil dieses «Live-Trackings» ist die Möglichkeit zum Verzicht auf implantierte Marker, da damit ein invasiver Eingriff vermieden wird und weder Röntgenstrahlen noch elektromagnetische Wellen zur intrafraktionellen Überwachung benötigt werden.
Nicht nur die Atemvariabilität der Organe ist ein bekanntes Phänomen, auch die Lagevariabilität der inneren Organe, insbesondere Magen und Darm, können bei der Strahlentherapie relevant werden (8). Am MRI-LINAC wird diese Variabilität berücksichtigt, indem täglich in Bestrahlungsposition eine Aufnahme durchgeführt wird und anhand dieser der Bestrahlungsplan täglich in ca. 15-20 Minuten adaptiert wird, während der Patient noch auf dem Behandlungstisch liegt. (Abb. 3)
Diese verlässlichere Darstellung der Lage der Normalgewebsstrukturen, des Tumors sowie deren Lagebeziehung zueinander hat zusammen mit den oben erwähnten weiteren Vorteilen des MRI-LINACs den Weg zur weiteren Dosiserhöhung innerhalb des Zielvolumens unter gleichzeitiger Schonung kritischer Risikostrukturen geebnet und damit die sogenannte Therapeutische Breite verbessert (9).
Dem erwarteten Nutzen bei ausgewählten Indikationen gegenüberzustellen ist der erhöhte Aufwand einer MRT-geführten Radiotherapie, der auch einhergeht mit einer deutlich längeren Liegezeit für den Patienten in immobilisierter Position. Diese erstreckt sich von im Mittel circa 40 Minuten, wenn keine tägliche Planadaptation erfolgt bis zu 47-60 Minuten, wenn eine Planadaptation erfolgt (10, 11). Der Arbeitsablauf im interprofessionellen Team wird in (Abb. 4) dargestellt.
Ein weiterer Aspekt ist, dass Radio-OnkologInnen heutzutage v.a. in der Beurteilung von CT-Bildern vertraut sind, da bisher auf dem CT, häufig gestützt durch fusionierte PET- oder MRI-Bildgebung, die Bestrahlungsplanung stattfindet und die IGRT bisher hauptsächlich mit CBCT erfolgt. Mit dem MRI-LINAC ist der Gebrauch von MRI-Bildern nicht mehr nur auf den initialen Planungsprozess beschränkt, sondern wird zum Haupt-Arbeitsinstrument. Folglich ist die Fähigkeit zur Interpretation von MRI-Bildern bei der Arbeit an der Maschine essentiell. Mittlerweile sind am MRIDIAN auch Aufnahmen in verschiedenen Sequenzen möglich – damit gewinnen radiologische Kenntnisse in der Radio-Onkologischen Weiterbildung an Bedeutung.
Aktuelle klinische und wissenschaftliche Fragestellungen
Die beschriebene adaptive Strahlentherapie wird die Radio-Onkologie entscheidend verändern. Dafür gilt es basierend auf den bisherigen Daten und praktischen Erfahrungen wichtige Aspekte zu verbessern und wissenschaftlich zu fundieren. Nur so wird eine flächendeckende und praktisch mögliche Umsetzung tatsächlich in greifbare Nähe kommen. Dazu gehören folgende Aspekte:
- Verbesserung des adaptiven Workflows: Verkürzung der Bildakquisitionszeit; Automatisierung der Konturadaptierung; Optimierung der Bestrahlungsplanung und Qualitätssicherung
- Tägliche Dosisakkumulation durch Berechnung der «Dose of the day», um eine präzisere Abschätzung der tatsächlich applizierten Dosis zu ermöglichen und Dosis-Wirkungsmodellierung verlässlicher zu machen
- Entwicklung von bildgebenden Biomarker unter Anwendung von klassischen qualitativen und semi-quantitativen Verfahren, um eine Patienten-individuelle Vorhersage des Tumoransprechens zu ermöglichen und Anpassung von Zielvolumina ohne Einbusse der lokalen Kontrolle auf eine biologische Basis zu stellen.
- Geräte, bei denen die Plananpassung auf CBCT-Basis erfolgen kann, sind in der klinischen Erprobung.
Copyright bei Aerzteverlag medinfo AG
Universitätsspital Zürich
Radioonkologie
Rämistrasse 100
8091 Zürich
Helena.Garcia@usz.ch
Universitätsspital Zürich
Radioonkologie
Rämistrasse 100
8091 Zürich
Nicolaus.Andratschke@usz.ch
Oberärztin, RadioOnkologie
Universitätsspital Zürich
Radioonkologie
Rämistrasse 100
8091 Zürich
Matea.Pavic@usz.ch
keine; NA: Forschungsstipendium ViewRay und Brainlab, Referentenhonorar ViewRay; MP: Forschungsstipendium ViewRay.
◆ Die Bildgestützte Einstellung mit verschiedensten Techniken ist Standard in der modernen Radioonkologie und insbesondere bei stereotaktischen Verfahren nicht mehr wegzudenken.
◆ Die MR-geführte Radiotherapie bringt Vorteile wie höhere Weichteilauflösung, die Möglichkeit einer täglichen Planadaptation bei variabler Anatomie und einem zuverlässigen intrafraktionellen Monitoring und Gating atembeweglicher Tumore. Demgegenüber steht die höhere Liegezeit für den Patienten mit einem aufwendigen und personalintensiveren Workflow.
◆ Bei richtiger Patientenselektion ist die MR-geführte Radiotherapie v.a. in Tumoren des Oberbauchs, Leber aber auch für Stereotaxie der Lunge und Prostata eine wertvolle Technik, die die Präzision erhöht und Potential birgt, Nebenwirkungsraten weiter zu verringern.
◆ Insbesondere laufende klinische Studien werden weiter dazu beitragen, die Kollektive zu erkennen, die besonders von dieser Technik profitieren können.
◆ Eine weitere Zunahme von MRI-LINAC Geräten ist aufgrund der Vorteile für bestimmte Krankheitsbilder in Zukunft zu erwarten. Aufgrund der zeit- und personalintensiven Abläufe ist jedoch ein flächendeckender Einsatz in nächster Zukunft unwahrscheinlich. Bis dahin können geeignete Patienten entsprechend an die Zentren mit verfügbarer Technik zugewiesen werden.
Messages à retenir
◆ L’ ajustement guidé par l’image à l’ aide d’ une grande variété de techniques est la norme en radio-oncologie moderne et est devenu indispensable, notamment pour les procédures stéréotaxiques.
◆ La radiothérapie guidée par RM apporte des avantages tels qu’ une résolution plus élevée des tissus mous, la possibilité d’ adapter le plan quotidien à une anatomie variable, ainsi qu’ un monitoring intrafractionnel fiable et le gating des tumeurs respiratoires. D’ un autre côté, le temps de repos du patient est plus long, car le flux de travail est plus complexe et nécessite davantage de personnel.
◆ Avec une sélection adéquate des patients, la radiothérapie guidée par RM est une technique précieuse, en particulier pour les tumeurs de l’ abdomen supérieur et du foie, mais aussi pour la stéréotaxie du poumon et de la prostate, qui augmente la précision et a le potentiel de réduire davantage les taux d’ effets secondaires.
◆ En particulier, les essais cliniques en cours permettront de mieux identifier les collectifs qui peuvent particulièrement bénéficier de cette technique.
◆ On peut s’ attendre à une nouvelle augmentation des appareils IRM-LINAC à l’ avenir, vu les avantages qu’ ils présentent pour certaines pathologies. Toutefois, en raison du temps et du personnel nécessaires, il est peu probable qu’ une utilisation généralisée soit envisagée dans un avenir proche. En attendant, les patients appropriés peuvent être orientés de manière adéquate aux centres disposant de la technologie disponible.
info@onco-suisse
- Vol. 11
- Ausgabe 3
- Juni 2021