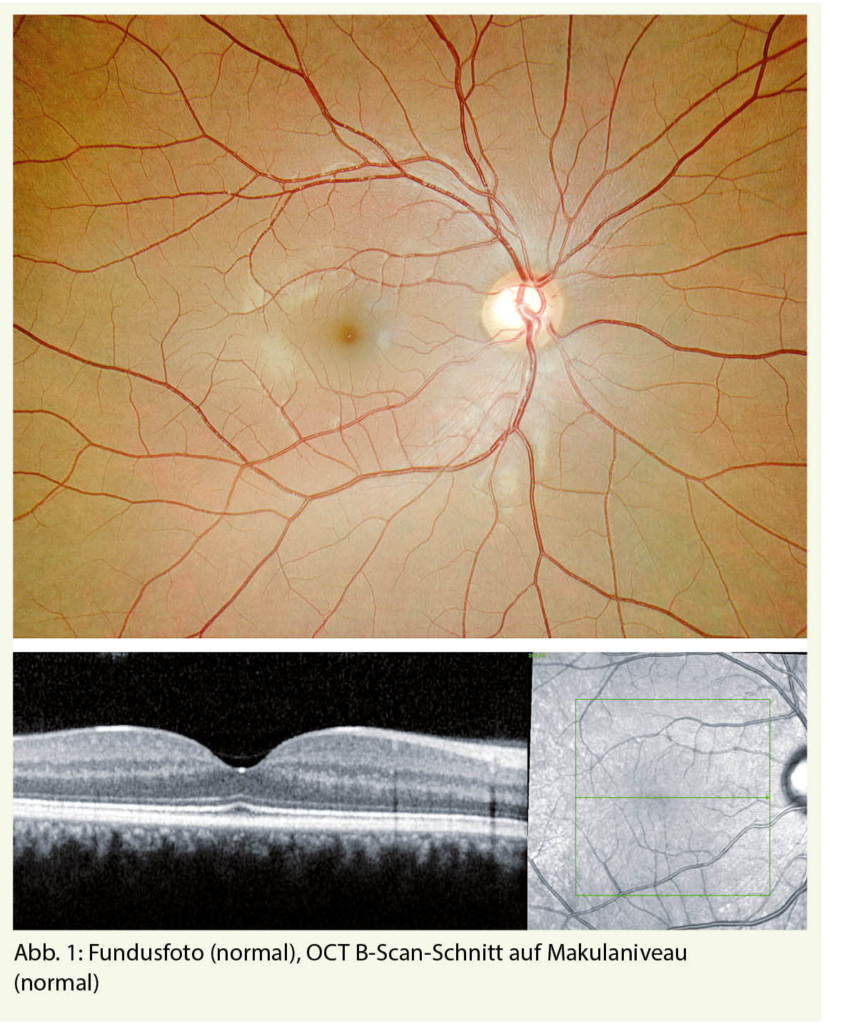
- Die Makulopathie
Makulopathie ist ein Oberbegriff, der alle Pathologien des zentralen Bereichs der Netzhaut, der Makula, definiert. Diese anatomische Region ist für das feine und präzise Sehen und weitgehend für die Farbwahrnehmung verantwortlich (1). Makulopathien sind in der Regel progressiv und erworben, obwohl es auch angeborene und genetische Formen gibt. Die häufigsten Formen sind die altersbedingte Makuladegeneration (AMD) und Makulopathien diabetischen Ursprungs. Es gibt auch toxische und medikamenteninduzierte Ursachen (z.B. Hydroxychloroquin). In diesem Artikel wird kurz auf die beiden häufigsten Makulopathien, AMD und diabetische Makulopathie, eingegangen.
Patienten mit Makulopathie verlieren selbst in schwersten Fällen ihr Augenlicht nicht vollständig und behalten ein peripheres Gesichtsfeld und eine gute visuelle Orientierung in ihrer Umgebung; sie können jedoch nicht mehr lesen, Auto fahren usw. und gelten als gesetzlich blind (gesetzliche Blindheit), wenn ihre Sehschärfe unter 0,1 liegt.
Obwohl die derzeitigen Methoden die Behandlung vieler Arten von Makulopathie verbessert haben, gibt es derzeit in den meisten Fällen keine kurative Behandlung. Darüber hinaus gibt es keine Möglichkeit, die verlorene Makulafunktion aufgrund einer Atrophie des Pigmentepithels oder des Netzhautgewebes wiederherzustellen.
Altersbedingte Makula-Degeneration (AMD)
Die AMD ist die häufigste Makulopathie (Abb. 1, 2). Sie betrifft ältere Menschen, in den meisten Fällen über 60 Jahre alt. Sie ist eine der Hauptursachen für Sehbehinderungen in den entwickelten Ländern. Gegenwärtig sind Millionen von Menschen davon betroffen. Die ursprüngliche Ursache der AMD ist nach wie vor unbekannt, obwohl Alter, genetische Faktoren und aktives Rauchen eindeutig als Risikofaktoren für AMD identifiziert wurden (2, 3, 4).
AMD im Frühstadium ist oft leicht oder sogar asymptomatisch. Bei fortgeschritteneren Formen bemerken die Patienten häufig Metamorphopsien (Linienverzerrung aufgrund von Unregelmässigkeiten im neuroretinalen System), verminderte Kontrastempfindlichkeit und erhöhten Lichtbedarf, zentrale Sehunschärfe und Verlust der Sehschärfe, Skotome und Farbsinnstörungen. Es gibt zwei Haupttypen von AMD, die trockene AMD und die feuchte AMD (5).
Trockene AMD
Die trockene AMD ist die häufigste und macht nach Angaben der American Academy of Ophthalmology 80% der Fälle aus. Stoffwechselprodukte, die sich an der Grenzfläche des Pigmentepithels (PE) und der äusseren Netzhaut ansammeln, werden in Form von Drusen gesehen. Das Ergebnis ist ein fortschreitender Verlust dieses interdependenten PE/Photorezeptor-Paares, was zu einer fortschreitenden Verschlechterung der zentralen Sehfunktion führt.
Feuchte AMD
Die feuchte AMD ist seltener, aber sie ist schwerwiegender als die trockene AMD, weil ihr Fortschreiten abrupter ist. Die beiden Formen schliessen sich nicht gegenseitig aus, und es kommt häufig zu einem abrupten Fortschreiten von der trockenen zur feuchten AMD mit akuter und schwerer Sehbehinderung. Dieser Zustand tritt auf, wenn sich abnorme Blutgefässe (so genannte Neo-Gefässe) unter/in der Netzhaut entwickeln, was zu einer grösseren Störung der mikroanatomischen Architektur der Makula und zum Auftreten einer Ansammlung von Flüssigkeit im Gewebe (sogar zu Blutungen) führt.
Symptome
Es ist wichtig, verdächtige Symptome der AMD zu erkennen, welche den Kliniker darauf aufmerksam machen sollten, den Patienten für eine umfassende Beurteilung an den Spezialisten zu überweisen und die Dringlichkeit der Behandlung zu bestimmen. Bei einer Person über 55 Jahren sind die alarmierenden Anzeichen wie folgt:
1) Allmähliche oder plötzliche Verminderung der Sehschärfe, die mit optischer Korrektur nicht verbessert werden kann
2) Zentralskotom
3) Metamorphopsien, Mikropsien oder Makropsien
4) Schwierigkeiten bei Aktivitäten des täglichen Lebens (z.B. Fernsehen, Lesen usw.).
Die Metamorphopsie ist ein Schlüsselsymptom bei der Beurteilung eines Patienten mit AMD. Metamorphopsien sind ein Hauptzeichen bei Patienten mit Makulaerkrankung und können mit Hilfe des Amsler-Netzes leicht erkannt werden. Patienten werden häufig gebeten, sich mit Hilfe eines Amsler-Netzes auf Linienverzerrungen oder partielle Gitteramputationen selbst zu überwachen. Wenn es keine Manifestation gibt, die auf ein Fortschreiten der AMD hindeutet, werden die Patienten jährlich überwacht.
Behandlung
Bei Patienten mit früher AMD ist es wichtig, veränderbare Risikofaktoren in Bezug auf den Lebensstil zu identifizieren. Es wird empfohlen, mit dem Rauchen aufzuhören und sich ausgewogen und gesund zu ernähren, reich an Obst, Gemüse (natürliche Antioxidantien) und Fisch (die Hauptquelle für mehrfach ungesättigte Omega-3-Fettsäuren wie Docosahexaensäure und Eicosapentaensäure) (7). Auch körperliche Aktivität scheint eine günstige Rolle zu spielen (schliesslich sind die Risiko- und Schutzfaktoren ähnlich wie bei Herz-Kreislauf-Erkrankungen).
Menschen mit frühen Formen der AMD können von der Einnahme von Nahrungsergänzungsmitteln, Vitaminen und Mineralien profitieren. Diese Nahrungsergänzungsmittel enthalten Vitamin C, Vitamin E, Beta-Carotin, Kupfer, Lutein, Zeaxanthin und Zink. Diese Vitamine heilen die AMD nicht, kehren sie nicht um oder beugen ihr vor, aber sie können das Fortschreiten der Krankheit verlangsamen, wie aus verschiedenen Studien hervorgeht, die einen Vorteil dieser Präparate gegenüber Placebo (AREDS und AREDS2) gezeigt haben (8, 9). Es ist anzumerken, dass die neuesten Präparate zunehmend frei von Beta-Carotin sind, das in Verbindung mit aktivem Rauchen das Risiko von Neoplasien der Lungen erhöht.
Gegenwärtig gibt es keine Heilung für diese Krankheit. Für die trockene AMD gibt es keine spezifische Behandlung. Für die feuchte Form der Erkrankung stehen seit etwa zehn Jahren intravitreale Injektionen von antivasoproliferativen Medikamenten (Anti-VEGF) zur Verfügung, die die Sehschärfe und das Makulaprofil durch Hemmung des Wachstums der neovaskulären Membranen stabilisieren und oft sogar verbessern. Leider nimmt die Wirksamkeit der Behandlung in den folgenden Wochen rapide ab, so dass eine enge Nachbeobachtung und zahlreiche Langzeitinjektionen erforderlich sind.
In sehr speziellen Situationen bleibt die Anwendung der dynamischen Phototherapie mit Visudyne (Verteporfin) als Monotherapie oder am häufigsten in Kombination mit Anti-VEGF-Injektionen indiziert. Bei der photodynamischen Therapie wird ein spezieller Laser eingesetzt, um eine Thrombose und Fibrose der neovaskulären Membran zu ermöglichen. Ein photosensibilisierendes Produkt (Verteporfin) wird in eine periphere Armvene injiziert und verteilt sich insbesondere im Auge mit einem erhöhten Tropismus für die neovaskuläre Membran. Das Laserlicht reagiert mit dem Verteporfin und ermöglicht die Zerstörung der Neovaskularisationen.
Diabetische Makulopathie
Die diabetische Makulopathie ist die häufigste Ursache für den Sehkraftverlust bei Menschen mit Diabetes (Abb. 3) (11).
Es gibt zwei Formen der diabetischen Makulopathie:
Ischämische Makulopathie: eine seltene Form der Makulopathie, die unheilbar ist und häufig zu einer schweren Sehbehinderung führt.
Ödematöse Makulopathie (auch als diabetisches Makulaödem (DMÖ) bekannt): die häufigste Form, ihre Prävalenz bei Patienten mit diabetischer Retinopathie liegt bei 2,7-11% (12, 13) und dies hängt von der Art des Diabetes und der Dauer der Erkrankung ab. Für beide Arten von Diabetes 1 und 2 beträgt sie nach 25 Jahren etwa 30%. Das Risiko, bei Diabetes ein diabetisches Makulaödem zu entwickeln, steigt mit der Anzahl der Diabetesjahre, einem höheren systolischen Blutdruck und schlecht kontrollierten Blutzuckerwerten. Der einzige okuläre Faktor, der mit DME assoziiert ist, ist der Schweregrad der diabetischen Retinopathie (DR); je weiter die DR fortgeschritten ist, desto grösser ist das Risiko für DME (14).
Symptome
Zu Beginn erzeugt das DMÖ keine besonderen Schmerzen oder Anzeichen. Das bedeutet, dass Menschen mit Diabetes betroffen sein können, ohne eine Sehstörung zu spüren und damit ohne es zu wissen. Mit der Zeit treten dann bestimmte Symptome auf:
1) Verminderung der Sehschärfe, einschliesslich verschwommenes Lesen, Schwierigkeiten beim Erkennen von Gesichtern usw.
2) Verlust der Kontrastempfindlichkeit
3) Schwierigkeit, Farben richtig wahrzunehmen.
Behandlung
Die Anerkennung der DMÖ-Risikofaktoren hat zu randomisierten klinischen Studien zur besseren Kontrolle des Blutdrucks und des Blutzuckerspiegels geführt mit dem Ziel, die Prävalenz der Krankheit zu verringern. The diabetes control and complications trial zeigte, dass eine strenge Blutzuckereinstellung bei Patienten mit Typ-1-Diabetes die kumulative Inzidenz des Makulaödems nach 9 Jahren Nachbeobachtung um 29% reduzierte und die Anwendung der fokalen Laserbehandlung bei DMÖ halbierte (15, 16). Die United Kingdom Prospective Diabetes Study war eine ähnliche randomisierte klinische Studie an Patienten mit Typ-2-Diabetes. Es zeigte sich, dass eine strengere Kontrolle des Blutzuckerspiegels die Notwendigkeit einer Laserbehandlung nach 10 Jahren um 29% reduzierte, verglichen mit einer weniger strengen Kontrolle; 78% der Laserbehandlungen wurden bei der DMÖ durchgeführt (17). Sie zeigte auch, dass eine mittlere Senkung des systolischen Blutdrucks um 10 mmHg und eine Senkung des diastolischen Blutdrucks um 5 mmHg über ein medianes Follow-up von 8,4 Jahren zu einer 35%-igen Verringerung der Netzhautlaserbehandlung führte, davon 78% für das DMÖ (18). Es besteht daher ein enger Zusammenhang zwischen diesen Veränderungen und retinalen Effekten. Eine multifaktorielle Intervention zur Senkung von HbA1c, erhöhtem Blutdruck und erhöhten Serumlipiden kann in nur 6 Wochen messbare Effekte auf die Makuladicke erzeugen und bietet eine rationale Grundlage für spezifische augenärztliche Eingriffe (19).
Spezifische augenärztliche Behandlungen
Für das DMÖ gibt es mehrere Behandlungsmodalitäten, wobei oft eine Kombination von Behandlungen verwendet wird, die je nach Situation variieren:
1) Intravitreale Injektionen von Anti-VEGF-Medikamenten
2) Intravitreale Kortikosteroidinjektionen (einschliesslich Implantate mit kontinuierlicher Freisetzung über mehrere Monate (Ozurdex®, Iluvien, etc.)
3) Kombinierte Injektionen von Anti-VEGF und intravitrealen Kortikosteroiden
4) Fokale/Gitter-Laserkoagulation
5) Unterschwellige Laser-Photokoagulation
6) Vitrektomie
Bei diesem Artikel handelt es sich um einen Zweitabdruck des in der « la gazette médicale » 06-2020 erschienen Originalartikels.
Copyright bei Aerzteverlag medinfo AG
Service d’ ophtalmologie de l’ Université de Lausanne
Hôpital ophtalmique Jules-Gonin
Fondation Asile des aveugles
Av. de France 15
CP 133
1000 Lausanne 7
mohamed.sherif@fa2.ch
Service d’ ophtalmologie de l’ Université de Lausanne
Hôpital ophtalmique Jules-Gonin
Fondation Asile des aveugles
Av. de France 15
CP 133
1000 Lausanne 7
Unité de chirurgie vitréo-rétinienne
Hôpital Ophtalmique Jules-Gonin
Fondation Asile des Aveugles
Département d’ Ophtalmologie
Université de Lausanne
Avenue de France 15
1004 Lausanne
retinechirurgicale@fa2.ch
Die Autoren haben in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
◆ Makulopathie ist ein Oberbegriff, der alle Pathologien des zentralen Bereichs der Netzhaut, der Makula, definiert.
◆ Die häufigsten Formen sind die altersbedingte Makuladegeneration (AMD) und die diabetische Makulopathie.
◆ Die Grundursache der AMD ist nach wie vor unbekannt, obwohl Alter, genetische Faktoren und aktives Rauchen eindeutig als Risikofaktoren identifiziert worden sind. Die trockene AMD ist am häufigsten, während die feuchte AMD seltener, aber schwerwiegender ist. Bei der feuchten AMD werden zur Stabilisierung der Sehschärfe intravitreale Injektionen von antivasoproliferativen Medikamenten (Anti-VEGF) eingesetzt.
◆ Die ödematöse Makulopathie ist die häufigste Form der diabetischen Makulopathie. Die strikte Kontrolle des Blutzuckers und eine moderate Senkung des Blutdrucks führten zu einer Verringerung der kumulativen Inzidenz des Makulaödems.
1. Kanski JJ. Clinical Ophthalmology: A Systematic Approach. 6th édition 2007.
2. Chen Y, Zeng J, Zhao C, et al. Assessing susceptibility to age-related macular degeneration with genetic markers and environmental factors. Arch Ophthalmol. 2011;129(3):344–351.
3. Velilla S, García-Medina JJ, García-Layana A, et al. Smoking and age-related macular degeneration: review and update. J Ophthalmol. 2013;2013:895147.
4. Myers CE, Klein BE, Gangnon R, Sivakumaran TA, Iyengar SK, Klein R. Cigarette smoking and the natural history of age-related macular degeneration: the Beaver Dam Eye Study. Ophthalmology. 2014;121:1949–1955.
5. Ferris FL, III, Wilkinson CP, Bird A, et al. Clinical classification of age-related macular degeneration. Ophthalmology. 2013;120(4):844–851.
6. Simunovic MP. Metamorphopsia and its quantification. Retina. 2015;35(7):1285–1291.
7. Carneiro Â, Andrade JP. Nutritional and lifestyle interventions for age-related macular degeneration: a review. Oxid Med Cell Longev. 2017;2017:6469138.
8. Age-Related Eye Disease Study Research Group A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no. 8. Arch Ophthalmol. 2001;119(10):1417–1436.
9. Age-Related Eye Disease Study 2 Research Group Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005–2015.
10. Age-Related Eye Disease Study 2 Research Group Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005–2015.
11. Klein R, Klein BE, Moss SE, Cruickshanks KJ. The Wisconsin epidemiologic study of diabetic retinopathy. XV. The long-term incidence of macular edema. Ophthalmology. 1995;102:7–16.
12. 4. Xie XW, Xu L, Wang YX, Jonas JB. Prevalence and associated factors of diabetic retinopathy. The Beijing eye study 2006. Graefes Arch Clin Exp Ophthalmol. 2008;246:1519–26.
13. Wong TY, Klein R, Islam FM, Cotch MF, Folsom AR, Klein BE, et al. Diabetic retinopathy in a multi-ethnic cohort in the United States. Am J Ophthalmol. 2006;141:446–55.
14. Klein R, Klein BE, Moss SE, Cruickshanks KJ. The Wisconsin epidemiologic study of diabetic retinopathy: XVII. The 14-year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes. Ophthalmology. 1998;105:1801–15.
15. Progression of retinopathy with intensive versus conventional treatment in the diabetes control and complications trial. Diabetes control and complications trial research group. Ophthalmology. 1995;102:647–61.
16. Early worsening of diabetic retinopathy in the diabetes control and complications trial. Arch Ophthalmol. 1998;116:874–86.
17. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). UK prospective diabetes study (UKPDS) group. Lancet. 1998;352:837–53.
18. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. UK prospective diabetes study group. BMJ. 1998;317:703–13.
19. Singh R, Abhiramamurthy V, Gupta V, Gupta A, Bhansali A. Effect of multifactorial intervention on diabetic macular edema. Diabetes Care. 2006;29:463–4.
der informierte @rzt
- Vol. 11
- Ausgabe 9
- September 2021