- Akuter Hirnschlag – Diagnostik und Behandlung
Die Akutbehandlung des Hirnschlages beginnt in der Prähospitalisationsphase und endet mit dem Festlegen einer individuell angepassten Sekundärprophylaxe, der auf die erfolgten Diagnostik beruht. Es handelt sich somit um ein Continuum von Erkennen der Symptome, Handeln unter Auswahl der besten Opportunitäten zur Therapie und Erarbeiten einer Hypothese zur Pathogenese, die schliesslich in der Sekundärprävention und Rehabilitation mündet. All dies erfordert eine individuelle Evaluation der Sekundärprophylaxe basierend auf allen relevanten Kriterien, individueller Co-Morbidität sowie bestehender und notwendiger Co-Medikation und daraus resultierenden individueller Nutzen-Risiko-Abwägung.
Acute treatment of cerebral stroke begins in the prehospitalization phase and ends with the establishment of an individualized secondary prophylaxis based on the diagnosis made. Thus, it is a continuum of recognizing the symptoms, acting by selecting the best opportunities for therapy, and elaborating a hypothesis on the pathogenesis, which finally leads to secondary prevention and rehabilitation. All this requires an individual evaluation of secondary prevention based on all relevant criteria, individual co-morbidity as well as existing and necessary co-medication and the resulting individual benefit-risk assessment.
Key Words: cerebral stroke, secondary prevention, cardio embolism
Die Behandlung des akuten Hirninfarktes ist zeitkritisch. Alle nötigen Prozesse und Entscheidungen müssen so schnell wie möglich getroffen werden. Mitentscheidend für das klinische Ergebnis ist bereits das Erkennen durch Laien. Die Hirnschlag-Differentialdiagnose beginnt beim ersten Kontakt mit der Rettung. Hier wird ein erster Verdacht auf einem Hirnschlag gestellt und das Zielspital bereits vor Ankunft alarmiert (1).
Bei Ankunft in der Notfallaufnahme des vorinformierten Spitals wird die Patientin/der Patient vom Arzt- und Pflege-Stroke Team direkt in Empfang genommen. Hier finden gleichzeitig eine fokussierte Anamnese sowie die erste klinische Beurteilung und laborchemische Analysen statt. Wichtig ist das Erheben der Uhrzeit des Symptombeginns, und falls die Patientin/der Patient nicht kommunikationsfähig ist, von der Rettung oder den Angehörigen zu erfragen ist.
Die klinische Untersuchung auf der Notfallstation hat das Ziel, die Vermutungsdiagnose zu bestätigen und andere potenzielle Diagnosen festzustellen oder auszuschliessen. Damit wird auch eine erste Schweregradbeurteilung des Hirnschlages bestimmt. Vor allem steht eine zeitnahe Beurteilung des Allgemeinzustandes, der Vitalparameter, sowie die gezielte neurologische Untersuchung im Vordergrund. Bei einem Hirnschlag ist die National Institutes of Health Stroke Skala (NIHSS) die bevorzugte erste neurologische Evaluation, damit der Patient schnell und standardisiert auf die wichtigsten hirnschlagrelevanten Befunde untersucht wird. Mit diesen Informationen und der aktuellen Medikamentenliste lässt sich auch eine erste ätiopathologische Beurteilung erstellen. Diagnosen von koronarer oder rhythmogener Herzkrankheit, Hypertension, Diabetes und Dyslipidämie oder eine aktuelle medikamentöse Therapie mit Thrombozytenaggregationshemmern oder Antikoagulanzien sind Hinweise. Parallel dazu ist eine Überwachung der Vital-Parameter mittels Monitoring entscheidend. Eine erste Blutentnahme zur Bestimmung von Elektrolyten, Glucose, Blutbild, Entzündungsparametern und Gerinnungswerten, insbesondere des INR-Wertes respektive der Heparin-Aktivität bei oraler Antikoagulation, sind mitentscheidend.
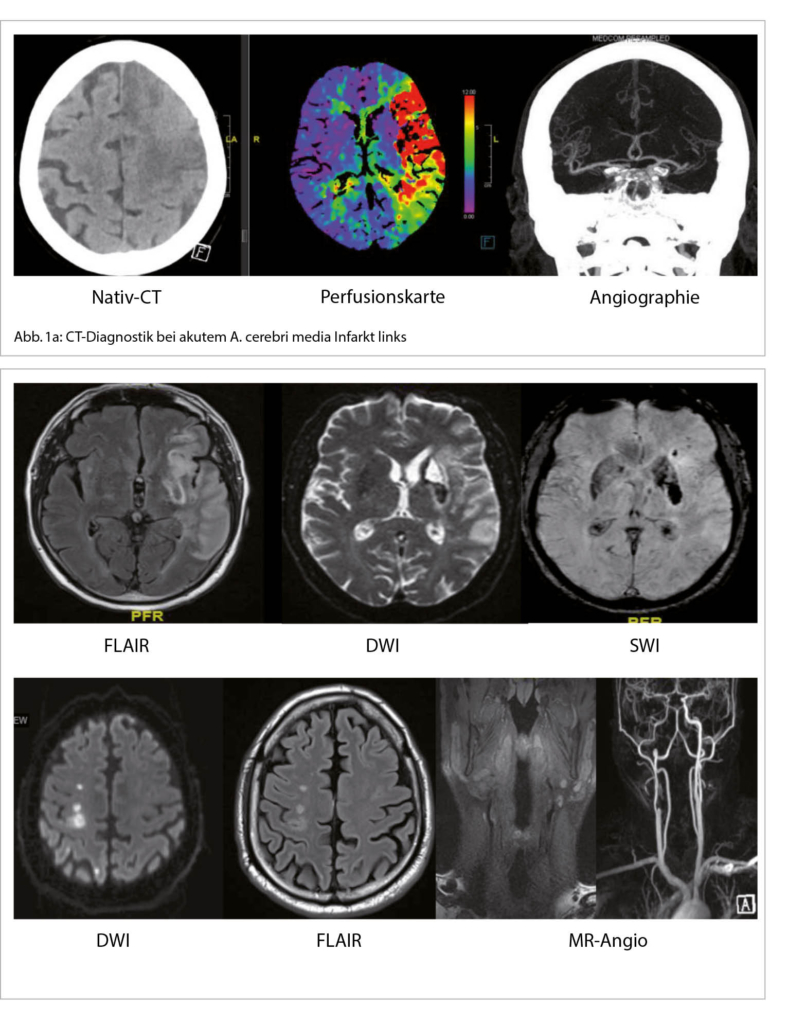
Wenn nach der ersten anamnestischen und klinischen Beurteilung die klinische Vermutung auf einen akuten Hirnschlag vorliegt, ist im Hinblick auf eine revaskularisierende Therapie der Ausschluss einer intrakraniellen Blutung sowie einer nicht vaskulären Pathologie wichtig. Gleichzeitig beginnt auch die Abklärung der Schlaganfall-Ätiologie. Dazu ist eine erste Bildgebung mittels CT- oder MRI-Untersuchung notwendig. Die Entscheidung zwischen CT oder MRI in der akuten Phase ist stark von Klinikressourcen und Zeit-Effizienz des entsprechenden Behandlungsprotokolls abhängig. Eine Vorgehensweise mit CT-Scan beinhaltet erst ein natives CT (ohne Kontrastmittelgabe), um eine intrakranielle Blutung als Ätiologie des Ereignisses auszuschliessen. Dafür ist das CT-Scan sehr zeiteffizient und präzise. Danach folgt die Kontrastmittel-Gabe mit CT-Angiographie, um den Status der hirnversorgenden Gefässe zu beurteilen und einen potentiellen Gefässverschluss zu diagnostizieren. Zuletzt dient die Perfusions-Untersuchung dazu, das Volumen des möglichen rettbaren Hirngewebes zu bestimmen und eine revaskularisierende Therapie zu indizieren (Abb. 1a). Eine MRI-Erstbildgebung ist sensitiver für die Hirnschlagdiagnose, da sehr früh das ischämische Gewebe erkannt werden kann. Die kernspintomographische Vorgehensweise beinhaltet diffusionsgewichtete (DWI) und suszeptibilitätsgewichtete (SWI) Aufnahme-Protokolle, die jeweils zwischen einem ischämischen und hämorrhagischen Ereignis differenzieren und eine genaue Lokalisation der Läsion geben können. Ergänzend dazu geben die ADC und FLAIR Protokolle hilfreiche Informationen bezüglich des zeitlichen Verlaufs der Läsion. Der Gefäss-Status kann im Hinblick auf signifikante Stenosen oder anderen Gefässerkrankungen wie Dissektionen, Vaskulitiden etc. mittels einer MR-Angiographie beurteilt werden (Abb. 1b, 2) (2, 3).
Das therapeutische Ziel nach der ersten Beurteilung und Diagnose eines drohenden ischämischen Hirninfarktes ist die Wiedereröffnung der durch Thromben okkludierten Arterien.
Bei mittelschweren und schweren (behindernden) Schlaganfällen ist, in Abwesenheit von Kontraindikationen, eine intravenöse Thrombolyse mittels Alteplase, rtPA (recombinant tissue Plasminogen Activator) indiziert. Wichtig ist, dass der Patient innerhalb von 4,5 (und in bestimmten Fällen von 6) Stunden nach Symptombeginn in einer entsprechend ausgerüsteten Institution behandelt wird. Eine gewichtsadaptierte Lyse-Therapie ist unmittelbar nach klinischer und bildmorphologischer Evaluation, insbesondere nach Ausschluss einer intrakraniellen Blutung, einzuleiten (4).
Der Verdacht auf Okklusion einer proximalen Hirnbasisarterie ist auf dem klinischen Syndrom und der nicht invasiven Gefässdarstellung mittels CT oder MR Angiographie basiert. Zudem ist die Bestimmung der ischämischen Penumbra wichtig. Die Penumbra ist das potenziell rettbare Hirngewebe, das in hypoxämischen Zustand, aber noch nicht infarziert ist. Je nach Ausdehnung wird zusätzlich eine mechanische Thrombektomie mittels Katheter-Technik indiziert (5, 67777).
Gleichwertig mit der akuten Behandlung ist die frühzeitige und gezielte supportive Behandlung in einer Stroke-Unit entscheidend. In der Stroke-Unit sind Hirnschlagpatientinnen/-patienten durch das Pflege- und ärztliches Personal eng überwacht. Dort beginnt die gleichzeitige Behandlung von Abweichungen des Blutdrucks, der Glucose, der Temperatur und das Erfassen von Rhythmusstörungen. Ferner werden die erkannten Komorbiditäten therapiert (1).
Ursachendiagnostik
Die ätiologische Abklärung auf Hirnschlag ist entscheidend für die sekundäre Prävention. Diese bildet die Grundlage einer wirkungsvollen evidenz-basierten Rezidivprophylaxe und führt zur messbaren Verminderung des Risikos für rezidivierende ischämische Ereignisse. Dies trifft nicht allein in den ersten Tagen zu, sondern gilt auch langfristig.
Die Grundlage bildet die klinische Untersuchung, indem aufgrund der neurologischen Ausfallssyndrome eine topische Zuordnung zu einer okkludierten Arterie getroffen werden kann. Die initiale Bildgebung mit nativen CT, CT-Angiographie und potenziell CT-Perfusion oder einem MRI mit DWI Protokoll, kann Hinweise für die Morphologie und Lokalisierung der Hirnläsionen geben, die zu den erhobenen klinischen Befunden passen müssen. Mit der ersten Bildgebung des Zerebrums ist auch die Unterscheidung zwischen ischämischen Läsionen und intrakranialen Blutungen möglich. Ferner können Befunde wie Arteriosklerose der zuführenden Halsarterien und intrakranialen Arterien erkannt werden. Mikroangiopathische Läsionen lassen sich im nativen zerebralen CT als Lakunen erkennen. Dies ist auch in der MR-Darstellung so, wo bereits in der Akutphase Läsionen als sog. DWI-positive Läsionen erscheinen. Chronische ischämische Läsionen erscheinen in den CTs als sog. Leukoaraiosis, währenddessen in der MR-Darstellung auf FLAIR-Sequenzen weisse Läsionen erkennbar sind, die dem gliotischen Gewebeumbau entsprechen. Zusätzlich können bei Hypertonie oder zerebraler Amyloidangiopathie Mikroblutungen erkannt werden. Ein EKG in der akuten Phase, das ein Vorhofflimmern/Vorhofflattern erkennen lässt, ist wegweisend für eine Embolie.
Wenn allein eine CT-basierte Bildgebung in der akuten Phase gemacht wurde, dann könnte eine MRT zur Bestätigung der Hirnpathologie und zur weiteren diagnostischen Abklärung wichtige Informationen erkennen lassen.
Die ätiologische Klassifizierung unterscheidet zwischen 5 Hauptgruppen ischämischer Hirninfarkte mit der sog. TOAST-Klassifikation (2, 3, 7).
1) Makroangiopathie durch Arteriosklerose grosser intra- und extrakranieller Hirngefässe, durch Thrombose im Bereich der arteriosklerotischen Plaques, hämodynamische Insuffizienz im post-stenotischen Stromgebiet oder arterio-arterielle Embolien
2) Kardiogene / aortogene Embolie: v. a. bei Vorhofflimmern, aber auch als Komplikation infolge Myokardinfarkt, Klappenersatz, Endokarditis, Kardiomyopathie
3) Mikroangiopathie: Erkrankungen/Arteriolosklerose kleiner Hirngefässe, meist hypertensiv, hereditär und altersbedingt
4) andere Ursachen, z. B. Vaskulopathien, Dissektionen oder Arteriitiden, Koagulopathien, paradoxe Embolien über Rechts-Links-Shunt
5) Hirninfarkte ohne geklärte Ätiologie – kryptogene Hirninfarkte
Zur Klärung der Ätiopathogenese und zum Erfassen individueller Co-Morbiditäten können folgende diagnostische Untersuchungen vorgenommen werden:
- CT oder MRT Schädel, sofern nicht bereits auf der Notfall-Station erfolgt. MRI 24h nach Symptombeginn. Das Läsions-Muster kann für die mögliche Hirnschlag-Pathophysiologie hinweisend sein.
- 12-Kanal-EKG und Langzeit-Elektrokardiogramm (Mindestens 72h und ggf. bis 7 Tage bei erhöhtem Verdacht auf kryptogenen Infarkt, evtl. Event-Recording mit Event-/Loop-Recorder oder Langzeitregistrierung) zum Nachweis von Herzrhythmusstörungen (8).
- Neurovaskuläre Ultraschalldiagnostik: Doppler-/Duplexsonographie der extra- und intrakraniellen hirnversorgenden Arterien. Dient zusammen mit der CT-Angiographie oder MR-Angiographie zum Beweis einer Gefässpathologie
(Stenosen, Okklusion, Kollateralen). - Transthorakale (oder Transösophageale) Echokardiographie: gemäss Indikation zum Nachweis von Emboliequellen im Herzen, Aortenbogen, Herzklappenpathologie oder akinetischen Herzwandabschnitten bei chronischen oder akuten Myokardinfarkten (möglicher Hinweis auf ein kardioembolisches Geschehen).
- Blutentnahme: Blutbild, Gerinnung, Chemogramm, Herzinfarkt-Marker, Lipidstatus, TSH und ggf. gezielte Laboruntersuchungen für Vaskulitis oder Thrombophilie.
- Weitere diagnostische Abklärungen und gezielte Labor- Untersuchungen erfolgen gemäss Indikation. Vor allem zum Erfassen von Risikofaktoren, entzündlichen Erkrankungen, metabolischen Störungen und Koagulopathien.
Gleichzeitig mit der ätiologischen Abklärung erfolgt auch eine kontinuierliche, nicht-invasive Überwachung (Monitoring) der Patienten, die mindestens Blutdruck, Herzfrequenz, Atemfrequenz, Sauerstoffsättigung, Temperatur und Herzrhythmus erfasst und dokumentiert.
Nach erfolgreichem Abschluss der Ursachendiagnostik kann eine frühe und gezielte sekundärprophylaktische Therapie erfolgen, um das Risiko eines Hirnschlag-Rezidivs maximal zu senken (Abb. 2).
Nachbehandlung aufgrund der ätiologischen Diagnosestellung
Genauso wichtig wie die akute Behandlung ist die rechtzeitige und zielorientierte Nachbehandlung nach ischämischen Hirnschlag. Die Sekundärprophylaxe fängt parallel mit dem Einsatz von akuten Massnahmen an und sollte langfristig weitergeführt werden, um Rezidive zu vermeiden. Die prophylaktische Nachbehandlung basiert zuerst auf der vermuteten oder der bisher durchgeführten Diagnostik einer schon erwiesenen Hirnschlag-Ursache, sollte jedoch auch auf die engmaschige Einstellung von vaskulären Risiko-Faktoren und Komorbiditäten achten. Eine rationale Therapie ist oft erst nach vollständiger ätiologischer Abklärung möglich und wird im Rahmen des intensiven Monitorings der Patienten in einer Stroke-Unit oft reevaluiert und angepasst. Es folgt eine Listung von Grundsätzen (2, 3, 9).
Arteriosklerose
Nach einem ischämischen Hirnschlag ist der frühzeitige Einsatz von antithrombotischen Substanzen empfohlen. Acetylsalicylsäure (ASS) ist die erste Wahl bei Hirnschlägen einer arterio- oder arteriolosklerotischen Genese, oder auch bei noch unbekannter Ätiologie. Ohne vorbestehende Plättchenhemmung erfolgt der Beginn der Behandlung (nach Ausschluss einer intrazerebralen Blutung, insbesondere nach Thrombolyse) für die ersten 14 Tage mit ASS 300mg tgl. mit anschliessender Weiterbehandlung mit 100mg tgl. Bei Auftreten des ischämischen Ereignisses unter bestehender Blutplättchenhemmung mit ASS kann eine Umstellung auf Clopidogrel erfolgen (einmalig 300mg als «loading dose», anschliessend 75mg tgl.). Eine duale Blutplättchenhemmung (Aspirin 100mg + Clopidogrel 75mg tgl.) kann bei TIA mit ABCD2-Score ≥4 Punkten oder Hirnschlägen mit NIHSS ≤ 3 zeitlich begrenzt (3 Wochen) verabreicht werden, gefolgt von Aspirin 100mg oder – falls das Ereignis unter ASS auftrat – Clopidogrel 75mg (10, 11). Bei hochgradigen intrakraniellen Arterienstenosen kann die duale plättchenhemmende Therapie bis 3 Monate nach Ereignis weitergeführt werden.
Je nach Berücksichtigung der Hirnschlagätiologie, des Ausmasses der Arteriosklerose an den hirnversorgenden Arterien sowie bei Anwesenheit einer koronaren Herzkrankheit oder anderen Komorbiditäten ist nach einem Hirnschlag/einer TIA das Ziel des gemessenen LDL-Cholesterinwertes <1.8mmol/l zu setzen (in bestimmten Fällen <1.4mmol/l oder <1.0mmol/l). Erstlinientherapie sind die Statine, z.Bsp. Atorvastatin oder Rosuvastatin. Bei Interaktionen oder Unverträglichkeit gegenüber Statinen könnte Ezetimib (NPC1L1 Inhibitor) alleine oder zusätzlich verwendet werden. Eine neue Kategorie von LDL-senkenden Medikamenten sind die PCSK9 Inhibitoren, die bei Patienten verwendet werden, bei denen das Ziel-LDL von <1.8mmol/l mit einer Kombinationstherapie mit Statin+Ezetimibe nicht erreicht werden kann. Bei hochgradigen Stenosen der Karotiden ist immer auch eine Revaskularisationstherapie mit Dilatation und Stenting oder operativ mittels Thrombendarterektomie zu evaluieren.
Kardioembolie
Bei Hirnschlägen mit einer kardioembolischen Genese wird meist Vorhofflimmern als Ursache diagnostiziert. Zu unterscheiden ist zwischen nicht-valvulärem und valvulärem Vorhofflimmern, die beide eine unterschiedliche sekundärprophylaktische Therapie benötigen. Bei nicht-valvulärem VHF ist ein direktes orales Antikoagulans (DOAK) mit einer auf die Nierenfunktion adaptierten Dosis indiziert (direkte Thrombininhibitoren Dabigatran/Pradaxa® oder Faktor Xa-Antagonisten Rivaroxaban/Xarelto®, Apixaban/Eliquis®, Edoxaban/Lixiana®). Bei valvulärem VHF, wobei es sich um eine mechanische Herzklappe oder eine schwergradige Mitralklappenstenose handeln kann, ist eine Antikoagulationstherapie mittels einem Vitamin K Antagonisten (VKA, Phenprocoumon/Marcumar®) indiziert. Bei einer solchen Therapie ist ein Ziel INR 2.0-3.0 zu erreichen. Dies muss regelmässig, mindestens monatlich, kontrolliert werden, sodass das Blutungsrisiko nicht deutlich erhöht ist. Bei allen Patienten sollte eine Bestimmung des Hirnschlag-Risikos mittels des CHA2DS2-VASc-Score sowie des Blutungs-Risikos mittels des HAS-BLED Score erfolgen. Der Beginn einer oralen Antikoagulation nach Hirnschlag richtet sich nach der Grösse des Infarktareals und dem Stroke-Risiko (CHA2DS2-VASc-Score). Die Entscheidung für den optimalen Beginn der oralen Antikoagulation bleibt jedoch immer eine individuelle Entscheidung, könnte aber auf der Basis der 1-3-6-12 Tage-Regel eingesetzt werden: 1=TIA, 3=Minor Stroke, 6=Moderate Stroke, 12=Severe Stroke. Eine besondere Form eines kardio-embolischen Hirnschlags ist die paradoxe Embolie bei offenen Foramen ovale (PFO). Hier ist es wichtig zu beurteilen, ob eine medikamentöse prophylaktische Therapie oder ein PFO-Verschluss zu empfehlen ist (1, 11).
Mikroangiopathie
Bei mikroangiopathisch-bedingten Hirnschlägen ist nebst der sekundärprophylaktischen Therapie mit Thrombozytenaggregationshemmung auch die Korrektur der zugrundeliegenden kardiovaskulären Risiko-Faktoren, vor allem Blutglukose und Blutdruck, entscheidend. Bezüglich der Blutglukose ist bei einem Schlaganfall weder eine Hyperglykämie noch eine Hypoglykämie zu tolerieren, da beides mit einem schlechteren Ergebnis verbunden ist. Eine Behandlung ist mit oralen, oder in der Akutphase parenteralen Massnahmen zu implementieren. Hinsichtlich des Blutdrucks in den ersten 24-48 Stunden seit Symptombeginn und in Abwesenheit von Endorganschädigung, sind hypertensive systolische Blutdruck-Werte bis 220/120mmHg ohne, 185/100mmHg mit Thrombolyse, noch zu tolerieren. Nach den ersten 24-72 Stunden ist graduell eine anti-hypertensive Behandlung, mit dem Ziel systolisch <140mmHg und diastolisch <90mmHg, einzuleiten (12, 13).
Abkürzungen:
ABCD2: Age ≥ 60 years, BP ≥ 140/90 mmHg, Clinical features,
Duration of symptoms, History of Diabetes
ADC: Apparent Diffusion Coefficient
ASS: Acetylsalicylsäure
CHA2DS2-VASc: Congestive heart failure, Hypertension, Age>=75, Diabetes Mellitus, prior Stroke or TIA or Thromboembolism, Vascular disease, Age 65-74, Sex Category – female
CT: Computed Tomography
DOAK: Direkte Orale Antikoagulanzien
DWI: Diffusion Weighted Imaging
FLAIR: Fluid-Attenuated Inversion Recovery
HAS-BLED: Hypertension, Abnormal renal and liver function, Stroke, Bleeding, Labile INR, Elderly, Drugs or alcohol
INR: International Normalized Ratio
MRI: Magnetic Resonance Imaging
NIHSS: National Institutes of Health Stroke Scale
PFO: Patent foramen ovale
rtPA: recombinant tissue Plasminogen Activator
SWI: Susceptibility Weighted Imaging
TIA: Transient Ischemic Attack
VHF: Vorhofflimmern
Copyright bei Aerzteverlag medinfo AG
Universitätsspital Basel
Neurologie, Stroke Center
Petersgraben 4
4031 Basel
Universitätsspital Basel
Neurologie, Stroke Center
Petersgraben 4
4031 Basel
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Kägi Georg, Schurter David, Niederhäuser Julien, De Marchis Gian Marco, Engelter Stefan, Arni Patrick, Nyenhuis Olivier, Imboden Paul, Bonvin Christophe, Luft Andreas, Renaud Susanne, Nedeltchev Krassen, Carrera Emmanuel, Cereda Carlo, Fischer Urs, Arnold Marcel, Michel Patrik. Prähospitalphase beim akuten Hirnschlag Swiss Med Forum. 2021;21(1920):322-328
2. Powers WJ, Rabinstein AA, Ackerson T, Adeoye OM, Bambakidis NC, Becker K, Biller J, Brown M, Demaerschalk BM, Hoh B, Jauch EC, Kidwell CS, Leslie-Mazwi TM, Ovbiagele B, Scott PA, Sheth KN, Southerland AM, Summers DV, Tirschwell DL. Guidelines for the Early Management of Patients With Acute Ischemic Stroke: 2019 Update to the 2018 Guidelines for the Early Management of Acute Ischemic Stroke: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-e418. doi: 10.1161/STR.0000000000000211. Epub 2019 Oct 30. Erratum in: Stroke. 2019 Dec;50(12): e440-e441. PMID: 31662037.
3. Kurzlehrbuch Neurologie. Mattle H, Fischer U, Hrsg. 5., überarbeitete Auflage. Stuttgart: Thieme; 2021. doi:10.1055/b000000093
4. Neurologie compact. Hufschmidt A, Lücking C, Rauer S, Glocker F, Hrsg. 8., unveränderte Auflage. Stuttgart: Thieme; 2020. doi:10.1055/b-007-170972
5. Berge E, Whiteley W, Audebert H, De Marchis GM, Fonseca AC, Padiglioni C, de la Ossa NP, Strbian D, Tsivgoulis G, Turc G. European Stroke Organisation (ESO) guidelines on intravenous thrombolysis for acute ischaemic stroke. Eur Stroke J. 2021 Mar; 6(1):I-LXII. doi: 10.1177/2396987321989865. Epub 2021 Feb 19. PMID: 33817340; PMCID: PMC7995316.
6. Turc G, Bhogal P, Fischer U, et al. European Stroke Organisation (ESO) – European Society for Minimally Invasive Neurological Therapy (ESMINT) Guidelines on Mechanical Thrombectomy in Acute Ischaemic StrokeEndorsed by Stroke Alliance for Europe (SAFE). European Stroke Journal. 2019;4(1):6-12. doi:10.1177/2396987319832140
7. Turc G, Tsivgoulis G, Audebert HJ, Boogaarts H, Bhogal P, De Marchis GM, Fonseca AC, Khatri P, Mazighi M, Pérez de la Ossa N, Schellinger PD, Strbian D, Toni D, White P, Whiteley W, Zini A, van Zwam W, Fiehler J. European Stroke Organisation (ESO)-European Society for Minimally Invasive Neurological Therapy (ESMINT) expedited recommendation on indication for intravenous thrombolysis before mechanical thrombectomy in patients with acute ischemic stroke and anterior circulation large vessel occlusion. J Neurointerv Surg. 2022 Mar;14(3):209. doi: 10.1136/neurintsurg-2021-018589. Epub 2022 Feb 3. PMID: 35115395.
8. Ay H, Furie KL, Singhal A, Smith WS, Sorensen AG, Koroshetz WJ. An evidence-based causative classification system for acute ischemic stroke. Ann Neurol. 2005 Nov;58(5):688-97. doi: 10.1002/ana.20617. PMID: 16240340.
9. Wasserlauf J, Volgman AS. Monitoring for atrial fibrillation after stroke. Lancet Neurol. 2021 Jun;20(6):410-411. doi: 10.1016/S1474-4422(21)00106-X. PMID: 34022159.
10. Ahmed N, Audebert H, Turc G, Cordonnier C, Christensen H, Sacco S, Sandset EC, Ntaios G, Charidimou A, Toni D, Pristipino C, Köhrmann M, Kuramatsu JB, Thomalla G, Mikulik R, Ford GA, Martí-Fàbregas J, Fischer U, Thoren M, Lundström E, Rinkel GJ, van der Worp HB, Matusevicius M, Tsivgoulis G, Milionis H, Rubiera M, Hart R, Moreira T, Lantz M, Sjöstrand C, Andersen G, Schellinger P, Kostulas K, Sunnerhagen KS, Keselman B, Korompoki E, Purrucker J, Khatri P, Whiteley W, Berge E, Mazya M, Dippel DW, Mustanoja S, Rasmussen M, Söderqvist ÅK, Escudero-Martínez I, Steiner T. Consensus statements and recommendations from the ESO-Karolinska Stroke Update Conference, Stockholm 11-13 November 2018. Eur Stroke J. 2019 Dec;4(4):307-317. doi: 10.1177/2396987319863606. Epub 2019 Sep 2. PMID: 31903429; PMCID: PMC6921948.
11. Dawson J, Merwick Á, Webb A, Dennis M, Ferrari J, Fonseca AC; European Stroke Organisation. European Stroke Organisation expedited recommendation for the use of short-term dual antiplatelet therapy early after minor stroke and high-risk TIA. Eur Stroke J. 2021 Jun;6(2):VI. doi: 10.1177/23969873211027006. Epub 2021 Jun 18. PMID: 34414307; PMCID: PMC8370061.
12. Klijn CJ, Paciaroni M, Berge E, Korompoki E, Kõrv J, Lal A, Putaala J, Werring DJ. Antithrombotic treatment for secondary prevention of stroke and other thromboembolic events in patients with stroke or transient ischemic attack and non-valvular atrial fibrillation: A European Stroke Organisation guideline. Eur Stroke J. 2019 Sep;4(3):198-223. doi: 10.1177/2396987319841187. Epub 2019 Apr 9. PMID: 31984228; PMCID: PMC6960695.
13. Sandset EC, Anderson CS, Bath PM, Christensen H, Fischer U, Gąsecki D, Lal A, Manning LS, Sacco S, Steiner T, Tsivgoulis G. European Stroke Organisation (ESO) guidelines on blood pressure management in acute ischaemic stroke and intracerebral haemorrhage. Eur Stroke J. 2021 Jun;6 (2):II. doi: 10.1177/23969873211026998. Epub 2021 Jun 18. PMID: 34780579; PMCID: PMC8370067.
14. Sandset EC, Anderson CS, Bath PM, et al. European Stroke Organisation (ESO) guidelines on blood pressure management in acute ischaemic stroke and intracerebral haemorrhage. European Stroke Journal. 2021;6(2):XLVIII-LXXXIX. doi:10.1177/2396987321101213314
der informierte @rzt
- Vol. 12
- Ausgabe 3
- März 2022