- Elektrische Felder in der Onkologie
Worldwide, cancer remains one of the leading causes of death. Many cancers eventually become resistant to common therapeutic approaches, justifying the need for novel therapeutic approaches. Tumor Treating Fields (TTFields) represent one of those new modalities. They are alternating electric fields with a low-level intensity (1-3 V/cm) and a frequency of 100-300 kHz which are orthogonally applied to the skin around the tumor by means of four transducer arrays to form two current fields. Preclinical research shows that cell death occurs mainly during metaphase and cytokinesis and further mechanisms of action are progressively discovered. A phase III randomized trial showed that TTFields improved progression-free overall survival in newly diagnosed glioblastoma compared to standard therapy. This promising therapeutic approach is now being evaluated with encouraging preliminary results in other indications including mesothelioma and ovarian, lung and pancreatic cancer.
Weltweit ist Krebs nach wie vor eine der häufigsten Todesursachen. Viele Krebsarten werden mit der Zeit resistent gegen gängige Therapieansätze, was den Bedarf an neuen Therapieansätzen rechtfertigt. Tumor Treating Fields (TTFields) stellen eine dieser neuen Anwendungen dar. Dabei handelt es sich um elektrische Wechselfelder mit geringer Intensität (1-3 V/cm) und einer Frequenz von 100-300 kHz, die mit Hilfe von vier Transducer Arrays orthogonal auf die Hautoberfläche rund um den Tumor aufgebracht werden, um zwei Stromfelder zu bilden. Die präklinische Forschung zeigt, dass der Zelltod hauptsächlich während der Metaphase und der Zytokinese eintritt, und weitere Wirkmechanismen werden nach und nach entdeckt. Eine randomisierte Phase-III-Studie zeigte, dass TTFields das progressionsfreie Gesamtüberleben bei neu diagnostiziertem Glioblastom im Vergleich zur Standardtherapie verbessert. Dieser aussichtsvolle therapeutische Ansatz wird nun mit vielversprechenden vorläufigen Ergebnissen in anderen Indikationen wie Mesotheliom, Eierstock-, Lungen- und Bauchspeicheldrüsenkrebs untersucht.
Key Words: Tumor Treating Fields (TTFields), Glioblastom, PFS, OS
Es ist seit langem bekannt, dass die elektrische Aktivität eine Schlüsselrolle bei einer Vielzahl von biologischen Prozessen spielt. Bei sehr niedrigen Stromfrequenzen (<1 KHz) werden erregbare Zellen, wie z. B. Neuronen und Muskelzellen depolarisiert. Dieser Effekt wird beispielsweise für die Anwendung von Neurostimulatoren und Herzschrittmachern genutzt. Sehr hohe Frequenzen erzeugen Wärme im Gewebe und werden für die Radiofrequenz angewendet. Bei mittleren Frequenzen (zwischen 10 und 1000 KHz) und wenn eine ausreichende Stromstärke angelegt wird, konnten verschiedene biologische Effekte nachgewiesen werden, darunter eine spezifische Blockade der Zellteilung. Da die Zellteilung zu jedem beliebigen Zeitpunkt stattfinden kann, ist eine längere Exposition gegenüber elektrischen Feldern von entscheidender Bedeutung, um diese Effekte beobachten zu können.
Präklinische Experimente an Zellkulturen und Tiermodellen zahlreicher Krebslinien mit sogenannten Tumor Treating Fields (TTFields, 1-3 V/cm, 100-500 kHz) haben eine Wirkung auf die mitotische Spindel gezeigt, indem sie auf Moleküle mit wichtigen Dipolen wie Septine und Mikrotubuli der Spindel abzielen: TTFields verhindern die Polymerisation der Mikrotubuli und blockieren die mitotische Spindel, wodurch die Zellteilung und die Trennung der Chromosomen gefährdet werden. TTFields wirken auch, indem sie bestimmte Gene blockieren, die für Mechanismen zur Korrektur von DNA-Schäden verantwortlich sind, wie z.B. das Gen für die Fanconi-Anämie. Zellen, die TTFields ausgesetzt sind, weisen auch eine erhöhte Autophagie und Zelltod durch Nekroptose auf, was durch einen Anstieg der Autophagosomen, die Erweiterung des endoplasmatischen Retikulums und abnormale mitochondriale Strukturen nachgewiesen wird. Die Zellmembranen, die den elektrischen Feldern ausgesetzt sind, werden auch durchlässiger, wodurch die Chemotherapie-Moleküle stärker eindringen können und somit synergistisch wirken. Darüber hinaus können TTFields die Zellmigration blockieren (1).
Um das klinische Potenzial von TTFields zu bewerten, wurde ein tragbares Gerät mit Akku entwickelt (Optune®, Novocure, Haifa, Israel). Die elektrischen Felder werden mithilfe von 4 Transducer Arrays angelegt, die auf die rasierte Haut geklebt und alle 3-4 Tage ausgetauscht werden.
Klinische Erfahrungen mit TTFields
Die ersten klinischen Versuche wurden an Patienten mit Hautmetastasen von Melanomen oder Brustkrebs durchgeführt und konnten eine Reduktion oder sogar deren vollständiges Verschwinden zeigen. Die Behandlung mit TTFields ist jedoch eine lokal-regionale Behandlung und aus diesem Grund wurden Glioblastome, die fast ausschließlich im Gehirn rezidivieren, schnell als ideale Kandidaten identifiziert, um das Potenzial der TTFields in prospektiven Studien abschließend zu demonstrieren. Außerdem ist die Anbringung der Transducer Arrays auf der rasierten Kopfhaut relativ einfach. Die Sicherheit und Durchführbarkeit wurde zunächst in einer kleinen Pilotstudie nachgewiesen. Anschließend wurden zwei Phase 3 randomisierte klinische Studien abgeschlossen, zunächst in Situationen mit rezidivierendem Glioblastom (Studie EF-11) und dann auch in Ergänzung zu einer herkömmlichen Radiochemotherapie beim neu diagnostizierten Glioblastom (Studie EF-14).
TTFields bei rezidivierendem Glioblastom
In der EF-11-Studie wurden 237 Patienten 1:1 zwischen einer konventionellen Chemotherapie und einer Behandlung mit alternierenden elektrischen Feldern randomisiert, wobei der primäre Endpunkt das Gesamtüberleben war. Aufgrund eines medianen Überlebens von nur 6,0 versus 6,6 Monaten war der Unterschied zwischen den beiden Gruppen statistisch nicht signifikant. Durch ihr Design wies diese Studie jedoch eine Reihe intrinsischer Einschränkungen auf, darunter eine unbegrenzte Anzahl früherer Behandlungslinien, was zu einer sehr heterogenen Population und Patienten mit fortgeschrittener Krankheit und geringerer Lebenserwartung führte. Interessanterweise wurden jedoch bei 14% der Patienten unter TTFields vs. 9,6% der Patienten unter Chemotherapie objektive radiologische Ansprechen beobachtet.
TTFields beim neu diagnostizierten Glioblastom (EF-14-Studie)
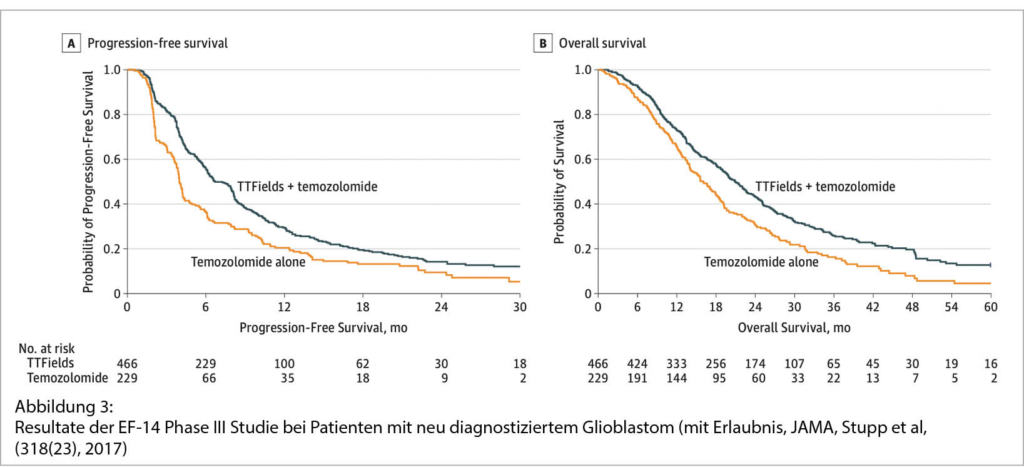
In dieser internationalen Phase-III-Studie wurden 695 Patienten (1:2) mit Glioblastom in der ersten Behandlungslinie randomisiert, um entweder Temozolomid zur Erhaltung allein (Kontrollgruppe) oder in Kombination mit elektrischen Wechselfeldern (Experimentalgruppe) zu erhalten. Der primäre Endpunkt dieser Studie war das progressionsfreie Überleben. Die Patienten wurden standardgemäss, nach dem Grad der Resektion (Biopsie, partielle & komplette Resektion) und dem Methylierungsstatus des MGMT-Promotors stratifiziert. Die Patientencharakteristika waren zwischen den beiden Gruppen homogen in Bezug auf Alter, Geschlechterverteilung sowie Leistungs- und MGMT-Status. Eine vorspezifizierte Zwischenanalyse, bei der 315 Patienten randomisiert wurden und eine mediane Nachbeobachtungszeit von 18 Monaten hatten, zeigte eine signifikante Verbesserung des progressionsfreien Überlebens und rechtfertigte die Entscheidung des Data Safety Monitoring Board (DSMB), das Ende der klinischen Studie zu empfehlen und allen Patienten, die sich noch in der Kontroll–gruppe in Behandlung befanden, die TTFields-Therapie anzubieten (2). Die endgültige Analyse, die 2017 veröffentlicht wurde, zeigte eine Verbesserung des progressionsfreien Überlebens von 4,0 Monaten auf 6,7 Monate unter Optune®. Das mediane Überleben wurde ebenfalls verbessert und stieg von 16,0 Monaten auf 20,9 Monate. Der Prozentsatz der Patienten, die nach 3 und 5 Jahren noch am Leben waren, verbesserte sich ebenfalls signifikant von 16% auf 26% bzw. von 5% auf 13%. Die Behandlung mit TTFields wurde gut vertragen und es traten keine signifikanten Nebenwirkungen auf, abgesehen von geringfügigen Hautreaktionen im Zusammenhang mit den Transducer Arrays. Die Analysen zur Lebensqualität zeigten, dass die zusätzliche TTFields-Behandlung keine negativen Auswirkungen auf die Lebensqualität der Patienten hatte, abgesehen von Hautjucken (3), das leicht durch topische Pflege oder eine vorübergehende Unterbrechung der TTFields Therapie behandelt werden konnte (4).
Nach ihrer Veröffentlichung lösten die Ergebnisse in der neuroonkologischen Fachwelt heftige Diskussionen aus, vor allem angesichts des völlig neuartigen Ansatzes. Kritik wurde auch geäußert, insbesondere wegen des Fehlens einer doppelblinden Randomisierung, der Wahrnehmung, dass diese Behandlung für die Patienten eher umständlich sei und dass die Wirkungsmechanismen von TTFields nur teilweise geklärt seien. Im Laufe der Zeit konnten diese Kritikpunkte jedoch ausgeräumt werden, insbesondere weil in der Neuroonkologie bislang keine zugelassene Behandlung doppelblind getestet wurde, die Messungen der wahrgenommenen Lebensqualität während der klinischen Studie EF-14 keine negativen Auswirkungen der Behandlung zeigten und die Wirkungsmechanismen der TTFields immer besser aufgeklärt werden. Aus diesen Gründen wird in den Leitlinien für die Behandlung des Glioblastoms vorgeschlagen, die Hinzufügung dieser Behandlung zur Temozolomid-Erhaltungsbehandlung in Betracht zu ziehen (5, 6). Seit April 2021 wird Optune® von den Grundversicherungen in der Schweiz für die Behandlung des neu diagnostizierten Glioblastoms erstattet.
Die Ergebnisse der EF-14-Studie liefern Evidenz der Klasse I, die zeigt, dass TTFields das Tumorwachstum bei Glioblastomen positiv beeinflussen und das Überleben der Patienten verbessern können. Diese Ergebnisse ermöglichen es, TTFields auch in anderen onkologischen Situationen zu testen, die von einer lokoregionalen Behandlung profitieren könnten, wie z.B. im Mesotheliom, Hirnmetastasen, Lungen-, Eierstock- und Bauchspeicheldrüsenkrebs. Erste ermutigende Daten liegen bereits vor: So zeigte eine Phase-II-Studie, dass die Zugabe von TTFields zu einer Gemcitabin-Therapie bei Patienten mit Bauchspeicheldrüsenkrebs eine partielle Ansprechrate von 30% und ein medianes progressionsfreies Überleben von 8,3 Monaten erzielte. Vor kurzem empfahl eine DSMB-Überprüfung der Interimsdaten der Phase-III-Studie LUNAR, die nach dem Einschluss von 210 Patienten mit nicht-kleinzelligem Lungenkrebs im Stadium IV, die mit einer Immuntherapie mit Checkpoint-Inhibitoren oder Docetaxel mit oder ohne Zusatz von TTFields behandelt wurden durchgeführt wurde, den Einschluss von 534 auf 276 Patienten zu verringern. Diese Zahl wird ihrer Ansicht nach ausreichen, um die statistische Aussagekraft zu erreichen, die zur Bestätigung der primären und sekundären Endpunkte der Studie erforderlich ist.
Copyright bei Aerzteverlag medinfo AG
Départements d’Oncologie, de Radiothérapie et
des Neurosciences Cliniques, UNIL-CHUV
Rue du Bugnon 46
1011 Lausanne
Départements d’Oncologie, de Radiothérapie et
des Neurosciences Cliniques, UNIL-CHUV
Rue du Bugnon 46
1011 Lausanne
Départements d’Oncologie, de Radiothérapie et
des Neurosciences Cliniques, UNIL-CHUV
Rue du Bugnon 46
1011 Lausanne
RDM und LS haben keine Interessenkonflikte. AFH hat von Novocure einen Grant für wissenschaftliche Forschung erhalten, der an das CHUV gezahlt wird.
◆ Mit diversen vielversprechenden Ergebnissen erweisen sich TTFields als eine neue, wirksame Behandlungsmethode, die in Kombination
mit dem gesamten bereits vorhandenen Therapiearsenal eingesetzt werden kann und deren Anwendungsbereich weit über den Bereich der Neuroonkologie hinausgehen wird.
1. Karanam, NK, Story, MD: An overview of potential novel mechanisms of action underlying Tumor Treating Fields-induced cancer cell death and their clinical
implications. Int J Radiat Biol 2021, 97:1044-1054.
2. Stupp, R, Taillibert, S, Kanner, AA, Kesari, S, Steinberg, DM, Toms, SA, Taylor, LP, Lieberman, F, Silvani, A, Fink, KL et al. : Maintenance Therapy With Tumor-Treating Fields Plus Temozolomide vs Temozolomide Alone for Glioblastoma:
A Randomized Clinical Trial. JAMA 2015, 314:2535-2543.
3. Taphoorn, MJB, Dirven, L, Kanner, AA, Lavy-Shahaf, G, Weinberg, U, Taillibert, S, Toms, SA, Honnorat, J, Chen, TC, Sroubek, J et al: Influence of Treatment With Tumor-Treating Fields on Health-Related Quality of Life of Patients With Newly Diagnosed Glioblastoma: A Secondary Analysis of a Randomized Clinical Trial. JAMA Oncol 2018,
4. Lacouture, ME, Davis, ME, Elzinga, G, Butowski, N, Tran, D, Villano, JL, DiMeglio,
L, Davies, AM, Wong, ET: Characterization and management of dermatologic adverse events with the NovoTTF-100A System, a novel anti-mitotic electric field device for the treatment of recurrent glioblastoma. Semin Oncol 2014, 41 Suppl 4:S1-14.
5. Mohile, NA, Messersmith, H, Gatson, NT, Hottinger, AF, Lassman, A, Morton,
J, Ney, D, Nghiemphu, PL, Olar, A, Olson, J, Perry, J, Portnow, J, Schiff, D,
Shannon, A, Shih, HA, Strowd, R, van den Bent, M, Ziu, M, Blakeley, J. Therapy for Diffuse Astrocytic and Oligodendroglial Tumors in Adults: ASCO-SNO Guideline. J Clin Oncol. 2021 Dec 13. Online ahead of print. PMID: 34898238.
6. Roth, P, Hottinger, AF, Hundsberger, T, Läubli, H, Schucht, P, Reinert, M,
Mamot, C, Roelcke, U, Pesce, G, Hofer, S, Weller, M: A contemporary perspective on the diagnosis and treatment of diffuse gliomas in adults. Swiss Med Wkly 2020, 150:w20256.
info@onco-suisse
- Vol. 12
- Ausgabe 2
- März 2022