- Genexpressionstests beim lokalisierten Prostatakarzinom
In der Schweiz wird jedes Jahr bei mehr als 6000 Männern eine Prostatakrebsdiagnose gestellt. Die Krankheit ist sehr heterogen und reicht von indolenten Karzinomen, welche am besten beobachtet werden, bis zu aggressiven Karzinomen, welche rasch in eine metastasierte Situation übergehen. Im Arzt-Patienten Gespräch ist gerade bei der Neudiagnose eines lokalisierten Prostatakarzinoms eine realistische Risikoeinschätzung und Beratung bezüglich der möglichen Therapie-Optionen essentiell. Traditionell beruht die Risikoklassifikation in der lokalisierten Situation auf PSA, Gleason/ISUP Grad und bildgebenden Informationen (MRI zum lokalen Staging, PSMA PET/CT fürs systemische Staging). In Zukunft können möglicherweise Genexpessionstests wichtige Zusatzinformationen liefern.
In Switzerland, more than 6000 men are diagnosed with prostate cancer each year. The disease is very heterogeneous and ranges from indolent carcinomas, which are best observed, to aggressive carcinomas, which rapidly progress to a metastatic situation. In the doctor-patient discussion, a realistic risk assessment and advice regarding the possible therapy options is of great importance, especially in the case of a new diagnosis of a localized prostate carcinoma. Traditionally, risk classification in the localized situation is based on PSA, Gleason/ISUP grade and imaging information (MRI for local staging, PSMA PET/CT for systemic staging). In future, gene expression tests may provide important additional information.
Key Words: Prostate cancer, Gene expression tests
Klinische Einordnung von Genexpressionstests
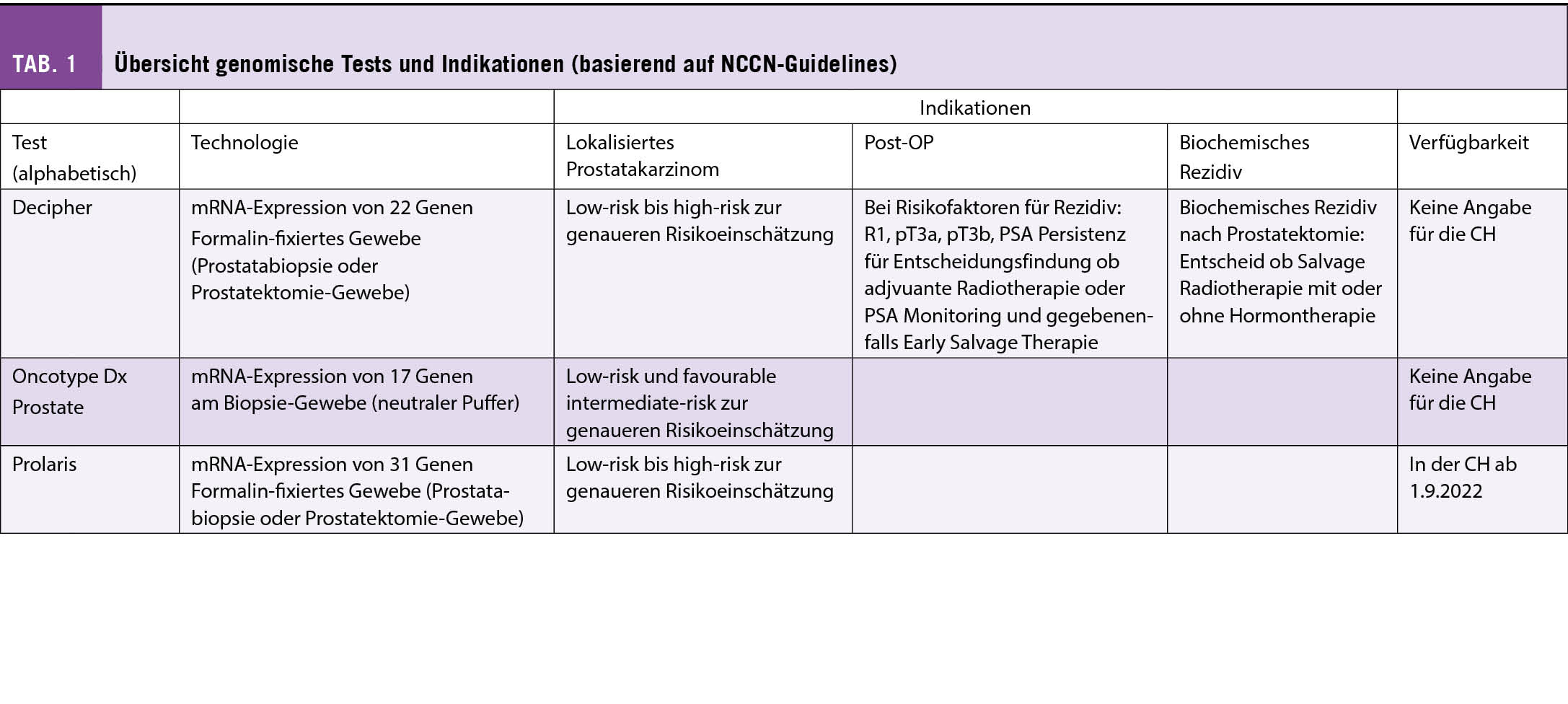
In den letzten Jahren sind im Bereich des lokalisierten Prostatakarzinoms verschiedene Genexpressionstests entwickelt, evaluiert und kommerzialisiert worden. Das übergeordnete Ziel: eine personalisierte Risikoeinschätzung, welche gezieltere Therapievorschläge erlaubt. Diese Tests untersuchen mRNA Expressions-Profile am Tumorgewebe und umfassen dabei 20-30 Gene. Verschiedene Tests sind aktuell vor allem in den USA verfügbar: Decipher®, Prolaris® und Oncotype Dx Prostate®.
Beim lokalisierten Prostatakarzinom sind mehrere Fragestellungen interessant, für die Genexpressionstests eine relevante Zusatzinformation bringen können:
- Bei lokalisiertem Prostatakarzinom mit niedrigem Risiko:
Welche Patienten sollten aktiv überwacht werden, welche benötigen eine aktive Therapie? - Bei lokalisiertem Prostatakarzinom mit intermediärem Risiko: Welche Patienten benötigen eine Hormontherapie zusammen mit der Strahlentherapie, bei welchen reicht eine alleinige Radiotherapie?
- Bei Prostatakarzinom nach radikaler Prostatektomie: Welche Patienten mit Risikofaktoren profitieren von einer adjuvanten Strahlentherapie mit oder ohne Hormontherapie und welche können überwacht werden?
- Beim biochemischen Rezidiv nach radikaler Prostatektomie: Welche Patienten profitieren bei der Salvage Radiotherapie von einer zusätzlichen Hormontherapie?
Die NCCN-Guidelines haben diese Genexpressionstests bereits als Option in die Algorithmen als zusätzliche Information für die Entscheidungsfindung aufgenommen. Die europäischen Guidelines (EAU) äussern sich noch zurückhaltend zum Einsatz dieser Tests. Wenn Genexpressionstests angewendet werden, dann sollten unbedingt alle anderen klinischen Faktoren auch berücksichtig werden und ein Therapieentscheid nicht rein auf die molekulare Diagnostik gestützt werden.
Limitationen der Genexpressionstests sind zum aktuellen Zeitpunkt: Die Mehrheit der Daten stammt aus retrospektiven Studien – grosse, randomisierte prospektive Studien sind aber bereits lanciert worden. Langzeitdaten, vor allem zu onkologisch relevanten Endpunkten wie Gesamtüberleben, fehlen. Wichtig ist auch zu beachten, dass Gewebe-basierte genomische Tests eine allfällige
intratumorale Heterogenität nur ungenügend abbilden können und zum Beispiel primär am Gewebe einer Stanzbiopsie gemacht werden, ohne die übrigen Biopsien zu berücksichtigen.
Patientenbeispiel
Anamnese
Ein 64-jähriger Mann wird abgeklärt bei PSA Erhöhung auf 7.5 ohne Auffälligkeiten bei der Miktion.
In der klinischen Untersuchung zeigt sich die Prostata nicht vergrössert und ohne palpable Indurationen. Relevante Nebendiagnosen liegen nicht vor.
Die multiparametrische MRI-Untersuchung ergibt: Prostatavolumen 28ml, eine auffällige Läsion in der peripheren Zone links (PI-RADS 4), keine weiteren Auffälligkeiten, die PSA-Dichte ist mit 0.27 ng/ml/cc deutlich erhöht.
Die MRI-TRUS Fusionsbiopsie zeigt mittels 16 Biopsien (gezielt und systematisch) folgendes Resultat:
4 positive Biopsien:
- Links: Gleason 3+3, ISUP Gruppe 1, Zylinderbefall 10%
- Links: Gleason 3+3, ISUP Gruppe 1, Zylinderbefall 15%
- Rechts: Gleason 3+3, ISUP Gruppe 1, Zylinderbefall 30%
- Rechts: Gleason 3+3, ISUP Gruppe 1, Zylinderbefall 60%
Die zusätzlich durchgeführte PTEN-Analyse ergibt immunhistochemisch keinen Anhaltspunkt für PTEN-Verlust.
Therapie-Empfehlung
Zusammengefasst liegt ein lokalisiertes Prostatakarzinom vor. Die TNM-Klassifikation stellt aber bereits eine Herausforderung dar:
Nach klassischen Kriterien wäre der Tumor als T1c einzustufen, nach MRI-Kriterien als T2a und in der Biopsie wurde letzten Endes ein Prostatakarzinom bilateral in der Prostata gefunden. Je nach T-Stadium fällt der Patient mit den übrigen oben erwähnten Kriterien in eine low-risk oder sogar eine high-risk Kategorie und entsprechend variieren auch die Therapie-Empfehlungen. Wichtig ist hier aber zu betonen, dass nach aktuellen Guidelines für das T-Staging nur die digital rektale Untersuchung (DRU) verwendet wird und die MRI-Information noch nicht. Insgesamt wurde dem Patienten bei Vorliegen aller Befunde eine aktive Therapie im Sinne einer radikalen Prostatektomie beziehungsweise einer Radiotherapie der Prostata mit oder ohne begleitende Hormontherapie über 6 Monate empfohlen.
Patientenwunsch
Aktive Überwachung und zurzeit keine aktive Therapie.
Können Genexpressionstests in dieser Situation hilfreich sein?
Die Genexpressionstests könnten hier helfen, eine bessere Einteilung vorzunehmen. In einer kürzlich veröffentlichten Arbeit wurden lokalisierte Prostatakarzinome anhand der vorhandenen klinischen und pathologischen Variablen in die klassischen 6 Risiko-Kategorien nach NCCN eingeteilt. Die Integration des mRNA-Expressionsprofils am Prostatakarzinomgewebe mittels Decipher Score zusammen mit den klinischen Variablen hat zu einer Reklassifizierung innerhalb der 6 NCCN-Risikogruppen in 67% der Patienten geführt (Spratt et al. J Clin Oncol 36:581-590). Am ASCO 2022 wurde eine Arbeit vorgestellt, in welcher der Decipher Score retrospektiv an Tumorgewebeproben einer grossen Phase III Studie mit lokalisiertem Prostatakarzinom (intermediate risk) untersucht wurde. Der Decipher Score konnte als unabhängiger prognostischer Wert bestätigt werden (Spratt et. al. J Clin Oncol 40, 2022 suppl 6; Abstr 269).
Ein genetischer Test wie beispielsweise «Prolaris» könnte im oben erwähnten Fall als Entscheidungshilfe hinzugezogen werden. Wichtig ist zu beachten, dass diese Tests nur zusätzliche prognostische Informationen liefern und nicht prädiktiv sind für eine spezifische Therapiemodalität. Der Prolaris Molecular Score (CCP) wird mit dem CAPRA-Score des Patienten kombiniert. Daraus resultiert der Combined Clinical Cell Cycle Risk (CCR)-Score, der alle verfügbaren prognostischen Informationen als Prognose-Faktoren vereint. Bei einem CCR-Score von >0.8 hätte der Patient ein geschätztes Risiko von knapp 10-15% an seinem Prostatakarzinom innerhalb von 10 Jahren zu versterben, bei einem CCR-Score von <0.8 wäre das Risiko am Prostatakarzinom innerhalb von 10 Jahren zu versterben bei geschätzt 2%.
Grosse, randomisierte Phase III Studien sind aktiviert worden (z.B. PREDICT-RT, G-MAJOR, ERADICATE, G-MINOR, NRG GU 008), welche diese neuen Tests in verschiedenen Krankheitssituationen prospektiv, untersuchen. Bis erste Resultate vorliegen wird es aber noch einige Jahre dauern.
In den EAU Guidelines wird diskutiert, dass diese Tumorgewebe basierten Genexpressionstest die prognostische Sicherheit von multivariablen Modellen zur Identifikation von Patienten, welche eher von einer aktiven Überwachung profitieren, beziehungsweise eher von einer aktiven Therapie, deutlich verbessern. Da onkologische Langzeitdaten (Gesamtüberleben) fehlen, wird der Einsatz dieser Tests zurzeit nicht routinemässig empfohlen. Bei Fällen, welche zum Beispiel grenzwertig für die aktive Überwachung qualifizieren, kann als Zusatzinformation zu den bereits verfügbaren klinisch-pathologischen Variablen aber ein Einsatz der Tests in Betracht gezogen werden.
Copyright bei Aerzteverlag medinfo AG
Onkozentrum Zürich
Seestrasse 259
8038 Zürich
Onkozentrum Zürich
Seestrasse 259
8038 Zürich
Zentrum für Urologie Zürich, Klinik Hirslanden
Witellikerstrasse 40
8032 Zürich
stephan.bauer@hirslanden.ch
Die Autoren haben keinen Interessenskonflikt in
Zusammenhang mit diesem Artikel deklariert.
◆ Beim lokalisierten Prostatakarzinom, in der postoperativen Situation und im biochemischen Rezidiv, stehen verschiedene Therapie-Optionen zu Verfügung.
◆ Die verfügbaren klinischen Faktoren sind oft unbefriedigend für die Risikoeinschätzung und Entscheidungsfindung in der individuellen Patienten-Situation.
◆ Tumorgewebe-basierte Genexpressionstests, welche die mRNA-Expression von 17-31 Genen untersuchen (Decipher®, Prolaris®, Oncotype Dx Prostate®)
sind entwickelt worden und werden zunehmend Einzug halten in die
klinische Praxis.
◆ Die Guidelines empfehlen zurzeit noch keinen routinemässigen Einsatz
dieser Tests, aber im Einzelfall kann die genetische Information einen Zusatznutzen erbringen im Sinne einer besseren Risikoeinschätzung und personalisierten Therapieempfehlung, insbesondere beim lokalisierten Prostatakarzinom in den Kategorien «low risk» und «intermediate risk».
◆ Die Information eines genetischen Tests ersetzt nicht die sorgfältige Beratung und Risiko-Abwägung im Rahmen eines fachärztlichen Gesprächs.
info@onco-suisse
- Vol. 12
- Ausgabe 5
- August 2022