- Akuter Thoraxschmerz
Akute thorakale Schmerzen sind häufig und benötigen eine notfallmässige Abklärung, um lebensbedrohliche Erkrankungen nachzuweisen oder auszuschliessen. Kardiovaskuläre Erkrankungen sind weiterhin weltweit die häufigste Todesursache, sodass ein früher Ein- respektive Ausschluss eines akuten Koronarsyndroms von entscheidender prognostischer Bedeutung ist. Die Diagnostik beinhaltet klinische Präsentation und Untersuchung, das 12-Kanal-Elektrokardiogramm sowie das kardiale Troponin als Herz-spezifischer Nekrosemarker. Durch die Verwendung neuer Algorithmen basierend auf den hochsensitiven kardialen Troponinen ist ein schneller und sicherer Ausschluss beziehungsweise eine akkurate Diagnose eines akuten Myokardinfarktes möglich. Mit neuen point-of-care-Assays können diese Algorithmen in Zukunft auch in der Hausarztpraxis angewendet werden.
Acute chest pain is a frequent cause for presentation and needs an immediate work-up to rule in or rule out life-threatening diseases. An early diagnosis of an acute coronary syndrome is of vital importance as cardiovascular diseases are amongst the most common causes of death worldwide. Initial diagnostics include the clinical presentation, a 12-lead-electrocardiogram and cardiac troponin as heart-specific biomarker. Since the introduction of algorithms based on high-sensitivity cardiac troponin, it has been possible to rapidly and safely rule out or accurately rule in an acute myocardial infarction. With new point-of-care-Assays, it will become possible to use the high-sensitivity cardiac troponin and early triage algorithms in the ambulatory setting, e.g. in private practices.
Key Words: Acute chest pain, acute myocardial infarction, electrocardiogram, high-sensitivity cardiac troponin
Einleitung
Akute thorakale Schmerzen sind häufig und machen etwa 10% der Vorstellungen auf Notfallstationen aus. Die Differentialdiagnose des akuten Thoraxschmerzes ist sehr breit und beinhaltet kardiale, pulmonale, gastrointestinale, muskuloskelettale sowie psychologische Ätiologien. Einige sind akut lebensbedrohlich wie ein akutes Koronarsyndrom (ACS), Lungenembolien oder eine Aortendissektion. Andere sind in der ambulanten Praxis zwar häufig, insgesamt jedoch ungefährlich wie zum Beispiel die muskuloskelettalen Thoraxschmerzen. Die lebensbedrohlichen von den ungefährlichen Ursachen zu unterscheiden, kann aufgrund der meist unspezifischen Klinik äusserst herausfordernd sein.
Die frühe Erkennung von akut lebensbedrohlichen Ursachen ist von entscheidender Bedeutung. Das gilt insbesondere für das akute Koronarsyndrom, da kardiovaskuläre Erkrankungen nach wie vor die weltweit häufigste Todesursache darstellen. Ein schneller und sicherer Einschluss, «rule-in», oder Ausschluss, «rule-out», eines akuten Myokardinfarktes (AMI) erlaubt es, eine frühzeitige Therapie einzuleiten respektive den Spitalaufenthalt signifikant zu reduzieren.
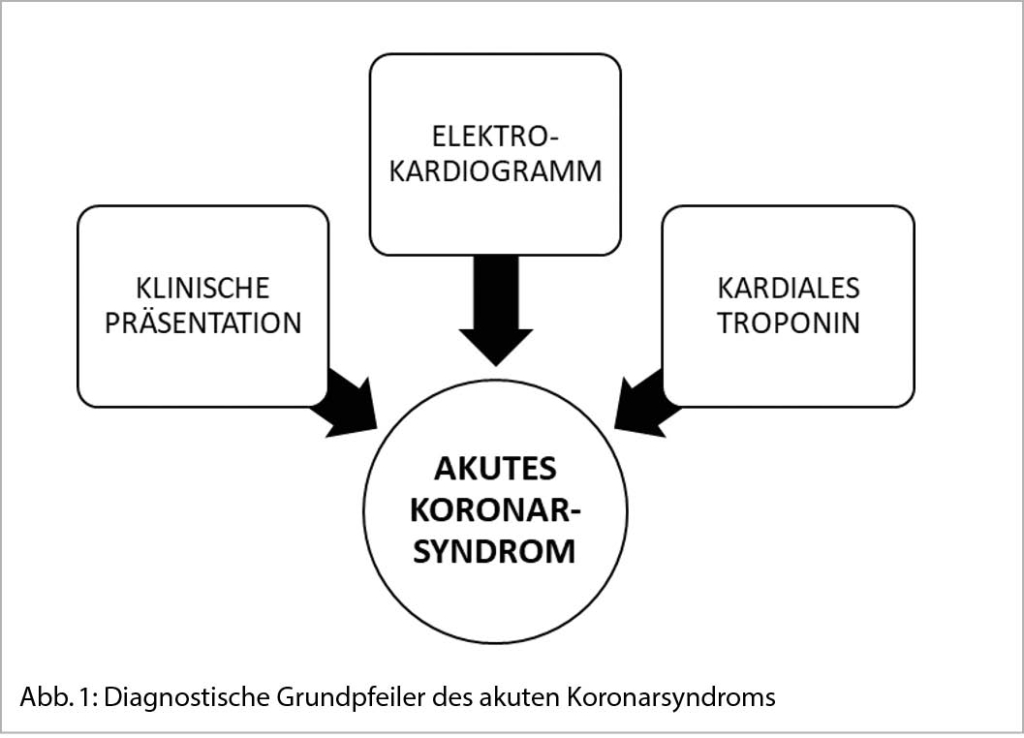
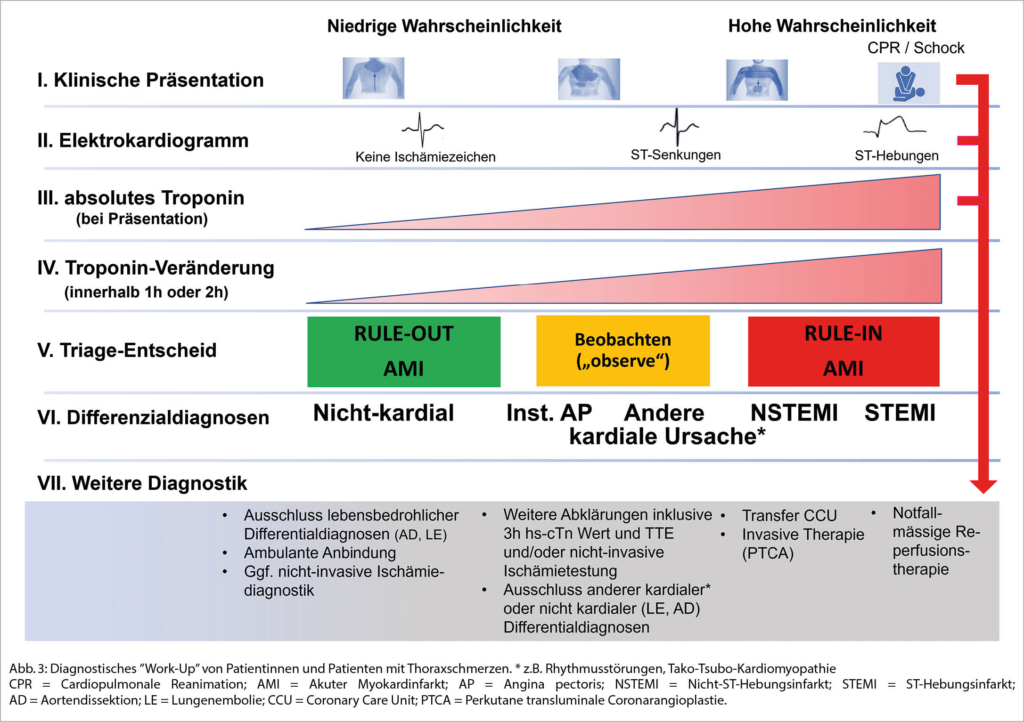
Im Folgenden beschränken wir uns auf einen Überblick über die initiale Diagnostik des akuten kardialen Thoraxschmerzes basierend auf Häufigkeit und klinischer Relevanz. Insgesamt stützt sich dessen Diagnostik auf folgende drei Grundpfeiler: klinische Präsentation, Elektrokardiogramm (EKG) sowie kardiale Troponine (cTn). Mittels EKG kann ein ST-Hebungsinfarkt (STEMI) frühzeitig erkannt werden, während die Diagnostik des Nicht-ST-Hebungsinfarktes (NSTEMI) vor allem auf den kardialen Troponinen beruht. Natürlich sollte die Suche nach anderen lebensbedrohlichen Ursachen eines akuten Thoraxschmerzes nicht vergessen werden, weshalb weitere Laboruntersuchungen (z.B. CRP, D-Dimere) und apparative Abklärungen (z.B. Computertomogramm des Thorax oder Echokardiographie) je nach Situation sinnvoll sind (1–4).
Klinik
Kardiale Thoraxschmerzen können in typische und atypische Angina Pectoris (AP) sowie in nicht-anginöse Thoraxbeschwerden eingeteilt werden. Die typische AP-Symptomatik ist durch das gemeinsame Auftreten der drei folgenden Kriterien definiert: retrosternales Druck- oder Engegefühl mit Ausstrahlung in linken Arm, Hals oder Kiefer, auslösen der Beschwerden durch eine körperliche oder psychische Belastung sowie vollständige Regredienz innerhalb von fünf Minuten durch Ruhe oder Einnahme von Nitraten. Bei der atypischen Angina pectoris liegen nur zwei der drei genannten Kriterien vor. Ist nur eines oder keines der Kriterien erfüllt, so handelt es sich um einen nicht-anginösen Thoraxschmerz. Oft präsentieren sich Patienten, insbesondere Frauen, jedoch auch mit sehr unspezifischer Symptomatik wie z.B. Dyspnoe, Nausea, Oberbauchschmerz oder Schwäche. Insbesondere eine isolierte Dyspnoe kann durchaus als AP-Äquivalent auftreten(2–4).
Bei der stabilen Angina pectoris verlaufen die Schmerzepisoden immer gleich und bessern sich in Ruhe oder nach Einnahme von Nitroglycerin prompt. Als instabile AP werden AP-Beschwerden bezeichnet, welche erst seit Kurzem vorhanden sind (de-novo-Angina) oder an Dauer, Häufigkeit oder Intensität zunehmen (Crescendo-Angina). Des Weiteren gelten AP-Beschwerden in Ruhe oder innerhalb der ersten zwei Wochen nach abgelaufenem AMI ebenfalls als instabile AP (Ruhe-Angina resp. Postinfarkt-Angina). Die instabile AP unterscheidet sich vom NSTEMI durch ein normales oder nur leicht erhöhtes Troponin ohne signifikante Dynamik. Patienten mit instabiler AP sollten zum Nachweis/Ausschluss eines AMI umgehend in ein Spital, zugewiesen werden(1–4).
Elektrokardiogramm
Die wichtigste initiale apparative Diagnostik zur Beurteilung einer Myokardischämie ist immer noch das Elektrokardiogramm, welches in den ersten 10 Minuten nach Vorstellung erfolgen sollte. Insbesondere kann damit frühzeitig zwischen einem STEMI und einem NSTEMI differenziert werden. Der STEMI ist definiert durch ST-Streckenhebungen, gemessen am J-Punkt, in zwei benachbarten Ableitungen (I+aVL, II+III+aVF, V1-V6) mit einer Amplitude von ≥0.1mV. Als signifikant werden ST-Streckenhebungen in den Ableitungen V2 und V3 bei einer Amplitude von ≥0.15mV bei Frauen und ≥0.25mV bei Männern <40 Jahren respektive ≥0.2mV bei Männern ≥40 Jahren gewertet. Die Lokalisation der Repolarisationsstörungen erlaubt zudem Rückschlüsse auf das Infarktgebiet und das betroffene Koronargefäss. Bei Vorliegen von ST-Streckensenkungen in V1-3 oder bei inferiorem Myokardinfarkt kann die Aufzeichnung von posterioren (V7-9) respektive rechtsventrikulären Ableitungen (V3R, V4R) hilfreich sein. Zeigt sich im EKG ein STEMI, so muss eine sofortige Zuweisung in ein Spital mit Katheterlabor erfolgen (3).
Ein Linksschenkelblock (LSB) kann die Interpretation des EKGs und die Diagnose eines STEMIs massgeblich erschweren. Nach den aktuellen Richtlinien der Europäischen Gesellschaft für Kardiologie sollten Patienten mit LSB und klinischem Verdacht auf eine Myokardischämie gleich wie Patienten mit STEMI behandelt werden. Dies gilt unabhängig davon, ob es sich um einen neu aufgetretenen oder vorbestehenden LSB handelt. Hilfreich ist bei Vorliegen eines kompletten Linksschenkelblocks die Anwendung der sogenannten Sgarbossa-Kriterien (3).
Die EKG-Veränderungen bei einem NSTEMI oder einer instabilen AP können sich unterschiedlich präsentieren. Typischerweise finden sich ST-Streckensenkungen oder T-Negativierungen, allerdings ist das EKG in über 30% der NSTEMI unauffällig (2, 3, 5).
Das Auftreten von signifikanten Q-Zacken im EKG weist auf einen abgelaufenen Infarkt hin (2, 3).
Das kardiale Troponin
Das kardiale Troponin (cTn) ist ein Proteinkomplex aus der Gruppe der Troponine, dessen Untereinheiten Troponin T und Troponin I in den Herzmuskelzellen exprimiert und bei deren Schädigung in die periphere Blutbahn freigesetzt werden. Troponin T und Troponin I (nicht das Troponin C) können als Biomarker für eine Myokardnekrose, insbesondere im Rahmen eines AMI, benutzt werden. Die Verwendung von kardialen Troponinen erlaubt auch eine quantitative Aussage über das Ausmass der Myokardnekrose. Je höher der Troponin-Wert, desto ausgeprägter ist die Schädigung der Kardiomyozyten. Dank der Entwicklung der hoch-sensitiven Troponine (hs-cTn) können nun auch erhöhte Troponinwerte im tiefen Bereich nachgewiesen werden, was zu einer höheren diagnostischen Präzision zum Zeitpunkt der Präsentation führt und auch eine frühere Diagnosestellung erlaubt (2).
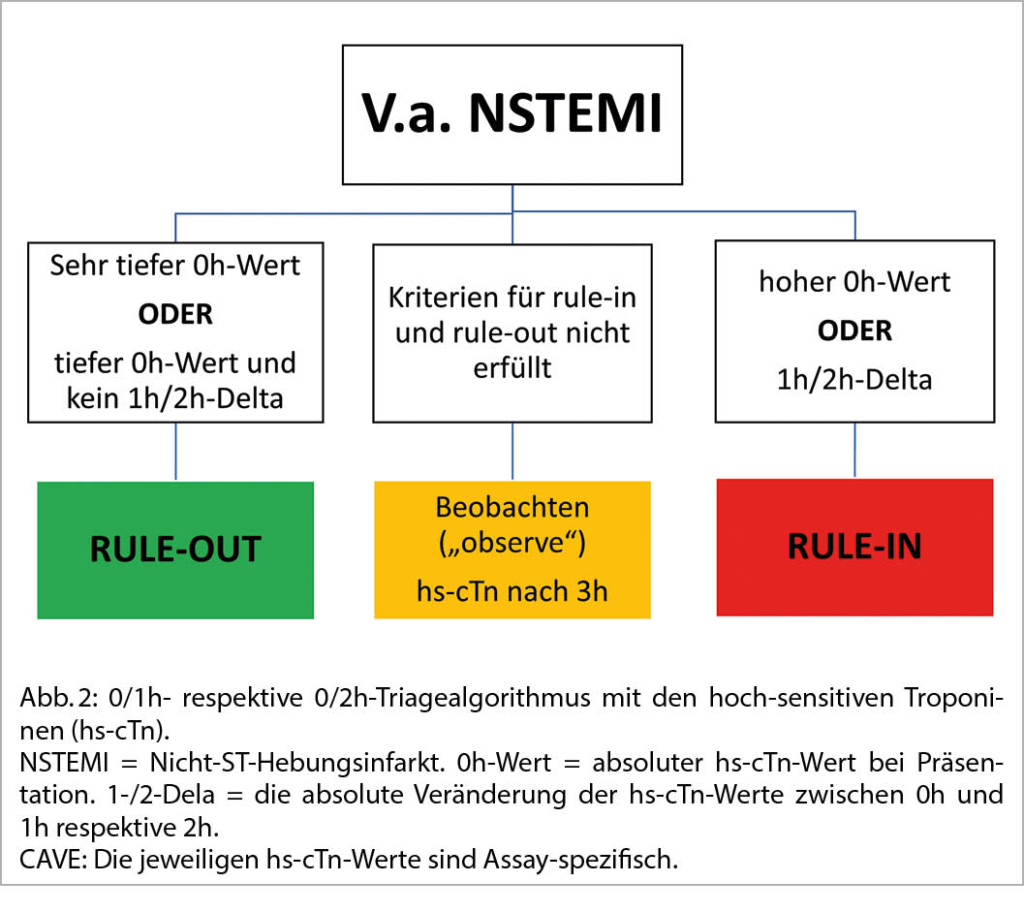
In den letzten Jahren wurden zur Diagnostik eines Myokardinfarktes mittels hs-cTn eine Vielzahl an Algorithmen entwickelt, welche den schnellen und sicheren Aus- respektive Einschluss eines AMI erlauben. Die aktuellen Richtlinien der Europäischen Gesellschaft für Kardiologie empfehlen die Verwendung des 0/1-Stunden- sowie des 0/2-Stunden-Algorithmus. Diese beiden Algorithmen basieren auf den absoluten Troponin-Werten bei Präsentation sowie den absoluten Werten nach einer respektive zwei Stunden. Ebenfalls wird die Dynamik der Troponin-Veränderung, also das absolute Delta der zwei Troponin-Werte, berücksichtigt. Es gilt jedoch zu beachten, dass sich die jeweiligen Werte je nach rule-in/rule-out-Algorithmus und Assay unterscheiden.
In verschiedenen Studien zeigten sich der 0/1h- resp. 0/2h-Algorithmus als sehr sicher, der negativ prädiktive Wert für ein korrektes «rule-out» lag bei über 99%. Falls die «rule-out»-Kriterien, nämlich ein tiefes hs-cTn bei Vorstellung sowie das Fehlen eines signifikanten Anstieges des hs-cTn, erfüllt sind, kann in Zusammenschau mit Klinik und EKG ein AMI mit grosser Sicherheit ausgeschlossen werden. Bei Vorliegen eines Myokardinfarktes («rule-in») zeigen sich entweder initial hohe hs-cTn-Werte und/oder signifikante hs-cTn-Veränderungen nach 1 respektive 2 Stunden (6–10).
Weiter korrelieren die rule-out-Kriterien mit einem sehr tiefen Auftreten von unerwünschten Ereignissen in den ersten 30 Tagen. Patienten, bei denen ein NSTEMI mittels Algorithmus ausgeschlossen wurde, haben dementsprechend ein gutes Outcome (11, 12).
Bisher war der Einsatz von hoch-sensitiven Troponinen nur auf der Notfallstation möglich, da lediglich die weniger sensitiven cTn-Assays als point-of-care (POC)-Assays erhältlich waren. Vor Kurzem wurden die ersten point-of-care hs-cTn-Assays validiert, wobei das Ergebnis der rule-in/rule-out- Algorithmen mit den bisher validierten Zentrallabor-Assays vergleichbar war. Durch den Einsatz dieser neuen POC-Assays können die Triagealgorithmen und die damit verbundenen Vorteile in der Zukunft auch im hausärztlichen Setting genutzt werden (13).
Zusammenfassung
Patienten, die sich mit akuten Thoraxschmerzen in der Hausarztpraxis oder auf einer Notfallstation vorstellen, sind häufig und stellen aufgrund der vielen Differentialdiagnosen den Kliniker vor eine Herausforderung. Die Grundpfeiler der Diagnostik bestehen aus Klinik, EKG und den kardialen Troponinen. Insbesondere durch die Entwicklung der hoch-sensitiven Troponine und den darauf basierenden rule-out/rule-in-Algorithmen kann ein AMI schnell und sicher von einer instabilen AP respektive einem extrakardialen Thoraxschmerz unterschieden werden. Dies erlaubt es, Patienten in der rule-in-Gruppe frühzeitig zur Therapie in ein Spital mit Koronarangiographie zuzuweisen. Andererseits können Patienten ohne Hinweis auf ein akutes Koronarsyndrom ebenfalls mit grosser Sicherheit nach Hause entlassen werden, was zu einer kürzeren Aufenthaltsdauer im Spital führt. Dank der neuen point-of-care-Assays können die schnellen Triagealgorithmen zukünftig auch in der Hausarztpraxis zur Anwendung kommen und dabei helfen, die Belastung der Notfallstationen zu verringern sowie dem Patienten einen unnötigen Aufenthalt auf der Notfallstation zu ersparen.
Copyright by Aerzteverlag medinfo AG
Klinik für Kardiologie
Universitätsspital Basel
Petersgraben 4
4031 Basel
dominiknicolas.breitenbuecher@usb.ch
Klinik für Kardiologie
Universitätsspital Basel
Petersgraben 4
4031 Basel
jasper.boeddinghaus@usb.ch
Leiter interventionelle Kardiologie
Klinik für Kardiologie
Universitätsspital Basel
Petersgraben 4
4031 Basel
christoph.kaiser@usb.ch
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Der akute Thoraxschmerz ist sehr häufig. Eine rasche Unterscheidung von lebensgefährlichen von den ungefährlichen Ätiologien ist eine Herausforderung für den Kliniker.
◆ Herzkreislauferkrankungen sind die häufigste Todesursache weltweit, sodass insbesondere die Abklärung respektive die Diagnose des
akuten Koronarsyndroms sehr wichtig ist.
◆ Die initiale Diagnostik des akuten Koronarsyndroms besteht aus der klinischen Präsentation, dem Elektrokardiogramm sowie den kardialen Troponinen.
◆ Durch die Einführung der auf den hoch-sensitiven Troponinen basierenden Triagealgorithmen kann die Differentialdiagnose des akuten Myokardinfarktes frühzeitig sicher ausgeschlossen und akkurat eingeschlossen werden.
◆ Dank den neuen point-of-care-Assays können diese Algorithmen in Zukunft auch in der Hausarztpraxis angewendet werden.
1. Thygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ, Morrow DA, et al. Fourth Universal Definition of Myocardial Infarction (2018). Circulation [Internet]. 2018 Nov 13 [cited 2022 Feb 5];138(20):e618–51. Available from: https://www.ahajournals.org/doi/abs/10.1161/CIR.0000000000000617
2. Collet J-P, Thiele H, Barbato E, Barthélémy O, Bauersachs J, Bhatt DL, et al. 2020 ESC Guidelines for the management of acute coronary syndromes in
patients presenting without persistent ST-segment elevationThe Task Force for the management of acute coronary syndromes in patients presenting without
persistent ST-segment elevation of the European Society of Cardiology
(ESC). European Heart Journal [Internet]. 2021 Apr 7 [cited 2022 Jan 29];42(14):1289–367. Available from: https://academic.oup.com/eurheartj/
article/42/14/1289/5898842
3. Ibanez B, James S, Agewall S, Antunes MJ, Bucciarelli-Ducci C, Bueno H, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in
patients presenting with ST-segment elevationThe Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). European Heart Journal [Internet]. 2018 Jan 7 [cited 2022 Jan 29];39(2):119–77. Available from: https://academic.oup.com/eurheartj/article/39/2/119/4095042
4. Neumann FJ, Sechtem U, Banning AP, Bonaros N, Bueno H, Bugiardini R, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary
syndromesThe Task Force for the diagnosis and management of chronic coronary
syndromes of the European Society of Cardiology (ESC). European Heart Journal [Internet]. 2020 Jan 14 [cited 2022 Jan 29];41(3):407–77. Available from:
https://academic.oup.com/eurheartj/article/41/3/407/5556137
5. Reichlin T, Twerenbold R, Reiter M, Steuer S, Bassetti S, Balmelli C, et al.
Introduction of high-sensitivity troponin assays: impact on myocardial infarction incidence and prognosis. The American journal of medicine [Internet]. 2012 Dec [cited 2022 Mar 1];125(12):1205–13. Available from: https://pubmed.ncbi.nlm.nih.gov/23164485/
6. Twerenbold R, Neumann JT, Sörensen NA, Ojeda F, Karakas M, Boeddinghaus J, et al. Prospective Validation of the 0/1-h Algorithm for Early Diagnosis of Myocardial Infarction. Journal of the American College of Cardiology [Internet]. 2018 Aug 7 [cited 2022 Jan 30];72(6):620–32. Available from: https://pubmed.ncbi.nlm.nih.gov/30071991/
7. Neumann JT, Twerenbold R, Ojeda F, Sörensen NA, Chapman AR, Shah ASV, et al. Application of High-Sensitivity Troponin in Suspected Myocardial Infarction.
The New England journal of medicine [Internet]. 2019 Jun 27 [cited 2022 Jan 30];380(26):2529–40. Available from: https://pubmed.ncbi.nlm.nih.gov/31242362/
8. Reichlin T, Cullen L, Parsonage WA, Greenslade J, Twerenbold R, Moehring B, et al. Two-hour algorithm for triage toward rule-out and rule-in of acute myocardial
infarction using high-sensitivity cardiac troponin T. The American journal of medicine [Internet]. 2015 Apr 1 [cited 2022 Jan 30];128(4):369-379.e4. Available from: https://pubmed.ncbi.nlm.nih.gov/25446294/
9. Boeddinghaus J, Reichlin T, Cullen L, Greenslade JH, Parsonage WA, Hammett C, et al. Two-Hour Algorithm for Triage toward Rule-Out and Rule-In of Acute Myocardial Infarction by Use of High-Sensitivity Cardiac Troponin I. Clinical chemistry [Internet]. 2016 Mar 1 [cited 2022 Jan 30];62(3):494–504. Available from: https://pubmed.ncbi.nlm.nih.gov/26797687/
10. Boeddinghaus J, Nestelberger T, Twerenbold R, Wildi K, Badertscher P, Cupa J, et al. Direct Comparison of 4 Very Early Rule-Out Strategies for Acute Myocardial Infarction Using High-Sensitivity Cardiac Troponin I. Circulation [Internet]. 2017 Apr 25 [cited 2022 Jan 30];135(17):1597–611. Available from: https://pubmed.ncbi.nlm.nih.gov/28283497/
11. Twerenbold R, Costabel JP, Nestelberger T, Campos R, Wussler D, Arbucci R, et al. Outcome of Applying the ESC 0/1-hour Algorithm in Patients With Suspected Myocardial Infarction. Journal of the American College of Cardiology. 2019
Jul 30;74(4):483–94.
12. Stoyanov KM, Hund H, Biener M, Gandowitz J, Riedle C, Löhr J, et al. RAPID-CPU: a prospective study on implementation of the ESC 0/1-hour algorithm and safety of discharge after rule-out of myocardial infarction. European Heart Journal Acute Cardiovascular Care [Internet]. 2020 Feb 1 [cited 2022 Feb 9];9(1):39–51. Available from: https://academic.oup.com/ehjacc/article/9/1/39/5933825
13. Boeddinghaus J, Nestelberger T, Koechlin L, Wussler D, Lopez-Ayala P, Walter JE, et al. Early Diagnosis of Myocardial Infarction With Point-of-Care High-Sensitivity Cardiac Troponin I. Journal of the American College of Cardiology. 2020
Mar 17;75(10):1111–24.
der informierte @rzt
- Vol. 12
- Ausgabe 10
- Oktober 2022