- Tuberkulose Update
Die Tuberkulose (TB) bleibt die führende Todesursache unter den durch ein Pathogen verursachten Infektionen. Weltweit starben im Jahr 2021 1.6 Millionen Menschen an einer TB. In der Schweiz ist die Inzidenz weiterhin rückläufig, doch auch hier bleibt die TB eine wichtige Erkrankung. Die pulmonale Tuberkulose ist die häufigste klinische Manifestation, jedoch liegt oft gleichzeitig ein extrapulmonaler Befall, bzw. seltener eine isoliert extrapulmonale Manifestation (EPTB) vor. Am häufigsten sind hierbei die Lymphknoten und die Pleura betroffen, es kann aber grundsätzlich jedes Organ befallen sein. Zur Diagnosestellung werden heute in erster Linie Nukleinsäureamplifikationstests (NAAT) aus Sputum oder Gewebe empfohlen. Die Kultur bleibt wichtig angesichts der zunehmend beobachteten Resistenzen. Die seit über vier Jahrzehnten etablierte Rifampicin-basierte antibiotische Therapie über sechs Monate erzielt hohe Heilungsraten. Bei inkorrekter Verschreibung, schlechter Medikamentenadhärenz oder in gewissen Settings auch schlechter Medikamenten-Qualität kann es jedoch zu Therapieversagen und Resistenzbildung kommen. In diesen Fällen ist eine prolongierte Therapie mit teilweise schlechter verträglichen Reservemedikamenten notwendig. Eine sehr positive Entwicklung ist, dass sich in den vergangenen Jahren sowohl für die pansensible wie auch für die resistente Tuberkulose kürzere Therapieschemata mit neuen Substanzen als gleichwertig gezeigt haben.
Tuberculosis (TB) remains the leading cause of death among infections caused by a pathogen. Worldwide, 1.6 million people died from TB in 2021. In Switzerland, the incidence continues to decline, but tuberculosis remains an important disease here as well. Pulmonary tuberculosis is the most frequent clinical manifestation, however there is often a simultaneous extrapulmonary involvement, or less frequently an isolated extrapulmonary manifestation (EPTB). The lymph nodes and the pleura are most frequently affected, but in principle any organ can be affected.
Today, nucleic acid amplification tests (NAAT) from sputum or tissue are primarily recommended for diagnosis. Culture remains important in view of the increasingly observed resistance. Rifampicin-based antibiotic therapy over six months, which has been established for more than four decades, achieves high cure rates. However, in the case of incorrect prescription, poor drug adherence or, in certain settings, poor drug quality, treatment failure and the development of resistance can occur. In these cases, prolonged therapy with sometimes poorly tolerated reserve drugs is necessary. A very positive development is that in recent years’ shorter therapy regimens with new substances have been shown to be equivalent for both pan-sensitive and resistant tuberculosis.
Key Words: pulmonale Tuberkulose, extrapulmonale Tuberkulose
Epidemiologie
Die Tuberkulose bleibt eine der wichtigsten Mortalitätsursachen weltweit. 2021 starben 1.6 Millionen Personen an TB, ca. 10.6 Millionen erkrankten daran. Es wird geschätzt, dass ein Viertel der Weltbevölkerung mit TB-Bakterien infiziert ist, wovon letztendlich 5-10% Symptome entwickeln und manifest an einer TB erkranken (1). In der Schweiz ist das Auftreten von TB rückläufig mit zuletzt 360 Fällen im Jahr 2022. Davon sind 41.3% pulmonal, 50.5% pulmonal und extrapulmonal, 3.6% extrapulmonal und 4.6% mit unbekannter Lokalisation (2).
Die Lunge ist das am häufigsten betroffene Organ (pulmonale TB; PTB), wobei gleichzeitig ein pulmonaler und extrapulmonaler Befall vorliegen kann, oder auch seltener eine extrapulmonale TB (EPTB) ohne Lungenmanifestationen. Zu den Risikofaktoren, an einer TB zu erkranken, gehören unter anderem HIV, Malnutrition, Diabetes, Rauchen, Alkoholabusus, Alter (Kleinkinder und ältere Menschen), Kortikosteroide oder andere Immunsuppressiva (z.B. TNF-alpha-Blocker), Armut und Obdachlosigkeit (3). Weibliches Geschlecht, terminale Niereninsuffizienz, Nichtrauchen und kein Diabetes waren in einer Studie unabhängige Risikofaktoren zur Entwicklung einer EPTB im Vergleich mit einer PTB (4).
Eine grosse Herausforderung sind primäre oder erworbene Resistenzen auf einzelne oder mehrere Substanzen des Therapieregimes. Eine genaue Schätzung der Prävalenz gestaltet sich schwierig, da insbesondere in den mehrheitlich davon betroffenen, ärmeren Ländern eine Sputum-Kultur und Sensibilitätstestung nicht routinemässig durchgeführt werden kann. In der Schweiz wurden 2021 19 Personen mit einer Resistenz auf mindestens ein Medikament dokumentiert, was einem Anstieg von 5% zum Vorjahr entspricht (5).
Klinik
Nach primärem Befall der Lunge, welcher auch asymptomatisch verlaufen kann, können die Tuberkulosebakterien lymphogen oder hämatogen nahezu jedes Organ oder Kompartiment befallen. Bei der Miliartuberkulose kommt es zur disseminierten Streuung, welche insgesamt eher selten auftritt und gehäuft ist bei HIV-positiven und schwer immunsupprimierten Patienten (6). Die meisten Patienten präsentieren sich nebst der fokalen Klinik mit einem oder mehreren Zeichen der «B-Symptomatik» (Fieber, Nachtschweiss, Gewichtsverlust, Abgeschlagenheit > 2 Wochen).
Die häufigste extrapulmonale Manifestation ist die Lymphknoten-TB, die sich durch schmerzlose Schwellung insbesondere der zervikalen und supraklavikulären Lymphknoten bemerkbar macht (7). Initial sind die Lymphknoten meist einzeln palpabel, im Verlauf kommt es zum Konglomerat, u.U. auch mit Fistelgängen, aus denen sich eitriges Sekret entleert.
Ein pleuraler Befall wird in ca. 20-40% der extrapulmonalen Fälle beobachtet (8, 9). Die Klinik kann von asymptomatisch bei sehr geringem Erguss bis zu pleuritischen Atembeschwerden, Dyspnoe und Fieber bei ausgeprägtem Befall reichen. Eine Komplikation ist das tuberkulöse Empyem. Hierbei kann es zur bronchopleuralen Fistelung kommen.
Die urogenitale TB gehört ebenfalls zu den häufigeren extrapulmonalen Manifestationen (3-6%) (8, 9). Die Beschwerden ähneln denen einer bakteriellen Zystitis oder Pyelonephritis, es sind aber auch asymptomatische Verläufe möglich. Eine genitale Mitbeteiligung ist bei Frauen häufiger als bei Männern. Es sind vor allem die Salpingen sowie das Endometrium betroffen – bei Männern kann es zu Nebenhodenbefall kommen.
Eine gefürchtete Komplikation ist die ZNS-Beteiligung (ca. 5%) (8, 9), welche sich als tuberkulöse – oftmals basale – Meningitis manifestieren kann. Die Klinik kann analog einer Meningitis anderer Ätiologie von Kopfschmerzen bis hin zur Lethargie reichen, der Verlauf ist allerdings eher subakut. Als initiale Manifestation können auch lediglich Persönlichkeitsveränderungen oder psychiatrische Symptome auftreten. Aufgrund des typischerweise ausgeprägten Befalls der Hirnstammregion kann es zu Hirnnervenausfällen kommen. Intrazerebrale Raumforderungen (Tuberkulome) treten seltener auf und können mit Krampfanfällen einhergehen.
Weitere typische Lokalisationen sind der Gastrointestinaltrakt, osteo-artikuläre Strukturen und das Perikard, seltener treten auch kutane Manifestationen auf (7, 10).
In einer Analyse der Tuberkulosefälle in der Schweiz sowie Liechtenstein im Zeitraum von 2009 bis 2019 waren die extrathorakalen (16.7%) bzw. intrathorakalen Lymphknoten (14.2%) sowie die Pleura (9.1%) die am häufigsten befallenen extrapulmonalen Strukturen (11).
Diagnostik
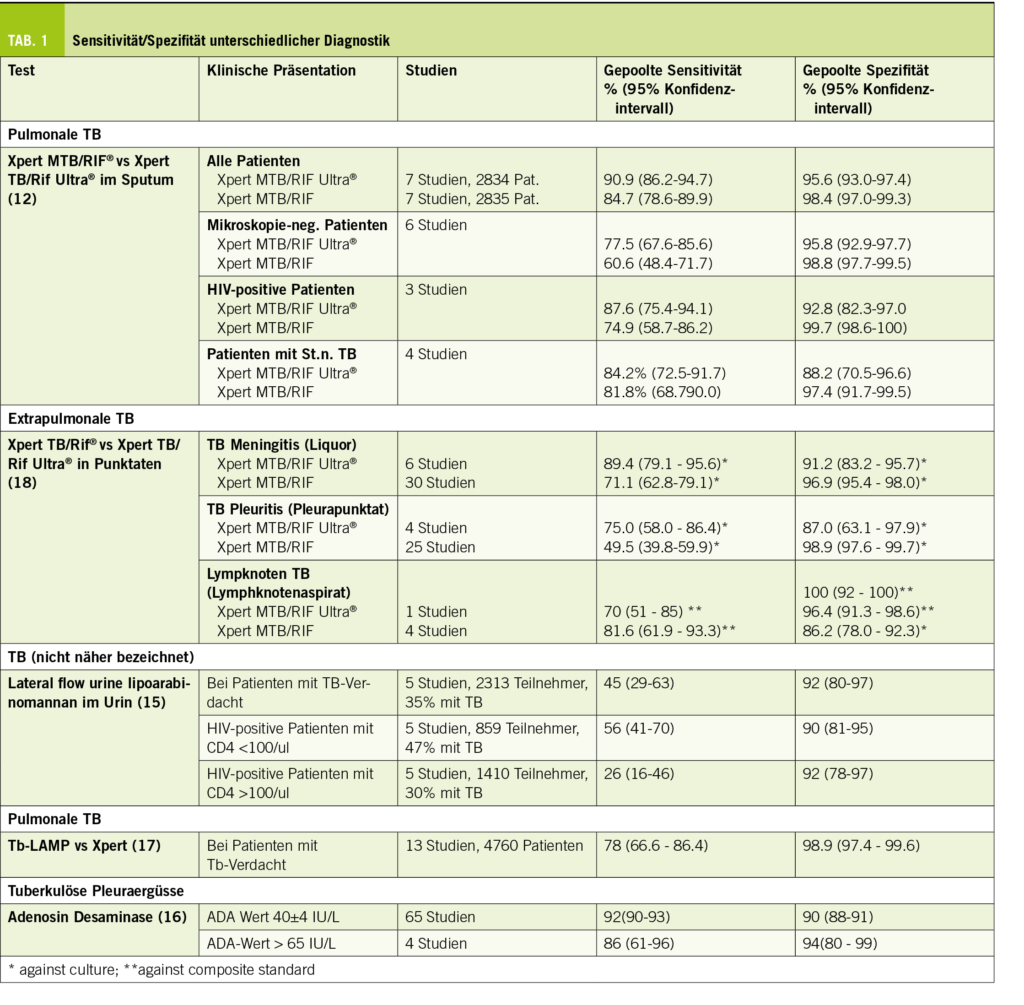
Eine rasche und akkurate Diagnostik ist essentiell um die Therapie möglichst früh und resistenzgerecht zu beginnen. Bei klinischem Verdacht sind heutzutage initial Nukleinsäuren-Amplifikationstests (NAAT) wie beispielsweise der Xpert MTB/RIF-Assay Standard. Damit können innerhalb weniger Stunden Mykobakterien wie auch eine allfällige Rifampicinresistenz nachgewiesen werden bei Keimmengen von bis 102-103. Diese Tests werden laufend verbessert – für den neueren Xpert MTB/RIF Ultra konnte eine deutlich verbesserte Sensitivität, insbesondere bei der Mikroskopie-negativen TB sowie HIV-positiven Patienten, gezeigt werden, zu Ungunsten einer leicht verminderten Spezifität (12). Die NAAT sind sowohl zur Diagnose der pulmonalen, wie auch EPTB indiziert und können in Lymphknotenbiopsien, pleuralen, perikardialen, peritonealen oder synovialen Aspiraten sowie im Urin angewendet werden (13). Eine Unterscheidung zwischen lebenden oder toten Bakterien ist mit NAAT nicht möglich, weshalb sie sich nicht für die Beurteilung des Therapieansprechens eignen.
Der traditionelle mikroskopische Nachweis von säurefesten Stäbchen mit Ziel-Neelsen-Färbung oder Auramin-Rhodamin-Färbung mit anschliessender Fluoreszenzmikroskopie aus dem Sputum braucht eine Keimmenge von 104-106/ml zum Nachweisen. Sie bleibt in vielen Ländern als Triage im Einsatz und behält auch einen wichtigen Stellenwert in der Diagnose von nicht-tuberkulösen Mykobakterien (7). Die mikroskopische Beurteilung behält zudem insbesondere zur Verlaufsbeurteilung für das Therapieansprechen einen hohen Stellenwert (14).
Für die Durchführung von phänotypischen Resistenztests sind mykobakterielle Kulturen notwendig. Diese können sowohl in flüssigen (u. a. Mycobacterial Growth Indicator Tube) oder festen Medien (z.B. Löwenstein-Jensen-Agar oder Middlebrook-7H10-Agar) angelegt werden.
Eine Voraussetzung, um das WHO-Ziel «End TB» – die Reduktion neuer TB Fälle um 80% bis 2030 – zu erreichen, ist eine frühe Diagnose der TB-Erkrankten in hochendemischen und oftmals ressourcenärmeren Regionen. Hier sind nicht-sputum basierte Tests von grossem Wert, die keiner invasiven Diagnostik bedürfen und damit einfach anwendbar sind. Dabei ist beispielsweise der Nachweis von Lipoarabinomannan (LAM)-Antigen im Urin mittels Lateral Flow Assay als Point-of-care Test eine wertvolle diagnostische Ergänzung. Lipoarabinomannan ist eine Glykolipid-Komponente in der mykobakteriellen Zellwand und wird bei aktiver Infektion sezerniert. Der Test besitzt eine tiefere Detektionsrate als NAAT, kann aber insbesondere bei HIV-positiven Patienten mit tiefer CD4+-Zellzahl, zusammen mit Sputum-Mikroskopie die Test-Sensitivität deutlich erhöhen (15).
Der TB-LAMP (Loop mediated isothermal amplification) Test ist eine weitere diagnostische Option, welcher weniger als eine Stunde zur Durchführung braucht und in peripheren Laboratorien mit eingeschränkten Möglichkeiten die Sputum-Mikroskopie bei Personen mit einer TB-typischen Klinik ergänzen oder ersetzen könnte (13).
In Pleura- und Perikarderguss oder im Aszites kann bei V. a. TB die Bestimmung der Adenosin Desaminase (ADA) hilfreich sein. ADA ist ein Enzym, welches von Lymphozyten produziert wird und im Purinmetabolismus eine wichtige Rolle spielt. Der gemessene Wert kann je nach Höhe, zusammen mit der Vortestwahrscheinlichkeit, suggestiv für eine Pleuritis tuberculosa sein bzw. zu deren Ausschluss beitragen (16).
Eine Übersicht der Sensitivität/Spezifität der verschiedenen Untersuchungen findet sich in Tabelle 1 (12, 15–18).
Therapie
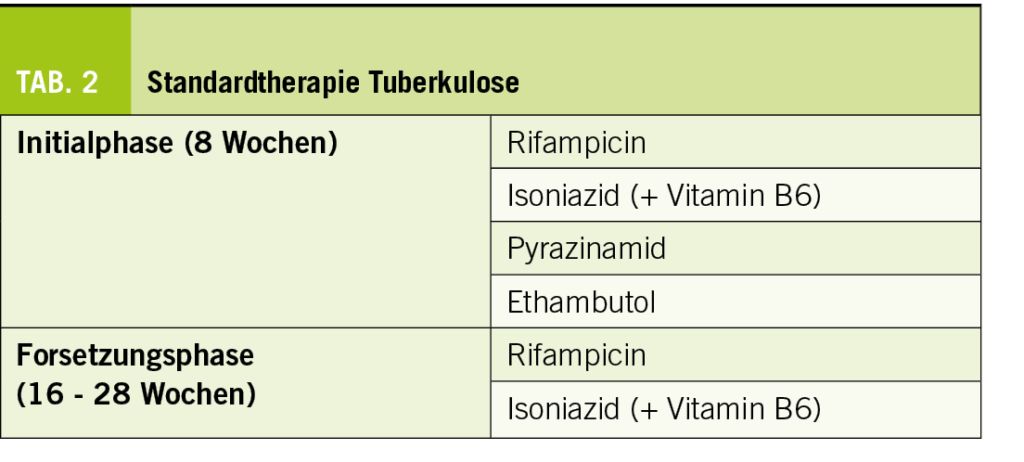
Die Therapie der pulmonalen sowie der meisten EPTB besteht seit vielen Jahren aus einer 4er-Kombination (Rifampicin, Isoniazid, Pyrazinamid, Ethambutol), bzw. 3er-Kombination bei nachgewiesenem, pansensiblem Erreger für die Initialphase in den ersten zwei Monaten, und im Anschluss eine 4-monatige 2er-Kombination (Rifampicin, Isoniazid) bei nachgewiesener Medikamentenempfindlichkeit (Tab. 2). Bei der kavernösen pulmonalen TB wird die Therapiedauer auf 9 Monate verlängert, sollte die Sputum Kultur nach 8-Wochen Therapie weiterhin Wachstum von M. tuberculosis zeigen.
Die Dauer von 6 Monaten ist möglicherweise für viele der Betroffenen mit unkompliziertem Verlauf nicht notwendig, so dass auch kürzere Schemata untersucht wurden. In einer kürzlich publizierten Studie konnte für Patienten mit einer Rifampicin-sensiblen TB und gutem klinischen Ansprechen eine Nicht-Unterlegenheit eines alternativen Schemas mit Linezolid, Bedaquilin, Isoniazid, Pyrazinamid und Ethambutol für 8 Wochen gezeigt werden (19). Dies ist allerdings so noch nicht in den Richtlinien aufgenommen.
Die Therapie der EPTB ist analog derjenigen für eine pulmonale TB. Ausnahmen bildet die miliare und die ZNS-Tuberkulose, die für mindestens 12 Monate behandelt werden. Bei der ZNS-TB wird initial zusätzlich Dexamethason verabreicht. Die Therapiedauer einer TB mit ausgeprägtem ossären bzw. artikulären Befall wird ebenfalls auf 9-12 Monate verlängert.
Therapie der resistenten Tuberkulose
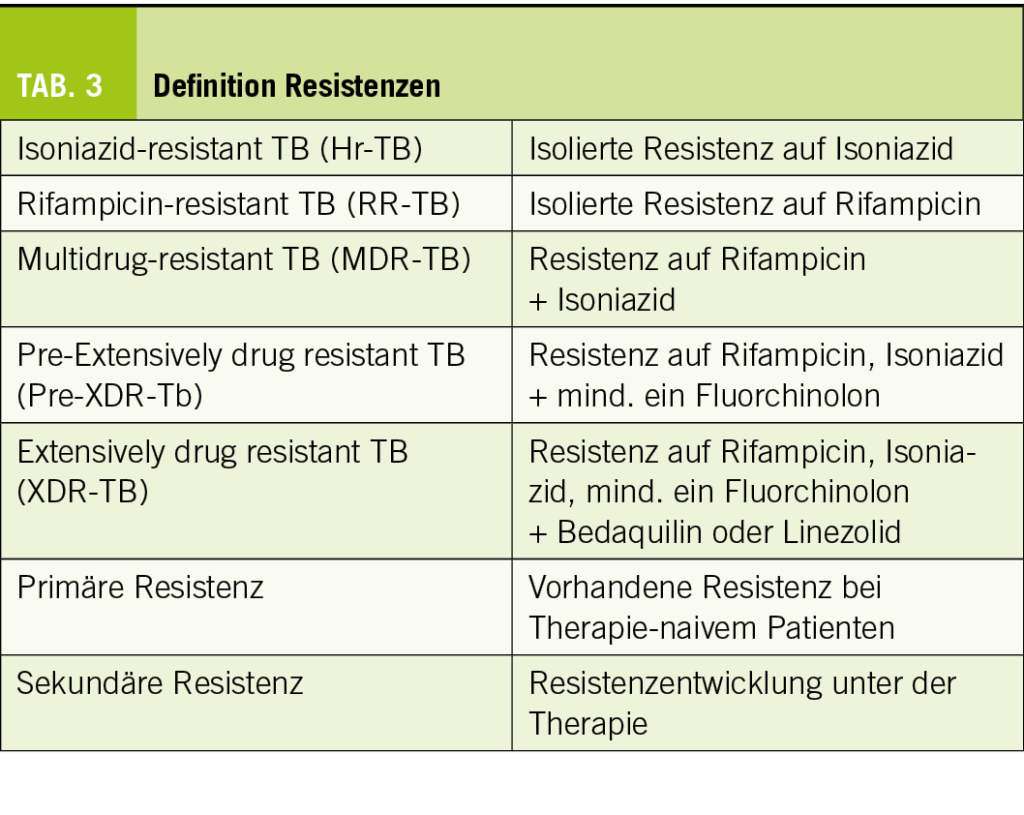
Der Global Tuberculosis Report 2021 der WHO schätzte, dass ca. 3% der Neuinfektionen sowie 18% der TB-Rezidiv-Infektionen durch Rifampicin-Monoresistente TB (RR-TB) oder eine multiresistente TB (MDR-TB) verursacht wurden (20). Bei nachgewiesener Medikamentenresistenz hängt die Kombination und Dauer der Therapie von der zugrundeliegenden Resistenz ab. Bis vor kurzem waren lange, komplexe und nebenwirkungsreiche Therapie-Schemata bis 2 Jahre Standard, wobei auch hier erfreulicherweise dank Entwicklung neuer antimykobakterieller Substanzen die Tendenz Richtung kürzere Schemata geht. Die Definitionen der verschiedenen Resistenzen sind in Tabelle 3 aufgelistet.
Nachdem Studien den Nutzen neuer Tuberkulostatika demonstrieren konnten, hat die WHO 2022 bei MDR- oder RR-Resistenz eine 6-monatige Therapie mit Bedaquilin, Pretomanid, Linezolid und Moxifloxacin (BPaLM) in die Richtlinien aufgenommen. Dies kann bei allen TB-Formen ausser bei einer ZNS-, Knochen- oder Gelenksbeteilung oder Miliartuberkulose eingesetzt werden (21–23). Auch neu ist ein weiteres, rein orales Regime mit gleicher Indikationsstellung bestehend aus Bedaquilin, Levo- oder Moxifloxacin, Clofazimin, Ethionamid, Ethambutol, Isoniazid und Pyrazinamid. Wenn es darunter nach 4 Monaten zur Sputumkonversion kommt, wird auf eine 5er- bzw. 4er-Kombination für weitere 5 Monate gewechselt (insgesamt 9 Monate). Wenn das Sputum positiv bleibt, wird die 7-fache Therapie für weitere zwei Monate fortgeführt und im Anschluss auf eine 4er-Kombination reduziert (insgesamt 11 Monate).
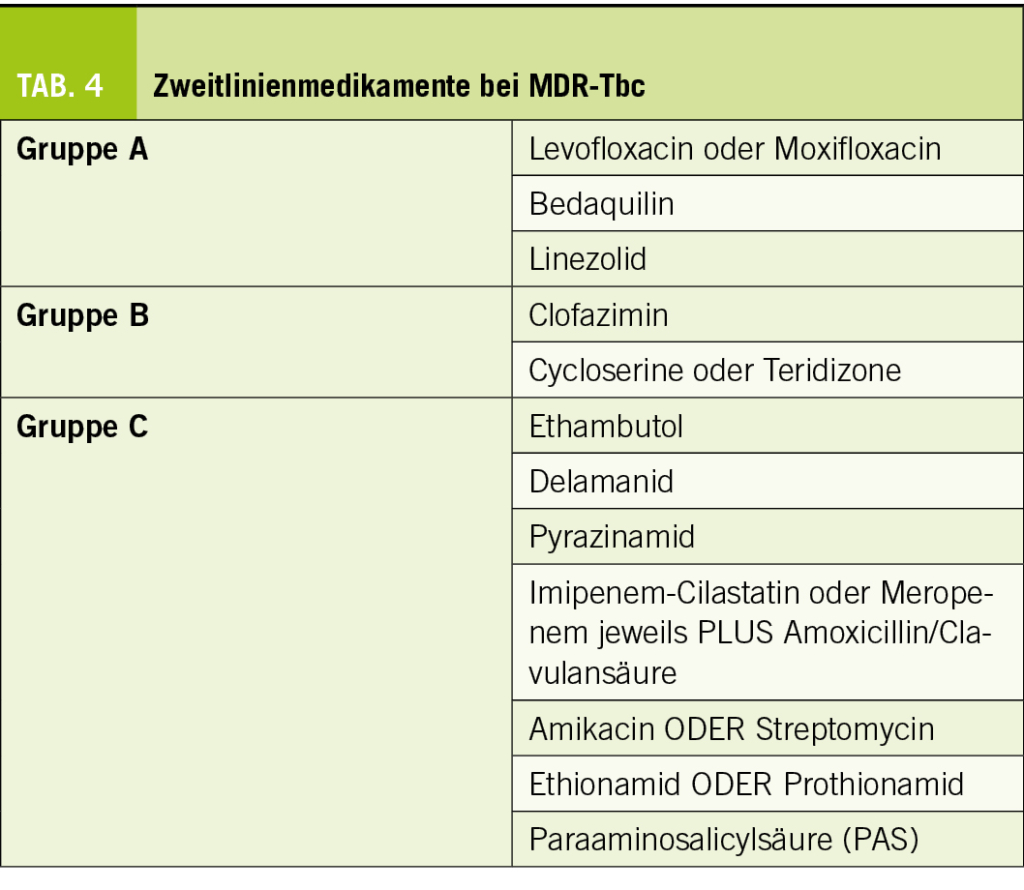
Bei Personen mit extensivem pulmonalen (bipulmonalen Kavernen, Parenchymdestruktion) bzw. extrapulmonalen Befall (ZNS, osteoartikulär, Miliartuberkulose) und/oder XDR-TB bleibt eine individualisierte, bis 18-monatige Therapie mit mindestens vier aktiven Medikamenten, welche mit Zweitlinienmedikamenten ergänzt werden, empfohlen. Diese werden in Gruppen A, B oder C eingeteilt, wobei die Erstlinientherapie primär mit Substanzen aus der Gruppe A («highly recommended») oder B («conditionally recommended») ergänzt werden sollten (Tab. 4). Bei isolierter Isoniazid-Resistenz ist eine 6-monatige Kombination aus Rifampicin, Ethambutol, Pyrazinamid und Levofloxacin empfohlen (24).
Die Tuberkulose bleibt somit eine relevante Erkrankung, welche sich klinisch sehr breit manifestieren kann und in den differentialdiagnostischen Überlegungen, sowohl im Spital wie in der Praxis, insbesondere bei vorhandenen Risikofaktoren, miteinbezogen werden sollte. Die Therapie bleibt langwierig, im Falle von Resistenzen komplex und bedarf oft interdisziplinärer Teams, bestehend aus Infektiologie, Pneumologie und Innerer Medizin, im stationären sowie ambulanten Setting, aber nicht selten auch Einbezug von Sozialdiensten und Apotheken und bei MigrantInnen entsprechenden Institutionen und Behörden, um eine gute Versorgung und lückenlose Behandlung zu gewährleisten.
Copyright bei Aerzteverlag medinfo AG
Klinik für Infektiologie & Spitalhygiene
Universitätsspital Basel
Petersgraben 4
4031 Basel
Klinik für Infektiologie & Spitalhygiene
Universitätsspital Basel
Petersgraben 4
4031 Basel
Die AutorInnen haben keine Interessenkonflikte im
Zusammenhang mit diesem Artikel deklariert.
◆ Die Tuberkulose bleibt eine wichtige Differentialdiagnose bei prolongierten pulmonalen Beschwerden und B-Symptomatik bei entsprechender epidemiologischer Exposition.
◆ Extrapulmonale Manifestationen manifestieren sich am häufigsten pleural und als Lymphadenopathie, sind aber an fast allen Lokalisationen möglich und sollten bei entsprechendem Verdacht in die
Diagnostik einbezogen werden.
◆ Eine rasche und akkurate Diagnostik inklusive Resistenzprüfung sind elementar für eine frühe und resistenzgerechte Therapieeinleitung.
◆ Die Therapie besteht weiterhin aus einer antibiotischen Kombinationstherapie in der Regel über sechs Monate. In den vergangenen Jahren konnte die 18-monatige Therapiedauer bei resistenten Erregern dank wirksameren neuen Substanzen und besser verträglichen Schemata für die meisten Patienten verkürzt werden.
◆ Um den Therapieerfolg zu gewährleisten ist eine interdisziplinäre Betreuung sowohl im stationären Rahmen wie auch in der ambulanten Weiterbehandlung in der Hausarztpraxis essentiell.
1. World Health Organization. Tuberculosis. WHO Web page. Published April 21, 2023. Accessed May 27, 2023. https://www.who.int/news-room/fact-sheets/detail/tuberculosis
2. Bundesamt für Gesundheit. BAG-Bulletin 43/2022 (Deutsch). www.bag.admin.ch
3. Robert Koch Institut. Startseite Infektionsschutz RKI-Ratgeber Tuberkulose. https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Tuberkulose.html
4. Lin JN, Lai † C H, Chen YH, et al. Risk Factors for Extra-Pulmonary Tuberculosis Compared to Pulmonary Tuberculosis. Vol 13.; 2009.
5. StopTBPartnership. Tuberculosis Dashboard. Accessed July 22, 2023. https://dashboards.stoptb.org/country-profile.html
6. Surendra Kumar Sharma AMASDKM. Miliary tuberculosis: new insights into an old disease. Lancet Infet Dis. 2005;5:415-430. doi:doi: 10.1016/S1473-3099(05)70163-8.
7. Jameson JL 1952, Fauci AS 1940, Kasper DL. Harrisons Innere Medizin Register.
8. Peto HM, Pratt RH, Harrington TA, LoBue PA, Armstrong LR. Epidemiology of extrapulmonary tuberculosis in the United States, 1993-2006. Clinical Infectious Diseases. 2009;49(9):1350-1357. doi:10.1086/605559
9. Gomes T, Reis-Santos B, Bertolde A, Johnson JL, Riley LW, Maciel EL. Epidemiology of Extrapulmonary Tuberculosis in Brazil: A Hierarchical Model.; 2014. http://www.biomedcentral.com/1471-2334/14/9
10. Nardell EA. Extrapulmonary Tuberculosis (TB). https://www.msdmanuals.com/professional/infectious-diseases/mycobacteria/extrapulmonary-tuberculosis-tb
11. Altpeter Ekkehardt S, Schmidt Axel J. Surveillance of tuberculosis in switzerland and the principality of liechtenstein, 2009 to 2019. Swiss Med Wkly. 2021;151(35). doi:10.4414/SMW.2021.w30032
12. Zifodya JS, Kreniske JS, Schiller I, et al. Xpert Ultra versus Xpert MTB/RIF for pulmonary tuberculosis and rifampicin resistance in adults with presumptive pulmonary tuberculosis. Cochrane Database of Systematic Reviews. 2021;2021(2). doi:10.1002/14651858.CD009593.pub5
13. World Health Organization. Module 3: Diagnosis WHO Consolidated Guidelines on Tuberculosis Rapid Diagnostics for Tuberculosis Detection. Accessed May 30, 2023. https://www.who.int/publications/i/item/9789240029415
14. Schoch OD, Barben J, Berger C, et al. Tuberkulose in Der Schweiz – Leitfaden Für Fachpersonen Des Gesundheitswesen. www.lungenliga.ch
15. Shah M, Hanrahan C, Wang ZY, et al. Lateral flow urine lipoarabinomannan assay for detecting active tuberculosis in HIV-positive adults. Cochrane Database of Systematic Reviews. 2016;2016(5). doi:10.1002/14651858.CD011420.pub2
16. Aggarwal AN, Agarwal R, Sehgal IS, Dhooria S. Adenosine deaminase for diagnosis of tuberculous pleural effusion: A systematic review and meta-analysis. PLoS One. 2019;14(3). doi:10.1371/journal.pone.0213728
17. Shete PB, Farr K, Strnad L, Gray CM, Cattamanchi A. Diagnostic accuracy of TB-LAMP for pulmonary tuberculosis: a systematic review and meta-analysis. BMC Infect Dis. 2019;19(1). doi:10.1186/s12879-019-3881-y
18. Kohli M, Schiller I, Dendukuri N, et al. Xpert MTB/RIF Ultra and Xpert MTB/RIF assays for extrapulmonary tuberculosis and rifampicin resistance in adults. Cochrane Database of Systematic Reviews. 2021;2021(1). doi:10.1002/14651858.CD012768.pub3
19. Paton NI, Cousins C, Suresh C, et al. Treatment Strategy for Rifampin-Susceptible Tuberculosis. New England Journal of Medicine. 2023;388(10):873-887. doi:10.1056/nejmoa2212537
20. World Health Organization. GLOBAL TUBERCULOSIS REPORT 2021.; 2021. Accessed June 2, 2023. https://www.who.int/publications/i/item/9789240037021
21. World Health Organization. WHO Consolidated Guidelines on Tuberculosis Module 4: Treatment Drug-Susceptible Tuberculosis Treatment. Accessed June 2, 2023. https://www.who.int/publications/i/item/9789240048126
22. World Health Organization. WHO Operational Handbook on Tuberculosis Module 4: Treatment Drug-Susceptible Tuberculosis Treatment. Accessed June 2, 2023. https://www.who.int/publications/i/item/9789240050761
23. World Health Organization. Meeting Report of the WHO Expert Consultation on the Definition of Extensively Drug-Resistant Tuberculosis, Meeting Report of the WHO Expert Consultation on the Definition of Extensively Drug-Resistant Tuberculosis. Accessed June 2, 2023. https://www.who.int/publications/i/item/9789240018662
24. World Health Organization. WHO Consolidated Guidelines on Drug-Resistant Tuberculosis Treatment. Accessed June 2, 2023. https://apps.who.int/iris/handle/10665/311389
der informierte @rzt
- Vol. 13
- Ausgabe 8
- August 2023