- Deutliche Zunahme durch neue Therapie- Indikationen für PARP-Inhibitoren
Genetische Beratungen und molekular-genetische Testungen werden bei hereditären Krebserkrankungen und entsprechender Prädisposition standardmässig durchgeführt. Dadurch können familiäre Risiken erkannt sowie Früherkennungs-Modalitäten individuell festgelegt werden. Neuerdings stehen auch Therapieoptionen zur Verfügung, deren Indikation ebenfalls von einer genetischen Beratung und (Keimbahn-)Testung abhängen. Dies sind die Poly[ADP-Ribose]-Polymerase-)Inhibitoren (PARPi), welche zuerst beim Ovarialkarzinom als Erhaltungstherapie erfolgreich eingesetzt wurden, dann beim Mammakarzinom in der adjuvanten als auch palliativen Situation ihre Wirksamkeit zeigten. PARP-Inhibitoren haben nun auch beim Prostata- und Pankreaskarzinom ihren festen Platz erhalten. Dies sind Therapie-Fortschritte für unsere PatientInnen und bedeuten eine enorme Zunahme an Indikationen für genetische Beratungen und Testungen. Wie können wir diesen Herausforderungen begegnen?
Genetic counseling and molecular genetic testing are performed as standard for hereditary cancers and corresponding predisposition. Thus, familial risks can be identified and early detection modalities can be individually defined. Recently, therapeutic options have become available whose indication also depends on genetic counseling and (germline) testing. These are the poly[ADP-ribose] polymerase) inhibitors (PARPi), which were first successfully used in ovarian cancer as maintenance therapy, then showed efficacy in breast cancer in the adjuvant as well as palliative situation. PARP inhibitors have now also become firmly established in prostate and pancreatic cancer. These are therapeutic advances for our patients and represent a tremendous increase in indications for genetic counseling and testing. How can we meet these challenges?
Keywords: genetic testing with therapeutic intent, PARP inhibitors, pathogenic BRCA1,2 variants, HBOC
Genetische Beratung in der Schweiz
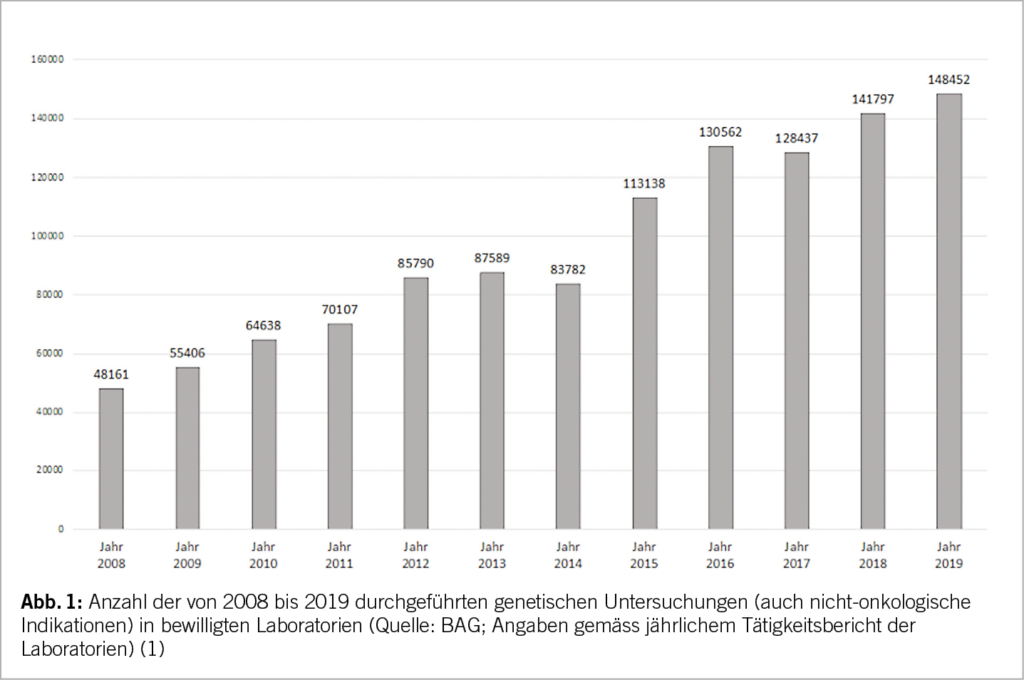
Die genetische Beratung und Testung bei Krebsleiden und -prädispositionen haben sich in den letzten Jahren etabliert in der onkologischen Praxis. Deren Umfang nimmt in allen Zentren zu (Abb. 1). Im Rahmen des «Netzwerks für die Testung auf eine genetische Krebsprädisposition und Risikoberatung» («Network for Cancer Predisposition Testing and Counseling» [CPTC]) der Schweizerischen Arbeitsgemeinschaft für klinische Krebsforschung (SAKK) wird einerseits ein nationaler fachlicher Austausch geschaffen, es werden aber auch regelmässige Fortbildungen angeboten anlässlich der Halbjahresversammlungen sowie interessierte ÄrztInnen kontinuierlich zu genetischen BeraterInnen ausgebildet für deren Tätigkeit in den jeweiligen Zentren. Aufgrund der Bedarfszunahme an genetischen Beratungen werden sogenannte Genetic Counsellors ausgebildet, dies in den USA, Kanada und Australien sowie zunehmend in Europa (z.B. UK, Frankreich, Norwegen, Schweden und Spanien). Neu gibt es auch Ausbildungslehrgänge dafür in Italien und Österreich. In der Schweiz gibt es bisher nur wenige, im Ausland ausgebildete Genetic Counsellors, dies vor allem in der Westschweiz (1). stehen. High-risk Patienten sollten, sofern verfügbar, im Rahmen von Phase 3 Studien behandelt werden.
Hereditäres Brust- und Ovarial-karzinomrisiko (HBOC)
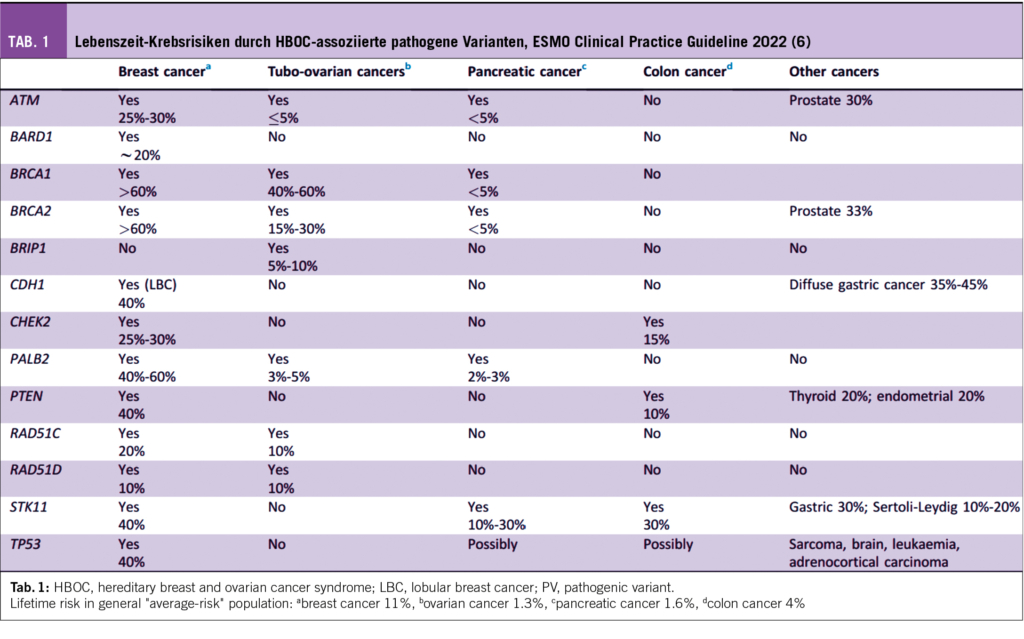
Bei Brustkrebspatientinnen finden sich in ca. 5% aller Fälle pathogene Varianten (PV’s, früher Mutationen genannt) in HBOC-Genen (Hereditäres Brust- und Ovarialkarzinomrisiko). Diese Varianten werden mittels Keimbahnanalyse diagnostiziert. Sie treten gehäuft auf bei entsprechender Familienanamnese, jüngerem Alter, mit synchronen oder metachronen kontralateralen Mammakarzinomen oder bei Ovarialkarzinomen (2).
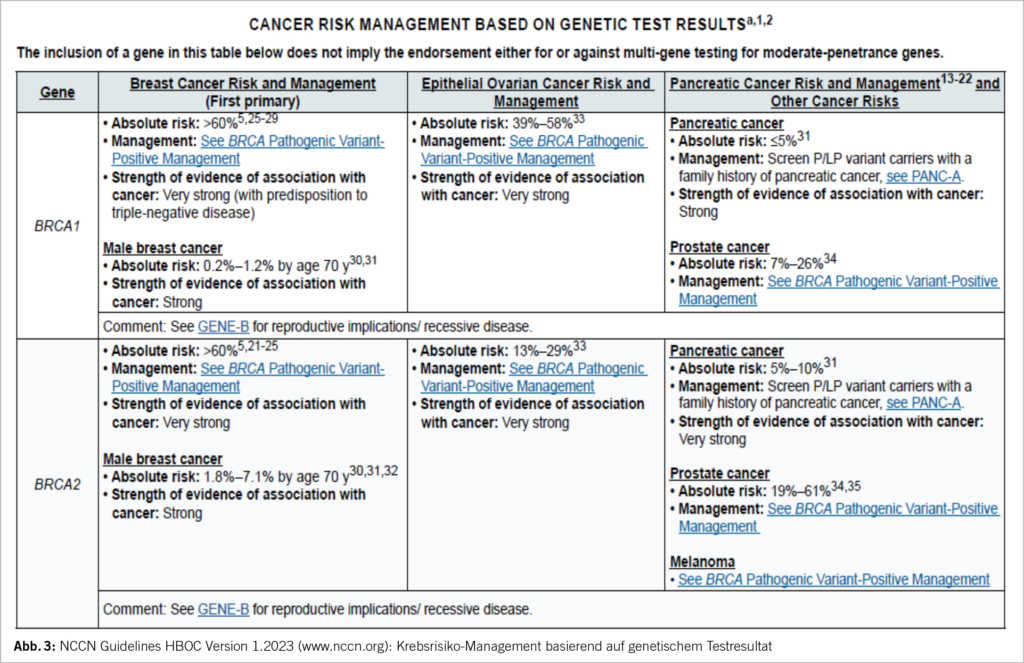
Im Jahr 2021 wurden erstmals in den NCCN guidelines auch die Pankreas- und Prostata-Karzinome zu den HBOC-assoziierten Krankheiten hinzugefügt mit entsprechenden Test-Indikationen und Screening-Empfehlungen (www.nccn.org). Eine Häufung an hereditären Krebsrisiken kann es auch in ethnischen Gruppen mit sogenannten Founder-Varianten geben. Pathogene Varianten werden einerseits als sog. Hochrisiko-Gene (high-risk genes) klassifiziert. Sie erhöhen das Risiko, an einem Mamma- oder Ovarial-Karzinom zu erkranken, um ca. das Vierfache (> 30%), dies sind BRCA1,2, PALB2, PTEN, CDH1, STK11, TP53. Andererseits gibt es sog. moderate-risk Gene wie CHEK2, ATM, BARD1, RAD51C, RAD51D mit Risikoerhöhung um das Zwei-bis Vierfache (3, 4).
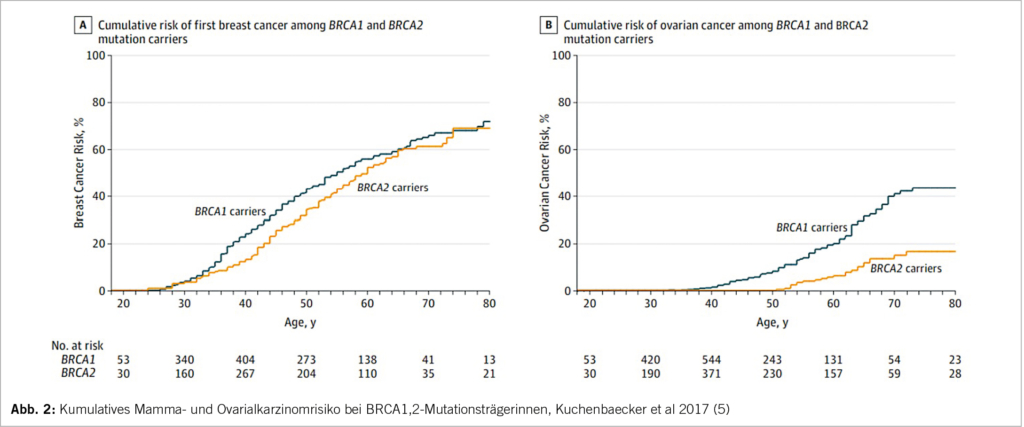
In den Sprechstunden für genetische Beratungen werden Hochrisiko-Patientinnen und deren Familien hinsichtlich erblicher Krebsrisiken informiert (Abb. 1). Hierbei sind die Beratenden oft mit unvollständiger Familienanamnese oder (zunehmend) sehr kleinen Familien konfrontiert (zB weniger als zwei weibliche erst- oder zweitgradig Verwandte > 45 Jahre). Hier besteht das Risiko der Unterschätzung der Wahrscheinlichkeit, dass eine pathogene oder mögliche pathogene Variante (P/LP) vorliegen könnte. Sind viele Familienangehörige gesund geblieben, gibt dies starke Hinweise auf ein niedriges Risiko für eine P/LP Variante. Der nun häufigere Einsatz von Multigen-Tests mittels NGS (next-generation sequencing) hat den klinischen Alltag in den letzten wenigen Jahren verändert. Die CPTC der SAKK hat dies in ihrer praxisnahen Empfehlung zur Zusammensetzung der Gen-Panels festgehalten (www.sakk.ch). Hier werden massgeschneiderte, auf die Krankheit fokussierte Genpanels für klinisch relevante Krebs-Suszeptibilitäts-Gene empfohlen, im Gegensatz zu grossen Multigen-Panels mit unklarer oder unbekannter klinischer Bedeutung. Je breiter das Genpanel gewählt wird, umso höher ist das Risiko auf VUS (variants of unknown significance). In den 9 Genen des BRCA Ovar Panels werden auch sog. intermediär-penetrante Gene (= moderate-risk Gene) bestimmt. Für immer mehr dieser Genvarianten haben wir fundierte Daten zu Krebsrisiken sowie Empfehlungen für ein Risko-Management, z.B. durch die NCCN-Guidelines (www.nccn.org), (Abb. 2).
Somatische Testung
Oftmals wird in der Onkologie eine Tumortestung auf bestimmte, therapie-hinweisende Mutationen hin veranlasst, die sog. somatische Testung. Wird eine pathogene oder möglicherweise pathogene (P/LP) Variante gefunden, welche eine klinische Relevanz aufweist für die PatientIn oder weitere gesunde Familienmitglieder, ist die Verifizierung an der Keimbahn (EDTA-Blut) der nächste Schritt. Diese und weitere Testindikationen für die Keimbahntestung wurden von der SAKK (CPTC) 2019 erstmals und 2021 in einem up-date publiziert (Update Swiss guideline for genetic counselling and testing-09.21.pdf (sakk.ch)). Die genetische Testung wird durch die im September 2022 revidierte Bundesgesetzgebung über genetische Untersuchungen beim Menschen (GUMG) geregelt und bedarf, auch im Falle der rein somatischen Testung, eines mündlichen und schriftlichen Einverständnisses der zu testenden Person (sog. «informed consent») (www.bag.admin.ch). Eine alleinige Tumortestung birgt das Risiko, dass bis zu 10% klinisch relevante Keimbahnvarianten übersehen werden (zB Deletionen, Duplikationen oder sog. splicing variants) (7). Möglicherweise werden ctDNA -Assays in Zukunft Auskunft darüber geben, ob eine bestimmte Gen-Variante eine genügend hohe VAF (variant allele frequency) aufweist, welche klar auf eine Keimbahnvariante hinweist (8). Noch gibt es allerdings keine validierten Tests hierfür.
Polygenic Risk Score (PRS)
Der Polygenic Risk Score kann Auskunft geben über das genetische Gesundheitsrisiko eines Individuums gegenüber anderen Menschen mit einer anderen genetischen Konstitution. Er kann in Risikoberechnungsmodellen eingesetzt werden wie z. B. dem CanRisk-Berechnungsmodell (www. canrisk.org). Aktuell besteht keine Empfehlung, routinemässig eine Bestimmung des PRS zu veranlassen, da die Interpretation unklar bleibt. Im Rahmen klinischer Studien jedoch wird er breit angewandt (9, 10).
Genetische Testung von DNA-Reparatur-Genen in therapeutischer Hinsicht
Genetische Beratung und Testung bei Brust- und Eierstockkrebs sowie Prostata- und Pankreaskarzinomen wurde bis vor kurzem aufgrund eines erhöhten hereditären Risikos (HBOC, hereditäres Brust- und Ovarialkarzinom-Syndrom) gestellt. Diese Leistungspflicht der Krankenkasse ist in der KLV (Krankenpflege-Leistungsverordnung) Art. 12d lit. f als „Massnahmen der Prävention“ begründet. Die entsprechenden Schweizerischen Richtlinien für genetische Beratung und Testung wurden oben erwähnt. Diese Leitlinien sollten jedoch nicht angewendet werden, wenn eine BRCA1,2-Keimbahntestung zur Evaluation einer Therapieoption bei Krebspatienten primär in therapeutischer Hinsicht erfolgt. Dies ist auch für die Kostengutsprache-erteilenden Vertrauensärzte der Krankenversicherungen ein neuer Umstand, der beachtet werden muss, im Sinne einer massgeschneiderten Therapie für die PatientInnen.
PARP (Poly[ADP-Ribose]-Polymerase)-Inhibitoren
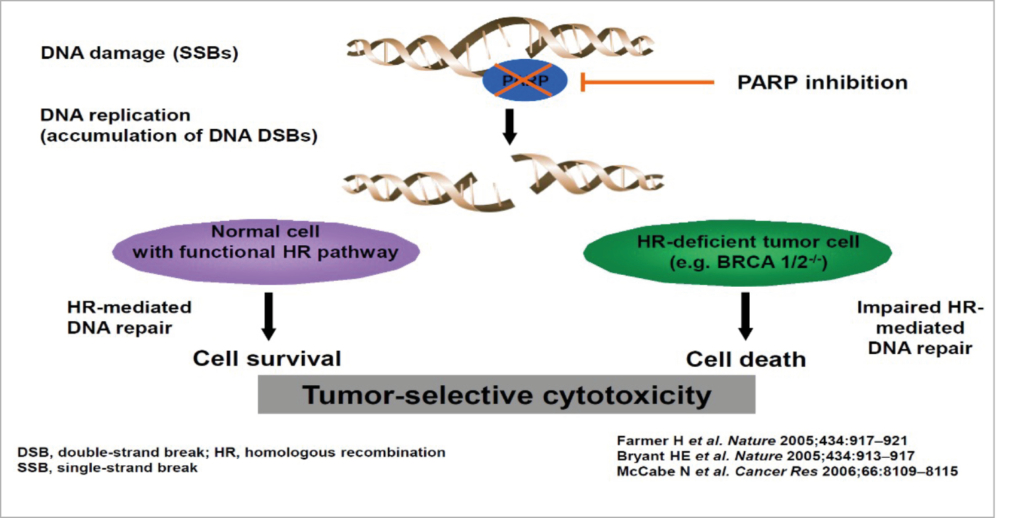
Bei verschiedenen Tumor-Entitäten haben wir im Falle einer pathogenen Variante in DNA-Reparatur-Genen wie BRCA1 und BRCA2 einen Prädiktor für das Ansprechen auf PARP-Inhibitoren (PARPi). Sie sind erstmals in der Erhaltungstherapie beim hochgradig-serösen Ovarialkarzinom erfolgreich eingesetzt worden (11).
Abbildung 5 zeigt den Wirkmechanismus bei gesunden Zellen im Vergleich zu HR-defizienten Tumorzellen.
A. Ovarialkarzinome
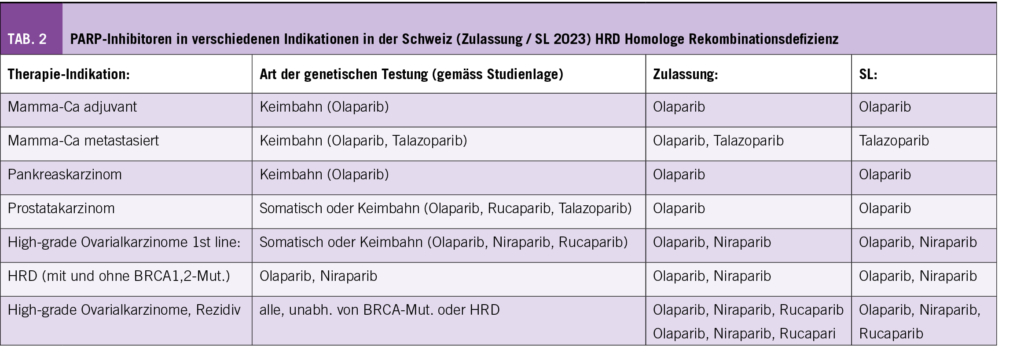
Aus Daten von drei randomisierten Phase 3-Studien (SOLO1, PRIMA, PAOLA-1) (12, 13, 14) haben wir drei verschiedene PARPi-Erhaltungstherapie-Strategien beim Ovarialkarzinom in der ersten Linie, welche alle eine FDA- und EMA-Zulassung haben. Die Regulierung für die Schweiz ist in Tabelle 2
ersichtlich.
Mittlerweile konnte ein Überlebensvorteil bei Frauen mit DNA-Reparaturgen-Defekten (BRCA1,2-Mutationen sowie weiteren HR (Homologe Rekombinations)-Defizienzen) mit dieser oralen Therapie (die meist ordentlich toleriert wird) in der Ovarialkarzinom-Erstlinienbehandlung gezeigt werden (12). In der Situation des platin-sensitiven Rückfalls ist die Indikation für die Erhaltungstherapie mit PARPi nicht an einen DNA-Reparaturdefekt gekoppelt.
B. Mammakarzinome
Weitere Indikationen für PARPi bestehen beim Mammakarzinom (in der adjuvanten (mit Olaparib) und metastasierten Situation (mit Olaparib oder Talazoparib). Beim frühen Mammakarzinom konnte dadurch ein Überlebensvorteil erreicht werden (15, 16,17).
C. Prostata-Karzinome
In der Schweiz gibt es ca. 7000 Neuerkrankungen an Prostatakarzinomen; dies ist somit die häufigste Krebsart beim Mann. Bis zu 25% aller Patienten mit einem metastasierten Prostatakarzinom weisen eine somatische oder Keimbahn-DNA-Reparaturgen-Alteration auf. Bereits als Standard werden nun die PARPi in der metastasierten, kastrations-resistenten Situation (mCRPC) angesehen. Mit Olaparib konnte das Gesamtüberleben nach mindestens einer «neuen Hormontherapie» (NHT) bei Männern in der Kohorte mit pathogenen BRCA1,2- sowie ATM-Varianten verbessert werden (PROfound-Studie) (19) und ist in dieser Indikation in der Schweiz zugelassen (Tab. 2). Auch für andere PARPi, wie z.B. Niraparib, gibt es vielversprechende Phase 2-Daten (20). Grundsätzlich profitieren Prostatakarzinom-Patienten mit einer BRCA1,2-Mutation am meisten von PARPi, dies wird im Kommentar der Autoren der European Association of Urology (21) hervorragend herausgearbeitet. Eine klare Übersicht über die neuen Aspekte der Molekulargenetik beim Prostatakarzinom und deren Umsetzung in der Praxis gibt der Artikel von PD Dr. med. Aurelius Omlin et al. im SMF 2022 (22).
D. Pankreas-Karzinome
Als einziger PARPi ist Olaparib in der Schweiz in der Erhaltungstherapie als Monotherapie bei metastasiertem Adenokarzinom des Pankreas zugelassen aufgrund einer randomisierten Phase 3-Studie (Pancreas Cancer Olaparib Ongoing (POLO) (23). Es bedarf des Nachweises einer Keimbahnmutation in den BRCA1,2-Genen. Zudem darf die Erkrankung nach mindestens 16 Wochen einer platinhaltigen Erstlinien-Chemotherapie nicht fortgeschritten sein und ein Performance Status ECOG 0 – 1 vorliegen. Die Behandlung erfolgt hier bis zur Progression.
Schlussfolgerung
Aufgrund neuer Therapieindikationen für PARP-Inhibitoren, welche teils nur mittels Keimbahnnachweis einer Mutation in DNA-Reparaturgenen eingesetzt werden können, wird die Nachfrage nach genetischen Beratungen und Testungen in unseren Sprechstunden noch deutlicher zunehmen. Im Sinne der Prävention werden daraufhin auch vermehrt gesunde Familienangehörige beraten und auf eine etwaige Trägerschaft hin abgeklärt. Dies bedeutet für unseren Klinikalltag eine enorme Herausforderung an Personal und Infastruktur.
Copyright bei Aerzteverlag medinfo AG
Stv. Leitende Ärztin Medizinische Onkologie
FMH Medizinische Onkologie
Kantonsspital Graubünden
Loestrasse 170
7000 Chur
ursula.hasler-strub@ksgr.ch
Die Autorin hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Genetische Beratung und Testung bei Brust- und Eierstockkrebs sowie Prostata- und Pankreaskarzinomen wurden bis vor kurzem aufgrund eines erhöhten hereditären Risikos (HBOC, hereditäres Brust- und Ovarialkarzinom-Syndrom) gestellt
◆ Neu werden die Beratungen zunehmen, da therapeutische Optionen für PARP-Inhibitoren bestehen. Zusätzlich zum Ovarialkarzinom gibt es neue Indikationen beim Mamma-, Prostata- und Pankreaskarzinom.
◆ Für die Zukunft müssen wir an Lösungen arbeiten, die diese oft aufwändigen genetischen Beratungsgespräche in hoher Qualität und auch zeitnah sicherstellen (zB mit Hilfe von Genetic Counsellors)
1. Amstad H. Genetic Counsellors in der Schweiz. Bericht zuhanden der Eidg. Kommission für genetische Untersuchungen beim Menschen (GUMEK), 2021 bericht-genetic-counsellors-in-der-schweiz-de-pdf.pdf
2. Greenberg S, Buys SS, Edwards SL, et al. Population prevalence of individuals meeting criteria for hereditary breast and ovarian cancer testing. Cancer Med. 2019;8(15):6789-6798
3. Breast Cancer Association ConsortiumDorling L, Carvalho S, Allen J, et al. Breast cancer risk genes – association analysis in more than 113,000 women. N Engl J Med. 2021;384(5):428-439.
4. Hu C, Hart SN, Gnanaolivu R, et al. A population-based study of genes previously implicated in breast cancer. N Engl J Med. 2021;384(5):440-451
5. Kuchenbaecker KB, Hopper JL, Barnes DR, et al. Risks of breast, ovarian, and contralateral breast cancer for BRCA1 and BRCA2 mutation carriers. JAMA. 2017;317(23):2402-2416
6. C. Sessa et al Risk reduction and screening of cancer in hereditary breast-ovarian cancer syndromes: ESMO Clinical Practice Guideline, available online 25th of october 2022, https://doi.org/10.1016/j.annonc.2022.10.004
7. Rowley SM, Mascarenhas L, Devereux L, et al. Population-based genetic testing of asymptomatic women for breast and ovarian cancer susceptibility. Genet Med. 2019;21(4):913-922
8. Wentzensen N, Clarke MA. Liquid biopsy for cancer detection: Clinical and epide miologic considerations. Clin Cancer Res. 2021;27(21):5733-5735
9. Clinical Implementation of a Polygenic Risk Score (PRS) for Breast Cancer: Impact on Risk Estimates, Management Recommendations, Clinical Outcomes, and Patient Perception (NCT03688204 )
10. GENetic Risk Estimation of Breast Cancer Prior to Decisions on Preventive Therapy Uptake, Risk Reducing Surgery or Intensive Imaging Surveillance (GENRE2) NCT04474834
11. M.Friedlander et al Long-term efficacy, tolerability and overall survival in patients with platinum-sensitive, recurrent high-grade serous ovarian cancer treated with maintenance olaparib capsules following response to chemotherapy, British Journal of Cancer (2018) 119:1075–1085; https://doi.org/10.1038/s41416-018-0271-
12. Paul DiSilvestro et al Overall Survival With Maintenance Olaparib at a 7-Year Follow-Up in Patients With Newly Diagnosed Advanced Ovarian Cancer and a BRCA Mutation: The SOLO1/GOG 3004 Trial, J Clin Oncol 41:609-617. © 2022 by American Society of Clinical Oncolog
13. Antonio Gonzalez Martin Niraparib in Patients with Newly Diagnosed Advanced Ovarian Cancer, N Engl J Med 2019; 381:2391-2402
14. I. Ray-Coquard et.al Olaparib plus Bevacizumab as First-Line Maintenance in Ovarian Cancer, N Engl J Med 2019;381:2416-28.
15. Tutt ANJ, Garber JE, Kaufman B, et al. Adjuvant olaparib for patients with BRCA1- or BRCA2-mutated breast cancer. N Engl J Med. 2021;384(25):2394-2405.
16. M.E. Robson et al OlympiAD final overall survival and tolerability results: Olaparib versus chemotherapy treatment of physician’s choice in patients with a germline BRCA mutation and HER2-negative metastatic breast cancer, Annals of Oncology 30: 558–566, 2019
17. Jennifer K Litton et al. Talazoparib in Patients with Advanced Breast Cancer and a Germline BRCA Mutation, N Engl J Med 2018 Aug 23;379(8):753-763.
18. www.krebsliga.ch
19. de Bono J, Mateo J, Fizazi K, et al. Olaparib for metastatic castrationresistant prostate cancer. N Engl J Med 2020;382:2091–102.
20. Fizazi K, Piulats JM, Reaume MN, et al. Rucaparib or physician’s choice in metastatic prostate cancer. N Engl J Med 2023;388:719–32.
21. Nick Beije et. al. PARP Inhibitors for Prostate Cancer: Tangled up in PROfound and PROpel (and TALAPRO-2) Blues, https://doi.org/10.1016/j.eururo.2023.03.038
22. A. Omlin et al, Molekulargenetik und Molekular¬pathologie beim Prostatakarzinom, Schweizerisches Medizin-Forum 2022;22(1–2):28–34
23. Golan, T, et al. Maintenance Olaparib for Germline BRCA-Mutated Metastatic Pancreatic Cancer. N. Engl. J. Med. 2019, 381, 317–327.
info@onco-suisse
- Vol. 13
- Ausgabe 5
- August 2023