- Polymedikation und orale antitumorale Therapien – welche Arzneimittelinteraktionen gilt es zu beachten?
Orale antitumorale Therapien bieten verschiedene Vorteile, bergen aber auch Risiken aufgrund ihrer Toxizität und engen therapeutischen Breiten. Da diese Arzneimittel vermehrt auch bei Patienten und Patientinnen mit bestehender Polymedikation als Dauertherapien eingesetzt werden, ist das Identifizieren und Beurteilen von potentiellen Arzneimittelinteraktionen für eine sichere und effektive Therapie von grosser Bedeutung. Dieser Artikel bietet einen Überblick zu den häufigsten pharmakokinetischen und pharmakodynamischen Arzneimittelinteraktionen zielgerichteter antitumoraler Therapien, mit Fokus auf die Wirkstoffklasse der Proteinkinaseinhibitoren.
Einführung
Orale zielgerichtete Tumortherapien wie Proteinkinaseinhibitoren haben in der Onkologie in den letzten Jahren stark an Bedeutung gewonnen. Proteinkinasen sind Enzyme, die einem Protein eine Phosphatgruppe hinzufügen und dadurch seine Funktion ändern. Proteinkinaseinhibitoren sind Arzneistoffe, welche eine oder mehrere Proteinkinasen hemmen. Die Hemmung der kinaseabhängigen Phosphorylierung kann eine Vielzahl von Zellprozessen beeinflussen. Vor allem bei malignen Zellen spielt die Aktivität von Proteinkinasen eine Schlüsselrolle, da mutierte oder überexprimierte Proteinkinasen zu enthemmtem Tumorwachstum führen. Durch den Einsatz von Proteinkinaseinhibitoren können Tumorzellen in die Apoptose getrieben werden.
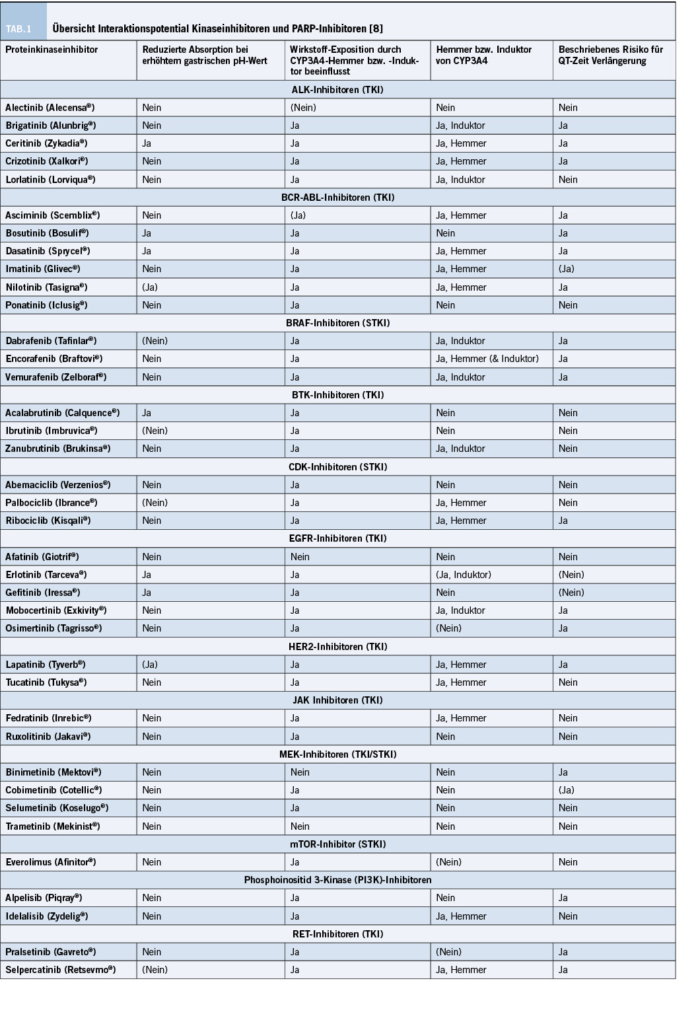
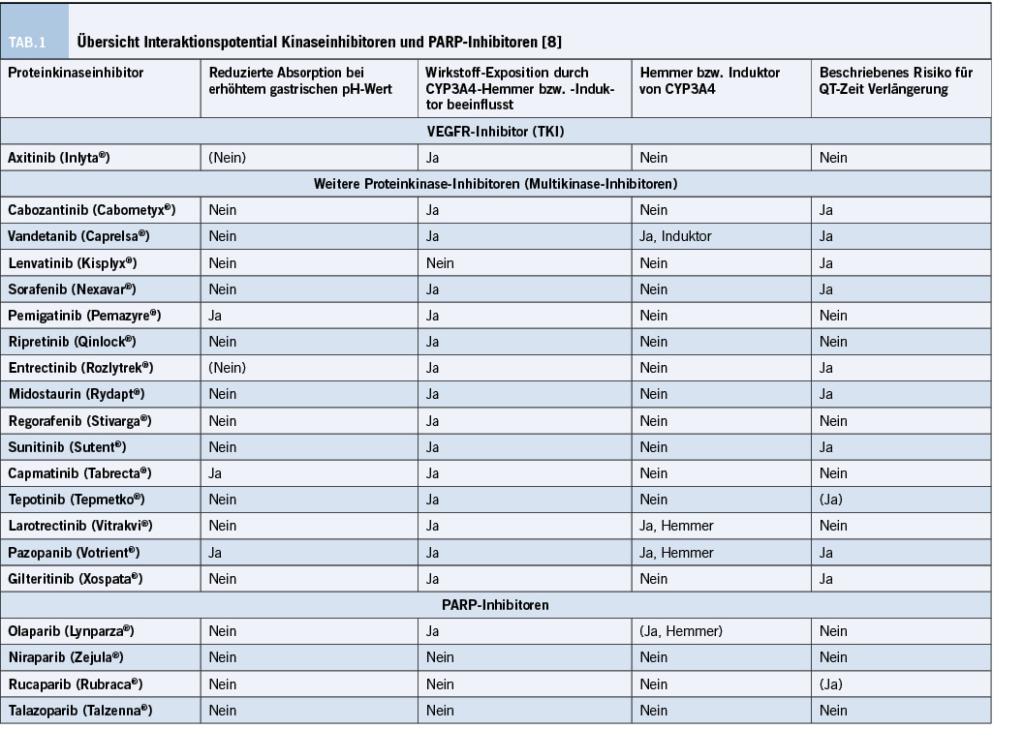
Proteinkinaseinhibitoren werden in drei Hauptgruppen kategorisiert: Serin/Threoninkinase Inhibitor (STKI), Tyrosinkinase Inhibitoren (TKI) und Multikinaseinhibitoren (Tabelle 1).
Neben verschiedenen Vorteilen in Hinblick auf die Lebensqualität der Patientinnen und Patienten sind die antitumoralen Wirkstoffe, aufgrund ihrer Toxizität und der engen therapeutischen Breite, mit einem hohen Risiko für unerwünschte Arzneimittelwirkungen und Interaktionen assoziiert. Ältere Krebspatienten und -patientinnen sind besonders anfällig für Arzneimittelinteraktionen und unerwünschte Arzneimittelwirkungen, da oft verschiedene Medikamente sowohl für die Behandlung von tumorassoziierten Beschwerden wie auch für andere Co-Morbiditäten eingesetzt werden. Zusätzlich sind Veränderungen in den pharmakokinetischen Parametern zu beachten, welche die Arzneimittelabsorption, die Metabolisierung und Elimination beeinflussen können [1].
Untersuchungen zur Prävalenz zeigen, dass 27-58% der Patientinnen und Patienten unter oraler Tumortherapie von mindestens einer Arzneimittelinteraktion betroffen sind [1,2], wobei davon etwa ein Drittel als potentiell schwerwiegend eingestuft wird [2]. Als die häufigsten Folgen von Arzneimittelinteraktionen wurden eine reduzierte Wirksamkeit der antitumoralen Therapie und Risiko für QT-Zeit Verlängerung identifiziert [3].
Wie können Arzneimittelinteraktionen mit oralen antitumoralen Therapien entstehen?
Pharmakokinetische Interaktionen
Pharmakokinetische Interaktionen treten auf, wenn ein Arzneistoff die Absorption, die Verteilung, den Metabolismus und/oder die Ausscheidung eines anderen Wirkstoffes beeinflusst [1]. Solche Arzneimittelinteraktionen können zu reduziertem Therapieansprechen wie auch zu verstärkter Toxizität führen.
Da relevante pharmakokinetische Arzneimittelinteraktionen bei oralen Onkologika häufig auftreten, ist ein sorgfältiges Überprüfen auf solche Wechselwirkungen äusserst wichtig.
Für manche Arzneistoffe ist eine Blutspiegel-Bestimmung möglich. Lassen sich gewisse Arzneimittelinteraktionen nicht verhindern, kann eine solche Laboranalyse in ausgewählten Fällen zur Abschätzung des Ausmasses einer veränderten Wirkstoffexposition hilfreich sein.
Absorption
Die Bioverfügbarkeit eines Arzneistoffes ist unter anderem abhängig von der Freisetzung aus der Arzneiform und der Löslichkeit des Wirkstoffes. Diese wiederum ist beeinflusst durch den vorliegenden pH Wert im Gastrointestinal-Trakt.
Viele Proteinkinaseinhibitoren sind schwache Basen. Bei höheren pH Werten verschiebt sich deren Löslichkeitsgleichgewicht, abhängig von den spezifischen chemischen Wirkstoffeigenschaften, vermehrt zu der schwerer löslichen nicht-ionisierten Form [4]. Werden Proteinkinaseinhibitoren gleichzeitig mit Medikamenten verabreicht, welche den Magen pH erhöhen, kann deren Absorption aus dem Gastrointestinal-Trakt in relevantem Ausmass vermindert sein, was infolgedessen zu einer Abnahme der antitumoralen Wirksamkeit führen kann.
Das Ausmass und somit die Relevanz dieser Interaktion unterscheidet sich für die verschiedenen Wirkstoffe (Tabelle 1). Werden orale antitumorale Therapien mit pH-abhängiger Löslichkeit eingesetzt, soll die Indikation für eine gleichzeitige Verschreibung von Protonenpumpen-Inhibitoren und Antazida streng gestellt werden. Wenn immer möglich, ist auf eine Co-Medikation zu verzichten.
Für weitere orale Tumortherapie Klassen wie Poly-(ADP-Ribose)-Polymerase (PARP) Inhibitoren und antihormonelle Therapien ist keine Beeinflussung der Absorption durch Protonenpumpen Inhibitoren zu erwarten [5].
Metabolismus
Eine Vielzahl der zielgerichteten oralen Tumortherapien wird über das Cytochrom 3A4 (CYP3A4), dem wichtigsten Enzym im Arzneistoffmetabolismus, verstoffwechselt und ist deshalb anfällig für pharmakokinetische Interaktionen (Tabelle 1).
Von grosser klinischer Relevanz sind Wechselwirkungen von CYP3A4 Substraten mit starken Enzym-Induktoren bzw. –Inhibitoren, da eine bis zu fünf-fach erhöhte oder erniedrigte Wirkstoffexposition resultieren kann [6]. Aber auch für moderate Enzym-Induktoren bzw. –Inhibitoren können die Auswirkungen auf die Wirkstoffexposition der oralen Tumortherapien von Bedeutung sein.
Eine Überprüfung von Arzneimittelinteraktionen soll, insbesondere auch bei oralen antitumoralen Therapien, bei jeder Veränderung der Begleitmedikation erfolgen. Entsprechende Kontraindikationen und Empfehlungen zu Dosisanpassungen sind den jeweiligen Fachinformationen zu entnehmen.
Therapeutisches Drug Monitoring ist bislang für orale Tumortherapien nicht routinemässig etabliert. Für einige der zielgerichteten Tumortherapien ist eine Blutspiegelbestimmung jedoch möglich und kann hilfreich sein, um das Ausmass einer unumgänglichen Arzneimittelinteraktion abzuschätzen. Ein Therapeutisches Drug Monitoring kann somit bereits heute in ausgewählten Fällen sinnvoll sein, um eine wirksame und sichere Anwendung der zielgerichteten oralen Tumortherapien zu unterstützen [7]. Es wird sich zeigen, ob zukünftig eine routinemässige Blutspiegelbestimmung im klinischen Alltag Einzug finden wird.
Proteinkinaseinhibitoren sind nicht nur Substrate von CYP3A4, sie fungieren teilweise auch als Hemmer oder Induktoren dieser Enzyme (Tabelle 1) und können so die Verstoffwechselung anderer Medikamente beeinflussen.
Pharmakodynamische Interaktionen
Pharmakodynamische Wechselwirkungen resultieren aus der Kombination von Arzneimitteln mit ähnlichen Wirkungs- bzw. Nebenwirkungsmechanismen, welche sich synergistisch, additiv oder auch antagonistisch verhalten können. Klinische Effekte bzw. unerwünschte Arzneimittelwirkungen können verstärkt oder auch abgeschwächt auftreten.
Für orale antitumorale Therapien wurde ein erhöhtes Risiko für QT-Zeit Verlängerung als die häufigste pharmakodynamische Arzneimittelinteraktion identifiziert [3]. Proteinkinaseinhibitoren mit QT-Zeit Verlängerung als unerwünschte Arzneimittelwirkung sind in der Tabelle 1 aufgelistet. Zusätzlich kann eine durch Chemotherapie vermittelte Dyselektrolytämie das Risiko für kardiale unerwünschte Arzneimittelwirkungen begünstigen. Auch wenn eine Torsade de pointes als schwerwiegende Komplikation nur mit einer niedrigen Inzidenzrate auftritt, kann diese fatale Folgen haben, weshalb ein sorgfältiges Monitoring diesbezüglich indiziert ist. Um einer arzneimittelinduzierten QT-Zeit-Verlängerung vorzubeugen, soll vor Behandlungsbeginn das patientenspezifische Risiko diesbezüglich identifiziert werden. Auf die Kombination mit weiteren QT-Zeit verlängernden Medikamenten soll, wenn möglich, verzichtet werden [3]. Falls eine gleichzeitige Einnahme von Arzneimitteln mit Risiko für QT-Zeit Verlängerung indiziert ist, soll ein Monitoring des Elektrokardiogramms (EKG) 24-48 Stunden vor und 1 Woche nach Behandlungsbeginn erfolgen [4]. Arzneimittelspezifische Empfehlungen zur EKG Überwachung sind, sofern vorhanden, den entsprechenden Fachinformationen zu entnehmen.
Im Gegensatz zu vielen Proteinkinaseinhibitoren sind PARP-Inhibitoren nicht mit einer klinisch relevanten QT-Zeit Verlängerung assoziiert [9]. Jedoch ist in der Fachliteratur ein Fall von Torsade des pointes in Assoziation mit Rucaparib bei einem Patienten mit vorbestehender QT-Zeit Verlängerung berichtet worden [10].
Zusammenfassend ist festzuhalten, dass orale antitumorale Therapien verschiedenen pharmakokinetischen und pharmakodynamischen Arzneimittelinteraktionen unterliegen können. Die obenstehende Tabelle bietet einen Überblick zu den Interaktionsrisiken verschiedener oraler Tumortherapien in Hinblick auf die in Studien am häufigsten identifizierten Wechselwirkungen. Weitere Arzneimittelinteraktionen, z.B. durch die Beeinflussung anderer am Arzneistoffmetabolismus beteiligter Cytochrome oder Transportproteine, wie auch Wechselwirkungen mit Nahrungsmitteln sind möglich. Ein sorgfältiger Interaktionscheck ist bei jeder Anpassung der Medikation indiziert.
Kantonsspital Baselland Liestal
Rheinstrasse 26
4410 Liestal
anne.leuppi-taegtmeyer@ksbl.ch
keine
1. Riechelmann RP, Tannock IF, Wang L, Saad ED, Taback NA, Krzyzanowska MK. Potential drug interactions and duplicate prescriptions among cancer patients. J Natl Cancer Inst. 2007, Apr 18;99(8):592–600.
2. Van Leeuwen RWF, Brundel DHS, Neef C, et al. Prevalence of potential drug-drug interactions in cancer patients treated with oral anticancer drugs. British Journal of Cancer. 2013, 108:1071–8.
3. Kim SH, Suh Y, Ah YM, Jun K, Lee JY. Real-world prevalence of potential drug-drug interactions involving oral antineoplastic agents: a population-based study. Supportive Care in Cancer. 2020 Aug 1;28(8):3617–26.
4. Van Leeuwen RWF, Van Gelder T, Mathijssen RHJ, Jansman FGA. Review Drug-drug interactions with tyrosine-kinase inhibitors: a clinical perspective. 2014. Available from: www.thelancet.com/oncology
5. Bridoux M, Simon N, Turpin A. Proton Pump Inhibitors and Cancer: Current State of Play. Vol. 13, Frontiers in Pharmacology. Frontiers Media S.A.; 2022.
6. DeRemer D. Clinically Relevant Drug Interactions in the Cancer Setting. J Adv Pract Oncol. 2022 Apr 1;13(3):231–5.
7. Escudero-Ortiz V, Domínguez-Leñero V, Catalán-Latorre A, Rebollo-Liceaga J, Sureda M. Relevance of Therapeutic Drug Monitoring of Tyrosine Kinase Inhibitors in Routine Clinical Practice: A Pilot Study. Pharmaceutics. 2022 Jun 1;14(6).
8. Fachinformationen CH [cited 2023 July 07] Available from: https://www.swissmedicinfo.ch
9. Coppola C, Rienzo A, Piscopo G, Barbieri A, Arra C, Maurea N. Management of QT prolongation induced by anti-cancer drugs: Target therapy and old agents. Different algorithms for different drugs. Cancer Treat Rev. 2018 Feb 63:135-143.
10. Segan L, Beekman A, Parfrey S, Perrin M. PARP inhibitor-induced torsades de pointes in long QT syndrome: a case report. Eur Heart J Case Rep. 2019 Dec 31;4(1):1-5.
Therapeutische Umschau
- Vol. 80
- Ausgabe 8
- Oktober 2023