- Übersicht und Therapie-Update Colitis ulcerosa
Die Colitis ulcerosa ist eine chronisch entzündliche Darmerkrankung, die auf die Mukosa des Kolons beschränkt ist und deren Ausdehnung nach proximal variiert. Die Hauptsymptome sind Durchfälle teilweise mit Blutbeimengungen und Bauchschmerzen, mit Phasen von Krankheits-Schüben und Phasen der Remission. Die Diagnose der Colitis ulcerosa wird aufgrund der Klinik, dem endoskopischen Befund und dem histologischen Resultat gestellt. Derzeit wirken die verschiedenen medikamentösen Behandlungsmöglichkeiten u.a. durch eine lokale oder systemische Aktivitätsreduktion des Immunsystems. Bei leichten bis mittelschweren Formen der Colitis ulcerosa bilden die 5-ASA- Präparate den Hauptpfeiler, sowohl der Induktions-, wie auch der Erhaltungstherapie. Bei schwereren Krankheits-Schüben ist Kortison die Behandlung der Wahl. Um die längerfristige oder wiederholte Einnahme von Kortikosteroiden zu limitieren und eine Remission zu induzieren oder die Remission zu erhalten, gibt es mehrere therapeutische Optionen von Biologika mit unterschiedlichen Wirkungsspektren und Sicherheitsprofilen. Neben dem Erreichen der klinischen Remission entwickeln sich die therapeutischen Ziele weiter. Die endoskopische und histologische Remission sind neue Ziele, um die Lebensqualität der Patienten weiter zu verbessern und um langfristige Komplikationen, wie z. B. Darmkrebs, zu reduzieren.
Einleitung
Allgemeines und Epidemiologie
Die Colitis ulcerosa (CU) gehört zusammen mit dem Morbus Crohn (MC) zu den chronisch-entzündlichen Darmerkrankungen (IBD, inflammatory bowel disease). Die exakte Ätiologie ist derzeit noch immer ungeklärt. Nach heutigem Wissensstand handelt es sich um eine komplexe multifaktorielle Erkrankung, bei der genetische Faktoren, Umweltfaktoren (wie z.B. Ernährung, Hygiene und der Antibiotika –
Gebrauch), die Mikrobiota und das Immunsystem eine Rolle in der Entstehung spielen (1).
Derzeit leiden 0,2% der europäischen Bevölkerung an IBD, wobei die Inzidenz der CU zwischen 2,4 und 44 pro 100.000 Personenjahre liegt (2). Diese Inzidenz nimmt vor allem in den westlichen Ländern zu, was den Verdacht aufkommen lässt, dass unser Lebensstil teilweise mitverantwortlich sein könnte. Eine Ernährung, reich an rotem Fleisch und zugesetztem/verändertem Zucker, ist ein Risikofaktor (3). Die mediterrane Diät dagegen hat einen protektiven Effekt (3). Das Rauchen führt bei Morbus Crohn zu einem problematischeren Verlauf, hingegen bei CU zu einer Verringerung der Auftretenswahrscheinlichkeit der Erkrankung (3).
Bevölkerungsstudien haben keine Unterschiede in der Verteilung zwischen Männern und Frauen gezeigt (4). Es gibt zwei Inzidenzspitzen: eine erste im Alter von 20 bis 30 Jahren und eine zweite nach dem fünften Lebensjahrzehnt (4).
Definition
Die CU ist eine chronisch-entzündliche Erkrankung, die auf die Kolonschleimhaut beschränkt ist und sich vom Rektum nach proximal ausbreitet. In Rahmen einer Pancolitis kann sich die Entzündung in vereinzelten Fällen in das terminale Ileum ausbreiten, was als backwash ileitis bezeichnet wird. Der Rest des Verdauungstrakts bleibt unbetroffen (5). Die Diagnose wird histologisch (Koloskopie mit Biopsien) bestätigt, wobei eine diffuse transmukosale Entzündung mit basaler Plasmozytose und Kryptitis nachgewiesen wird (5).
Klinik
Klinisch stellen sich Patienten mit CU (im akuten Entzündungs-Schub) mit Bauchschmerzen, Tenesmen und schleimig-blutigen Durchfällen mit Stuhldrang vor. Dies kann zu Mangelernährung und Gewichtsverlust führen. Bei Kindern kommt es häufig zu einem Unterbruch in der Wachstumskurve (6,7). Zudem können die Patienten auch an extra-
intestinalen Manifestationen der CU mit z. B. Gelenkschmerzen, Hautläsionen oder ophthalmologischen Entzündungen leiden. Dies betrifft bis zu 50 % der Patienten mit IBD (8) und wird in einem späteren Artikel in dieser Zeitschrift ausführlich beschrieben.
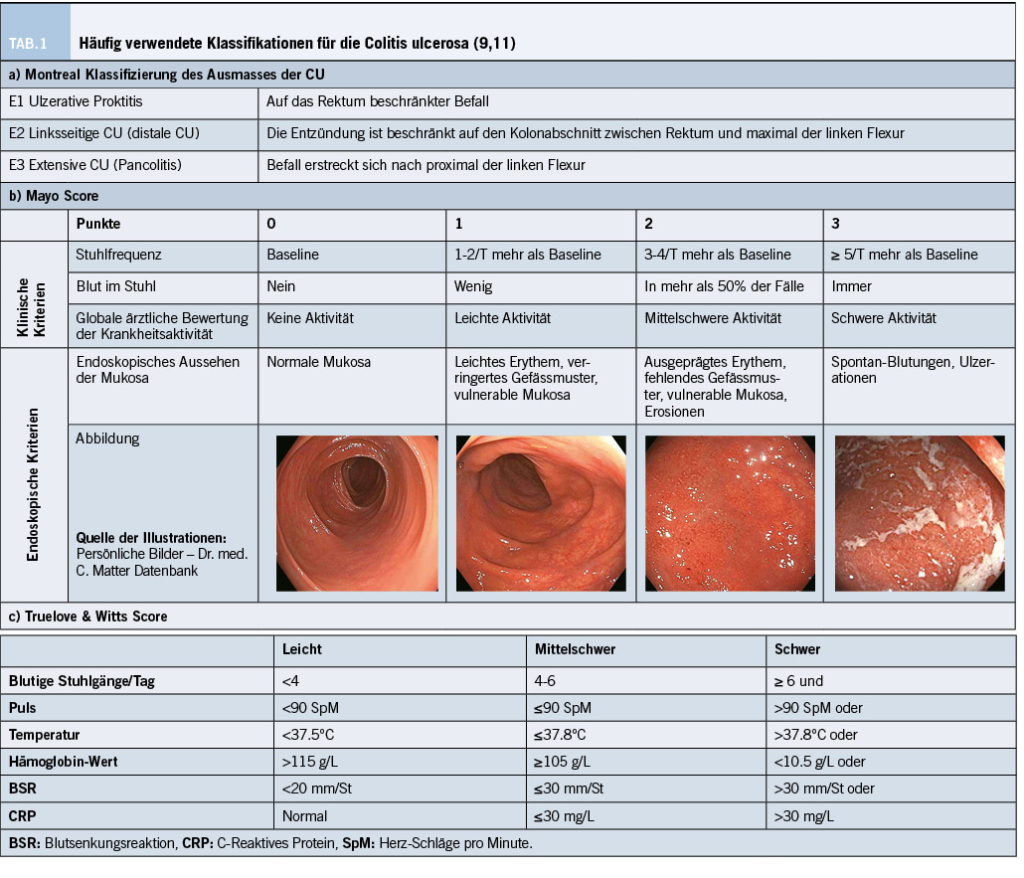
Labortechnisch können eine Anämie und ein Vitaminmangel vorliegen. Die intestinale Entzündung lässt sich durch einen pathologisch erhöhten Calprotectin-Wert im Stuhl messen. Aufgrund des oberflächlichen, mukosalen Befalles der CU kann der CRP-Wert trotz einer ausgedehnteren Colitis Ulcerosa noch normal oder tief-normal ausfallen. Das CRP ist hingegen sehr nützlich als Marker für einen schweren Verlauf der Colitis, gemäss den Kriterien nach Truelove & Witts (Figur 1c) (9). Das toxische Megakolon, das durch eine nicht obstruktive Kolon-Dilatation von ≥5.5cm definiert ist, stellt eine gefürchtete Komplikation dar, die rasch erkannt und behandelt werden muss, da sonst eine Perforation auftreten kann (7,10). Je nach Klinik muss eine abdominale Bildgebung, z.B. mit einem CT – Abdomen, zur Suche nach einer solchen Komplikation durchgeführt werden (7).
In der Koloskopie zeigt sich die Darmschleimhaut (im akuten Entzündungs-Schub) erythematös, ödematös und ulzeriert. Der Befall ist von unterschiedlicher Ausdehnung, verläuft aber klassischerweise immer vom Rektum kontinuierlich nach proximal, mit einer scharfen Abgrenzung zur gesunden Schleimhaut (7). Zu beachten ist, dass sich der entzündliche Befall unter einer (v.a. lokalen) medikamentösen Therapie atypisch manifestieren kann (5).
Der Darmultraschall entwickelt sich zunehmend zur kosteneffizienten und zuverlässigen nicht-invasiven Technik für die Lokalisation und Evaluation der Entzündungsaktivität (7).
Der Mayo-Score hat eine klinische und endoskopische Komponente und wird häufig zur Bestimmung des Schweregrades der CU verwendet (Figur 1b).
Bei der CU handelt es sich um eine chronische Krankheit, die sich klinisch unterschiedlich präsentieren kann, mit Phasen von Krankheits-Schüben und Phasen der Remission (11). Klassischerweise wird das Ausmass der Erkrankung in drei Kategorien unterteilt: Isolierter rektaler Befall (Proktitis), linksseitiger Kolonbefall (max. bis zur linken Flexur) und ausgedehnter Befall (über die linke Flexur hinaus resp. eine Pancolitis). Dies entspricht der Montreal-Klassifikation (Figur 1a). Die Ausdehnung verändert sich im Laufe der Zeit. Bis zu 40% der Patienten mit einer Proktitis und 70% der Patienten mit einer linksseitigen Kolitis werden irgendwann im Verlauf ihrer Erkrankung eine ausgedehnte Kolitis entwickeln (10).
Prognose
Die CU erhöht das Risiko für ein kolorektales Karzinom (KRK) im Vergleich zur Allgemeinbevölkerung (12). Die Hauptrisikofaktoren bei IBD – Patienten sind die Intensität der Entzündung und die Dauer der Erkrankung (11). Eine Metaanalyse schätzte die Kolonkarzinom – Inzidenz auf ca. 2% nach 10 Jahren Krankheit und auf 18% nach 30 Jahren (12).
Die Sterblichkeit bei Patienten mit CU ist im Vergleich
zur Allgemeinbevölkerung leicht erhöht, sinkt aber aktuell u.a. aufgrund einer verbesserten Früherkennung des Kolonkarzinomes (13).
Therapieoptionen
Derzeit gibt es keine kurative Behandlung für die CU. Die Therapie zielt auf eine Reduktion der Entzündungsaktivität der Colitis und den Remissionserhalt. Es gibt mehrere Behandlungsziele (STRIDE-II-Konsens) (16). Zuerst gibt es klinische Ziele, die darauf abzielen, dass der Patient schnell beschwerdefrei wird. Zudem gibt es auch endoskopische und sogar histologische Remissionsziele, um ein Fortschreiten der Krankheit und insbesondere langfristige Komplikationen wie z.B. ein Kolonkarzinom zu verhindern. Das Ziel ist, dass die Patienten trotz Erkrankung so wenig wie möglich in ihrer Lebensqualität beeinträchtigt werden (14).
Weiter ist es wichtig, zwischen einer Therapie zur Remissions-Induktion (Eliminierung der Entzündung) und einer Therapie zur Remissions-Erhaltung (Beibehaltung des entzündungsfreien Zustandes der Kolonmukosa) zu unterscheiden. Gewisse Medikamente können beides erreichen, andere Substanzen sind primär für die Remissions-Erhaltung (nicht jedoch für die Remissions-Induktion) geeignet.
Um die am besten geeignete Therapie auszuwählen, muss das Ziel definiert (Remissions – Induktion und/oder Remissions-Erhaltung), das Ausmass und der Schweregrad der Krankheit evaluiert und auch die Eigenschaften des Patienten (Alter, Präferenzen (z.B. s.c. oder i.v. Therapie), Komorbiditäten, Schwangerschafts-Wunsch, assoziierte extra-
intestinale Manifestationen, medikamentöse Vorbehandlung, usw.) berücksichtigt werden.
Konventionelle Therapie
5-ASA
Mesalamin ist ein Spaltprodukt des ursprünglichen 5-ASA-Wirkstoffes Sulfasalazin. Es wurde in den 1940er Jahren synthetisiert und die Wirksamkeit bei CU wurde in den 1960er Jahren etabliert (15). Obwohl es sich um einen schon lang bekannten und verwendeten Grundpfeiler der Behandlung bei CU handelt, ist der exakte Wirkmechanismus nach wie vor unklar. Der therapeutische Effekt erfolgt über die Hemmung mehrerer Pfade der Entzündungskaskade (u. a. Hemmung der Cyclooxygenase und verminderte Aktivierung des Transkriptionsfaktors NF-κB) (16).
In den neuesten europäischen Empfehlungen wird 5-ASA als Induktions- und Erhaltungstherapie bei leichten bis mittelschweren Formen der CU empfohlen (17).
Die Galenik spielt eine wichtige Rolle für die lokale Effektivität der Therapie.
Bei isoliertem rektalem Befall ist die Behandlung der Wahl das 5-ASA-Suppositorium, da es eine lokal höhere 5-ASA-Konzentration ermöglicht. Bei linksseitigem Befall sind der Schaum und der Einlauf zu bevorzugen (19). Bei rekto-sigmoidalem oder ausgedehnterem Befall gibt es einen Nutzen für die Induktion der Remission, falls die topische 5-ASA-Behandlung mit einer systemischen Behandlung (oral) kombiniert wird (19). Die klinische Effektivität ist dosis-
abhängig, mit einer maximalen Wirkung bei einer 5-ASA Dosis bis höchstens 4,5g/Tag (bez. der maximalen Dosierung bezüglich dem jeweiligen 5-ASA-Präparat bitten wir um Konsultation der Packungsbeilage) (18).
Die einmalige oder über den Tag verteilte Einnahme zeigt die gleiche Wirksamkeit und kann je nach Präferenz des Patienten festgelegt werden (19). Ebenso sind die verschiedenen oralen 5ASA-Präparate in Bezug auf ihre Wirksamkeit vergleichbar (19). Wie bei jeder Behandlung ist die Compliance für die Wirksamkeit der Behandlung von entscheidender Bedeutung (20).
Sobald der Patient in Remission ist, wird empfohlen, die Behandlung mit 5-ASA in der geringstmöglichen wirksamen Dosierung fortzusetzen. Wiederum ist eine topische Behandlung bei distalem Befall zu bevorzugen (21). Als Richtwert werden Mindestdosen von 2g/Tag für orale 5-ASA bei E2 und E3-Befall und 3g/Woche für 5-ASA als Zäpfchen bei Proktitis (E1) empfohlen (9).
Was die Nebenwirkungen anbelangt haben 5-ASA-Präparate, abgesehen von dem fast nicht mehr verwendeten Sulfasalazin, ein gutes Sicherheitsprofil (23). Die wichtigsten Nebenwirkungen sind unspezifisch (Übelkeit, Kopfschmerzen, Durchfall und Nasopharyngitis). Eine Erhöhung der Leberwerte wurde bei bis zu 3% der Patienten berichtet. Seltene Fälle (<1%) von Nierenschäden (interstitielle Nephritis, Nierenversagen) sind beschrieben. Einige Fallberichte existieren bezüglich einer Myokarditis (22).
Angesichts dieser Daten ist es wichtig, die Nieren- und Leberfunktion zum Zeitpunkt der Therapie-Einführung zu kontrollieren und diese Laborwerte in regelmässigen Abständen zu überprüfen.
Kortison
Bei mittelschweren bis schweren Formen der CU wird systemisches Kortison als Induktionstherapie empfohlen (17). Wie bei jeder Verschreibung von Kortikosteroiden ist anzuraten ein degressives Schema zu verwenden, um das Risiko einer sekundären Nebenniereninsuffizienz zu begrenzen (23).
Eine Kortisonbehandlung sollte aufgrund des Nebenwirkungsprofils nicht länger als drei Monate verschrieben werden (17). Die Einnahme von systemischem Kortison, vor allem über einen längeren Zeitraum, ist mit zahlreichen möglichen unerwünschten Nebenwirkungen und Komplikationen verbunden: Herz-Kreislauf (arterielle Hypertonie), Stoffwechsel (Diabetes, Osteoporose, sekundäre Gewichtszunahme durch gesteigerten Appetit), Infektionen und Augenerkrankungen (Katarakt, Glaukom) (24). Zudem besteht ein Risiko für nicht zu unterschätzende psychologische Probleme wie Depressionen und Angstzustände, die bei bis zu 20 % der Patienten berichtet wurden und bei fast 5 % der Patienten zu Selbstmordgedanken führen können.
Um die systemischen Nebenwirkungen zu begrenzen, kann bei leichtem bis mittelschwerem Befall topisches Kortison verwendet werden. Zum Beispiel Budesonid-Schaum (Budenofalk-Schaum®) bei rektalen oder rektosigmoidalen Formen, sowie orales Kortison mit Freisetzung im Kolon wie Budenosid MMX (Cortiment®) bei ausgedehnteren Formen.
Da die topischen Kortison-Formen teilweise absorbiert werden, sind die oben genannten Nebenwirkungen ebenfalls möglich, wenn auch in weit geringerem Ausmass.
Daher ist es wichtig, jede Verschreibung von Kortikosteroiden sorgfältig zu prüfen und frühzeitig über kortikosteroidsparende Strategien nachzudenken (23).
Azathioprin
Azathioprin ist ein Prodrug des Purin-analogon 6-TGN, das die Proliferation von T-Lymphozyten hemmt (25).
Thiopurine haben wegen der zu langen Wartezeit bis zum effektiven Wirkungseintritt keinen Platz in der Induktionstherapie der CU (17).
Gemäss den europäischen Empfehlungen der ECCO (European Crohn´s and Colitis Organisation) wird bei Nichtverträglichkeit von 5-ASA oder einem kortikoidabhängigen Verlauf der CU, Azathioprin als Erhaltungstherapie empfohlen (17). Dies ermöglicht eine einfache (orale), kostengünstige Grundbehandlung, bei der die langfristigen Nebenwirkungen der Kortikosteroidtherapie vermieden werden können.
Azathioprin ist jedoch nicht frei von Nebenwirkungen. Bis zu einem Drittel der Patienten berichtet über Nebenwirkungen, insbesondere gastrointestinaler Art (wie z.B. Übelkeit), die in etwa 20% der Fälle zum Abbruch der Behandlung führen (26). Myelosuppression (dosisabhängige Leukopenie), Hepatotoxizität (dosisabhängig) und Pankreatitis (idiosynkratisch) wurden beschrieben, die jeweils 4% der Patienten betrafen (26). Das Lymphomrisiko ist sowohl bei jungen (<35Jahre) EBV-negativen Männern (bei denen diese Behandlung kontraindiziert ist) als auch bei älteren Patienten, die eine Langzeitbehandlung erhalten, erhöht (27). Aus diesen Gründen wird diese Behandlung für Patienten über 65 Jahren nicht empfohlen (17). Langfristig wird zudem das Risiko von Hautkrebs erhöht (25,28).
Es ist wichtig, dass Patienten unter Azathioprin mit regelmässigen klinischen und labortechnischen Kontrollen (u.a. komplettes Blutbild und Leberwerte) überwacht werden (28). Regelmässige dermatologische Screenings sind ebenfalls empfehlenswert (28).
Angesichts der Nebenwirkungen von Azathioprin und mit dem Erscheinen neuer Moleküle mit einem besseren Sicherheitsprofil, werden diese neue Therapien in der täglichen gastroenterologischen Praxis oft bevorzugt und der Stellenwert der Thiopurine als Monotherapie ist Gegenstand von Diskussionen (29).
Biologika
TNFa-Inhibitoren
TNFα-Inhibitoren binden neutralisierend an das proinflammatorische Zytokin TNFα (Tumor-Nekrose-Faktor α) und führen u.a. damit zu einer Hemmung der Entzündungskaskade (30).
Seit über 20 Jahren stehen uns zur Behandlung von chronisch-entzündlichen Darmerkrankungen mehrere TNFα-Inhibitoren zur Verfügung. Infliximab wurde 1998 in den USA und 1999 in der Schweiz zugelassen (30). Es handelt sich um einen chimären Mensch/Maus-Antikörper. Weitere für die CU zugelassene Substanzen sind Adalimumab und Golilumab. Certolizumab ist in der Schweiz nur für die Behandlung des Morbus Crohn und Golilumab nur für die Therapie der CU zugelassen.
Die Biologika-Klasse der TNFα-Inhibitoren kommen zur Anwendung, falls beim Bestehen einer aktiven moderaten bis schweren CU ein Therapieansprechen mit einer konventionellen Therapie, wie z.B. mit 5-ASA Präparaten und/oder Cortison, nicht erreicht werden kann oder diese nicht vertragen wird (17). Falls trotz einer Therapie mit hochdosiertem Cortison keine Remission (Entzündungs-Abheilung) induziert werden kann, wird von einer steroid-refraktären CU gesprochen. Von einer steroidabhängigen CU spricht man, falls die Cortison-Therapie nicht komplett ausgeschlichen werden kann ohne erneutes Aufflammen der Entzündung. In beiden letztgenannten Fällen ist die Indikation für den Einsatz eines TNFα-Inhibitors gegeben.
Zusätzlich ist der Einsatz der TNFα-Blocker sehr hilfreich falls, zusätzlich zur CU, auch eine extraintestinale Manifestation der chronisch entzündlichen Darmerkrankung, wie z.B. eine Spondyloarthritis oder ein (steroidrefraktäres) Erythema nodosum besteht (7). Weiterhin auch beim zusätzlichen Bestehen von anderen Autoimmunkrankheiten wie z.B. einer rheumatoiden Arthritis oder einer Psoriasis-Arthritis.
TNFα-Inhibitoren können durchaus auch länger angewendet werden. Limitierende Faktoren sind das Auftreten von neutralisierenden Antikörpern gegen das Medikament (in 10 – max. 20% der Fälle / Jahr), die zu einem (sekundären) Wirkungsverlust und Abbruch der Behandlung führen können. Deshalb ist eine Kombinationstherapie des TNFα-Inhibitors mit einem Immunomodulator wie Azathioprin (wenigstens in den ersten 6 Monaten) hilfreich, um die Antikörper-Bildung zu reduzieren und den Medikamenten-Spiegel zu erhöhen. Dies konnte allerdings nur für die Kombination von Infliximab und Azathioprin gezeigt werden, nicht aber für andere TNFα-Inhibitoren (31,32). Zusätzlich finden regelmässig Messungen der Medikamenten- und Antikörper-Spiegel statt. Auch Nebenwirkungen wie Infektionen, kutane Veränderungen oder Gelenksbeschwerden können zum Abbruch der Therapie führen.
α4β7-Integrin-Antagonisten
Der in der Schweiz seit 2015 zugelassene Antikörper Vedolizumab bindet hochselektiv an das α4β7- Integrin auf Lymphozyten im Darm und verhindert somit das Andocken der Lymphozyten an das (sich in den Blutgefässen der Darmschleimhaut befindliche) mucosale Adhäsions-Molekül Madcam-1. Einfach gesagt können die Lymphozyten aufgrund dieser Blockierung nicht an der Gefässwand andocken, um abzubremsen und in Folge durch das Endothel hindurch zum Entzündungsort (z.B. der Darm-Mukosa) zu «wandern» (33).
Mit Vedolizumab steht eine hochselektive Antikörper-Therapie zur Verfügung, die ein gutes Nebenwirkungsprofil (z.B. bez. infektiösen Komplikationen) ausweist und eine sehr gute Effektivität zur Behandlung der CU zeigt. Die mukosale Entzündung kann unter Vedolizumab komplett abheilen. Weiterhin kann das Medikament auch über längere Zeit effektiv angewendet werden. Ein zu beachtender Faktor ist der verzögerte Wirkungseintritt bezüglich der Entzündungshemmung der CU. Es kann durchaus mehrere Wochen (bis einige Monate) dauern bis das Medikament sein volles Potential ausgeschöpft hat, weshalb bei akuten Entzündungen andere Medikamente (ggf. zusätzlich) zur Anwendung kommen. Zudem ist Vedolizumab bei extraintestinalen Manifestationen (wie z.B. axialer Spondyloarthritis) und anderen entzündlichen Autoimmunkrankheiten (wie der Psoriasis- und rheumatoiden Arthritis) weniger bis nicht effektiv (hier wäre z.B. eine TNFα-Inhibitor-Therapie angezeigt) (7).
Interleukin-12/23-Antagonisten
Der humane monoklonale Interleukin 12/23-Antikörper Ustekinumab ist in der Schweiz seit 2020 für die Behandlung der CU zugelassen. Der Antikörper bindet an die p40 Untereinheit der IL-12 und IL-23-Zytokine und verhindert somit die Interaktion mit dem IL-12-Rezeptor. Dies führt zu einer reduzierten zellulären Aktivität und einer reduzierten Zytokin-Produktion und Sekretion.
Ustekinumab zeigt ein sehr gutes Nebenwirkungsprofil, sowie eine sehr gute Effektivität zur Behandlung der CU auch über längere Zeit (26,34). Gerade bei Patienten, die zusätzlich an einer kutanen Psoriasis oder einer Psoriasis-Arthritis leiden, ist die Behandlung mit diesem Antikörper ideal. Wie bei Vedolizumab kann es unter Ustekinumab zu Nebenwirkungen wie Kopfschmerzen und nasopharyngealen Infektionen kommen. Weiterhin kann es bei einer Behandlung mit Ustekinumab mehrere Wochen (bis einige Monate) dauern, bis das volle Wirkungs-Potential des Medikamentes erreicht worden ist. Die Behandlung erfolgt mit einer initialen Infusion und im Anschluss s.c. Medikamenten-Verabreichungen alle 8-12 Wochen.
Janus-Kinase-Inhibitoren
Janus-Kinase-Inhibitoren, abgekürzt JAK-Inhibitoren, sind eine relativ neue Klasse von Medikamenten, welche über die Blockade der intrazellulären Enzyme, der Janus-Kinasen, ihre Wirkung entfalten. Sie beeinflussen hierbei die Signalweiterleitung von der Zellmembran zum Zellkern und damit die Genexpression und bewirken damit einen spezifischen immunsuppressiven, antiphlogistischen und antiproliferativen Effekt. Die bisher in der Schweiz für die CU (seit 2018) zugelassene Substanz ist Tofacitinib (Xeljanz®), ein «small molecule», welches als orale Tablette eigenommen werden kann. Tofacitinib ist ein Pan-JAK-Inhibitor und hemmt JAK1, JAK2, JAK3 und weniger auch die TyK2. Der Wirkungseintritt erfolgt rasch, innerhalb von wenigen Tagen. Vorsicht ist v.a. bei Patienten ab 50 Jahren geboten, die kardiovaskuläre Risikofaktoren ausweisen. Hier wurde in den Studien eine erhöhte Rate von kardiovaskulären Ereignissen (wie z.B. Herzinfarkt) und auch opportunistischen Infekten (v.a. Herpes zoster) beschrieben (35). Zudem zeigte sich auch eine erhöhte Inzidenz von malignen Erkrankungen. Vor dem Therapiestart sollte eine Impfung gegen Herpes zoster durchgeführt werden und die Behandlung mit dem JAK-Inhibitor durch einen erfahrenen IBD-Spezialisten erfolgen.
Sphingosin-1-Phosphat-(S1P)-Rezeptormodulator
Seit Ende letztem Jahr (2022) ist der S1P-Rezeptormodulator Ozanimod (Zeposia®) für die Behandlung der CU zugelassen. Ozanimod wird als orale Tablette einmal pro Tag eingenommen. Das Medikament wurde bereits vorgängig für die Behandlung der multiplen Sklerose zugelassen und angewendet. Der genaue Wirkungsmechanismus von Ozanimod ist nicht ganz klar. Es wird davon ausgegangen, dass Ozanimod Lymphozyten (reversibel) am Verlassen von Lymphknoten hindert und somit eine Migration der Lymphozyten zum Entzündungsort in den Darm und in das ZNS unterdrückt (36). Vor Beginn einer Therapie mit Ozanimod muss ein EKG durchgeführt werden, da die Substanz zu Bradykardien führen kann. Bei bekannten Herzerkrankungen muss vor Behandlungs-Start ein kardiologisches Konsilium eingeholt werden.
Ausblick
Insgesamt geht die Entwicklung neuer Medikamente hin zu selektiveren Wirkungsmechanismen. Wahrscheinlich nächstes Jahr dürfte der selektive Janus-Kinasen 1-Inhibitor Upadacitinib für die Behandlung von chronisch entzündlichen Darmerkrankungen zugelassen werden. Upadacitinib ist in der Schweiz bereits unter dem Handelsnamen Rinvoq® für die rheumatoide Arthritis und Psoriasis-Arthritis zugelassen. Die bisherigen Studiendaten bez. der CU sehen sehr vielversprechend aus. Bisher gibt es mit Ustekinumab einen IL-12/23-Antikörper, der für die CU und den Morbus Crohn zugelassen ist. Aktuell befinden sich die selektiven IL-23 Inhibitoren Mirikizumab und Guselkumab in klinischer Erforschung und Risankizumab kurz vor der Zulassung in der Schweiz für Patienten mit chronisch entzündlichen Darmerkrankungen.
Weitere therapeutische Möglichkeiten
Mikrobiom
Da die Pathogenese der CU auch eine Veränderung des Mikrobioms mit sich bringt, ist die Darmflora ein mögliches Ziel von therapeutischen Interventionen (37).
Zur Remissionserhaltung kann das Probiotikum E. coli Nissle verwendet werden (z.B. Mutaflor®). Dieses zeigte in mehreren randomisiert kontrollierten Studien eine vergleichbare Effektivität wie eine 5-ASA-Therapie bezüglich der Remissionserhaltung bei CU (38).
Mehrere randomisierte kontrollierte Studien haben eine Wirksamkeit der fäkalen Mikrobiota-Transplantation (FMT) bei der Behandlung von CU gezeigt. Deshalb spricht sich eine aktuelle schweizerische Expertenempfehlung dafür aus, dass die FMT bei ausgewählten CU-Patienten in spezifischen Situationen angeboten werden könnte (39).
Komplementäre Medizin
Eine deutsche Studie ergab, dass etwa 50% der CED-Patienten im Verlauf ihrer Krankheit komplementärmedizinische Angebote in Anspruch genommen haben (40). Mehrere Studien zeigen positive Signale, insbesondere für die Verwendung von Curcumin, aber es fehlen qualitative Studien (41). In den Empfehlungen der DGVS 2023 wird erwähnt, dass Plantago ovata, Curcumin und Pflanzenkombinationen (Myrrhe, Kamillenblütenextrakt und Kaffeekohle) als ergänzende Behandlung in Remissionsphasen eingesetzt werden können (42).
Körperliche Aktivität
Regelmässige körperliche Aktivität wird bei IBD-Patienten empfohlen (43). Dies scheint einen positiven Einfluss auf die chronische Müdigkeit und die Lebensqualität zu haben und könnte auch das Risiko eines aktiven Krankheitsschubs reduzieren. Für letzteres fehlen jedoch noch belastbare wissenschaftliche Daten (44).
Chirurgie
Bei einer medikamentös nicht beherrschbaren schweren CU muss eine chirurgische Behandlung in Betracht gezogen werden (45). Dies wird in einem späteren Artikel in dieser Zeitschrift ausführlich beschrieben.
Spezialfälle
ASUC
Die akute schwere Colitis ulcerosa (ASUC) kann als Erstmanifestation der CU bei bis zu 1/3 der Patienten auftreten (in den anderen 2/3 der Fälle tritt sie im Verlauf der Erkrankung auf). Klinische Zeichen für eine schwere Erkrankung liefern z.B. die Kriterien von Truelove & Witts (Figur 1). Sind diese Kriterien erfüllt, sollte eine rasche und (falls notwendig) stationäre Behandlung dieser Patienten durchgeführt werden. Die Erstbehandlung umfasst die intravenöse Kortikosteroid-Therapie und bei Nichtansprechen eine Behandlung mittels TNF-α-Inhibitoren oder Immunsuppressiva (z.B. Ciclosporin oder Tacrolimus) (9,45). Eine frühzeitige Involvierung des Chirurgen und eine engmaschige interdisziplinäre Betreuung dieser schwerkranken Patienten ist empfohlen, da eine Rettungs-
kolektomie bei medikamentösem Nichtansprechen zeitnah in Betracht gezogen werden muss (9,10,45).
NSAR (Nichtsteroidales Antirheumatikum)
Bezüglich dem Zusammenhang zwischen der Einnahme von NSAR und dem Auftreten von Krankheitsschüben der CU zeigen mehrere Studien widersprüchliche Ergebnisse (46). Die jüngsten Empfehlungen der ECCO bleiben vorsichtig und schlagen vor, die Verschreibung von NSAR von Fall zu Fall zu bewerten (7).
Primär sklerosierende Cholangitis (PSC)
Die PSC ist eine chronische (meist progrediente) cholestatische Erkrankung unklarer Ätiologie, die eine diffuse Entzündung, Fibrosierung und Stenosierung der intra- und extrahepatischen Gallenwegen bewirkt. Die Erkrankung führt zu einem wesentlich erhöhten Risko der Entwicklung einer (biliären) Leberzirrhose, eines Malignomes (s. unten) und zu erhöhter Mortalität (47). Die PSC kommt bei chronisch entzündlichen Darmerkrankungen (v.a. der CU) gehäuft vor (Prävalenz von PSC von 2-8% bei IBD – Patienten, dabei wesentlich häufiger bei CU- als bei Morbus Crohn Patienten) (7). Die PSC führt bei IBD Patienten zu einem stark erhöhten Risiko eines kolorektalen Karzinomes, um den Faktor 2.4, und erhöht auch die Gefahr für die Entwicklung eines Cholangiokarzinomes bis um den Faktor 400 in gewissen Studien (48).
Patienten mit einer chronisch entzündlichen Darmerkrankung und einer PSC müssen deshalb jährlich eine Kontroll-Koloskopie zur Suche nach Dysplasien erhalten.
Für den Hausarzt ist es wichtig zu wissen, dass bei IBD-Patienten mit chronisch erhöhten Cholestase-Parametern an eine PSC gedacht und diese mit MRCP (Magnetresonanz-Cholangiopankreatikographie) aktiv gesucht werden muss.
Empfehlungen an den Hausarzt bezüglich der Betreuung von Colitis ulcerosa Patienten
Patienten, die mit Biologika behandelt werden, sollten falls möglich, durch einen IBD erfahrenen Gastroenterologen betreut werden. Patienten mit leichten bis mittelschweren Formen der Colitis ulcerosa können sehr gut vom Hausarzt behandelt werden, v.a. wenn die Krankheit über einen längeren Zeitraum stabil geblieben ist. In diesem Fall ist es wichtig, regelmässige Calprotectin-Kontrollen (je nach klinischem Verlauf) alle 3 bis 6 Monate durchzuführen, um die Remission der Entzündung mit einem Calprotectin-Zielwert von <150 – 200µg/g zu bestätigen (6). Der Patient kann trotz klinischer Remission und subjektiver Beschwerdefreiheit eine Rest-
entzündungsaktivität haben, nach der mit dieser nicht-invasi-
ven Messung (Calprotectin Bestimmung im Stuhl) proaktiv gesucht werden sollte (10). Bei den klinischen Verlaufskontrollen wird empfohlen, mittels Blutentnahme Nebenwirkungen der IBD-Therapie zu suchen und auch eine Anämie und einen Vitaminmangel im Rahmen der entzündlichen Erkrankung auszuschliessen. Mittelfristig ist es wichtig, dass der Patient an einem Darmkrebs-Screening teilnimmt, welches ca. 6-8 Jahre nach der Erstdiagnose begonnen werden sollte und dann (je nach Risikofaktoren) alle 1 bis 5 Jahre durchgeführt wird (6). Abbildung 2 fasst die aktuellen Empfehlungen der ECCO zu diesem Thema zusammen.
Bei einem Krankheitsschub ist es wichtig, nach einem auslösenden Faktor zu suchen. In diesem Zusammenhang sollte eine infektiöse Ursache, insbesondere eine Infektion mit C. difficile, systematisch ausgeschlossen werden (6,10). Denn auch ohne Antibiotikatherapie sind Patienten mit IBD inhärent gefährdet, eine C. difficile-Kolitis zu entwickeln, und bei Durchfall sollte daran gedacht werden (49). Weitere häufige Ursachen für Krankheitsschübe sind z.B. das Absetzen der Basismedikation und das kürzliche Aufgeben des Rauchens bei der CU (10).
Bei einem nicht schweren Krankheits-Schub der CU, kann der behandelnde Hausarzt die Behandlung optimieren, indem er 5-ASA einführt/erhöht oder eine Steroid-Therapie beginnt. Wenn dies nicht ausreichen sollte, oder bei Hinweisen auf eine schwere Entzündung der CU ist anzuraten, rasch mit einem IBD-erfahrenen Gastroenterologen Kontakt aufzunehmen. Weiterhin sollte bei mehr als 2 (medikamentös) kontrollierbaren Krankheitsschüben der UC pro Jahr eine Evaluation einer immunsuppressiven Basistherapie durch einen IBD-Spezialisten erfolgen (50).
Assistenzärztin Gastroenterologie
Intesto, Gastroenterologische Praxis und Crohn-Colitis-Zentrum
Bern und Freiburg
Bremgartenstrasse 119
3012 Bern
RossierL@intesto.ch
FMH Gastroenterologie & Innere Medizin
Mitinhaber Intesto, Gastroenterologische Praxis und Crohn-Colitis
Zentrum, Bern und Freiburg
Bremgartenstrasse 119
3012 Bern
MatterC@intesto.ch
Laura Rossier hat keine Interessenkonflikte. Christoph Matter hat Beraterhonorare, Vortragshonorare oder Kongress-Support von AbbVie, Dr Falk, Janssen, Pfizer, Sandoz, Takeda, Vifor erhalten.
- Die Diagnose der Colitis Ulcerosa wird aufgrund der Klinik, dem endoskopischen Befund und dem histologischen Resultat gestellt.
- Ein Krankheits-Schub der Colitis ulcerosa kann am besten mithilfe der Klinik und nicht invasiven Hilfsmitteln wie dem Calprotectin im Stuhl und der Darmsonographie detektiert werden. Lassen Sie sich nicht von einem normalen CRP täuschen. Zudem ist es wichtig eine infektiös bedingte Colitis auszuschliessen.
- Bei einem schweren Krankheits – Schub der CU, wie z.B. bei Erfüllung der True-Love-Witts-Kriterien, sollte rasch zur Therapie-Einleitung mit einem IBD-erfahrenen Gastroenterologen Kontakt aufgenommen werden.
- 5-ASA-Präparate bleiben bei leichten bis mittelschweren Formen der Colitis ulcerosa die Therapie der ersten Wahl. Hier sollte unbedingt auch die lokale Therapie (Suppositorien, Einläufe und Schäume) berücksichtigt werden.
- Biologika können häufig auch schwere und komplexe Verlaufsformen der Colitis ulcerosa in Remission bringen und in Remission halten. Zudem können gewisse Biologika auch bei extraintestinalen Manifestationen der Colitis ulcerosa therapeutisch helfen.
- Koloskopien in regelmässigem Intervall (s. Abb. 2) sind bei Colitis ulcerosa Patienten für die Früherkennung von Dysplasien und Verhinderung von kolorektalen Malignomen von entscheidender Bedeutung.
1. de Souza HSP, Fiocchi C. Immunopathogenesis of IBD: current state of the art. Nat Rev Gastroenterol Hepatol 2016;13:13–27. https://doi.org/10.1038/nrgastro.2015.186.
2. Zhao M, Gönczi L, Lakatos PL, Burisch J. The Burden of Inflammatory Bowel Disease in Europe in 2020. J Crohns Colitis 2021;15:1573–87. https://doi.org/10.1093/ecco-jcc/jjab029.
3. Piovani D, Danese S, Peyrin-Biroulet L, Nikolopoulos GK, Lytras T, Bonovas S. Environmental Risk Factors for Inflammatory Bowel Diseases: An Umbrella Review of Meta-analyses. Gastroenterology 2019;157:647-659.e4. https:// doi.org/10.1053/j.gastro.2019.04.016.
4. Gajendran M, Loganathan P, Jimenez G, Catinella AP, Ng N, Umapathy C, et al. A comprehensive review and update on ulcerative colitis,. Dis Mon 2019; 65:100851. https://doi.org/10.1016/j.disamonth.2019.02.004.
5. Magro F, Langner C, Driessen A, Ensari A, Geboes K, Mantzaris GJ, et al. European consensus on the histopathology of inflammatory bowel disease. J Crohns Colitis 2013;7:827–51. https://doi.org/10.1016/j.crohns.2013.06.001.
6. Maaser C, Sturm A, Vavricka SR, Kucharzik T, Fiorino G, Annese V, et al. ECCO-ESGAR Guideline for Diagnostic Assessment in IBD Part 1: Initial diagnosis, monitoring of known IBD, detection of complications. J Crohns Colitis 2019;13:144-164K. https://doi.org/10.1093/ecco-jcc/jjy113.
7. Gordon H, Burisch J, Ellul P, Karmiris K, Katsanos K, Allocca M, et al. ECCO Guidelines on Extraintestinal Manifestations in Inflammatory Bowel Disease. J Crohns Colitis 2023:jjad108. https://doi.org/10.1093/ecco-jcc/jjad108.
8. Magro F, Gionchetti P, Eliakim R, Ardizzone S, Armuzzi A, Barreiro-de Acosta M, et al. Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 1: Definitions, Diagnosis, Extra-intestinal Manifestations, Pregnancy, Cancer Surveillance, Surgery, and Ileo-anal Pouch Disorders. J Crohns Colitis 2017;11:649–70. https://doi.org/ 10.1093/ecco-jcc/jjx008.
9. Harbord M, Eliakim R, Bettenworth D, Karmiris K, Katsanos K, Kopylov U, et al. Third European Evidence-based Consensus on Diagnosis and Management of Ulcerative Colitis. Part 2: Current Management. J Crohns Colitis 2017;11: 769–84. https://doi.org/10.1093/ecco-jcc/jjx009.
10. Rubin DT, Ananthakrishnan AN, Siegel CA, Sauer BG, Long MD. ACG Clinical Guideline: Ulcerative Colitis in Adults. Am J Gastroenterol 2019;114:384–413. https://doi.org/10.14309/ajg.0000000000000152.
11. Lutgens MWMD, van Oijen MGH, van der Heijden GJMG, Vleggaar FP, Siersema PD, Oldenburg B. Declining risk of colorectal cancer in inflammatory bowel disease: an updated meta-analysis of population-based cohort studies. Inflamm Bowel Dis 2013;19:789–99. https://doi.org/10.1097/MIB. 0b013e31828029c0.
12. Eaden JA, Abrams KR, Mayberry JF. The risk of colorectal cancer in ulcerative colitis: a meta-analysis. Gut 2001;48:526–35. https://doi.org/10.1136/gut.48.4.526.
13. Bewtra M, Kaiser LM, TenHave T, Lewis JD. Crohn’s disease and ulcerative colitis are associated with elevated standardized mortality ratios: a meta-analysis. Inflamm Bowel Dis 2013;19:599–613. https://doi.org/10.1097/MIB.0b013e31827f27ae.
14. Turner D, Ricciuto A, Lewis A, D’Amico F, Dhaliwal J, Griffiths AM, et al. STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology 2021;160:1570–83. https://doi.org/10.1053/j.gastro.2020.12.031.
15. Mayberry J. The history of 5-ASA compounds and their use in ulcerative colitis–trailblazing discoveries in gastroenterology. J Gastrointest Liver Dis JGLD 2013;22:375–7.
16. Veloso PM, Machado R, Nobre C. Mesalazine and inflammatory bowel disease – From well-established therapies to progress beyond the state of the art. Eur J Pharm Biopharm Off J Arbeitsgemeinschaft Pharm Verfahrenstechnik EV 2021;167:89–103. https://doi.org/10.1016/j.ejpb.2021.07.014.
17. Raine T, Bonovas S, Burisch J, Kucharzik T, Adamina M, Annese V, et al. ECCO Guidelines on Therapeutics in Ulcerative Colitis: Medical Treatment. J Crohns Colitis 2022;16:2–17. https://doi.org/10.1093/ecco-jcc/jjab178.
18. Schroeder KW, Tremaine WJ, Ilstrup DM. Coated Oral 5-Aminosalicylic Acid Therapy for Mildly to Moderately Active Ulcerative Colitis. N Engl J Med 1987;317:1625–9. https://doi.org/10.1056/NEJM198712243172603.
19. Murray A, Nguyen TM, Parker CE, Feagan BG, MacDonald JK. Oral 5-aminosalicylic acid for induction of remissi on in ulcerative colitis. Cochrane Database Syst Rev 2020;8:CD000543. https://doi.org/10.1002/14651858.CD00 0543.pub5.
20. Bernick SJ, Kane S. Optimizing use of 5-ASA in the treatment of ulcerative colitis: Focus on patient compliance and adherence. Patient Relat Outcome Meas 2010;1:57–63. https://doi.org/10.21 47/prom.s8382.
21. Di Paolo MC, Paoluzi OA, Pica R, Iacopini F, Crispino P, Rivera M, et al. Sulphasalazine and 5-aminosalicylic acid in long-term treatment of ulcerative colitis: report on tolerance and side-effects. Dig Liver Dis 2001;33:563–9. https://doi.org/10.1016/S1590-8658(01)80108-0.
22. Sehgal P, Colombel J-F, Aboubakr A, Narula N. Systematic review: safety of mesalazine in ulcerative colitis. Aliment Pharmacol Ther 2018;47:1597–609. https://doi.org/10.1111/apt.14688.
23. Blackwell J, Selinger C, Raine T, Parkes G, Smith MA, Pollok R. Steroid use and misuse: a key performance indicator in the management of IBD. Frontline Gastroenterol 2020;12:207–13. https://doi.org/10.1136/flgastro-2019-101288.
24. Rice JB, White AG, Scarpati LM, Wan G, Nelson WW. Long-term Systemic Corticosteroid Exposure: A Systematic Literature Review. Clin Ther 2017; 39:2216–29. https://doi.org/10.1016/j.clinthera.2017.09.011.
25. Mallick B, Malik S. Use of Azathioprine in Ulcerative Colitis: A Comprehensive Review. Cureus n.d.;14:e24874. https://doi.org/10.7759/cureus.24874.
26. Chaparro M, Ordás I, Cabré E, Garcia-Sanchez V, Bastida G, Peñalva M, et al. Safety of thiopurine therapy in inflammatory bowel disease: long-term follow-up study of 3931 patients. Inflamm Bowel Dis 2013;19:1404–10. https://doi.org/10.1097/MIB.0b013e318281f28f.
27. Beaugerie L. Lymphoma: The Bête Noire of the Long-term Use of Thiopurines in Adult and Elderly Patients With Inflammatory Bowel Disease. Gastroenterology 2013;145:927–30. https://doi.org/10.1053/j.gastro.2013.09.035.
28. Peyrin–Biroulet L, Khosrotehrani K, Carrat F, Bouvier A-M, Chevaux J-B, Simon T, et al. Increased Risk for Nonmelanoma Skin Cancers in Patients Who Receive Thiopurines for Inflammatory Bowel Disease. Gastroenterology 2011;141:1621-1628.e5. https://doi.org/10.1053/j.gastro.2011.06.050.
29. Sousa P, Ministro P, Armuzzi A, Dignass A, Høivik ML, Barreiro-de Acosta M, et al. Thiopurines: Use them or lose them? International survey on current and future use of thiopurines in inflammatory bowel disease. Dig Liver Dis 2021;53:1571–9. https://doi.org/10.1016/j.dld.2021.05.038.
30. Billmeier U, Dieterich W, Neurath MF, Atreya R. Molecular mechanism of action of anti-tumor necrosis factor antibodies in inflammatory bowel diseases. World J Gastroenterol 2016;22:9300–13. https://doi.org/10.3748/wjg.v22.i42.9300.
31. Colombel JF, Sandborn WJ, Reinisch W, Mantzaris GJ, Kornbluth A, Rachmilewitz D, et al. Infliximab, azathioprine, or combination therapy for Crohn’s disease. N Engl J Med 2010;362:1383–95. https://doi.org/10.1056/NEJMoa0904492.
32. Fousekis FS, Papamichael K, Kourtis G, Albani EN, Orfanidou A, Saridi M, et al. The efficacy of immunomodulators in the prevention and suppression of anti-drug antibodies to anti-tumor necrosis factor therapy in inflammatory bowel disease. Ann Gastroenterol 2022;35:1–7. https://doi.org/10.20524/aog.2021.0682.
33. Wyant T, Fedyk E, Abhyankar B. An Overview of the Mechanism of Action of the Monoclonal Antibody Vedolizumab. J Crohns Colitis 2016;10:1437–44. https://doi.org/10.1093/ecco-jcc/jjw092.
34. Sands BE, Sandborn WJ, Panaccione R, O’Brien CD, Zhang H, Johanns J, et al. Ustekinumab as Induction and Maintenance Therapy for Ulcerative Colitis. N Engl J Med 2019;381:1201–14. https://doi.org/10.1056/NEJMoa1900750.
35. Ytterberg SR, Bhatt DL, Mikuls TR, Koch GG, Fleischmann R, Rivas JL, et al. CardiovASUClar and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med 2022;386:316–26. https://doi.org/10.1056/NEJMoa2109927.
36. Sandborn WJ, Feagan BG, D’Haens G, Wolf DC, Jovanovic I, Hanauer SB, et al. Ozanimod as Induction and Maintenance Therapy for Ulcerative Colitis. N Engl J Med 2021;385:1280–91. https://doi.org/10.1056/NEJMoa2033617.
37. Guo XY, Liu XJ, Hao JY. Gut microbiota in ulcerative colitis: insights on pathogenesis and treatment. J Dig Dis 2020;21:147–59. https://doi.org/ 10.1111/1751-2980.12849.
38. Kruis W, Fric P, Pokrotnieks J, Lukás M, Fixa B, Kascák M, et al. Maintaining remission of ulcerative colitis with the probiotic Escherichia coli Nissle 1917 is as effective as with standard mesalazine. Gut 2004;53:1617–23. https://doi.org/10.1136/gut.2003.037747.
39. Rossier L, Matter C, Burri E, Galperine T, Hrúz P, Juillerat P, et al. Swiss expert opinion: current approaches in faecal microbiota transplantation in daily practice. Swiss Med Wkly 2023;153:40100. https://doi.org/10.57187/smw. 2023.40100.
40. Bauer N, Kairey L, Schlee C, Uecker C, Öznur Ö, Langhors t J. Use of complementary and alternative medicine (CAM) in patients with inflammatory bowel disease (IBD): results from a German nationwide survey of 2019 compared to a previous survey of 2002. Scand J Gastroenterol 2022;57:1209–15. https://doi.org/10.1080/00365521.2022.2078667.
41. Chandan S, Mohan BP, Chandan OC, Ahmad R, Challa A, Tummala H, et al. Curcumin use in ulcerative colitis: is it ready for prime time? A systematic review and meta-analysis of clinical trials. Ann Gastroenterol 2020;33:53–8. https://doi.org/10.20524/aog.2019.0439.
42. Diagnostik und Therapie der Colitis ulcerosa. DGVS – Dtsch Ges Für Gastroenterol Verdau- Stoffwechselkrankheiten n.d. https://www.dgvs.de/wissen/leitlinien/leitlinien-dgvs/colitis-ulcerosa/ (accessed June 11, 2023).
43. Ananthakrishnan AN, Kaplan GG, Bernstein CN, Burke KE, Lochhead PJ, Sasson AN, et al. Lifestyle, behaviour, and environmental modification for the management of patients with inflammatory bowel diseases: an International Organization for Study of Inflammatory Bowel Diseases consensus. Lancet Gastroenterol Hepatol 2022;7:666–78. https://doi.org/10.1016/S2468-1253(22)00021-8.
44. Kim B, Chae J, Kim EH, Yang HI, Cheon JH, Kim TI, et al. Physical activity and quality of life of patients with inflammatory bowel disease. Medicine (Baltimore) 2021;100:e26290. https://doi.org/10.1097/MD.0000000000026290.
45. Spinelli A, Bonovas S, Burisch J, Kucharzik T, Adamina M, Annese V, et al. ECCO Guidelines on Therapeutics in Ulcerative Colitis: Surgical Treatment. J Crohns Colitis 2022;16:179–89. https://doi.org/10.1093/ecco-jcc/jjab177.
46. Moninuola OO, Milligan W, Lochhead P, Khalili H. Systematic review with meta-analysis: association between acetaminophen and nonsteroidal anti-inflammatory drugs (NSAIDs) and risk of Crohn’s disease and ulcerative colitis exacerbation. Aliment Pharmacol Ther 2018;47:1428–39. https://doi.org/10.1111/apt.14606.
47. Silveira MG, Lindor KD. Primary sclerosing cholangitis. Can J Gastroenterol J Can Gastroenterol 2008;22:689–98. https://doi.org/10.1155/2008/824168.
48. Trivedi PJ, Crothers H, Mytton J, Bosch S, Iqbal T, Ferguson J, et al. Effects of Primary Sclerosing Cholangitis on Risks of Cancer and Death in People With Inflammatory Bowel Disease, Based on Sex, Race, and Age. Gastroenterology 2020;159:915–28. https://doi.org/10.1053/j.gastro.2020.05.049.
49. Berg AM, Kelly CP, Farraye FA. Clostridium difficile Infection in the Inflammatory Bowel Disease Patient. Inflamm Bowel Dis 2013;19:194–204. https://doi.org/10.1002/ibd.22964.
50. Matter C, Seibold F. State of the Art – Leitlinien, moderne Behandlung. HAUSARZT Prax 2019 CME – Fortibuldung n.d.;14.
Therapeutische Umschau
- Vol. 80
- Ausgabe 9
- Dezember 2023