- Chronisch entzündliche Darmerkrankungen bei älteren Personen
Chronische entzündliche Darmerkrankungen werden zunehmend auch im höheren Alter (> 60 Jahre) diagnostiziert. Die Klinik unterscheidet sich dabei häufig von den Symptomen jüngerer Patienten, der Krankheitsverlauf ist dabei oft milder und ein extraintestinaler Befall kommt seltener vor. Die Therapiemöglichkeiten und -indikationen entsprechen derjenigen, die bei jüngeren Patienten angewendet werden. Aufgrund potenzieller Nebenwirkungen und Arzneimittelinteraktionen müssen bei der Auswahl des Medikamentes die Begleiterkrankungen und Ko-medikation der Patienten beachtet werden und bezüglich Risiko-Nutzen für den einzelnen Betroffenen gut abgewogen werden. Bei schwierigen therapierefraktären Verläufen stellen chirurgische Interventionen auch bei älteren Patienten ein probate Therapieoption dar. Generelle Massnahmen wie eine gesunde, ausgewogene Ernährung, Impfungen, Prävention vor Infektionen und Krebsvorsorgeuntersuchungen (Hautkrebs oder Dickdarmkrebs) sind bei dieser, vulnerablen, Patientenpopulation besonders wichtig.
Epidemiologie
Die Prävalenz und Inzidenz von chronisch entzündlichen Darmerkrankungen (CED) mit den beiden Hauptentitäten Morbus Crohn (MC) und Colitis ulcerosa (CU) nehmen in der westlichen Welt zu [1]. Die Erstmanifestation einer CED wird sehr häufig zwischen dem 20. und 40. Lebensjahr beobachtet. Ein weiterer Krankheitspeak besteht zwischen der sechsten bis achten Lebensdekade [2]. Auch bei älteren Personen (> 60 Jahre) wird eine steigende Inzidenz beobachtet. Ein erhöhtes Bewusstsein über die CED bei Patienten und Ärzten sowie verbesserte diagnostische Modalitäten sind Faktoren, welche wahrscheinlich zu einer Zunahme der Diagnosen führen. Schätzungen nach sind ca. 3 – 17 / 100,000 Personen > 60 Jahre von einer CU betroffen und in etwa 3 – 6 / 100,000 von einem MC [3]. Im Vergleich zur jüngeren Population, wo beide Krankheitsbilder in etwa gleich häufig vorkommen, scheinen ältere Personen häufiger von einer CU betroffen zu sein.
Die Pathogenese zur Entstehung einer CED ist komplex, vielschichtig und nach wie vor nicht vollständig verstanden. Eine genetische Prädisposition wird sowohl bei MC als auch der CU postuliert [4]. Als zusätzliche auslösende Krankheitsfaktoren werden nebst dem Nikotinabusus, , Umweltfaktoren wie Infekte im Kindesalter, Luftverschmutzung, Diäten (vermehrter Verzehr von rotem Fleisch, fettreicheichen und zuckerhaltigen Speisen), der Gebrauch von NSAR sowie eine primäre oder sekundäre Veränderung der Zusammensetzung des Mikrobioms genannt [5]. Weshalb es bei gewissen Patienten erst zu einem Krankheitsausbruch im höheren Lebensalter kommt, ist zurzeit unklar.
Klinische Präsentation und Diagnostik
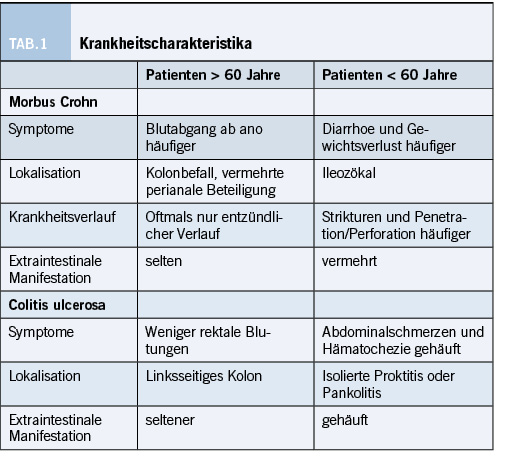
Der Krankheitsphänotyp mit entsprechender Klinik, sowie der Krankheitsverlauf ist bei jedem Patienten individuell und dabei abhängig vom Ausmass und Lokalisation der entzündlichen Aktivität im Gastrointestinaltrakt respektive vom extraintestinalen Befall. Die Einteilung des Befalls im Gastrointestinaltrakt erfolgt sowohl bei MC als auch der CU nach der Montréal-Klassifikation. Während die klassische und häufigste Lokalisation bei jüngeren Personen mit einem MC die Ileozoekalregion darstellt, findet sich bei älteren Personen häufiger ein solitärer Befall des Kolons und/oder ein isolierter perianaler Befall in Form von Fisteln. Folglich kommt es bei diesen Patienten mit MC u.a. häufiger zu Symptomen mit rektalem Blutabgang. Jüngere Patienten weisen oftmals auch einen aggressiveren Krankheitsverlauf mit Strikturen und Penetration der entzündlichen Läsionen auf im Vergleich zu Personen mit einem «late onset» MC [6].
Personen > 60 Jahre mit einer CU weisen bei der Erstmanifestation häufig einen Befall des linken Kolons (Proktosigmoiditis, linksseitige Kolitis), etwas seltener auch eine Pankolitis auf. Eine isolierte Proktitis kommt bei dieser Patientengruppe seltener vor und ein Progress der Erkrankung in eine Pankolitis wird weniger beobachtet [6].
Die Unterschiede bezüglich der Lokalisation und der Klinik zwischen älteren und jüngeren Personen mit CED sind in der Tabelle 1 nochmals dargestellt. Auch ein extraintestinaler Befall in dieser Patientengruppe kommt deutlich seltener vor [7], wobei es dazu nur eingeschränkte Erkenntnisse aus der Literatur gibt, da systematisch weniger Studien bei älteren Personengruppen durchgeführt wurden.
Häufig sind die Symptome bei älteren Personen subtiler und weniger stark ausgeprägt als bei jüngeren Personen, weshalb es nicht selten zu einer gewissen Latenz kommt bis zur Diagnosestellung einer CED. In einer Studie von Katz et. al. [8] wird ein Delay bei der Diagnosestellung bei Personen > 60 Jahren mit bis zu sechs Jahren beschrieben, bei der jüngeren Population betrug die mittlere Dauer zur Diagnosestellung zwei Jahre in der genannten Studie.
Die Diagnose eines MC oder einer CU kann wie auch bei jüngeren Patienten nur in Zusammenschau der klinischen, biochemischen (Entzündungswerte, Calprotectin) endoskopischen, histologischen und ggf. radiologischen Befunde gestellt werden. Bei älteren Personen sollten bei den Differenzialdiagnosen, insbesondere die malignen Erkrankungen speziell beachtet werden. Zu den weiteren, im Vergleich zu jüngeren Patienten zunehmenden möglichen Differenzialdiagnosen bei dieser Patientengruppe gehören u.a. eine Divertikulitis, ischämische Kolitis, Strahlenkolitis respektive eine infektiöse Genese oder auch eine medikamentös induzierte (NSAR, onkologische Immuntherapien) Kolitis.
Therapie
Ziel einer jeden immunsupprimierenden Therapie ist primär die klinische Remission, d.h. die Beschwerdefreiheit für den Patienten. Gemäss verschiedenen Guidelines (ECCO, ASGE, DGVS) ist zudem eine biochemische (CRP, Calprotectin) sowie endoskopisch-histologische Remission erstrebenswert, mit dem klaren Ziel, der Verhinderung von Komplikationen wie Fisteln, Abszesse, Perforationen und natürlich auch Malignome.
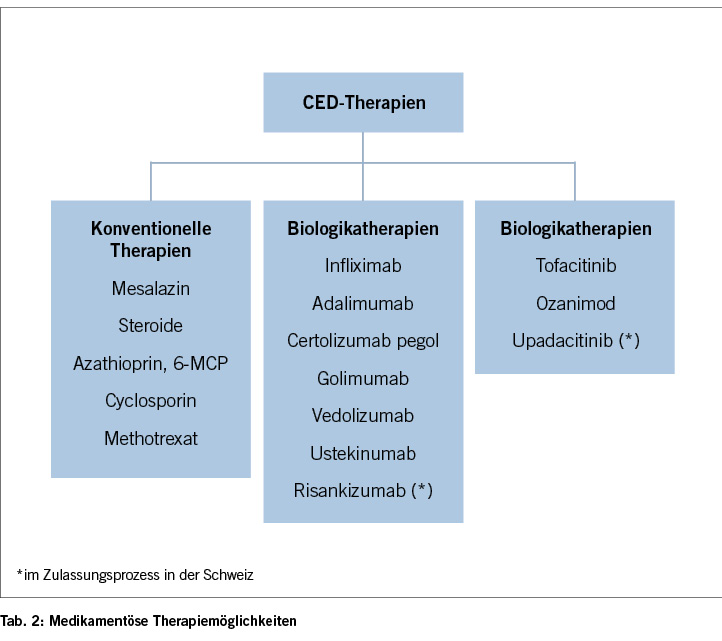
Dank intensiver Forschung auf dem Gebiet der chronisch entzündlichen Krankheiten stehen den Patienten mit CED immer mehr medikamentöse Therapien mit unterschiedlichen Wirkungsmechanismen zur Verfügung. Nebst den konventionellen Medikamenten wie Steroide, 5-ASA-Präparate oder auch Azathioprin sind in den letzten 20 Jahren biologische und niedermolekulare Wirkstoffe (engl.: small molecules) welche spezifische Entzündungsprozesse regulieren können, zur Behandlung einer CED entwickelt worden. Nebst Biologika stehen mittlerweile auch kostengünstigere Nachahmerprodukte (Biosimilars) als monoklonale Antikörper zur Verfügung. Es handelt sich hierbei um biotechnologisch aus humanen oder tierischen Organismen hergestellte Proteine. Im Gegensatz hierzu weisen die neu für die Therapie der CED zur Verfügung stehenden niedermolekularen Wirkstoffe im Vergleich zu den Biologika eine deutlich geringere Molekülmasse auf und werden in Tablettenform eingenommen.
Eine der Herausforderungen in der Behandlung von älteren CED-Patienten im klinischen Alltag ist die Übertragbarkeit der Studienresultate auf ältere Personen, da diese, sowie auch polymorbide Patienten sehr häufig von den Zulassungsstudien der Medikamente ausgeschlossen wurden. Die Wirksamkeit der verschiedenen Biologika und Small Molecules wurde in Zulassungsstudien jeweils gegenüber einer Placebotherapie gemessen. Grundsätzlich kann man ein partielles Ansprechen auf eine Therapie in bis zu 60 % und eine klinische Remission in bis zu 35 % der Patienten erwarten. Jedoch sind Head-to-Head Studien mit direktem Vergleich der Wirksamkeit von zwei verschiedenen biologischen Therapien in der Literatur bisher unterrepräsentiert, was eine Vergleichbarkeit erschwert [9/10]. Die Wahl der Therapie hängt also von verschiedenen Faktoren ab wie der Krankheitsausdehnung und des Schweregrades der entzündlichen Aktivität, den Patientenwünschen, den Arzneimittelnebenwirkungen sowie den Komorbiditäten und der Ko-medikation. Die drei letztgenannten Punkte müssen bei jeder Therapieauswahl für ältere Menschen mit CED berücksichtigt werden. Eine sorgfältige individuelle Therapieauswahl mit genauem Abwägen des Nutzen-Risiko-Profils einer jeden angedachten Therapie ist unerlässlich bei dieser vulnerablen Patientenpopulation. Eine schematische Darstellung der verfügbaren Therapieoptionen zur Behandlung eines MC oder CU ist in der Tabelle 2 aufgeführt.
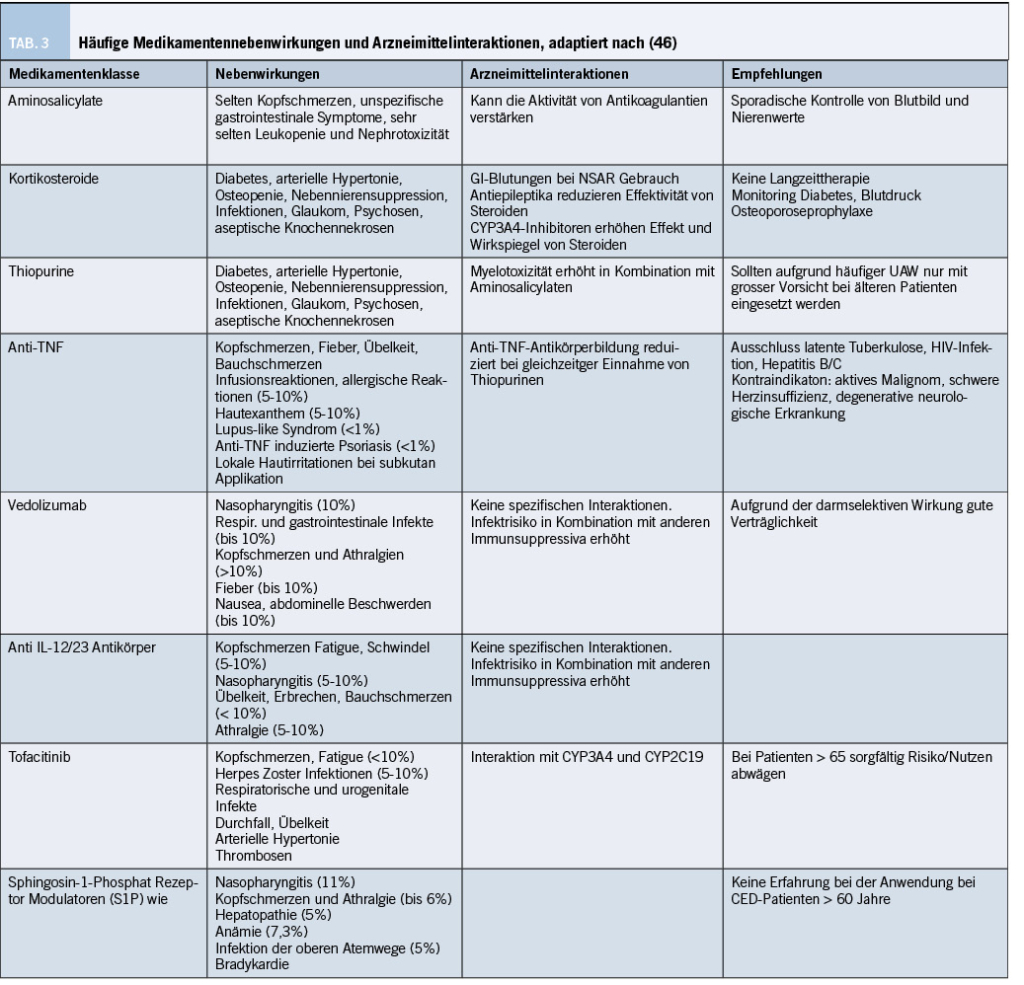
Im kommenden Abschnitt werden die aktuell verfügbaren Therapiemöglichkeiten in der Schweiz zur Behandlung einer CED erläutert, tabellarisch sind die Medikamente mit den möglichen Interaktionen und Nebenwirkung in der Grafik 3 zusammengefasst.
5-ASA Präparate
Aminosalycilate (topisch – Suppositorien, Klysmen, Schaum und/oder systemisch – Granulat/Tablette) sind nach wie vor empfohlen als Erstlinientherapie einer leichten bis mittelschweren CU aufgrund der guten Remissionserhaltung [11-12]. Der genaue Wirkungsmechanismus des entzündungshemmenden Effektes im Dickdarm ist unbekannt. Die Mesalazintherapie spielt hingegen bei der MC-Therapie eine untergeordnete Rolle [13]. Aminosalicylate ist die am häufigsten verschriebene Therapie zur Behandlung einer CED bei älteren Personen, nicht zuletzt aufgrund der guten Verträglichkeit. Nebenwirkungen wie eine Hepatotoxizität oder interstitielle Nephritis sind sehr selten und unabhängig von der Dosis. Ein möglicher protektiver Effekt bzgl. kolorektalem Karzinom bei CU-Patienten wird diskutiert [11], so dass oftmals eine Basistherapie mit 5-ASA Produkten auch bei gutem Ansprechen auf eine andere Therapie beibehalten wird.
Kortikosteroide
Kortikosteroide sollen hauptsächlich im akuten Schub einer CED eingesetzt werden. Von einer Erhaltungstherapie mit Kortikosteroiden wird aufgrund der potenziellen langfristigen Arzneimittelnebenwirkungen wie eine Osteopenie/Osteoporose, ein Steroiddiabetes, Steroidpsychose, kardiovaskulären und metabolischen Nebenwirkung insbesondere bei älteren Patienten abgeraten. Unter Steroidtherapie kann es auch zu einer Verschlechterung vorbestehender Erkrankungen kommen, wie ein Diabetes mellitus oder ein Katarakt. Das Risiko für eine obere gastrointestinale Blutung steigt zudem an, insbesondere bei zusätzlicher Einnahme von NSAR. Bei dieser Patientenpopulation soll daher grosszügig eine Protonenpumpeninhibitorprophylaxe verschrieben werden, zusammen mit Calcium und Vitamin D zur Osteopenie/-porose Vorsorge.
Thiopurine
Azathioprin und 6-Mercaptopurin werden bei älteren Patienten im Vergleich zu jüngeren Patienten aufgrund häufiger, teils schwerwiegender Nebenwirkungen kaum mehr angewendet. Arzneimittelnebenwirkungen, wie Übelkeit, Erbrechen, grippale Symptome und Infektionen oder eine Pankreatitis treten auch bei älteren Patienten [14] auf und sind dosisabhängig, weshalb die genannte Therapie auch in Anbetracht des zusätzlich erhöhten Risikos für ein Lymphom oder nicht melanozytärer Hauttumore bei dieser Patientengruppe nicht oder nur mit grosser Vorsicht oder bei fehlenden anderen Therapieoptionen etabliert werden sollte.
Cyclosporin (Calcineurininhibitor)
ist eine weitere Therapieoption. Diese wird nur noch selten als Rescue-Therapie bei schweren Krankheitsschüben der CU bei jüngeren Patienten verabreicht und sollte bei älteren Personen aufgrund des hohen Nebenwirkungsprofils nach Möglichkeit nicht eingesetzt werden.
Methotrexat
ist ein strukturelles Analogon zur Folsäure mit immunsuppressiven und antineoplastischen Eigenschaften, wird nur selten zur Behandlung bei MC eingesetzt. In einer retrospektiven Kohorte zeigte Methotrexat eine ähnliche Wirksamkeit bei älteren Personen wie bei jüngeren Patienten [15]. Die Methotrexat-therapie hat bei der CU keinen Stellenwert. Bei einer Therapie mit Methotrexat muss immer eine zusätzliche Folsäuresubstitution erfolgen.
Biologika
TNF-Inhibitoren sind monoklonale Antikörper, die den Tumornekrosefaktor, ein wichtiges proinflammatorisches Zytokin in der Entzündungskaskade der CED, binden und neutralisieren. Die Gabe erfolgt je nach Präparat und Patientenwunsch intravenös oder mittels subkutaner Applikation. TNF-Inhibitoren finden sowohl bei der CU als auch beim MC als Remissionsinduktion respektive als Erhaltungstherapie ihre Verwendung, ebenso zeigt sich eine gute Wirkung bzgl. einzelner extraintestinaler Manifestationen sowie bei Fistelleiden. Eine schwere Herzinsuffizienz, ein Malignom in den vergangenen fünf Jahren sowie schwere, degenerative neurologische Erkrankungen wie die Multiple Sklerose sind Kontraindikationen für diese Medikamentenklasse. Eine jährliche dermatologische Kontrolle bei leicht erhöhtem Risiko für Hauttumoren wird ebenfalls empfohlen. In einer retrospektiven Observationsstudie [16] zeigte sich eine gleiche Wirksamkeit einer Anti-TNF Therapie bei älteren und jüngeren Patienten. Hingegen wird ein vermehrter Therapieabbruch aufgrund von Infektionen und Nebenwirkungen unter der Therapie bei Patienten > 60 Jahren beschrieben [17].
α4β7-Integrin-Antagonisten wie Vedolizumab blockieren selektiv das zelluläre Adhäsionsmolekül α4β7-Integrin auf den Lymphozyten und verhindern so deren Bindung zu MAdCAM-1 (Zelladhäsionsmolekül) und folglich Immigration der Lymphozyten in die Darmwand. MAdCAM-1 wird ausschliesslich auf Darmgewebe hochreguliert, weshalb sich die antiinflammatorische Wirkung Vedolizumab praktisch vollständig auf den Gastrointestinaltrakt beschränkt und es selten zu Nebenwirkungen kommt mit folglich in der Regel sehr guter Verträglichkeit. Vedolizumab kann sowohl bei CU als MC eingesetzt werden [18-19]. Nach einer Induktionsphase mit intravenöser Applikation kann wahlweise auch auf eine subkutane Applikation gewechselt werden. Da bei gewissen Patienten die Wirkung langsam einsetzen kann, sollte zur definitiven Beurteilung des Wirkungseintritts mindestens bis 3 Monate zugewartet werden. Die nebenwirkungsarmen Eigenschaften und gute Effektivität des Medikamentes war in einer italienischen Kohortenstudie bei älteren und jüngeren Patienten vergleichbar [20], weshalb Vedolizumab gerne bei älteren CED-Patienten bei entsprechender Indikation als Erstlinientherapie eingesetzt wird. Wie effizient Patienten mit extraintestinalen Manifestationen aufgrund der darmselektiven Wirkung behandelt werden können, ist gegenwärtig nicht gänzlich geklärt.
Interleukin (IL)12/23-Inhibitoren sind Antikörper, welche an die gemeinsame p40 Rezeptoruntereinheit der humanen Zytokine IL 12 und IL 23 binden, welche bei MC und CU in erhöhter Konzentration im Darm und in den Lymphknoten des GI-Traktes vorkommen. Durch die Hemmung dieser Interleukine wird eine Aktivierung der T-Helferzellen (Th1 und Th17) unterbunden, welche eine wichtige Rolle in der Entzündungskaskade bei CED spielen. Ustekinumab, das bislang einzig zugelassene Präparat in der Schweiz kann sowohl zur Behandlung eines MC und CU eingesetzt werden [21/22]. Weitere Medikamente aus dieser Klasse stehen kurz vor der Zulassung zur Therapie. Diese Medikamente binden an die p19 Untereinheit und sind somit in ihrer Wirkung spezifischer [23-25]. Erste Daten von Ustekinumab bei der Behandlung eines MC bei Personen > 60 Jahren zeigte ein vergleichbares Ansprechen auf die Therapie und eine gute Verträglichkeit wie bei jüngeren Patienten. Nebenbefundlich wurde ein leicht gehäuftes Auftreten von Neoplasien in der Gruppe der > 60 jährigen Personen bei jedoch prinzipiell sehr geringem de novo Malignomrisko beschrieben [26].
Januskinaseinhibitoren gehören in die Gruppe der niedermolekularen Wirkstoffe und werden in Tablettenform verabreicht. Sie blockieren einen spezifischen Prozess auf Zytokinrezeptoren, welche bei der Aktivierung von Lymphozyten eine wichtige Rolle spielt und so seine anti-entzündliche Wirkung entfaltet. Tofacitinib – ein JAK 1/JAK-3 Inhibitor – hat sich in der Behandlung von Patienten mit einer CU als wirksam erwiesen, die vorgängig auf eine biologische Therapie nicht angesprochen haben. Das Nebenwirkungsprofil von Tofacitinib, wie gehäufte Infektionen (v.a. Herpes Zoster Infektion), ein erhöhtes Risiko für thromboembolische Ereignisse ab dem 50. Lebensjahr oder bei zusätzlichen Risikofaktoren wie hormoneller Antikonzeption, bereits stattgehabten thromboembolischen Ereignissen oder einer Herzinsuffizienz, sowie auch ein leicht erhöhtes Karzinomrisiko (v.a. Lungentumore und Lymphome, nicht für melanozytäre Hauttumore) muss jedoch gut in einer Nutzen/Risiko Analyse vor allem bei älteren Patienten abgewogen werden [27]. Upadacitinib, ein im Zulassungsprozess stehender oraler, selektiver JAK-1 Inhibitor zeigte zur Behandlung einer CU oder MC erfreuliche Resultate zum Krankheitsansprechen sowie scheinbar etwas besserem Sicherheitsprofil [28]. Auch hier gilt es zu bemerken, dass die Zulassungsstudien für diesen selektiven JAK Inhibitor bei jüngeren Patientenpopulationen durchgeführt wurden.
Sphingosin-1-Phosphat Rezeptor Modulatoren (S1P) wie Ozanimod – ein weiterer niedermolekularer Wirkstoff, der in Tablettenform verabreicht wird – stellen eine erst kürzlich zugelassene Therapieoption bei moderater bis schwer aktiver CU dar [29]. Die S1P-Rezeptoren 1 bis 5 haben u.a. eine wichtige Funktion in der Differenzierung und Migration der Entzündungszellen wie Lymphozyten. Das ursprünglich zur Behandlung der Multiple Sklerose eingesetzte Medikament bindet mit hoher Affinität die S1P Rezeptoren 1 und 5 und vermindert so die Migration von Lymphozyten aus den Lymphknoten. Die Nebenwirkungen sind in der Tabelle 3 dargestellt, Daten über Anwendung des Medikamentes bei älteren Personen stehen zurzeit keine zur Verfügung.
Operation
Die Indikation für eine operative Therapie ist bei jüngeren und älteren Patienten identisch, d.h. bei therapierefraktären Verläufen oder komplizierenden Verläufen bei MC wie Strikturen, Fisteln oder Abszessen. Dank des meist milderen Krankheitsverlaufes ist eine intestinale Segmentresektion bei MC oder eine Kolektomie bei CU bei der älteren Patientenpopulation seltener [30]. Häufig ist die Spitalaufenthaltsdauer und die postoperative In-hospital Mortalitätsrate bei älteren Patienten jedoch erhöht [31]. Die postoperative Komplikations- und Mortalitätsrate konnte in den vergangenen Jahren gesenkt werden. Als Faktoren für einen begünstigenden postoperativen Verlauf werden u.a. ein erhöhtes Bewusstsein für eine ausgewogene Ernährung bei CED-Patienten mit konsekutiv gutem Ernährungszustand vor der Operation, eine frühe postoperative Mobilisation und dank vermehrter interdisziplinärer Besprechung zwischen Gastroenterologen und Viszeralchirurgen eine optimale Planung des Operationszeitpunktes [32] diskutiert.
Allgemeinmassnahmen und Prävention
Ernährung
Malnutrition ist ein häufiges Problem bei Patienten mit CED. Bis zu 14 % der Patienten mit MC und knapp 6 % mit CU sind mangelernährt. Eine verminderte Nahrungsaufnahme, Malabsorption, selbstauferlegte diätetische Einschränkungen der Patienten aufgrund von gastrointestinalen Symptomen bei Verzehr von unverträglichen Speisen, ein vermehrter Energieverbrauch aufgrund des katabolen, inflammatorischen Zustandes, sowie Inappetenz aufgrund Arzneimittelnebenwirkungen sind Faktoren, welche zu einer Malnutrition führen können. Das Risiko für Infektionen und weitere Krankheitskomplikationen ist bei mangelernährten Patienten erhöht [33]. Eine regelmässige Bestimmung des Nutrition Risk Scores inklusive Bestimmung des Körpergewichts ist bei den klinischen Kontrollen empfohlen, ebenso wie die mindestens jährliche Bestimmung von Vitamin B12, Folsäure, Eisen, Zink, Selen und Albumin. Nebst der ausgewogenen Ernährung ist eine regelmässige körperliche Aktivität, sowie v.a. bei MC ein Rauchstopp empfohlen.
Infektionen
Patienten mit CED haben ein erhöhtes Risiko für eine Cytomegalievirus assoziierte Kolitis, eine Clostridienkolitis, Herpes Zoster Infektion, Influenza und weitere Infektionen [34-36]. Das Infektionsrisiko für opportunistische Infektionen nimmt unter der immunsupprimierenden Therapie inklusive Biologika zu, insbesondere bei Patienten > 60 Jahren. Schwere opportunistische Infektionen sind glücklicherweise selten [37]. Bei schweren Infektionen soll die Biologikatherapie nach Möglichkeit pausiert werden bis zur Abheilung. Bei leichten Infektionen kann die CED-Therapie in der Regel fortgesetzt werden [38]. Vor Beginn einer immunmodulierenden Therapie soll eine Hepatitis B/C, sowie HIV und Tuberkulose ausgeschlossen werden, da diese Erkrankungen unter einer CED-Therapie, im Speziellen bei TNFα Blockern, reaktivieren können. Bei entsprechendem Nachweis einer latenten Tuberkulose-Infektion muss eine entsprechende Behandlung vor und während der Biologikagabe etabliert werden.
Impfung
Eine Überprüfung des landesspezifischen Impfstatus sollte spätestens vor Beginn einer immunsupprimierenden Therapie erfolgen, vorzugsweise bei der Erstdiagnose einer CED. Totimpfstoffe können problemlos auch unter immunsupprimierender verabreicht werden. Es ist zu beachten, dass die Impfantwort unter immunsupprimierender Therapie vermindert sein kann. Lebendimpfstoffe sind unter Immunsuppressivatherapie kontraindiziert. Nebst nationalen Vorgaben des Impfplanes soll eine jährliche Influenzaimpfung und die Pneumokokkenimpfung (Booster nach fünf Jahren nach Grundimmunisierung) verabreicht werden. Sollte eine Therapie speziell mit JAK Inhibitoren in Erwägung gezogen werden, ist eine Herpes Zoster Immunisierung mit Shingrix vor Beginn der Therapie indiziert.
Karzinomvorsorge
Patienten mit CED, insbesondere Patienten mit CU, haben ein erhöhtes Risiko zur Entwicklung eines kolorektalen Karzinoms im Vergleich zur Normalbevölkerung. Das Ausmass des Kolonbefalls sowie die entzündliche Aktivität, eine Primär Sklerosierende Cholangitis, die Krankheitsdauer sowie eine positive Familienanamnese für kolorektale Karzinome sind Risikofaktoren für die Entstehung eines Kolonkarzinoms [39]. Die krebsassoziierte Mortalitätsrate bei CED Patienten wird immer noch mit 10 -15 % beschrieben. Ein regelmässiges endoskopisches Tumorscreening ist daher unerlässlich. Eine erste Vorsorge-Kolonoskopie wird in der Regel spätestens acht Jahre nach Diagnosestellung empfohlen, der nächste Zeitpunkt einer Vorsorgeuntersuchung richtet sich dann nach den klinisch, endoskopisch-histologischen Befunden. Dank der zunehmenden Therapiemöglichkeiten sowie der intensivierten Screeningprogramme bei CED-Patienten, konnte die Tumorinzidenz und krebsassoziierte Mortalität bei CED Patienten gesenkt werden [40]. Einige Publikationen suggerieren, dass eine erste Vorsorgeuntersuchung bei Personen > 60 Jahren mit CED früher erfolgen soll, da das Alter selbst ein Risikofaktor für die Entstehung eines kolorektalen Karzinoms darstellt und einige Patienten bereits innerhalb von acht Jahren nach Diagnosestellung einer CED an einem Kolonkarzinom erkrankt sind [41]. Bei älteren CED-Patienten ist ein individuelles Vorsorgeprogramm anhand des Krankheitsschweregrades, den Komorbiditäten und der Lebenserwartung sinnvoll.
In einer französischen Kohortenstudie von 2016 wurde die Karzinomentwicklung bei CED Patienten > 60 Jahren beobachtet. Bei einem durchschnittlichen Follow-Up von sechs Jahren zeigte sich in dieser Population ein erhöhtes Risiko für die Entstehung von lympho- und myeloproliferativen Erkrankungen, unabhängig der Anwendung von immunmodulierenden Medikamenten [42]. Bei Frauen mit CED besteht gemäss einer weiteren Kohortenstudie ein erhöhtes Risiko für Cervixdysplasien/-karzinom, weshalb regelmässige gynäkologische Vorsorgeuntersuchungen nahegelegt werden [43].
Bei der Anwendung von Thiopurinen und anti-TNF besteht gemäss Literatur eine erhöhte Inzidenz von nicht-melanozytärem Hautkrebs. Bei Patienten unter der genannten Therapie soll eine jährliche dermatologische Kontrolle stattfinden [44/45]. Wie bereits bei der Beschreibung der Thiopurinen erwähnt, soll dieses Medikament aufgrund der möglichen Entstehung einer lymphoproliferativen Erkrankung bei älteren Personen nur mit grosser Vorsicht eingesetzt werden.
Nebst den oben erwähnten spezifischen Krebsrisiken bei CED-Patienten sollen die üblichen altersentsprechenden Tumorvorsorgeuntersuchungen, wie zum Beispiel Prostata- oder Mammakarzinom, gemäss den internationalen Richtlinien erfolgen.
Oberarzt Gastroenterologie/Hepatologie
Clarunis AG, Universitäres Bauchzentrum Basel
Gastroenterologie & Hepatologie
Postfach
4002 Basel
dominic.althaus@clarunis.ch
Der Autor hat keine Interessenkonflikte.
1. Ananthankrishnan AN. Changing Global Epidemiology of Inflammatory Bowel Diseases: Sustainin Health Care Delivery Into the 21st Century. Clin Gastroenterol Hepatol 2020 May;18(6):1252-1260.
2. Robertson DJ. Inflammatory bowel disease in the elderly. Gastroenterol, Clin North Am. 2001 Jun; 30(2): 409–26.
3. Jeuring SF. Epidemiology and Long-term Outcome of Inflammatory Bowel Disease Diagnosed at Elderly Age-An Increasing Distinct Entity? Inflamm Bowel Dis. 2016 Jun; 22(6): 1425–34.
4. Cleynen I. Inherited determinants of Crohn’s disease and ulcerative colitis phenotypes: a genetic association study, Lancet. 2016 Jan 9; 387(10014): 156–167.
5. Ananthakrishnan AM. Environmental triggers in IBD: a review of progress and evidence. Nat Rev Gastroenterol Hepatol2018 Jan;15(1):39-49.
6. Tran V. IBD in the Elderly: Management Challenges and Therapeutic Considerations, Curr Gastroenterol Rep 2019 Nov 27;21(11):60.
7. Stepaniuk P. Characterization of inflammatory bowel disease in elderly patients: A review of epidemiology, current practices and outcomes of current management strategies. Can J Gastroenterol Hepatol 2015 Aug-Sep;29(6): 327-33.
8. Katz S. Am J Gastroenterol 2011 Nov;106(11):1889-97.Inflammatory bowel disease of the elderly: frequently asked questions (FAQs)
9. Sands BE., Vedolizumab versus Adalimumab for Moderate-to-Severe Ulcerative Colitis N Engl J Med 2019; 381:1215-1226
10. Sands BE. Ustekinumab versus adalimumab for induction and maintenance therapy in biologic-naive patients with moderately to severely active Crohn’s disease: a multicentre, randomised, double-blind, parallel-group, phase 3b trial. Lancet. 2022 Jun 11;399(10342):2200-2211.
11. Sehgal P. Systematic review: safety of mesalazine in ulcerative colitis, Aliment Pharmacol Ther2018 Jun;47(12):1597-1609
12. Charpentier C. Natural history of elderly-onset inflammatory bowel disease: a population-based cohort study. Gut2014 Mar;63(3):423-32.
13. Torres J. ECCO Guidelines on Therapeutics in Crohn’s Disease: Medical Treatment. J Crohns Colitis. 2020 Jan 1;14(1):4-22.
14. Stournaras E., Thiopurine monotherapy is effective in ulcerative colitis but significantly less so in Crohn’s disease: long-term outcomes for 11 928 patients in the UK inflammatory bowel disease bioresource. Gut. 2021 Apr; 70(4): 677–686
15. Gonzalez-Lama Y. Methotrexate in inflammatory bowel disease: a multicenter retrospective study focused on long-term efficacy and safety. The Madrid experience. Eur J Gastroenterol Hepatol 2012 Sep;24(9):1086-91.
16. Lobaton T. Efficacy and safety of anti-TNF therapy in elderly patients with inflammatory bowel disease. Aliment Pharmacol Ther2015 Aug;42(4):441-51.
17. Desai A. Older age is associated with higher rate of discontinuation of anti-TNF therapy in patients with inflammatory bowel disease Inflamm Bowel Dis. 2013 Feb;19(2):309-15.
18. Feagan B. Vedolizumab as induction and maintenance therapy for ulcerative colitis, N Engl J Med 2013 Aug 22;369(8):699-710.
19. Sandborn WJ. Vedolizumab as induction and maintenance therapy for Crohn’s disease, N Engl J Med. 2013 Aug 22;369(8):711-21.
20. Pugliese D. Effectiveness and safety of vedolizumab in a matched cohort of elderly and nonelderly patients with inflammatory bowel disease: the IG-IBD LIVE study, Aliment Pharmacol Ther 2022 Jul;56(1):95-109.
21. Feagan B. Ustekinumab as Induction and Maintenance Therapy for Crohn’s Disease, N Engl J Med. 2016 Nov 17;375(20):1946-1960.
22. Sands BE. Ustekinumab as Induction and Maintenance Therapy for Ulcerative Colitis, N Engl J Med 2019 Sep 26;381(13):1201-121
23. Geert D’Haens. Risankizumab as induction therapy for Crohn’s disease: results from the phase 3 ADVANCE and MOTIVATE induction trials, Lance. 2022 May 28;399(10340):2015-2030
24. Sandborn WJ., Guselkumab for the Treatment of Crohn’s Disease: Induction Results From the Phase 2 GALAXI-1 Study, Gastroenterolog. 2022 May;162 (6):1650-1664.e8.
25. Sands BE. Efficacy and Safety of Mirikizumab in a Randomized Phase 2 Study of Patients With Crohn’s Disease. Gastroenterology. 2022 Feb;162 (2):495-508.
26. Casas-Deza D. Effectiveness and Safety of Ustekinumab in Elderly Patients with Crohn’s Disease: Real World Evidence From the ENEIDA Registry J Crohns Colitis. 2023 Jan 27;17(1):83-91.
27. Sandborn WJ. Tofacitinib as Induction and Maintenance Therapy for Ulcerative Colitis, N Engl J Med 2017 May 4;376(18):1723-1736.
28. Danese S. Upadacitinib as induction and maintenance therapy for moderately to severely active ulcerative colitis: results from three phase 3, multicentre, double-blind, randomised trials, Lancet 2022 Jun 4;399(10341): 2113-2128.
29. Sandborn WJ. Ozanimod as Induction and Maintenance Therapy for Ulcerative Colitis N Engl J Med 2021 Sep 30;385(14):1280-1291.
30. Ha Y C. Patients with late-adult-onset ulcerative colitis have better outcomes than those with early onset disease, Gastroenterol Hepatol 2010 Aug;8(8):682-687.e1.
30. Ananthakrishnan AN. Inflammatory bowel disease in the elderly is associated with worse outcomes: a national study of hospitalizations, Inflamm Bowel Dis2009 Feb;15(2):182-9.
32. Page MJ. Factors affecting surgical risk in elderly patients with inflammatory bowel disease, Gastrointest Surg . 2002 Jul-Aug;6(4):606-13.
33. Halmos EP. Dietary management of IBD-insights and advice Rev Gastroenterol Hepatol . 2015 Mar;12(3):133-46.
34. Epple HJ. Therapy- and non-therapy-dependent infectious complications in inflammatory bowel disease, Dig Dis. 2009;27(4):555-9.
35. Long MD. Increased risk of pneumonia among patients with inflammatory bowel disease, American J. Gastroenterol 2013 Feb;108(2):240-8.
36. Long MD. Increased risk of herpes zoster among 108 604 patients with inflammatory bowel disease, Aliment Pharmacol Ther. 2013 Feb;37(4):420-9.
37. Maneesh D. Opportunistic infections due to inflammatory bowel disease therapy, Bowel Dis 2014 Jan;20(1):196-212.
38. Click B. Managing Risks with Biologics, Curr Gastroenterol Rep. 2019
39. Dyson JK. Colorectal cancer in inflammatory bowel disease: what is the real magnitude of the risk? World J Gastroenterol. 2012 Aug 7;18(29):3839-48.
40. Clark WT. Colorectal cancer surveillance in inflammatory bowel disease: Practice guidelines and recent developments, World J Gastroenterol. 2019 Aug 14; 25(30): 4148–4157.
41. Baars JE. Age at diagnosis of inflammatory bowel disease influences early development of colorectal cancer in inflammatory bowel disease patients: a nationwide, long-term survey, J Gastroenterol 2012 Dec;47(12):1308-22.
42. Cheddani H. Cancer in Elderly Onset Inflammatory Bowel Disease: A Population-Based Study, Am J Gastroenterol. 2016 Oct;111(10):1428-1436
43. Rungoe C. Inflammatory bowel disease and cervical neoplasia: a population-based nationwide cohort study, Clin Gastroenterol Hepatol. 2015 Apr;13(4):693-700.e1.
44. Long MD. Increased risk for non-melanoma skin cancer in patients with inflammatory bowel disease, Clin Gastroenterol Hepatol. 2010 Mar;8(3):268-74.
45. McKenna MR. Melanoma and non-melanoma skin cancer in inflammatory bowel disease patients following tumor necrosis factor-α inhibitor monotherapy and in combination with thiopurines: analysis of the Food and Drug Administration Adverse Event Reporting System, J Gastrointestin Liver Dis. 2014 Sep;23(3):267-71
46. Hruz P. Management of the Elderly Inflammatory Bowel Disease Patient, Digestion. 2020;101 Suppl 1:105-119
Therapeutische Umschau
- Vol. 80
- Ausgabe 9
- Dezember 2023