- Oncogériatrie: une collaboration bicéphale entre oncologue et gériatre
L’oncogériatrie est une discipline en plein essor fondée sur l’incidence croissante des cancers avec l’âge et le vieillissement de la population. Afin d’adapter les soins oncologiques aux patients âgés, les prises de décision imposent un niveau d’expertise complémentaire entre oncologue et gériatre, sans oublier le regard du médecin de famille et l’avis du patient: le tout étant validé au tumor board. Les sociétés savantes ont approuvé le score G8 qui permet à l’oncologue de sélectionner quel patient nécessite le recours au gériatre et la classification de Balducci qui guide le gériatre dans son positionnement concernant le traitement oncologique. Le suivi conjoint est primordial pour réévaluer la cohérence du plan de soins. «Primum non nocere» reste le principe fondamental tout au long de la prise en charge: on privilégiera la qualité de vie du sujet âgé.
Decision-making requires a complementary level of expertise between oncologists and geriatricians, as well as the views of the family doctor and the patient: all validated on the tumorboard. Learned societies approved the G8 score, which enables the oncologist to select patients who need to be referred to the geriatrician, and the Balducci classification, which guides the geriatrician in his position regarding oncological treatment. Joint follow-up is essential to reassess the coherence of the care plan. “Primum non nocere” remains the fundamental principle throughout the treatment process: the elderly patient’s quality of life remains our priority.
Key Words: Oncogeriatrics, G8 scale Oncodage, Balducci’s classification, Elderly people and cancer
Le cancer: pathologie du sujet âgé?
Du point de vue épidémiologique, l’incidence des cancers augmente avec l’âge et 80% sont diagnostiqués après 70 ans, selon les données de l’OFS (1). En parallèle on assiste à un vieillissement de la population avec l’allongement de l’espérance de vie (2) et une hétérogénéité des profils de séniors (3) : c’est l’âge physiologique qui importe (4).
Dans ce contexte, le plan cancer Suisse se positionne pour une vision intégrative sans discrimination de l’âge, chaque individu ayant le droit au même accès au dépistage, diagnostic et traitement (5). Les patients âgés peuvent être autant demandeurs de traitements curatifs que les plus jeunes (6). Mais en pratique, les sujets âgés ont moins d’investigation, sont diagnostiqués à des stades plus évolués, ils sont sous-traités par rapport aux plus jeunes et participent moins aux essais cliniques (7).
Au niveau international, Balducci, un des pionniers de l’oncogériatrie (8) a déterminé un modèle de management des cancers des sujets âgés (9) validé par la Société Internationale d’OncoGériatrie. En parallèle, Extermann développe le process du Geriatric Assessment en oncologie (10) avec update d’évaluation (11): le tout promouvant l’inclusion des patients âgés dans les protocoles de recherche. En France, un maillage territorial par des unités de coordination et antennes en oncogériatrie permet aux patients âgés de bénéficier d’une prise en charge spécifique avec recours aux réunions de concertation pluriprofessionnelle oncogériatrique pour les cas les plus complexes (12). Un programme spécifique de réadaptation appelée Récupération Améliorée Après Chirurgie a été implémenté et l’intergroupe de recherche en oncogériatrie, DIALOG a été labellisé (12).
Apports de l’évaluation gériatrique en oncologie (EGO)
L’EGO vise à éviter les risques de sur- ou de sous-traitement liés aux décisions thérapeutiques basées exclusivement sur l’âge ou sur le seul jugement clinique du médecin (13).
En 2011, Caillet et al (14) ont montré qu’une EGO peut apporter des changements importants dans la prise en charge pour 21% des 375 patients de l’étude sous forme d’une intensification de traitements (10%) ou d’une réduction d’intensité de traitement (81%). Ceci suppose néanmoins pour 9% du collectif d’une augmentation du délai de 15 jours de prise en charge gériatrique avant le traitement oncologique. Concernant les réductions d’intensité, il s’agit dans 86% des cas d’un retrait d’une chimiothérapie au bénéfice des soins de support. Les facteurs gériatriques significatifs en lien avec ces changements concernent la diminution de l’autonomie fonctionnelle (-0,5 point ADL) et la dénutrition.
En 2022, la méta-analyse de Hamaker et al (15), recueillant les résultats de 61 études, a souligné que l’EGO intégrée à la prise de décision oncologique induit des changements de traitements (31%), une diminution des taux de toxicités (60%), une probabilité améliorée d’achèvement du traitement (65%), une amélioration fonctionnelle (100%) et de la qualité de vie du patient (30%) par mise en place d’un plan d’aides personnalisé (70%).
Collaboration bicéphale: l’évidence du binôme oncologue et gériatre
L’hétérogénéité de la population âgée s’ajoute à celle des cancers justifiant l’expertise conjointe de l’oncologue ou spécialiste d’organe gérant des patients cancéreux âgés et du gériatre. Tous les patients âgés ayant un cancer ne peuvent être vus par un gériatre formé à l’oncogériatrie alors le principe de base est de cibler la collaboration entre oncologues et gériatres. Les compétences de chacun permettant d’être plus efficients.
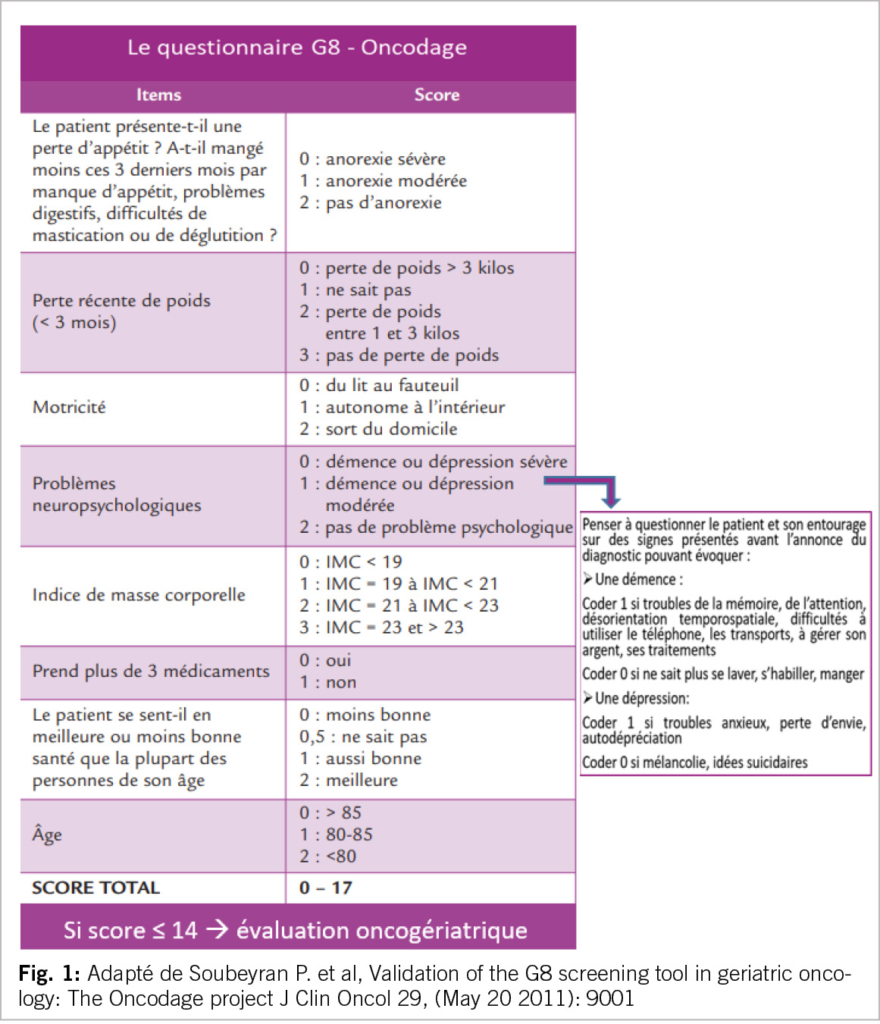
Rôle de l’oncologue et questionnaire G8
Le patient âgé est vu par l’oncologue qui évalue le type de cancer et son stade d’évolution. Il dispose d’un outil de screening Quand l’oncologue réfère le patient au gériatre, le questionnement du choix du traitement oncologique prioritaire et ses alternatives doit être clairement explicité pour cibler l’évaluation du gériatre et ses réponses.
Rôle du gériatre et classification de Balducci
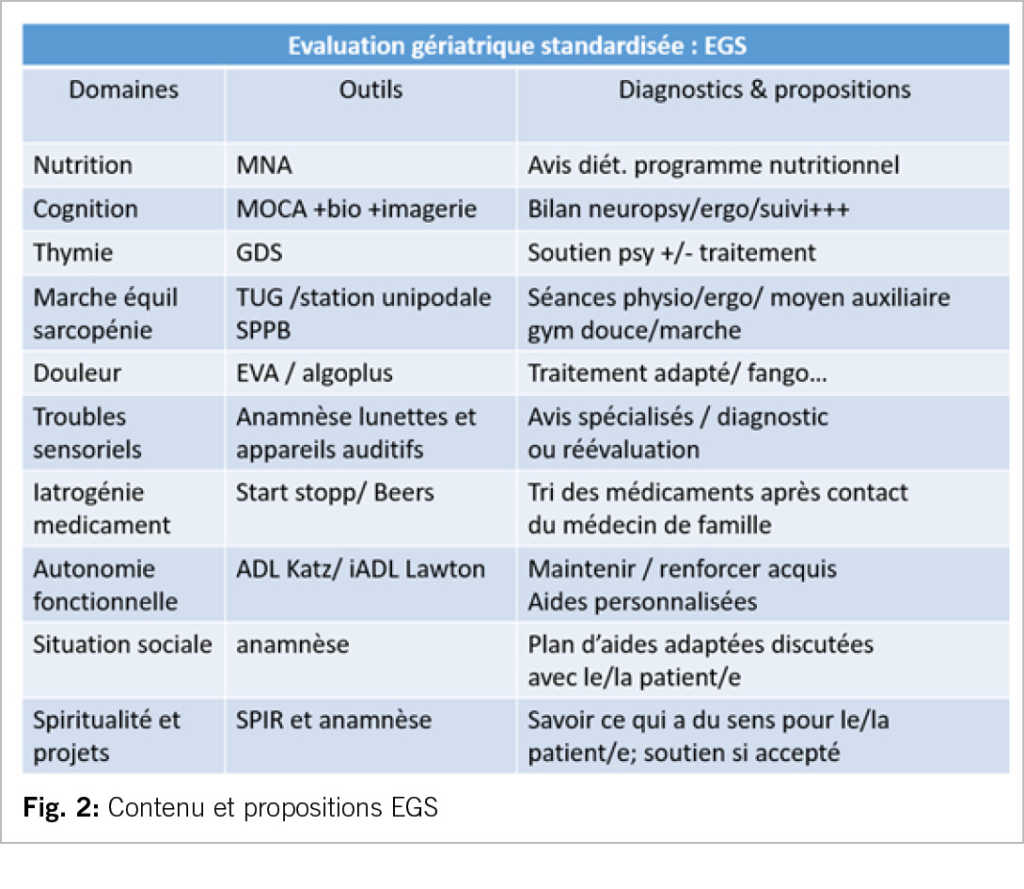
Le gériatre réalise une évaluation standardisée pour rechercher les syndromes gériatriques: dénutrition, trouble neurocognitif, dépression, troubles neuro sensoriels, chutes, polymédication par des tests validés pour déterminer l’autonomie fonctionnelle, décisionnelle, et le contexte de vie du patient. Une évaluation plus spécifique oncogériatrique détermine l’espérance de vie du patient selon tableaux OFS (2), les fragilités selon Fried (17) avec des tests d’expertise plus fine (vitesse de marche, force de préhension, asthénie, perte de poids, activité physique). La qualité de vie selon le patient est également définie avec une échelle d’autoévaluation numérique SF 36 (18) en précisant ce qui a du sens pour lui.
Le gériatre se focalise alors sur le risque en lien avec le traitement oncologique. L’échelle CIRS-G liste le niveau des comorbidités (19), sans oublier l’examen physique et la biologie en particulier la fonction rénale selon Cockroft, les posologies des médicaments étant basées sur ce calcul. Si l’option thérapeutique est une chimiothérapie, le score de CARG (20) ou CRASH (21) prédit le risque de survenue de toxicités de grade 3 à 5. Le risque chirurgical et péri-opératoire quant à lui, sera à évaluer au cas par cas en fonction du geste prévu et des éventuelles conséquences au décours, comme une colostomie définitive par exemple.
L’avis du patient et/ou de son référent thérapeutique par rapport au choix du traitement oncologique est capital : il faut clairement expliquer les effets secondaires et les bénéfices attendus. Le status réanimatoire sera discuté (fig 2).
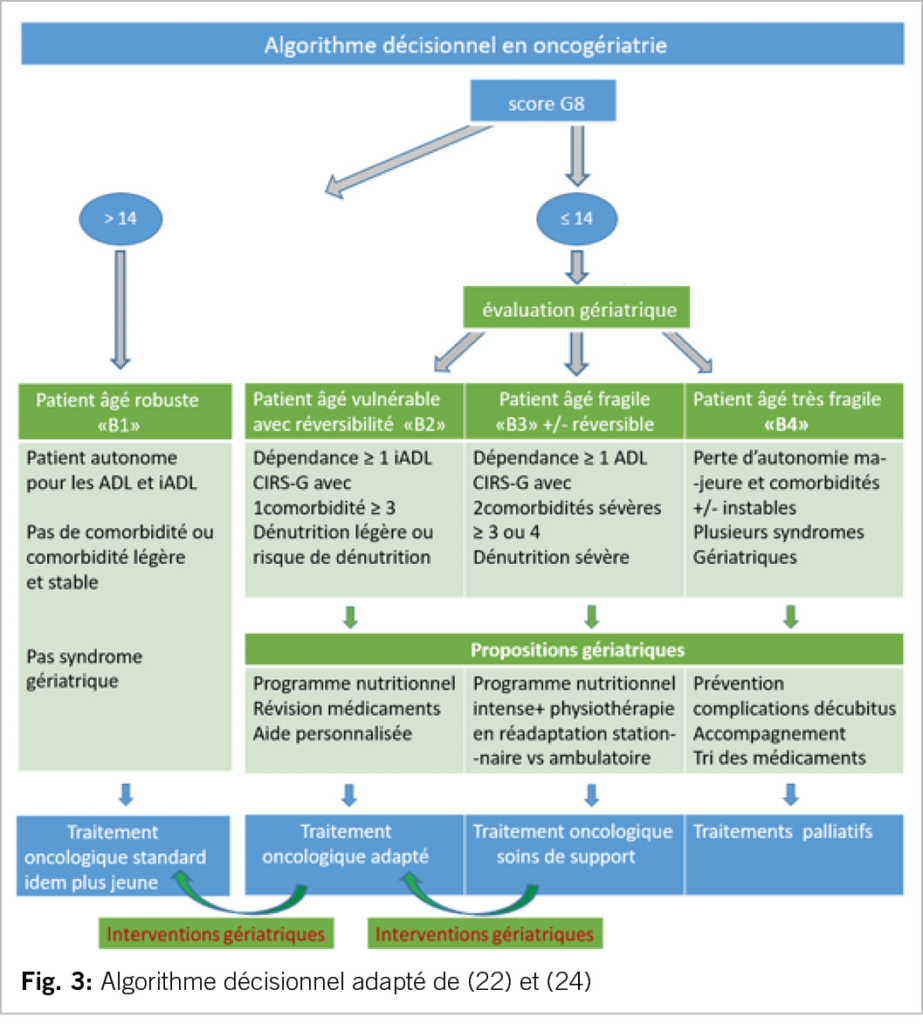
Le gériatre est alors en mesure de classer le sénior selon Balducci modifié en 4 profils (22) pour guider la prise en charge oncologique. B1 représente les patients âgés robustes qui peuvent bénéficier des traitements oncologiques comme les plus jeunes. B2 concerne les patients pour lesquels une adaptation de traitement est nécessaire. B3 sont des patients relevant de soins de support alors que la classe B4 regroupe les patients en phase palliative. La classification initiale (23) comportait 3 niveaux, mais l’expérience a permis d’ajouter une classe supplémentaire intermédiaire (24) permettant de prendre en compte le bénéfice d’un programme nutritionnel pour le critère de réversibilité potentielle : un patient classé B2 peut être upgradé en B1. Le passage de B3 vers B2 nécessite un programme de réadaptation nutritionnelle intense et de physiothérapie en milieu stationnaire (fig 3).
Outre son positionnement par rapport au traitement oncologique, le gériatre fera aussi d’autres propositions comme une révision médicamenteuse, des conseils de traitement antalgique, des mesures de prévention d’un état confusionnel, un soutien psychologique… Les options de réhabilitation (physio -ergothérapie, programme nutritionnel, support social…) pré-thérapeutique et en intercures sont expliquées pour définir avec le patient un plan d’aides personnalisé en ambulatoire ou en réadaptation oncologique stationnaire. L’avis gériatrique est tout sauf un cumul de scores incompréhensibles aux non-initiés : les scores aboutissent à des diagnostics qui débouchent sur des propositions concrètes.
Les directives anticipées sont alors abordées et à rédiger avec le médecin de famille de préférence. La réflexion est au cas par cas avec comme principe fondamental «Primum non nocere» à tous moments de la prise en soin.
Synthèse oncogériatrique
Une discussion a alors lieu entre gériatre et oncologue et un rapport de la consultation oncogériatrique est adressé à l’oncologue et au médecin de famille. C’est au tumorboard que la décision finale est prise. L’oncologue présente alors au patient le plan de soin oncologique et gériatrique. L’organisation d’un suivi gériatrique conjoint à celui de l’oncologue ou à sa demande optimise la prise en charge, comme cela a été démontré pour l’évaluation gériatrique standardisée (25).
Expériences au RHNe: cas clinique et perspectives
La consultation ambulatoire oncogériatrique se développe depuis 2018 principalement avec l’équipe du département d’oncologie et au Centre du Sein labellisé. L’expérience en pratique montre que l’avis oncogériatrique peut être demandé par l’oncologue sur la base de son sens clinique quand la prise de décision thérapeutique est complexe avec la suspicion d’un trouble neuro cognitif, des chutes répétées. À l’inverse, arrive le questionnement vis-à-vis des theranostics (26) pour le profil des «supers robustes», outrepassant le score G8.
Nos axes d’amélioration concernent les patients oncologiques hospitalisés avec la sensibilisation au recours à l’avis oncogériatrique via l’équipe mobile de gériatrie. La spécificité de celle-ci est sa mixité avec des acteurs du secteur gériatrique et d’autres issus des soins palliatifs. Par ailleurs, la mise en place récente du score IDpall (27) constitue une avancée pour la prise de conscience que les soins palliatifs ne sont pas réservés à la phase terminale.
Vignette clinique
A titre de partage d’expérience et parce que les maladies hémato-oncologiques du sujet âgé représentent des situations particulièrement complexes, voici la situation de Me B, 82 ans.
Contexte oncologique
Me B. est hospitalisée suite à une dyspnée sur épanchement pleural paranéoplasique avec découverte d’une masse médiastinale et métastase osseuse costale gauche: lymphome à grandes cellules B stade IV. Me B. ne prend aucun traitement. Dans ses ATCD, on retient un lymphome du même type au niveau de l’oropharynx traité par RCHOP en rémission depuis 13 ans.
Le questionnement de l’oncologue au gériatre concerne la réalisation d’un traitement par mini R CHOP : Me B. est alors sous prednisone.
Résumé Evaluation gériatrique:
Me B. a présenté une perte d’autonomie brutale récente, elle était autonome pour ses actes de vie quotidienne et activités instrumentales. Elle avait pour habitude de faire 45 minutes de marche tous les matins. Actuellement, elle a besoin d’aide pour sa toilette et habillage et marche avec un rollator en participant activement aux thérapies de réadaptation. Elle est nouvellement incontinente. Du point de vue neuro-cognitif, la patiente est collaborante et orientée et sa capacité de discernement est conservée par rapport au choix du traitement : elle est capable d’expliquer sa pathologie oncologique et elle sait qu’elle a déjà eu un cancer du même type. Elle souhaite bénéficier d’un traitement lourd et demande qu’on lui donne cette chance. Elle s’est déjà battue contre le cancer, elle sait que le traitement sera difficile, mais elle insiste. L’alternative d’une prise en charge type soins de confort n’est pas envisageable pour elle. Ses directives anticipées sont rédigées et son fils est son représentant thérapeutique. Elle présente une dénutrition sévère compliquée d’une perte d’autonomie brutale avec trouble thymique qui en découle. Le tout relève de l’évolution de sa pathologie oncologique avec pronostic sévère.
Résumé évaluation oncogériatrique: Me B. n’a pas de comorbidité évolutive. Selon la classification de Balducci, elle est considérée comme fragile en B3 potentiellement réversible en lien avec sa dénutrition. Le score CARG est à 8 ce qui implique un risque de 55% de développement des toxicités de grade III à V. En parallèle le bilan cardiaque est rassurant et la patiente a une insuffisance rénale chronique modérée KDIGO G3a.
Proposition oncogériatrique: C’est bien l’autonomie antérieure de la patiente et sa détermination soutenue par sa famille qui font basculer la décision. Un cadre est alors posé au vu du pronostic sombre : reconditionnement par alimentation entérale et physiothérapie, adaptation posologie mini RCHOP à la fonction rénale et si effets secondaires majeurs, on stoppe le protocole. En intercure, sera envisagée une réhabilitation oncologique.
Tumorboard: L’option du mini RCHOP adapté à la fonction rénale est validée.
Evolution: Absence de syndrome de renutrition inappropriée. Le rituximab est mal toléré avec un syndrome de lyse tumorale dès J1 traité, une pneumonie de bronchoaspiration et état confusionnel sur rétention aiguë d’urines. À J4, la biologie est normalisée et la patiente bénéficie d’une phase « lune de miel » avec reprise d’autonomie : elle marche aux côtés de son fils et profite de sa famille.
Discussion entre oncologue et gériatre: Au vu des complications en cascade sur le rituximab, le gériatre préconise alors de stopper le protocole et de passer à des soins de confort. Au vu d’une diminution de la masse tumorale, l’oncologue défend une attitude curative. Après réflexion commune, un délai de pause de 48h est convenu.
Evolution: Une dyspnée brutale hypoxémiante apparait sur un épanchement pleural récidivant paranéoplasique de 1l, ponctionné à visée de confort. Le gériatre préconise le relais par l’équipe de soins palliatifs en concertation avec l’oncologue. La cytométrie de flux diagnostique la transformation leucémique : le tumorboard confirme l’arrêt des traitements curatifs.
Des soins de confort sont instaurés. Un réseau est organisé avec la patiente et sa famille, reconnaissantes de la prise en charge intégrative dont ils ont bénéficié. Me B. décèdera paisiblement entourée des siens.
Épilogue: La collaboration entre oncologue et gériatre permet d’assumer en binôme la charge décisionnelle complexe et offrir des soins sur mesure, adaptés et coordonnés : le questionnement éthique restant sous-jacent tout au long des prises en charge.
Copyright Aerzteverlag medinfo AG
Médecin cheffe adjointe du Département de Gériatrie
Réadaptation et Soins Palliatifs RHNe Gériatre (F) avec
formation complémentaire en oncogériatrie
laure.poudens@rhne.ch
L’auteur n’a pas declaré de conflits d’intérêt.
◆ L’expertise conjointe de l’oncologue, spécialiste d’organe et du gériatre est indispensable pour les prises décisionnelles initiales et dans le
suivi du sujet âgé atteint d’un cancer, vue la disparité de la population âgée à laquelle s’ajoutent l’hétérogénéité des cancers et les avancées thérapeutiques. Le score G8 aide l’oncologue à dépister quel patient âgé peut bénéficier d’une évaluation oncogériatrique. Le gériatre doit déterminer si l’altération du patient âgé est en lien avec son cancer ou pré existant à une fragilité gériatrique et donner son avis concernant le traitement oncologique en se basant sur la classification modifiée de Balducci. Mais l’algorithme décisionnel ne doit pas enfermer le patient âgé dans une case, la notion de réversibilité potentielle offre des perspectives avec prise en charge adaptée aux besoins et à l’évolution du sujet âgé par ce binôme oncogériatrique.
1. Statistiques cancer Office Fédéral de la Statistique 2022 https://www.bfs.admin.ch/bfs/fr/home/statistiques/sante/etat-sante/maladies/cancer.html
2. Espérance de vie OFS 2022 https://www.bfs.admin.ch/bfs/fr/home/statistiques/population/naissances-deces/esperance-vie.html tableaux selon âge et sexe
3. Büla C, Beetschen P, David S et al. Rapport politique du canton de Vaud «Vieillissement et santé», 2012
4. Soubeyran P, Hœrni B, Progrès en oncogériatrie Med Hyg 2002;60:983-6
5. Stratégie nationale contre le cancer 2014-2020 https://www.bag.admin.ch/bag/fr/home/strategie-und-politik/nationale-gesundheitsstrategien/nationale-strategie-gegen-krebs-2014-2017.html
6. Yellen SB, Cella DF, Leslie WT. Age and clinical decision making in oncology patients. J Natl Cancer Inst 1994; 86: 1766-70.
7. Handforth C, Burkinshaw R, FreemanJ et al. Comprehensive geriatric assessment and decision-making in older men with incurable but manageable (chronic) cancer. Support Care Cancer 2019;27:1755-63.
8. Balducci L, Ershler WB, Lyman GH, Comprehensive Geriatric Oncology, Harwood academic publishers 1998
9. Balducci L, Extermann M, Management of Cancer in the Older Person : A Practical Approach The Oncologist 2000;5:224-237
10. Extermann M, Aapro M, Bernabei R, et al. Use of comprehensive geriatric assessment in older cancer patients: Recommendations from the task force on CGA of the International Society of Geriatric Oncology (SIOG) Crit Rev Oncol Hematol. 2005;55:241–252.
11. Wildiers H, Heeren P, Puts M, Extermann M, Falandry C, Hurria A, International Society of Geriatric Oncology Consensus on Geriatric Assessment in Older Patients With Cancer J Clin Oncol. 2014 Aug 20; 32(24): 2595–2603
12. Institut National du Cancer https://www.e-cancer.fr/Professionnels-de-sante/L-organisation-de-l-offre-de-soins/Oncogeriatrie/Les-unites-de-coordination-et-antennes-d-oncogeriatrie
13. Bruno B, De Ramon Ortiz E, Ligozat S, SAMII K et Pr CHEVALLEY T, Le myélome multiple chez la personne âgée : impact d’une évaluation gériatrique Rev Med Suisse 2019 ; 15 : 2032-8
14. Caillet P, Canoui-Poitrine F, Vouriot J, Berle M, Reinald N, Krypciak S, Bastuji-Garin S, Culine S, Paillaud E, Comprehensive geriatric assessment in the decision-making process in elderly patients with cancer: ELCAPA study. J Clin Oncol 2011;29(27):3636-42
15. Hamaker M, Lund C, te Molder M, Soubeyran P, Wildiers H, Van Huis L, Rostoft S, Geriatric assessment in the management of older patients with cancer – A systematic review (update) J Geriatr Oncol 2022 Jul;13(6):761-777
16. Petit-Monéger A, Rainfray M, Soubeyran P, Bellera C, Mathoulin-Pélissier S, Detection of frailty in elderly cancer patients: Improvement of the G8 screening test, J Geriatr Oncol 2016 Mar;7(2):99-107
17. Fried LP, Tangen CM, Walston J, et al. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci 2001;56:M146-56.
18. Bunevicius A. Reliability and validity of the SF-36 Health Survey Questionnaire in patients with brain tumors: a cross-sectional study Health Qual Life Outcomes 2017 May 4;15(1):92.
19. Extermann M, Overcash J, Lyman GH, Parr J, Balducci L. Comorbidity and functional status are independent in older cancer patients. J Clin Oncol 1998; 16: 1582-7.
20. Hurria A, Togawa K, Mohile SG et al, Predicting chemotherapy toxicity in older adults with cancer : a prospective multicenter study. J Clin Oncol. 2011 ;29(25) : 3457-65
21. Extermann M, Boler I, Reich RR, Lyman GH, Brown RH, DeFeliceJ, Levine RM, Lubiner ET, Reyes P, Schreiber FJ 3rd, Balducci L (2012) Predicting the risk of chemotherapy toxicity in older patients: the chemotherapy risk assessment scale for high-age patients score. Cancer 118(13):3377–3386
22. Ferrat E, Paillaud E, Caillet P, et al. Performance of Four Frailty Classifications in Older Patients With Cancer: Prospective Elderly Cancer Patients Cohort Study. J Clin Oncol. 2017;35(7):766-777.
23. Balducci L, Extermann M (2000) Management of cancer in the older person: a practical approach. Oncologist 2000;5(3):224–237
24. Droz JP, Balducci L, Monfardini S, Management of prostate cancer in older men: recommendations of a working group of the SIOG, BJUI 2010 (8) ; 462-9
25. Stuck A, Siu A, Wieland G, Adams J, Rubenstein L, Comprehensive geriatric assessment: a meta-analysis of controlled trials The Lancet 1993 Oct 23;342(8878):1032-6.
26. Turner J, Philosophy of Cancer Theranostics, Cancer Biother Radiopharm 2023 Feb;38(1):1-7
27. Segura J,Larkin P, Teike Lüthi F, Dépistage des besoins en soins palliatifs d’une population gériatrique : une étude descriptive transversale- Mémoire en Master ès sciences infirmières- Université de Lausanne, Haute Ecole spécialisée de Suisse Occidentale- juin 2021- en cours de validation.
la gazette médicale
- Vol. 13
- Ausgabe 1
- Januar 2024