- Chronische Hämodialyse – Die Schöne und das Biest
Seit über 60 Jahren steht die Hämodialyse für Patientinnen und Patienten mit chronischem Nierenversagen zur Verfügung. Trotz der kontinuierlichen Weiterentwicklung dieses lebensrettenden Verfahrens bleibt die Morbidität und Mortalität von chronischen Hämodialyse-Patienten mit terminalem Nierenversagen im Vergleich zur Normalbevölkerung erhöht. Den relevantesten Anteil an dieser Übersterblichkeit hat die deutlich erhöhte kardiovaskuläre Mortalität. In den letzten Jahren hat sich gezeigt, dass intermittierende Hämodialyse-Behandlungen systemische Hypoperfusionsepisoden auslösen können, die zu langfristigen kardialen und systemischen Organschäden führen können und dadurch zur erhöhten Mortalität und Morbidität beitragen. Gleichzeitig deuten neue Daten darauf hin, dass eine verlängerte Dialysebehandlung, die Vermeidung der Hypervolämie, eine kardiovaskuläre Basismedikation und eine tiefe Temperatur des Dialysates Hypotonie-Episoden vermeiden und so einen protektiven Effekt haben können.
Haemodialysis has been available to patients with chronic kidney failure for over 60 years. Despite the continuous development of this life-saving procedure, the morbidity and mortality of chronic haemodialysis patients with end-stage renal failure remains higher than in the general population. The most relevant factor in this excess mortality is the significantly increased cardiovascular mortality. In recent years, it has been shown that intermittent haemodialysis treatments can trigger systemic hypoperfusion episodes, which can lead to long-term cardiac and systemic organ damage and thus contribute to increased mortality and morbidity. At the same time, new data suggest that prolonged dialysis treatment, avoidance of hypervolaemia, baseline cardiovascular medication and a low temperature of the dialysate can prevent hypotension episodes and thus have a protective effect.
Key Words: haemodialysis, chronic kidney failure, systemic hypoperfusion episodes
Einleitung
Im März 1960 überlebte der 39-jährige US-Amerikaner Clyde Shields aus Seattle als weltweit erster Patient ein chronisches Nierenversagen dank der chronischen Hämodialyse. Dieser medizinische Durchbruch erlaubte es Shields weitere 11 Jahre zu leben, bis er während einer Dialysebehandlung an einem Myokardinfarkt verstarb. Sein Tod war der Auslöser für eine Überlebensanalyse der weltweit ersten 39 chronischen Hämodialyse-Patientinnen und Patienten, die 1974 im New England Journal of Medicine veröffentlicht wurde. Innerhalb der ersten 13 Jahre (mittleres Follow-Up 6,5 Jahre, mittleres Alter 37 Jahre) zeigte sich eine Gesamtmortalität von 56 % mit einer Überrepräsentation kardiovaskulärer Todesfälle von 60 % (1). Knapp 50 Jahre nach dieser Publikation werden in der Schweiz aktuell ca. 4500 Patientinnen und Patienten (medianes Alter 71 Jahre) chronisch hämodialysiert (2). Europaweit sind es ungefähr 310’000 Patientinnen und Patienten (3).
Obwohl die Hämodialyse-assoziierte Übersterblichkeit in den letzten Jahren leicht gesunken ist (4), beträgt die Lebenserwartung eines 40-jährigen Hämodialyse-Patienten in Europa weniger als 20 Jahre und ist vergleichbar mit der Lebenserwartung eines ca. 75-Jährigen in der Allgemeinbevölkerung (3).
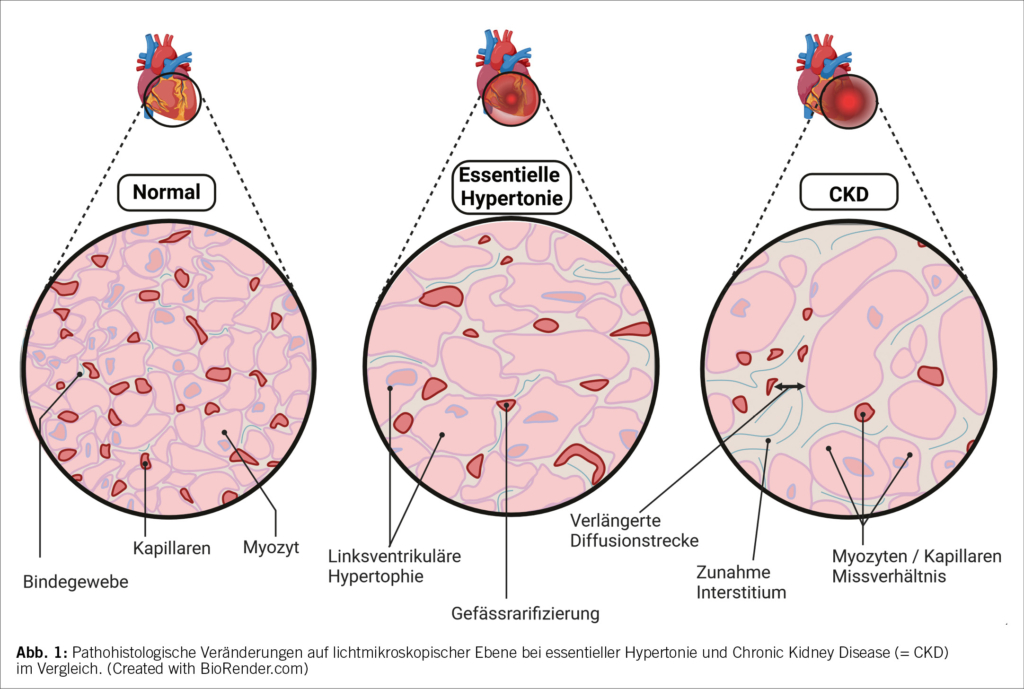
Die Gründe der Übersterblichkeit sind nur teilweise geklärt, den relevantesten Anteil stellt aber weiterhin die deutlich erhöhte kardiovaskuläre Mortalität (4). Die koronare Herzerkrankung scheint dabei allerdings nicht die Hauptursache für den Herztod bei chronischen Dialysepatienten zu sein, sondern die urämische Kardiomyopathie. Sie ist gekennzeichnet durch mediale Gefässkalzifikationen, erhöhte Gefässsteifigkeit, linksventrikuläre Hypertrophie, vermehrte interstitielle Fibrose und eine Rarefezierung kardialer Kapillaren (reviewed in (5)). Zusammen führen diese Veränderungen durch eine Abnahme des diastolischen Pulsdruckes, einem Myozyten/Kapillaren Missverhältnis und einer verlängerten Sauerstoffdiffusionsstrecke zu einer Neigung für Bedarfsischämien (Abb. 1).
Hämodynamische Effekte der Dialysebehandlung
Kurze, repetitive Hämodialyse-Behandlungen haben relevante hämodynamische Effekte. Eine Studie an 9 chronischen Hämodialyse-Pa-tientinnen und Patienten, von denen keiner einen vorhergehenden Myokardinfarkt oder klinische Anzeichen eines autonomen Versagens hatte, konnte zeigen, dass es während der Dialyse-Behandlung zu einem Blutdruckabfall von durchschnittlich 13 mmHg kam (6).
Eine ähnliche Studie mit 100 chronischen Hämodialyse-Patientinnen und Patienten ergab während ca. 20 % aller Dialyse-Behandlungen einen symptomatischen Blutdruckabfall über 20 mmHg systolisch, der eine pflegerische Intervention notwendig machte (7).
Aufgrund des Zusammenspiels dieser hämodynamischen Veränderungen und der kardialen Ischämieneigung besteht seit langem der Verdacht, dass repetitive Hämodialyse-Behandlungen eine Myokardischämie auslösen können (8).
Dialyse-induzierte kardiale Ischämie
Dieser Verdacht konnte durch eine H2150 PET-Studie, die den myokardialen Blutfluss mass, bestätigt werden. In einer Studie an 4 chronischen Hämodialyse Patienten zeigte sich, dass der globale myokardiale Blutfluss vor Beginn der Hämodialyse bei allen Patienten im normalen Bereich lag, während der Hämodialyse-Behandlung jedoch stark abnahm und sich über die Dialysedauer weiter verschlechterte. Eine koronare Herzerkrankung wurde im Vorfeld angiographisch ausgeschlossen. Am Ende der 4-stündigen Dialyse war der myokardiale Blutfluss in 90 % aller untersuchten Regionen reduziert und das Ausmass der Blutfluss Abnahme war mit dem Auftreten echokardiographischer Wandbewegungsstörungen assoziiert. Obwohl es nach der Dialyse zu einer Erholung des myokardialen Blutflusses kam, waren die Ausgangswerte auch 30 Minuten nach Beendigung der Hämodialyse-Behandlung noch nicht erreicht. Diese verlängerten Phasen von linksventrikulärer Dysfunktion sind als «myocardiales stunning» im Rahmen der koronaren Herzerkrankung gut bekannt und können langfristig zu einem irreversiblen Funktionsverlust und der Entwicklung einer Herzinsuffizienz beitragen. Weitere Arbeiten nutzten serielle intradialytische Echokardiographie, um die Häufigkeit des Hämodialyse-induzierten myokardialen Stunnings zu untersuchen. Dies wurde bewiesen durch das neue Auftreten und post-dialytische Verschwinden von regionalen Wandbewegungsstörungen und liess sich bei knapp 50 % aller Patientinnen und Patienten nachweisen (9, 10). Die wichtigsten Risikofaktoren für das Auftreten eines dialyse-induzierten myokardialen Stunnings waren einerseits vorbestehende kardiale Erkrankungen (i.e. höherer Linksventrikulärer Masse Index, geringere linksventrikuläre Ejektionsfraktion) und andererseits das Auftreten von intradialytischen Blutdruckabfällen, sowie die Menge des Ultrafiltrationsvolumens.
Besonders auffällig war die prognostische Bedeutung des dialyse-induzierten myokardialen Stunning: Patientinnen und Patienten, die bei der ersten Untersuchung ein myokardiales Stunning zeigten hatten nach einem Jahr eine signifikant niedrigere linksventrikuläre Pumpfunktion in Ruhe, eine zunehmende Ausdehnung der dialyse-induzierten Wandbewegungsstörungen und eine deutlich höhere Mortalität verglichen mit Patienten ohne myokardiales Stunning bei Studieneinschluss (9,10). Eindrücklicherweise hatten Patientinnen und Patienten ohne Zeichen eines dialyse-induzierten myokardialen Stunning ein 100 % Überleben in der 1-jährigen Nachbeobachtungszeit (9, 10).
Die hämodynamischen Effekte der Hämodialyse-Behandlung haben nicht nur kardiale, sondern auch systemische Auswirkungen.
Systemische Effekte der chronischen Hämodialyse
Eine Studie, die die renale Perfusion bei 29 chronischen Hämodialyse Patienten mittels CT-Perfusions-Studien vor, während und nach einer Hämodialyse-Behandlung untersuchte, konnte nachweisen, dass die renale Perfusion während der Dialyse Behandlung um 18 % abfiel und mit der Diureseabnahme nach Beginn der chronischen Hämodialyse assoziiert ist. Dabei ist die Restdiurese nach Dialysebeginn mit einer besseren Kontrolle von Serumphosphat, Hypervolämie, Bluthochdruck und sogar einem verbesserten Überleben verbunden. Der systemische hämodynamische Effekt der Dialyse-Behandlung wurde durch eine hohe Ko-Okkurrenz von myokardialen Stunning und reduzierter renaler Perfusion bestätigt (11). Erste Untersuchungen deuten sogar auf eine Umverteilung der hepatischen Perfusion mit negativem Einfluss auf die Leberfunktion und eine erhöhte Endotoxinfreisetzung während einer Hämodialyse-Behandlung hin (12).
Selbst die zerebrale Durchblutung wird durch die hämodynamischen Effekte der Hämodialyse beeinflusst. In MRI-Studien mit chronischen Hämodialyse-Patientinnen und Patienten konnte im Vergleich zu Kontrollpatienten eine diffuse Schädigung der weissen Hirnsubstanz nachgewiesen werden, die mit schlechteren Werten in neurokognitiven Tests korrelierten (13). In einem Beobachtungsverlauf von 12 Monaten kam es bei den Hämodialyse-Patientinnen und Patienten zu einer Zunahme der zerebralen Läsionen, wobei der Schweregrad der zerebralen Schädigung mit dem Ausmass der hämodynamischen Instabilität an der Hämodialyse zusammenhing (14).
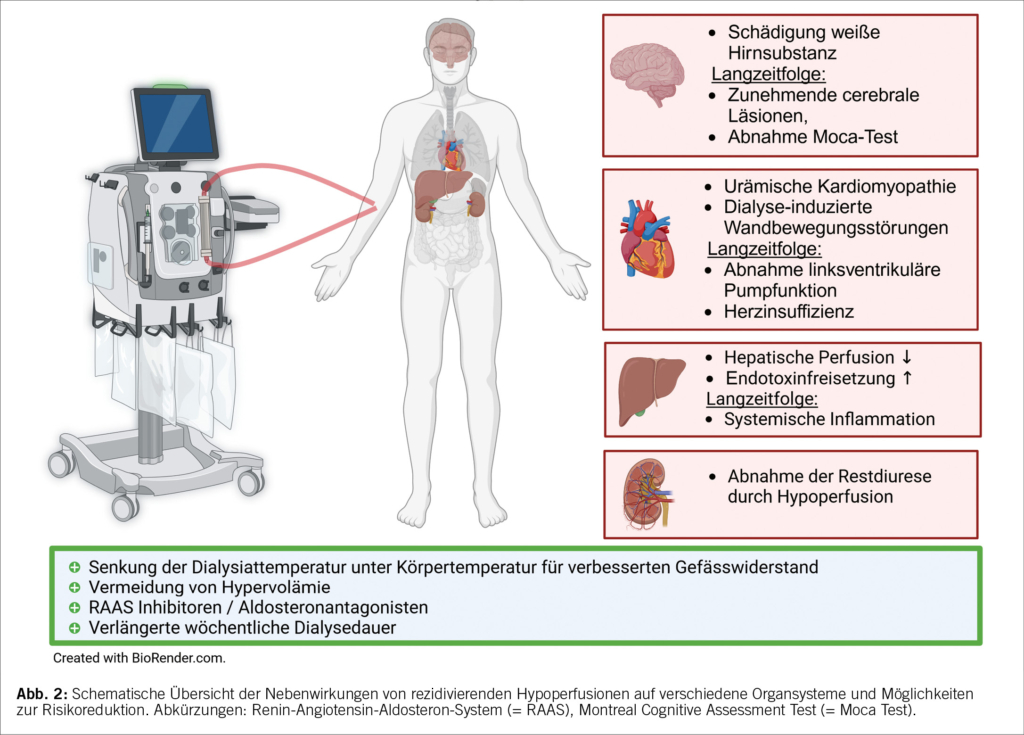
Zusammenfassend ist in den letzten Jahren deutlich geworden, dass Hämodialyse-Behandlungen eine erhebliche, wiederkehrende Kreislaufbelastung auslösen, die in vulnerablen Gefässbetten zu Hypoperfusionsepisoden führen kann und langfristig zu relevanten Organschäden führt. Interventionen mit dem Ziel, die erhöhte Mortalität und die organspezifischen Langzeitfolgen einer Dialysebehandlung zu senken, sollten daher primär versuchen, die dialyse-induzierte Kreislaufbelastung zu reduzieren.
Therapeutische Möglichkeiten zur Reduktion der Dialyse-induzierten Hypoperfusion
Eine der bestuntersuchten Interventionen zur Reduktion der dialyse-assoziierten Kreislaufbelastung ist die Senkung der Dialysat-Temperatur unter die Körpertemperatur, die im Vergleich zu einer Dialysat-Temperatur von 37.5°C die Häufigkeit intradialytischer Blutdruckabfälle, das Auftreten von dialyse-induzierten myokardialen Wandbewegungen und dialyse-assoziierter Schädigungen der weissen Hirnsubstanz signifikant reduzieren konnte (14–16). Es wird angenommen, dass diese positiven Effekte einer niedrigeren Dialysat-Temperatur hauptsächlich auf einen verbesserten Gefässwiderstand zurückzuführen sind.
Eine weitere Massnahme zur Vermeidung der Dialyse-assoziierten Kreislaufbelastung ist das Verhindern einer chronischen Hypervolämie bei Dialyse-Patientinnen und Patienten.
So konnte zum Beispiel eine Interventionsstudie mit 120 chronischen Dialysepatienten nachweisen, dass eine verbesserte Volämiebeurteilung durch den zusätzlichen Einsatz einer Bioimpedance-Messung im Vergleich zu einer rein klinischen Volumenbeurteilung innerhalb einer 12-monatigen Verlaufsbeurteilung zu einer Reduktion der prä- und postdialytischen Hypervolämie, der linksventrikulären Hypertrophie und des systolischen Blutdrucks bei einer geringeren Anzahl notwendiger Blutdruckmedikamente erreicht werden kann (17). Allerdings war nach 12 Monaten der Anteil anurischer Patienten in der Interventionsgruppe höher als in der Standardgruppe. Die bessere prädialytische Volumenkontrolle hat bei gleichbleibender Dauer einer Dialyse-Behandlung einen direkten positiven Einfluss auf den notwendigen Flüssigkeitsentzug (Ultrafiltrationsmenge) während der nachfolgenden Dialyse-Behandlung. Dies ist von Bedeutung, da die Menge des Flüssigkeitsentzugs nicht nur ein wichtiger Risikofaktor für Dialyse-assoziierte Hypotonie und kardiale Wandbewegungsstörungen ist, sondern grosse Entzugsmengen auch mit einer Übersterblichkeit einhergehen (18).
Die Dialyse-assoziierte Kreislaufbelastung kann zusätzlich durch eine Reduktion der Entzugsgeschwindigkeit (Ultrafiltrationsrate) positiv beeinflusst werden. Die kann neben einer Reduktion der Gewichtszunahme zwischen zwei Dialyse-Behandlungen auch durch die Dauer einer Dialyse-Behandlung beeinflusst werden. Insbesondere sehr kurze Dialyse-Behandlungen unter 3h, die eine hohe Ultrafiltrationsrate zur Erhaltung der Euvolämie benötigen, sind mit einer Übersterblichkeit verbunden (18).
Gleichzeitig konnte eine Reihe von nicht-randomisierten Studien zeigen, dass eine verlängerte wöchentliche Dialyse-Dauer (nächtliche Dialyse oder häufigere Dialyse-Behandlungen) mit einer verbesserten Lebensqualität, einer verbesserten Blutdruck- und Phosphat-Kontrolle und sogar einer Reduktion der linksventrikulären Hypertrophie verbunden war (19, 20).
Diese Ergebnisse wurden allesamt in der randomisierten Frequent Hemodialysis Network Study bestätigt, welche 245 Patienten in eine Standardgruppe mit dreimal wöchentlicher Dialyse oder eine Gruppe mit kürzerer, sechsmal wöchentlicher Dialyse, (insgesamt zwei Stunden längere wöchentliche Dialysedauer) randomisierte (21).
In der verlängerten Studienbeobachtung zeigte sich sogar, dass die durch die verlängerte Dialyse-Dauer erzielten positiven kardiovaskulären Veränderungen auch nach dem Wechsel auf eine dreimal wöchentliche Standarddialyse zu einer signifikanten Mortalitätssenkung führten (22).
Last but not least, erscheint eine gute kardiovaskuläre Basis-Therapie mit RAAS-inhibierenden Medikamenten und Aldosteronantagonisten nach neuesten Daten der Cochrane Library und der internationalen Dialysis Outcomes and Practice Patterns Study (DOPPS) nicht nur nicht schädlich zu sein, sondern sogar eine moderate Mortalitätsreduktion zu ermöglichen (23, 24).
Copyright
Aerzteverlag medinfo AG
-Basel Klinik für Innere Medizin,
Universitätsspital Basel
Petersgraben 4
4031 Basel
-Cardiovascular Research Institute,
Universitätsspital Basel
Spitalstrasse 2
4056 Basel
-Basel Klinik für Innere Medizin,
Universitätsspital Basel
Petersgraben 4
4031 Basel
-Cardiovascular Research Institute,
Universitätsspital Basel
Spitalstrasse 2
4056 Basel
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Die chronische Hämodialyse ermöglicht das Überleben von Patientinnen und Patienten mit einem terminalen Nierenversagen.
◆ Patientinnen und Patienten, die auf eine chronische Hämodialyse angewiesen sind, haben eine deutlich erhöhte Mortalität.
◆ In den letzten Jahren konnte gezeigt werden, dass kurze, intermittierende Hämodialyse-Behandlungen zu einer systemischen Hypoperfusion führen können.
◆ Diese Hypoperfusions-Phasen führen direkt zu Organschäden (e.g. kardiale Wandbewegungstörungen, zerebrale Schäden der weissen Substanz, renale Hypoperfusion) und tragen langfristig durch irreversiblen Funktionsverlust zur hohen Morbidität und Mortalität der Dialyse-Patientinnen und -Patienten bei.
◆ Eine gute kardiovaskuläre Basismedikation, das Vermeiden einer Hypervolämie und eine Dialyse-Behandlung mit gekühltem Dialysat tragen zu einer Reduktion dieser Hypoperfusion-Phasen bei.
◆ Eine verlängerte wöchentliche Dialyse-Dauer steigert die Lebensqualität, reduziert die kardiovaskuläre Belastung der Dialyse-Behandlung und ist mit einem verlängerten Überleben assoziiert. Patientenwunsch, ärztliche Präferenz, sowie organisatorische und abrechnungstechnische Probleme verhindern einen breiteren Einsatz dieser Methode.
1. Lindner A, Charra B, Sherrard DJ and Scribner BH. Accelerated atherosclerosis in prolonged maintenance hemodialysis. N Engl J Med. 1974;290:697-701.
2. Winzeler R and Ambühl PM. P1467DEMOGRAPHY OF THE DIALYSIS POPULATION IN SWITZERLAND IN 2018. Nephrology Dialysis Transplantation. 2020;35.
3. Astley ME, Boenink R, Abd ElHafeez S, Trujillo-Aleman S, Arribas F, Asberg A, Beckerman P, Bell S, Bouzas-Caamano ME, Farnes JC, Galvao AA, Gjorgjievski N, Kelmendi VG, Guidotti R, Helve J, Idrizi A, Indriethason OS, Ioannou K, Kerschbaum J, Komissarov K, Castro de la Nuez P, Lassalle M, Nordio M, Arevalo OLR, Santiuste C, Seyahi N, Roblero MFS, Steenkamp R, Ten Dam M, Zakharova EV, Ziginskiene E, Bonthuis M, Stel VS, Ortiz A, Jager KJ and Kramer A. The ERA Registry Annual Report 2020: a summary. Clin Kidney J. 2023;16:1330-1354.
4. Boenink R, Stel VS, Waldum-Grevbo BE, Collart F, Kerschbaum J, Heaf JG, de Meester J, Finne P, Garcia-Marcos SA, Evans M, Ambuhl PM, Arici M, Ayav C, Steenkamp R, Cases A, Traynor JP, Palsson R, Zoccali C, Massy ZA, Jager KJ and Kramer A. Data from the ERA-EDTA Registry were examined for trends in excess mortality in European adults on kidney replacement therapy. Kidney Int. 2020;98:999-1008.
5. Breidthardt T and McIntyre CW. Dialysis-induced myocardial stunning: the other side of the cardiorenal syndrome. Rev Cardiovasc Med. 2011;12:13-20.
6. Bos WJ, Bruin S, van Olden RW, Keur I, Wesseling KH, Westerhof N, Krediet RT and Arisz LA. Cardiac and hemodynamic effects of hemodialysis and ultrafiltration. Am J Kidney Dis. 2000;35:819-26.
7. Pavan M RR, Chaudhari AP, Aiyangar A, Upadhayaya KL, Mehta HJ. . Incidence and Measures to Prevent Intradialytic Hypotension in Patients on Maintenance Hemodialysis in a Tertiary Care Centre in India. J Nephrol Ther 2011;1.
8. Zuber M, Steinmann E, Huser B, Ritz R, Thiel G and Brunner F. Incidence of arrhythmias and myocardial ischaemia during haemodialysis and haemofiltration. Nephrol Dial Transplant. 1989;4:632-4.
9. Burton JO, Jefferies HJ, Selby NM and McIntyre CW. Hemodialysis-induced cardiac injury: determinants and associated outcomes. Clin J Am Soc Nephrol. 2009;4:914-20.
10. Assa S, Hummel YM, Voors AA, Kuipers J, Westerhuis R, de Jong PE and Franssen CF. Hemodialysis-induced regional left ventricular systolic dysfunction: prevalence, patient and dialysis treatment-related factors, and prognostic significance. Clin J Am Soc Nephrol. 2012;7:1615-23.
11. Marants R, Qirjazi E, Grant CJ, Lee TY and McIntyre CW. Renal Perfusion during Hemodialysis: Intradialytic Blood Flow Decline and Effects of Dialysate Cooling. J Am Soc Nephrol. 2019;30:1086-1095.
12. Marants R, Qirjazi E, Lai KB, Szeto CC, Li PKT, Li F, Lee TY and McIntyre CW. Exploring the Link Between Hepatic Perfusion and Endotoxemia in Hemodialysis. Kidney Int Rep. 2021;6:1336-1345.
13. Eldehni MT, Odudu A and McIntyre CW. Brain white matter microstructure in end-stage kidney disease, cognitive impairment, and circulatory stress. Hemodial Int. 2019;23:356-365.
14. Eldehni MT, Odudu A and McIntyre CW. Randomized clinical trial of dialysate cooling and effects on brain white matter. J Am Soc Nephrol. 2015;26:957-65.
15. Mustafa RA, Bdair F, Akl EA, Garg AX, Thiessen-Philbrook H, Salameh H, Kisra S, Nesrallah G, Al-Jaishi A, Patel P, Patel P, Mustafa AA and Schunemann HJ. Effect of Lowering the Dialysate Temperature in Chronic Hemodialysis: A Systematic Review and Meta-Analysis. Clin J Am Soc Nephrol. 2016;11:442-57.
16. Selby NM and McIntyre CW. A systematic review of the clinical effects of reducing dialysate fluid temperature. Nephrol Dial Transplant. 2006;21:1883-98.
17. Hur E, Usta M, Toz H, Asci G, Wabel P, Kahvecioglu S, Kayikcioglu M, Demirci MS, Ozkahya M, Duman S and Ok E. Effect of fluid management guided by bioimpedance spectroscopy on cardiovascular parameters in hemodialysis patients: a randomized controlled trial. Am J Kidney Dis. 2013;61:957-65.
18. Flythe JE, Curhan GC and Brunelli SM. Disentangling the ultrafiltration rate-mortality association: the respective roles of session length and weight gain. Clin J Am Soc Nephrol. 2013;8:1151-61.
19. Suri RS, Nesrallah GE, Mainra R, Garg AX, Lindsay RM, Greene T and Daugirdas JT. Daily hemodialysis: a systematic review. Clin J Am Soc Nephrol. 2006;1:33-42.
20. Graham-Brown MPM, Churchward DR, Hull KL, Preston R, Pickering WP, Eborall HC, McCann GP and Burton JO. Cardiac Remodelling in Patients Undergoing in-Centre Nocturnal Haemodialysis: Results from the MIDNIGHT Study, a Non-Randomized Controlled Trial. Blood Purif. 2017;44:301-310.
21. Group FHNT, Chertow GM, Levin NW, Beck GJ, Depner TA, Eggers PW, Gassman JJ, Gorodetskaya I, Greene T, James S, Larive B, Lindsay RM, Mehta RL, Miller B, Ornt DB, Rajagopalan S, Rastogi A, Rocco MV, Schiller B, Sergeyeva O, Schulman G, Ting GO, Unruh ML, Star RA and Kliger AS. In-center hemodialysis six times per week versus three times per week. N Engl J Med. 2010;363:2287-300.
22. Chertow GM, Levin NW, Beck GJ, Daugirdas JT, Eggers PW, Kliger AS, Larive B, Rocco MV, Greene T and Frequent Hemodialysis Network Trials G. Long-Term Effects of Frequent In-Center Hemodialysis. J Am Soc Nephrol. 2016;27:1830-6.
23. Karaboyas A, Xu H, Morgenstern H, Locatelli F, Jadoul M, Nitta K, Dasgupta I, Tentori F, Port FK and Robinson BM. DOPPS data suggest a possible survival benefit of renin angiotensin-aldosterone system inhibitors and other antihypertensive medications for hemodialysis patients. Kidney Int. 2018;94:589-598.
24. Hasegawa T, Nishiwaki H, Ota E, Levack WMM, Noma H.Aldosterone antagonists for people with chronic kidney disease requiring dialysis.Cochrane Database of Systematic Reviews 2021, Issue 2. Art. No.: CD013109.
info@herz+gefäss
- Vol. 14
- Ausgabe 4
- Juli 2024