- Troubles digestifs fonctionnels: Côlon irritable et estomac irritable
Les troubles fonctionnels de la digestion, en particulier le syndrome du côlon irritable (SCI) et l’estomac irritable (dyspepsie fonctionnelle, DF), font partie des maladies gastro-entérologiques les plus courantes et affectent considérablement la qualité de vie de nombreuses personnes concernées. La physiopathologie de ces troubles est complexe et comprend une hypersensibilité viscérale, une modification de la motilité intestinale, des dysbioses dans le microbiome ainsi qu’une perturbation de la communication intestin-cerveau. Le diagnostic repose sur des critères cliniques, les symptômes d’alerte nécessitant des examens complémentaires. Le traitement est axé sur les symptômes et comprend une combinaison de mesures médicamenteuses, diététiques et phytothérapeutiques. Une thérapie individualisée et holistique peut contribuer à réduire les symptômes et à améliorer durablement la qualité de vie des patients.
Functional digestive disorders, in particular irritable bowel syndrome (IBS) and functional dyspepsia (FD), are among the most com¬mon gastroenterological disorders and significantly impair the quality of life of many of those affected. The pathophysiology of these disorders is complex and includes visceral hypersensitivity, altered intestinal motility, dysbiosis in the microbiome, and impaired gut-brain communication. Diagnosis is based on clinical criteria, with alarm symptoms triggering further investigation. The therapy is symptom-oriented and includes a combination of medication, dietary and herbal measures. An individualized and holistic therapy can help to reduce the symptoms and sustainably improve the patient’s quality of life.
Key Words: Functional digestive disorders, irritable bowel syndrome and functional microbiome, therapy options
Définition et épidémiologie
Les troubles digestifs fonctionnels, qui comprennent le syndrome du côlon irritable (SCI) et la dyspepsie fonctionnelle, sont appelés « Disorders of Gut-Brain Interaction » (DGBI). Dans le cas de l’estomac irritable, les troubles se concentrent sur le tube digestif supérieur, tandis que dans le cas du côlon irritable, ils concernent le tube digestif inférieur. Ces troubles sont très répandus, touchant environ 10 à 15 % de la population, avec une prévalence plus élevée chez les femmes (1, 2, 3).
De nombreux patients souffrent d’une diminution considérable de leur qualité de vie, car les symptômes apparaissent souvent de manière imprévisible. Les patients souffrant de troubles graves sont parfois prêts à prendre des risques considérables pour soulager leurs symptômes (4)
Symptômes et classification
Le syndrome du côlon irritable se subdivise en cinq sous-types:
• IBS-C: avec constipation prédominante;
• IBS-D: avec prédominance de diarrhée;
• IBS-M: avec des habitudes de selles instables.
• IBS-U: IBS non classable.
L’estomac irritable peut quant à lui se présenter sous la forme d’un syndrome douloureux épigastrique (EPS) ou d’un syndrome de détresse postprandiale (SDP). Alors que l’EPS se caractérise par des douleurs et des brûlures dans la partie supérieure de l’abdomen, le PDS se manifeste par une sensation de satiété précoce et de plénitude après les repas.
De nombreux patients présentent des symptômes qui se chevauchent, de sorte qu’il est souvent difficile de faire une distinction claire entre les deux maladies (Fig. 1).
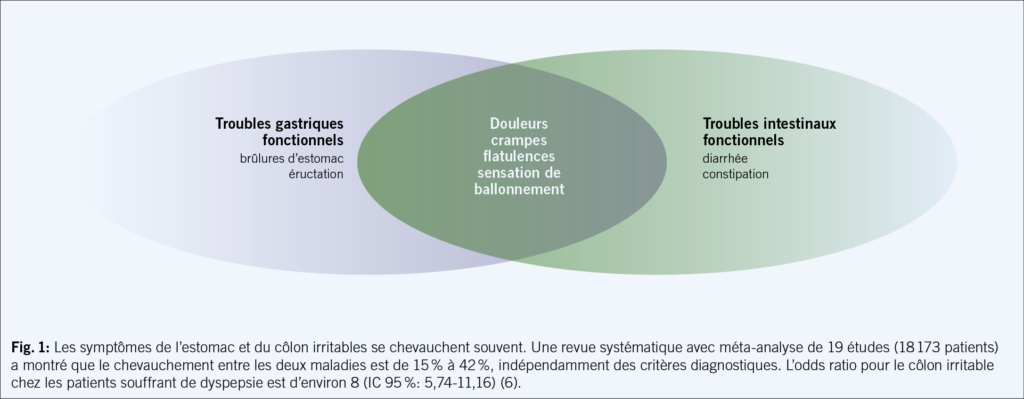
Une méta-analyse a révélé que le chevauchement des symptômes se situe entre 15 et 42 % (6).
Physiopathologie
Les causes exactes ne sont pas encore totalement élucidées. Des études récentes montrent toutefois que différents facteurs contribuent au développement de la maladie (7–13).
• Hypersensibilité viscérale: une sensibilité accrue à la douleur dans le tractus gastro-intestinal.
• Motilité intestinale perturbée: des modifications des schémas de mouvement de l’intestin peuvent entraîner aussi bien de la constipation que de la diarrhée.
• Des modifications du microbiome: les déséquilibres de la flore intestinale jouent un rôle dans l’apparition du SCI.
• Processus inflammatoires et activation immunitaire: les micro-inflammations chroniques peuvent jouer un rôle clé.
• Communication intestin-cerveau altérée: les interactions entre le système nerveux et le tube digestif sont modifiées chez les personnes atteintes.
• Le rôle de l’infection à Helicobacter pylori n’est pas encore totalement élucidé.
Diagnostic
Le diagnostic des troubles digestifs fonctionnels repose principalement sur les critères de ROME IV (14). Pour le SCI, il s’agit de:
– Douleurs abdominales récurrentes au moins un jour par semaine au cours des trois derniers mois.
– Lien entre les douleurs et l’évacuation des selles.
– Modification de la fréquence ou de la consistance des selles.
Pour la dyspepsie fonctionnelle, des symptômes tels qu’une douleur épigastrique, une sensation de plénitude ou de satiété précoce doivent être présents sans qu’une cause organique démontrable puisse être identifiée.
Symptômes d’alarme
Certains de ces symptômes (15 et 16) nécessitent un diagnostic plus approfondi afin d’exclure des maladies graves, notamment:
– des difficultés à avaler.
– perte de poids inexpliquée;
– sang dans les selles ou signes d’anémie;
– vomissements répétés;
– Ballonnements persistants ou présence d’un volume abdominal (ictère);
– Nouvelle apparition de la dyspepsie ou modification des habitudes de défécation chez les patients de plus de 40 ans.
– Indices de perte de sang ou d’anémie;
Options thérapeutiques:
Approches médicamenteuses:
Le traitement vise à améliorer la qualité de vie et à soulager les symptômes.
– Les spasmolytiques peuvent soulager les crampes (17).
– La rifaximine, un antibiotique non résorbable, peut être utilisée chez les patients présentant une mauvaise colonisation de l’intestin grêle (SIBO) (18).
– Les inhibiteurs de la pompe à protons (IPP) sont utiles en cas de dyspepsie fonctionnelle, notamment chez les patients H. pylori négatifs (19).
– Les antidépresseurs, tels que les antidépresseurs tricycliques ou les ISRS, sont utilisés pour soulager la douleur (20, 21).
– Les prébiotiques/probiotiques. Ils semblent être des traitements efficaces pour la DA, bien que les espèces et les souches individuelles qui sont les plus bénéfiques restent floues (22).
– Les prokinétiques favorisent la mobilité gastro-intestinale, notamment dans les cas de SDP (23).
Les produits phytopharmaceutiques
Les substances actives végétales jouent un rôle de plus en plus important dans le traitement:
– L’huile de menthe poivrée a un effet analgésique et décontractant (24).
– L’huile de cumin réduit les ballonnements et améliore la digestion (25).
– Huile de menthe poivrée et huile de cumin combinées (Carmenthin®) (26)
– L’anse amère peut réguler la musculature gastro-intestinale (27, 28).
– L’artichaut et le curcuma ont des effets antioxydants et anti-inflammatoires (29, 30).
– La camomille a des propriétés apaisantes et anti-inflammatoires (31).
– Les enveloppes de psyllium favorisent la digestion, en particulier dans le cas du SII-C (32–34).
Mesures diététique
– Le régime Low FODMAP est l’une des interventions alimentaires les plus efficaces, car les aliments riches en FODMAP peuvent provoquer des ballonnements et des diarrhées (35-38).
– Le régime sans gluten peut être utile pour certaines personnes, même en l’absence de maladie cœliaque (39, 40).
– Régime riche en fibres: il soutient le transit intestinal, les enveloppes de psyllium étant particulièrement efficaces (33, 34).
Autres options thérapeutiques:
Outre les médicaments et l’alimentation, il existe d’autres approches:
– Gestion du stress: les facteurs psychologiques tels que le stress et l’anxiété jouent un rôle important dans le SCI et la dyspepsie. Des techniques telles que l’entraînement à la pleine conscience ou la thérapie cognitivo-comportementale peuvent s’avérer utiles.
– L’exercice physique: une activité physique régulière améliore la motilité intestinale et réduit le stress.
– Éducation des patients: une information complète sur la maladie permet aux personnes concernées de mieux gérer leurs symptômes.
Carmenthin® (Menthacarin®): un effet cliniquement pertinent.
Supérieur au placebo.
L’étude a évalué l’efficacité et la sécurité de gélules gastro-résistantes contenant une combinaison fixe de 90 mg d’huile de menthe poivrée et 50 mg d’huile de carvi (Menthacarin®). Des patients souffrant de dyspepsie fonctionnelle ont été traités avec une gélule de Menthacarin® ou un placebo deux fois par jour pendant 28 jours (41). Les variables primaires d’efficacité étaient la variation intra-individuelle (i) de l’intensité de la douleur et (ii) de la pression, de la lourdeur et de la sensation de plénitude entre les jours 1 et 29, ainsi que l’évaluation (iii) de l’amélioration globale (Clinical Global Impression [CGI] item 2) par les investigateurs au jour 29. Au jour 29, l’intensité moyenne de la douleur avait diminué de 40 % dans le groupe Menthacarin® et de 22 % dans le groupe placebo par rapport à la valeur initiale. Pour la pression, la lourdeur et la sensation de plénitude, une réduction de 43 % a été constatée dans le groupe Menthacarine® et de 22 % dans le groupe placebo. Concernant la pression, la lourdeur et la sensation de plénitude, une réduction de 43 % a été constatée dans le groupe Menthacarin® et de 22 % dans le groupe placebo. Pour les trois paramètres cibles, la supériorité de Menthacarin® par rapport au placebo était statistiquement significative. Six patients (cinq sous Menthacarine® et un sous placebo) ont signalé des événements indésirables qui n’étaient pas liés à l’étude ou qui étaient dus à une aggravation de la maladie étudiée (42). Une autre étude multicentrique prospective, contrôlée par placebo, en double aveugle, a évalué l’efficacité de la Menthacarine® sur les symptômes et la qualité de vie (QoL) chez 114 patients présentant des symptômes de dyspepsie à l’origine de douleurs épigastriques ou de troubles digestifs postprandiaux (32). Les principaux résultats étaient les suivants: Après 2 et 4 semaines, le traitement actif était supérieur au placebo pour soulager les symptômes correspondant au PDS et à l’EPS (p < 0.001 pour tous les cas). Après quatre semaines de traitement, les scores de douleur et d’inconfort ont diminué de 7.6 ± 4.8 et 3.6 ± 2.5 points (analyse complète; moyenne ± écart-type) avec Carmenthin® et de 3.4 ± 4.3 et 1.3 ± 2.1 points avec le placebo.
Toutes les mesures d’efficacité secondaires ont montré l’avantage de Carmenthin®. Carmenthin® s’est avéré efficace pour soulager la douleur et l’inconfort ainsi que pour améliorer la qualité de vie spécifique à la maladie chez les patients atteints de DF. Ces résultats démontrent la bonne tolérance et le rapport bénéfice/risque favorable de Carmenthin® dans le traitement de la dyspepsie fonctionnelle (43). Carmenthin® a également montré son efficacité sur les symptômes typiques du côlon irritable, du syndrome du côlon irritable (SCI) et de la dyspepsie fonctionnelle (DF), qui sont des maladies gastro-intestinales fonctionnelles fréquentes présentant des symptômes similaires. L’efficacité et la sécurité de Carmenthin® ont été démontrées dans le traitement de la dyspepsie fonctionnelle. L’efficacité de Carmenthin® sur les symptômes associés à l’intestin irritable chez les patients atteints de DA a été examinée dans une analyse systématique d’essais contrôlés randomisés en double aveugle (43). Trois des cinq essais contrôlés randomisés (ECR) identifiés ont inclus un total de 111 sujets éligibles, ce qui a permis d’établir des statistiques synthétiques et de les inclure dans une analyse de sous-groupe pour les patients atteints de DA présentant des symptômes associés au SCI.
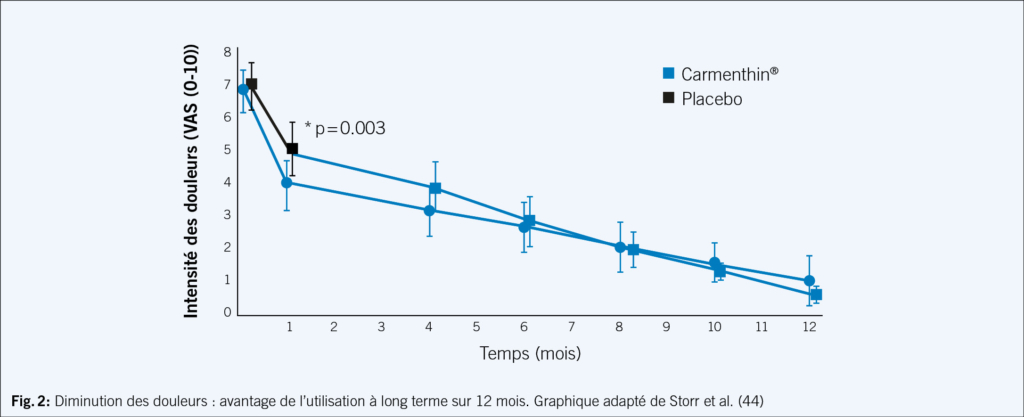
Les valeurs d’intensité de la douleur des patients présentant un syndrome du côlon irritable concomitant ont diminué en moyenne de 50 à 75 % pendant les 28 jours de traitement. L’analyse des sous-groupes indique ainsi des effets positifs du traitement à base de Carmenthin®, comparables à ceux observés chez les patients atteints de DA dans les analyses primaires. Dans les études cliniques, Carmenthin® s’est révélé efficace et sûr lors d’une utilisation à long terme chez les patients souffrant de dyspepsie fonctionnelle. Les résultats du traitement à long terme ont été enregistrés dans une étude ouverte de 12 mois sur le suivi du traitement (44). Les patients avaient auparavant été traités par Carmenthin® (une capsule gastro-résistante deux fois par jour vs placebo) dans le cadre d’une étude clinique en double aveugle de quatre semaines. Pendant le suivi, tous les patients ayant reçu auparavant du verum ou un placebo ont été traités avec une capsule de Carmenthin® deux fois par jour. Les critères d’évaluation étaient les changements d’intensité de la douleur (Fig. 2).
Copyright
Aerzteverlag medinfo AG
riesen@medinfo-verlag.ch
Les auteurs n’ont pas déclaré de conflit d’intérêts en rapport avec cet article.
- Les troubles digestifs fonctionnels, tels que le côlon irritable et l’estomac irritable, sont des maladies fréquentes qui occasionnent un stress considérable pour les personnes qui en souffrent.
- La pathophysiologie est complexe et comprend des facteurs tels que l’hypersensibilité viscérale, l’altération de la flore intestinale et la perturbation de la communication entre l’intestin et le cerveau.
- Le diagnostic repose sur des critères cliniques, les symptômes d’alarme nécessitant un examen plus approfondi. Le traitement doit être adapté individuellement et associer des mesures médicamenteuses, phytothérapeutiques et diététiques. L’efficacité et la sécurité du traitement par Carmenthin® ont été démontrées, même en cas d’utilisation à long terme.
- Une approche globale et centrée sur le patient permet de soulager les symptômes et d’améliorer la qualité de vie.
1. Simons J et al. Disorders of gut-brain interactions: Highly prevalent and bur densome yet under-thought within medical education. United Eur Gastroent erol J 2022;10:7436-7444.
2. Oka P et al. Global prevalence of irritable bowel syndrome according to Rome IIIor IV criteria : a systematic review and meta-analysis Lancet Gastroneterol. And Hepatol. 2020;Oct 5 (10) 908-917
3. Palsson OS et al. Prevalence and associated factors of disorders of gut-brain interaction in the United States : Comparison of two nationwide Internet surveys. Neurogastroenterol Motif 2023;35:e14564 doi: 10.1111/nmo.14564.
4. Lacy BE et al. IBS patients’ willingness to take risks with medications. Am J Gastroenterol 2012;10804-809.
5. Drossmann DA and Hasler Rome IV functional GI disease disorders of gut brain interaction . Gastroenterol. 2016; 150: 1257- 1261
6. Ford AC et al. Systematic review and meta-analysis of the prevalence of Irrita ble Bowel Syndrome in individuals with dyspepsia. Clin. Gastroenterol Hepatol 2010;8:401-409.
7. Holtmann GJ et al. Pathophysiology of Irritable Bowel Syndrome. Lancet Gastroenterol Hepatol 2016; Oct:1(2):123-146. Ford AC et al
8. Lawal A et al. Novel evidence for hypersensitivity of visceral sensory circuitry in irritable bowel syndrome patients. J Gastroenterol 2006; Jan 130(1):26-33.
9. Fukudo S et al. Impact of corticotropin-releasing hormone on gastrointestinal motility and adenocorticotropic hormone in normal controls and patients with Irritable Bowel Syndrome. Gut 1998 Jun;42(6):845-849.
10. Chadwick VS et al. Activation of the mucosal immune system in Irritable Bowel Syndrome Gastroenterol 2002 Jun;122(7):1779-1783.
11. Thabane M et al. Systematic review and meta-analysis: The incidence and prognosis of post-infectious Irritable Bowel Syndrome. Aliment. Pharmacol. Ther. 2007 Aug 15;26(4):535-544.
12. Crouzet L et al. The hypersensitivity to colonic dstension of IBS patients can be transferred to rats through their fecal microbiota. Neurogastroenterol Motil 2013 Apr;25(4): e272-282.
13. Longstreth G and Lacy BE. Functional dyspepsia in adults. UptoDate, November 2024.
14. Lacy BE and Patel NK. Rome IV criteria and a diagnostic approach to irritable bowel syndrome. J Clin Med 2017;6:99. doi: 10.3390/jcm6110099.
15. Fox M. Diagnose und Behandlung der funktionellen Dyspepsie in der klini schen Praxis. Schweiz. Gasteroenterologie 2023;4:7-18.
16. Häuser W et al. Funktionelle Darmbeschwerden bei Erwachsenen. Deutsches Aerzteblatt 2012;109:83-94.
17. Lacy, Brian E. et al Bowel Disorders. Gastroenterology, Volume 150, Issue 6, 1393 – 1407.e5
18. Pimentel M. Review of rifaximin as treatment for SIBO and IBS. Expert Opin Investig Drugs 2009;18:349-58. doi: 10.1517/13543780902780175.
19. Pinot-Sanchez M. Proton pump inhibitors for functional dyspepsia. Cochrane Database Syst Rev 2017;Nov 21:11(11):CDO11194.
20. Ford AC et al. Effect of antidepressants and psychological therapies in irritable bowel syndrome :an updated systematic review and metaanalysis. Am J Gas troenterol 2019;114 :21-39
21. Lacy BE et al. Bowel disorders. Gastroenterology 2016;150 :1353-1407
22. Zhang I et al. Efficacy of prebiotics and probiotics for functional dyspep sia. A systematic review and meta-analysis. Medicine (Baltimore 2020 Feb;99(7):e19107. doi: 10.1097/MD.0000000000019107.
23. Mbuzi EM et al.. Dyspepsia a more complex approach. Rev Med Suisse 2022 Sep 28,18(797):1784-1787. doi: 10.53738/REVMED.2022.18.797.1784.
24. Chumpitazi BP et al. The physiologic effects and safety of peppermint oil and ist efficacy in irritable bowel syndrome and other functional disorders. Aliment Pharmacol Ther 2018;47:738-752.
25. Mahboubi M. Caraway as Important Medicinal Plants in Management of Diseases. Nat Prod Bioprospect 2019;9:1-11.
26. Koch E et al. Beitrag schaumhemmender Effekte von Pfefferminz- und Küm melöl zu den karminativen Wirkungen von Menthacarin. Z Phytother 2015;36: (Suppl.1) S34-S35.
27. Reichling I and Saller R. [Iberis amara L. (bitter candytuft profile of a medici al plant]. Forschende Komplementarmedizin und Klassische Naturheilkunde = Research in Complementary and Natural Classical Medicine, 01 Dec 2002, 9 Suppl 1:21-33.
28. Melzer J et al. Meta-analysis: phytotherapy of functional dyspepsia with the herbal drug preparation STW 5 (Iberogast). Aliment Pharmacol Ther 2004;20:1279-87.
29. Hoffmann G. et al. Efficacy of artichoke leaf extract in the treatment of patients with functional dyspepsia : a six-week placebo-controlled double-blimd, multicentre trial. Aliment Pharmacol. Ther 2003; 18 : 1099-1105
30. Hawlings SI and Kalman DS. Cucurmin : A review of its effects on human health. Foods 2017; 6 92.
31. Dai Y et al. Chamomile. A review of ist traditional use, chemical constituents, pharmacological activitites and quality control studies. Molecules 2023;28:133.
32. Prior A and Whirwell PJ. Double blind study of isphaghula in irritable bowel disease. Gut 1987;28:1510-1513.
33. Andresen V et al. Aktualisierte S2k-Leitlinie chronische Obstipation der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechsel krankheiten (DGVS) und der Deutschen Gesellschaft für Neurogastroentero logie & Motilität (DGBN)- April 2022 – AWMF-Registriernummer: 021-019. Z. Gastroenterol 3033;60:1528-1572
34. Assessment report on Plantago afra L. et Plantago Indica L. semen. Eur Med. Agency Committee on Herbal Medicinal Products. 14 May 2013.
35. Rettura F et al. Role of FODMAP diet in functional dyspepsia: «Why», «When» and to «Whom». Best Practice & Research Clinical Gastroenterology 2023; s 62–63, 101831.
36. Bellini M et al. Low FODMAP Diet. Evidence , doubts and hopes. Nutrients 2020 Jan 4;12(1):148. doi: 10.3390/nu12010148. SPECIAL Carmenthin® Schwabe Pharma
37. Marsh A et al. Does a diet low in FODMAPs reduce symptoms associated with functional gastrointestinal disorders? Eur J Nutr 2016;55: 897-906.
38. Black CJ et al. Efficacy of a low FODMAP diet in irritable bowel syndrome. Systematic review and network metaanalysis. Gut 2022;71 :1117-1126
39. Eli L et al. Evidence for the Presence of Non-Celiac Gluten Sensitivity in Pa tients with Functional Gastrointestinal Symptoms: Results from a Multicenter Randomized Double-Blind Placebo-Controlled Gluten Challenge. Nutrients 2016;8(2):84. https://doi.org/10.3390/nu8020084.
40. Algera JP et al. Randomized controlled trial effects of gluten-free diet on symptoms and the gut microenvironment in irritable bowel sydrome. Aliment Pharmacol Ther 2022;56:1318-132.
41. May B et al. Efficacy and tolerability of a fixed combination of peppermint oil and caraway oil in patients suffering from functional dyspepsia. Aliment Pharmacol Ther 2000; 14: 1671-1677. 2.
42. Rich G et al. A randomized placebo-controlled trial on the effects of Menthacarin, a proprietary peppermint and caraway oil preparation, on symptoms and quality of life in patients with functional dyspepsia. Neurogastroenterol Motil 2017 Nov;29(11), doi: 10.1111/nmo.13132. Epub 2017 Jul 10.
43. Madisch A et al. Menthacarin, a proprietary peppemint oil and caraway oil combination improves multiple complaints in patients with functional gastrointestinal disorders. A systematic Review and Meta-Analysis. Dig Dis 2023;41(3):522-532. doi: 10.1159/000528553. Epub 2022 Dec 9.
44. Storr M and Stracke B. Menthacarin for long-term treatment of functional dyspepsia – Results from a clinical trial follow-up. Z. Gastroenterol. 2023 Mar; 61(3): 257–267.
la gazette médicale
- Vol. 14
- Ausgabe 2
- März 2025