- Stuhlinkontinenz
Stuhlinkontinenz ist definiert als unwillkürlicher Verlust von festem oder flüssigem Stuhl. Bei der Urge-Inkontinenz kommt es zu unkontrolliertem Verlust bei wahrgenommenem Stuhldrang. Demgegenüber steht die passive Inkontinenz, bei welcher es unbemerkt zu Stuhlverlust kommt. Der Artikel fasst die aktuellen Abklärungsschritte und Therapieoptionen zusammen.
Die genaue Prävalenz von Stuhlinkontinenz ist unbekannt. Eine Review aus 2015 zeigt eine mittlere Prävalenz von 7.7%, wobei je nach Definition von Inkontinenz und untersuchter Studienpopulation ein grosser Unterschied von 2.0 – 20.7% besteht (1). Ein Geschlechterunterschied scheint nicht zu bestehen.
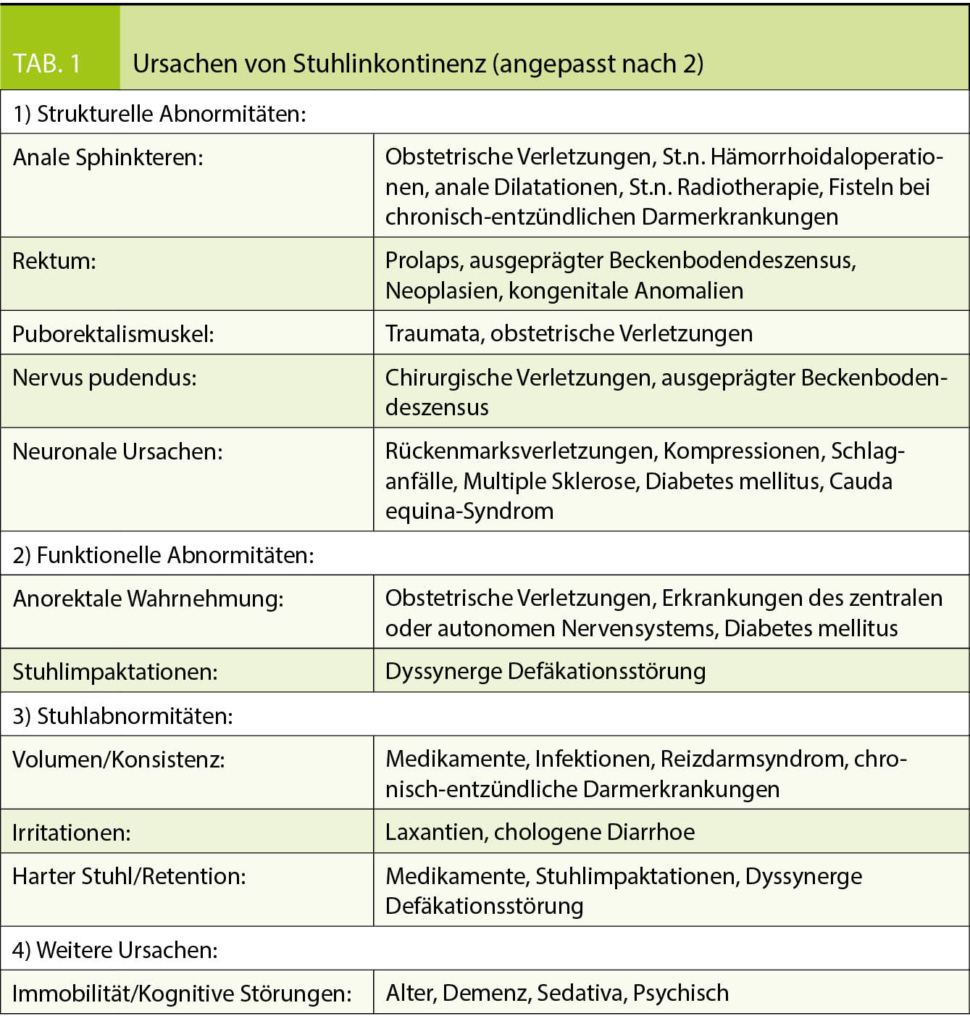
Als Hauptrisikofaktoren für Stuhlinkontinenz gelten Diarrhoe, zunehmendes Alter, Diabetes mellitus und gleichzeitige Urininkontinenz. Tabelle 1 zeigt in der detaillierteren Übersicht mögliche Ursachen für Stuhlinkontinenz (2).
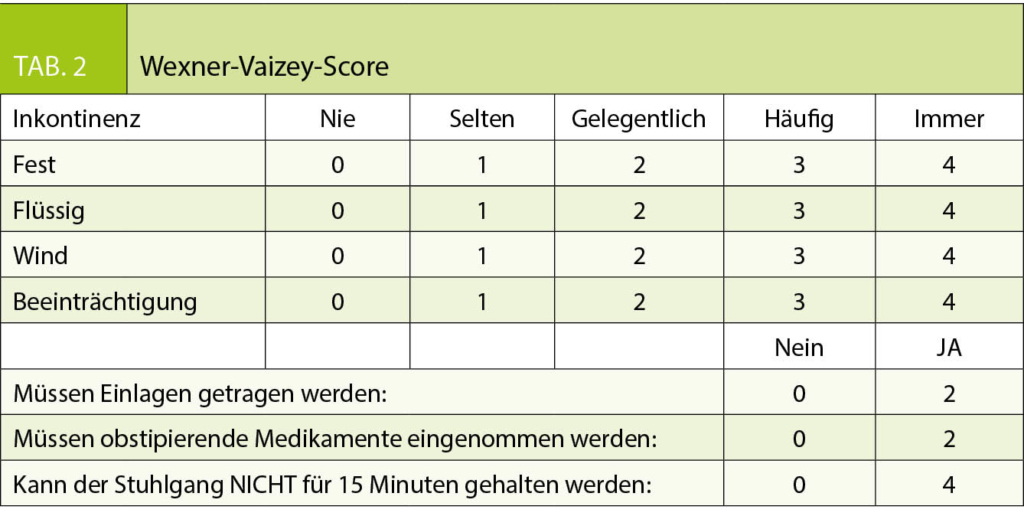
Zur Graduierung der Stuhlinkontinenz wird heutzutage am häufigsten der Wexner-Vaizey-Score verwendet (Tabelle 2). Maximal können 24 Punkte erreicht werden, was einer kompletten Stuhlinkontinenz entspricht.
Abklärungen
Nebst der genaueren Anamnese werden als weiter führende Abklärungen eine Endoskopie, eine anorektale Manometrie und ein endoanaler Ultraschall empfohlen.
In der Endoskopie sollten entzündliche oder neoplastische Veränderungen des Anorektums ausgeschlossen werden.
Bei der anorektalen Manometrie könnten die Druckwerte des M. sphincter ani internus (Ruhedruck) und des M. sphincter ani externus (Klemmdruck) gemessen werden.
Der M. sphincter ani internus ist ein zirkulärer Muskel von glatten Muskelzellen und wird über das autonome Nervensystem innerviert. Er kann daher nicht aktiv beeinflusst werden. Häufig wird bei passiver Inkontinenz ein isoliert zu tiefer Ruhedruck gemessen.
Der M. sphincter ani externus ist ein zirkulärer Muskel von quergestreifter Muskelzelle und wird über den N. pudendus (S3-S4) innerviert. Er kann somit aktiv kontrahiert und entspannt werden. Dabei sind weniger die Maximalkraft als die Mitteldruckwerte über 10 Sekunden für die Kontinenz entscheidend. Eine Insuffizienz des M. sphincter ani externus geht häufig mit einer Urge-Inkontinenz einher.
Nebst der Druckmessung kann bei der anorektalen Manometrie gleichzeitig noch die rektale Compliance (Rektumkapazität) und Perzeption (Wahrnehmungsschwelle) mitgemessen werden. Hierzu wird ein dehnbarer Ballon ins Rektum eingeführt und dann mit Luft- oder Flüssigkeit langsam gefüllt. Beispielsweise zeigen stuhlinkontinente Patienten mit Diabetes mellitus häufig eine herabgesetzte Wahrnehmung (erhöhte Schwelle) für Dehnungsreize im Rektum. Patientinnen und Patienten mit entzündlichen Veränderungen (Proktitis ulzerosa oder Strahlenproktitis) hingegen eine erhöhte Wahrnehmung (reduzierte Schwelle).
Der endoanale Ultraschall kann bei nachgewiesener Sphinkterinsuffizienz allfällig zugrunde liegende Sphinkterdefekte nachweisen. Abbildung 1 zeigt einen Normalbefund mit zirkulärem echoarmem Internusring. In der Abbildung 2 kann auf der anterioren Hemizirkumferenz (9-3 Uhr) der Internus nach obstetrischen Verletzungen nicht mehr abgegrenzt werden.
In ausgewählten Fällen, insbesondere bei vermutetem Beckenbodendeszensus oder präoperativ gewünschter Darstellung der Beckenorgane kann ergänzend eine Magnetresonanz-Defäkographie durchgeführt werden. Dabei können beim simulierten Anspannen/Pressen die intraabdominalen Bewegungen real-time dargestellt werden.
Therapiemöglichkeiten
Mit Quellmitteln kann versucht werden die Stuhlkonsistenz zu beeinflussen. Dies kann vor allem bei Inkontinenz wegen weicher, lockerer Stuhlkonsistenz helfen.
Loperamid hat nachgewiesen einen positiven Effekt bei Inkontinenz wegen zu wässriger Stuhlkonsistenz (3).
Die Biofeedbacktherapie ist eine gute und effektive Therapieoption bei Urge-Inkontinenz infolge Insuffizienz des M. sphincter ani externus. Hingegen kann eine isolierte Insuffizienz des Internus nicht mit Training beeinflusst werden. Hier hilft eine vorgängig durchgeführte anorektale Manometrie zur Unterscheidung.
Direkt injizierte Substanzen (beispielsweise Silikon) können bei isolierter Insuffizienz des Internus versucht werden, allerdings ist die Datenlage spärlich.
Eine chirurgische Reparatur des Analsphinkters kann bei nachgewiesenem Sphinkterdefekt und vorgängig erfolgloser Biofeedbacktherapie und/oder medikamentöser Beeinflussung durchgeführt werden.
Die sakrale Neuromodulation ist die nächste Option falls Medikamente/Biofeedback und Sphincterrepair keine Besserung der Inkontinenz erbracht haben (4). Bei dieser Methode werden die für die Kontinenz wichtigen Beckenbodennerven mittels Strom stimuliert. Ein Vorteil gegenüber anderen chirurgischen Verfahren ist sicher die Möglichkeit einer 14-tägigen Teststimulationsphase. Kommt es darunter zu einer Verbesserung der Kontinenz und verträgt der Patient die Elektrode kann in einem 2. Schritt der definitive Schrittmacher implantiert werden.
Weitere «high-end» chirurgische Möglichkeiten sind die Kolostomie, die dynamische Grazilisplastik oder der künstliche Sphinkterapparat. Diese Therapieformen sollten aber nur in spezialisierten Zentren evaluiert und durchgeführt werden.
FMH Gastroenterologie
Aerztehaus Fluntern
Zürichbergstrasse 70
8044 Zürich
marcel.halama@hin.ch
Der Autor hat in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
- Eine Stuhlinkontinenz kann Folge von strukturellen (postoperativ, neoplastisch, entzündlich, neuronal) und auch funktionellen Abnormitäten sein und wird auch durch allgemeine Erkrankungen und Stuhlabnormitäten beeinflusst
- Der Schweregrad einer Stuhlinkontinenz kann mit dem Wexner-Vaizey-Score abgeschätzt werden
- Die Diagnostik umfasst eine Endoskopie, eine anorektale Manometrie und ein endoanaler Ultraschall
- Die Basistherapie umfasst Quellstoffe, Loperamid und bei Urge-Inkontinenz infolge Insuffizienz des M. sphincter ani externus eine Biofeedbacktherapie.
1. Ng KS et al; Dis Colon Rectum 2015 ; 58 (12) : 1194
2. Lazarescu et al; Can J Gastroenterol; 2009; 23: 301
3. Markland et al; Dis Colon Rectum 2015 ; 58 (10) : 983-993
4. Matzel et al ; Lancet 2004 ; 363 (9417) : 1270
der informierte @rzt
- Vol. 9
- Ausgabe 5
- Mai 2019