- Perioperative Antikoagulation
Die natürliche Hämostase befindet sich in einem Gleichgewicht der Wirkung von prokoagulatorischen und antikoagulatorischen Faktoren. Eine Entgleisung endet oft entweder in Blutung oder in Thrombose. Der operative Eingriff ist eine Intervention, welche trotz kontrollierter blutstillender Verhältnisse eine prothrombotische Wirkung induziert. Bestimmende Faktoren dafür sind die Lokalisation des chirurgischen Traumas, die Dauer des Eingriffs, die Lädierung grosser Gefässe.
L’ hémostase naturelle se situe dans un équilibre de facteurs procoagulatoires et anticoagulatoires. Le déraillement se termine souvent par un saignement ou une thrombose. L’ intervention chirurgicale est une intervention qui induit un effet prothrombotique malgré une hémostase contrôlée. Les facteurs décisifs à cet égard sont l’ emplacement du traumatisme chirurgical, la durée de l’ opération et la lésion des gros vaisseaux.
Die postoperative Thromboseneigung wurde bereits in den 70er Jahren erkannt und systematisch mit Heparinen behandelt. Die niedermolekularen Heparine (LMWH) waren Produkte, welche an der Handhabung, Effizienz und Sicherheit dem älteren unfraktionierten Heparin überlegen waren und sich deswegen schnell als indizierte Mittel zur postoperativen Thromboseprophylaxe durchgesetzt haben. Mittlerweile haben die Vielfalt der Operationen, die Verfeinerung der operativen Techniken und die Entwicklung neuer Antikoagulantien die Planung der Thromboseprophylaxe, sowohl für eine bestehende Antikoagulation wie auch für den rein postoperativen Thromboseschutz zur Herausforderung gemacht.
Perioperative Überbrückung einer vorbestehenden Antikoagulation («Bridging»)
Vorhofflimmern und venöse thromboembolische Ereignisse treten mit zunehmendem Lebensalter häufiger auf. Auf Grund der Alterung der Gesellschaft ist es somit wahrscheinlich, dass immer mehr Menschen mit einer längerfristigen Antikoagulation behandelt werden. Wenn bei antikoagulierten Patienten ein invasiver Eingriff ansteht, stellen sich 3 Schlüsselfragen:
- Wie hoch ist das Risiko für den Patienten, wenn die Antikoagulation nicht unterbrochen wird?
- Wie hoch ist das Risiko für den Patienten, wenn die Antikoagulation unterbrochen wird?
- Wie hoch ist die Sicherheit und Wirksamkeit, wenn ein alternatives Antikoagulans zur Überbrückung («Bridging») eingesetzt wird?
Das klassische Konzept der Bridging-Therapie war die Überbrückung einer Antikoagulatin mit einem Vitamin-K Antagonisten (VKA; z.B. Phenprocoumon) mit einem unfraktionierten Heparin mit Dosisanpassung anhand der aktivierten Thromboplastinzeit (aPTT). In den letzten 20 Jahren wurde jedoch das unfraktionierte Heparin (LMWH) ersetzt. Diese können bei normaler Nierenfunktion in therapeutischer Dosierung subkutan und ohne Laborkontrolle in einem ambulanten Setting verabreicht werden und beinhalten zudem ein eindeutig kleineres Risiko für die Entwicklung einer Heparin-induzierten Thrombopenie. Mit der Einführung der noch neueren direkten oralen Antikoagulanzien (DOACs; z.B. Dabigatran, Apixaban, Edoxaban, Rivaroxaban) hat sich das Management der perioperativen Antikoagulation nochmals deutlich verändert.
Blutungsrisiko
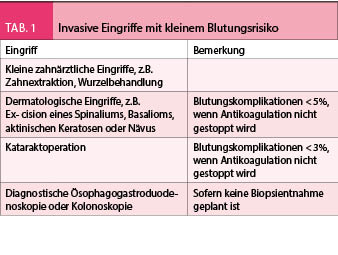
Nicht jeder operative Eingriff geht mit dem gleich grossen Blutungsrisiko einher. Bei einigen Eingriffen ist das Blutungsrisiko so klein, dass eine orale Antikoagulation gar nicht unterbrochen werden muss. Daher handelt es sich vor allem um kleine zahnärztliche, dermatologische oder ophthalmologische Eingriffe (Tab 1). Bei diesen Eingriffen lassen sich Blutungen in den meisten Fällen auch bei antikoagulierten Patienten mit lokalen Massnahmen bestens beherrschen. Das Blutungsrisiko muss jedoch selbstverständlich für jeden Patienten individuell abgeschätzt werden.
Thromboembolierisiko
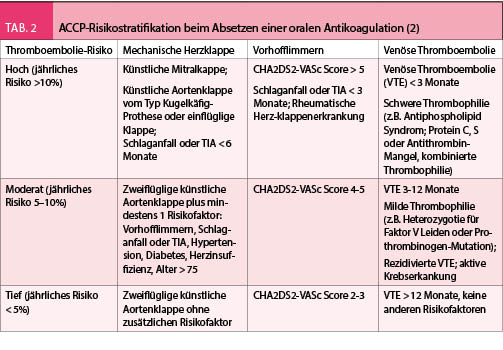
Die häufigsten Gründe für eine zeitliche unlimitierte Antikoagulation sind die Schlaganfallprophylaxe beim Vorhofflimmern, die unprovozierte und/oder rezidivierte venöse Thromboembolie und der mechanische Herzklappenersatz. Wird die Antikoagulation mit einem VKA durchgeführt, so ist bei einem präoperativen Absetzen des VKA eine überbrückende Antikoagulation nur bei einem relevanten Thromboembolierisiko notwendig. Dieses Risiko ist sowohl von der Indikation der Antikoagulation als auch vom Patienten selber abhängig. Gemäss den ACCP Guidelines von 2012 werden die Patienten bezüglich ihres jährlichen Thromboembolierisikos in der 3 Risikokategorien stratifiziert (Tab. 2). Während die Guidelines für Patienten mit einem hohen Risiko grundsätzlich ein Bridging empfehlen, kann bei Patienten mit einem niedrigen Risiko die Antikoagulation in den meisten Fällen ohne Bridging mit einer alternativen Substanz unterbrochen werden. Bei Patienten mit intermediärem Risiko müssen sowohl die Risiken des jeweiligen Eingriffs als auch die individuellen Risiken des Patienten zur Festlegung der Strategie einbezogen werden.
Praktisches Vorgehen bei Marcoumar und anderen VKA
Grundsätzlich ist das periprozedurale Blutungs- und Thromboembolie-Risiko eines invasiven Eingriffs bei allen Patienten mit dauerhafter Antikoagulation höher als bei Patienten ohne Antikoagulation. Diese Tatsache ist unabhängig von den Modalitäten der überbrückenden Antikoagulation und muss mit den Patienten in einem Aufklärungsgespräch besprochen werden. Die publizierten Leitlinien zur Überbrückung einer Antikoagulation beziehen sich meistens auf Warfarin, welches eine deutlich kürzere Halbwertszeit als das Pheprocoumon (Marcoumar®) hat. Beispielsweise wird in den ACCP Guidelines empfohlen, eine VKA-Therapie etwas 5 Tage vor einem invasiven Eingriff mit relevantem Blutungsrisiko zu stoppen und dann falls notwendig auf eine Bridging-Substanz umzusteigen. In der Praxis bewährt es sich jedoch, Phenprocoumon schon mindestens 7 Tage vor einem geplanten Eingriff zu pausieren. Sobald die INR unter 2.0 abgefallen ist, muss in Abhängigkeit des Risikos (Tab. 2) die Bridging-Therpie gestartet werden. Die aktuellen Guidelines sehen UFH und LMWH als gleichwertig an, enthalten jedoch keine genauen Angaben über die zu verwendende LMWH-Dosierung. In der Praxis werden heutzutage vorwiegend LMWH zum Bridging verwendet und es hat sich bewährt, die Dosierung Risiko-adaptiert zu wählen: bei hohem Thromboembolierisiko LMWH in therapeutischer Dosis (200 E/kg Körpergewicht/Tag); bei moderatem Thromboembolierisiko LMWH in (hoch-) prophylaktischer Dosis (100 E/kg Körpergewicht/Tag). Gemäss den ACCP Guidelines soll das UFH 6h vor einem invasiven Eingriff gestoppt werden, die letzte Dosis LMWH soll nicht später als 24h vorher appliziert werden. Es muss unbedingt sichergestellt werden, dass zum Zeitpunkt des Eingriffs keine relevante VKA-Wirkung mehr vorliegt. Dehalb empfiehlt es sich, die INR 24h vor dem Eingriff nochmals zu kontrollieren. Sollte sie zu diesem Zeitpunkt noch nicht unter 1.5 abgefallen sein, kann eine Dosis Vitamin K (z.B. 2-10 mg Konakion® p.o. oder i.v.) appliziert werden, um eine Korrektur bis zum Zeitpunkt des Eingriffs herbeizuführen (INR am Morgen des Eingriffs nochmals messen!). Nach erfolgtem Eingriff soll 48-72h bis zur Wiederaufnahme einer therapeutischen Antikoagulation in jedem Fall erst dann erfolgen, wenn klinisch kein relevanted Blutungsrisiko mehr besteht. Bei Patienten mit hohem Thromboembolierisiko kann postoperativ die Zeit bis zum Einsetzen einer therapeutischen Antokoagulation mit LMWH in prophylaktischer Dosierung überbrückt werden. Sobald postoperativ die Hämostase gesichert ist, darf auch der VKA wieder begonnen werden. DIe Bridging-Substanz sollte so lange gegeben werden, bis ein therapeutischer INR an zwei aufeinander folgenden Tagen dokumentiert ist.
Praktisches Vorgehen bei DOAC
Das perioperative Procedere bei Patienten, die mit einem DOAC antikoaguliert sind, ist auf Grund der relativ kurzen Halbwertszeit dieser Substanz denkbar einfach. In der Regel sollen DOAC 24h vor einem invasiven Eingriff mit Blutungsrisiko gestoppt werden, bei hohem Blutdruckrisiko schon 48h vorher. Sobald nach erfolgtem Eingriff die lokale Hämostase wieder gewährleistet ist, kann dann die Antikoagulation mit dem DOAC wieder aufgenommen werden, oft schon ab dem ersten postoperativen Tag. Bei hohem Blutungsrisiko ist es auch möglich, kurzzeitig prophylaktische Dosen zu verwenden. Bezüglich der Details für die einzelnen Substanzen ist auf www.swissmedicinfo.ch verwiesen. Ein eigentliches Bridging mit LMWH entfällt also bei den DOACs, weil die Pharmakokinetik dieser Medikamentenklassen identisch ist. Gelegentlich kann es aber notwendig sein, postoperativ beispielsweise bei nicht möglicher peroraler Medikamenteneinnahme vorübergehend auf eine parenterale Substanz auszuweichen.
Postoperative Thromboseprophylaxe ohne vorbestehende Antikoagulation
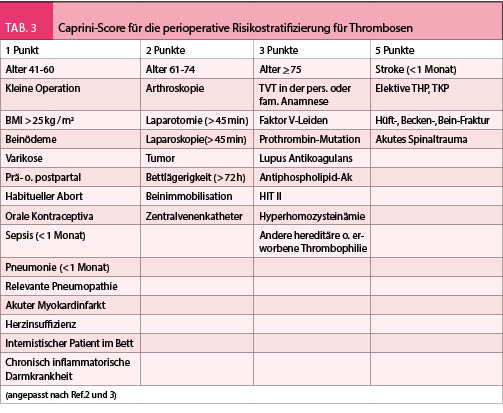
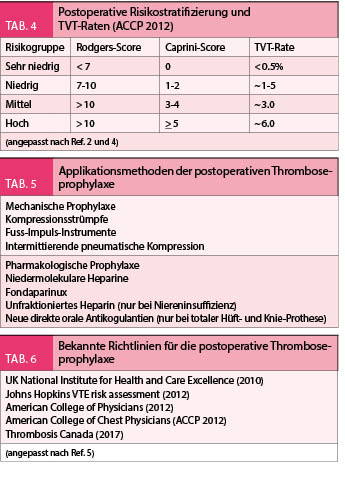
Das Risiko für postoperative Thrombosen wurde in verschiedenen Studien bereits früher vor 15 Jahren abgeschätzt, z.B. bei der totalen Hüft- oder Knieprothese lag die Rate der postoperativen Thrombosen zwischen 25-40%. Die prophylakrische postoperative Behandlung mit LMWH konnte diese Rate auf < 20% reduzieren. Neuere Operationstechniken und Materialien haben aktuell dieses Risiko auf 4-5% reduziert. Dem entsprechend besteht eine Tendenz das postoperative Risiko genauer zu gewichten und die Patienten demnach in Risikogruppen für Thrombosebildung zu stratifizieren. Dafür werden detaillierte Score-Systeme verwendet (z.B. Caprini-Score oder Rodgers-Score, Tab. 5), welche verschiedene klinische, anamnestische und medikamentöse Parameter, die mit Thrombosen assoziiert sind, festhalten. Die Stratifizierung kategorisiert die Patienten in 4 Stufen (sehr niedrig, niedrig, mittel, hoch). Die geschätzte Thromboserate je nach Stufe wird in Tabelle 4 angegeben. Je nach Risikokategorie wird ebenfalls die Auswahl der Form der Prophylaxe empfohlen, mechanische oder pharmakologische (Tab. 5). Je nach Operationstyp kann diese Empfehlung auch variieren.
In der Literatur sind verschiedene Richtlinien für die Handhabung der perioperativen Thromboseprophylaxe bekannt (Tab. 6). Alle münden in die gleiche Richtung ein, eine Risikostratifizierung z.B. nach Caprini-Score wird präoperativ verlangt, je nach Risikokategorie wird die Art der Prophylaxe ausgewählt. Bei den nicht-orthopädischen Eingriffen mit sehr niedrigem oder niedrigem Thromboserisiko werden konservative oder mechanische Massnahmen empfohlen, für mittleres oder hohes Thromboserisiko ist die pharmakologische Prophylaxe die bessere Auswahl. In der Schweiz sind die Empfehlungen der ACCP 2012 breiter bekannt. Die pharmakologische Prophylaxe wird mit niedermolekularen Heparinen appliziert (Dalteparin, Enoxaparin, Nadroparin), die Dosierung bleibt bei den allermeisten Fällen fixiert auf ca. 75 E/ Kg KG/ Tag als subkutane Gabe einmal pro Tag. Einige Einschränkungen sind hier zu berücksichtigen (kleines Gewicht < 50 Kg, Niereninsuffizienz GFR < 30 ml / min), welche zur Dosisadaptation führen. Die Herstellerangaben der Produkte sind hier zu befolgen.
Je nach Operation und Gewichtung der Blutungskonsequenzen kann diese Dosierung reduziert werden (z.B. ZNS-Operationen initial mit halbierter Dosis der LMWH).
Dauer der Thromboseprophylaxe
Lange sahen die Empfehlungen vor, die Thromboseprophylaxe nur während der Hospitalisation zu verabreichen. Neuere Studien insbesondere bei den orthopädischen Eingriffen empfehlen eine Dauer von 5 Wochen postoperativ, bzw. bei persistierenden Risikofaktoren für Thrombosen (Beinimmobilisation, Bettlägerigkeit) auch länger.
Start der Prophylaxe präoperativ oder postoperativ
Die offizielle Zulassung der LMWH in Europa schreibt vor, dass die erste Gabe der Prophylaxe 12h präoperativ verabreicht werden soll. Die Rationale dafür liegt Jahrzehnte zurück, als man festgestellt hatte, dass die meisten postoperativen Thrombosen bereits intraoperativ initiiert wurden. Mit der präoperativen Gabe wollte man allfällige thrombogene Herde im Gefässnetz Stunden vor der Provokation unterdrücken, sodass intraoperativ keine Thrombusbildung aktiviert wird. Mittlerweile haben Vergleichsstudien aus den USA mit Enoxaparin, wie auch die Vergleichsstudie mit den neuen direkten Antikoagulantien in der orthopädischen Chirurgie gezeigt, dass die präoperative Gabe eines LMWH keine Vorteile bedeutet. Demzufolge erlaubt die Empfehlung der ACCP 2012 die erste Gabe sowohl 12h präoperativ wie 12h postoperativ zu planen. Kürzeres postoperatives Fenster war mit mehr Blutungskomplikationen assoziiert.
Aspirin zur postoperativen Thromboseprophylaxe
Bereits seit den 90er Jahren war es bekannt, dass Aspirin einen Schutz gegen Thrombosen ausüben könnte, allerdings mit einer Effizienz von nur 50-60%. Im Vergleich zu den LMWH war die eindeutig ungenügend und daher war Aspirin nie für diese Indikation empfohlen. Neuere Daten signalisieren hier eine Wende. Eine kürzlich publizierte Vergleichsstudie zwischen Aspirin 100 mg/Tag und Rivaroxaban 10mg/Tag in einer selektionierten Patientenkohorte mit totaler Hüft- oder Knieprothese hat gezeigt, dass Aspirin gleich effizient und sicher war wie Rivaroxaban. Die Europäische Gesellschaft für Anästhesie hat dies bereits in den offiziellen Empfehlungen aufgenommen, allerdings für Patienten mit niedrigem Thromboserisiko oder für Patienten mit hohem Blutungsrisiko (1). Diese Empfehlung kann leider nicht auf Patienten mit nicht-orthopädischen Eingriffen übertragen werden.
Zentrum für Labormedizin, Hämostase- und Hämophiliezentrum St. Gallen
Frohbergstrasse 3
9001 St. Gallen
lukas.graf@zlmsg.ch
Klinik für Hämatologie
Hämatologische Diagnostik Labormedizin
Universitätsspital Basel und Blutspendezentrum beider Basel SRK
Petersgraben 4
4031 Basel
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Beitrag deklariert.
- Ein Bridging der therapeutischen Antikoagulation mit Vitamin K-Antagonisten kann mit einem LMWH je nach Thromboserisiko in therapeutischer (200 E/Kg KG / d) oder subtherapeutischer (100 E / Kg KG / d) Dosierung erfolgen.
- Ein eigentliches Bridging der DOAC mit LMWH entfällt aufgrund der identischen Pharmakokinetik.
- Postoperativ sind 2018 niedrigere Thromboserisiken zu beobachten als vor 15 Jahren.
- Die Risikostratifizierung für Thrombosen (Caprini- o. Rodgers-Score) postoperativ definiert die Art (mechanisch oder pharmakologisch) und die Dauer der Thromboseprophylaxe.
- Aspirin kann neu bei orthopädischen Eingriffen (Total-Knie- oder Hüftprothese) bei Patienten mit niedrigem Thromboserisiko postoperativ zur Thromboseprophylaxe eingesetzt werden (100 mg/d p.o.)
Messages à retenir
- Le pontage de l’ anticoagulation thérapeutique avec des antagonistes de la vitamine K peut être effectué avec un LMWH à des doses thérapeutiques (200 E / Kg KG / j) ou sous-thérapeutiques (100 E / Kg KG / j), selon le risque de thrombose.
- En raison de la pharmacocinétique identique, il n’ est pas nécessaire d’établir un pontage entre le DOAC et le LMWH
- En postopératoire, le risque de thrombose est plus faible en 2018 qu’ il y a 15 ans.
- La stratification du risque de thrombose (score Caprini ou Rodgers) post-opératoire définit le type (mécanique ou pharmacologique) et la durée de la prophylaxie thrombotique.
- L’aspirine peut maintenant être utilisée en postopératoire pour prévenir la thrombose (100 mg / j p.o.) dans les procédures orthopédiques (prothèse totale du genou ou de la hanche) chez les patients présentant un faible risque de thrombose.
Literatur
1. Jenny J-Y, Pabinger I, Samama CM. European guidelines on perioperative venous thromboembolism prophylaxis: Aspirin. Eur J Anaesthesiol. England; 2018 Feb;35(2):123–9.
2. Gould MK, Garcia DA, Wren SM, Karanicolas PJ, Arcelus JI, Heit JA, et al. Prevention of VTE in nonorthopedic surgical patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. United States; 2012 Feb;141(2 Suppl):e227S–e277S.
3. Caprini JA. Risk assessment as a guide for the prevention of the many faces of venous thromboembolism. Am J Surg. United States; 2010 Jan;199(1 Suppl):S3-10.
4. Falck-Ytter Y, Francis CW, Johanson NA, Curley C, Dahl OE, Schulman S, et al. Prevention of VTE in orthopedic surgery patients: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. United States; 2012 Feb;141(2 Suppl):e278S–e325S.
5. Murphy PB, Vogt KN, Lau BD, Aboagye J, Parry NG, Streiff MB, et al. Venous Thromboembolism Prevention in Emergency General Surgery: A Review. JAMA Surg. United States; 2018 May;153(5):479–86.
info@herz+gefäss
- Vol. 8
- Ausgabe 6
- November 2018







