- AGLA Update Meeting 2021
Breakout Session: Jenseits der Guidelines – Hyperlipidämie
Fallbeispiele von Prof. Dr. med. Isabella Sudano, Kardiologische Klinik USZ
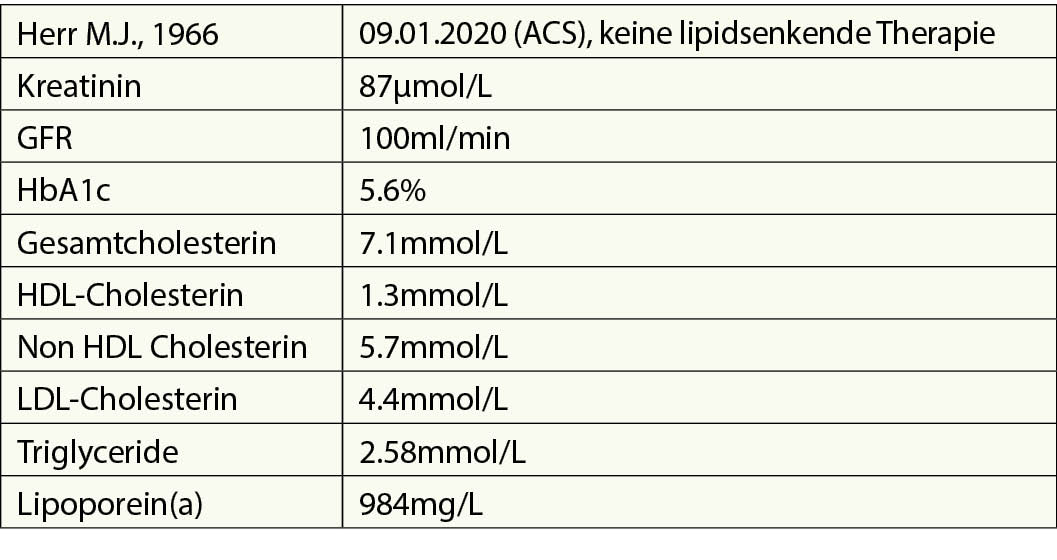
Fall 1: Herr M.J., 1966
Familienanamnese: Keine vorzeitige ASCVD, Diabetes, Bluthochdruck. Ob jemand Hypercholesterinämie hatte/hat, ist unbekannt. Ex-Raucher (40 PJ) hat Ende 2015 mit dem Rauchen aufgehört. 1985 M. Basedow. Eigentlich normale Schilddrüsenfunktion ohne Therapie. Größe 185 cm Gewicht 77 Kg, BMI 22,5 Kg/m2. Blutdruck (sitzender Mittelwert 2-3 Messwerte) 130/78 mmHg, HF 67/Min.
9. Jan 2020 STEMI (RIVA-Stenose): 2 PTCA/Stenting
Die Referentin zeigte die Risikoschätzung nach den ESC Guidelines 2021. Der Patient hat ein sehr hohes Risiko aufgrund seiner persönlichen Anamnese.
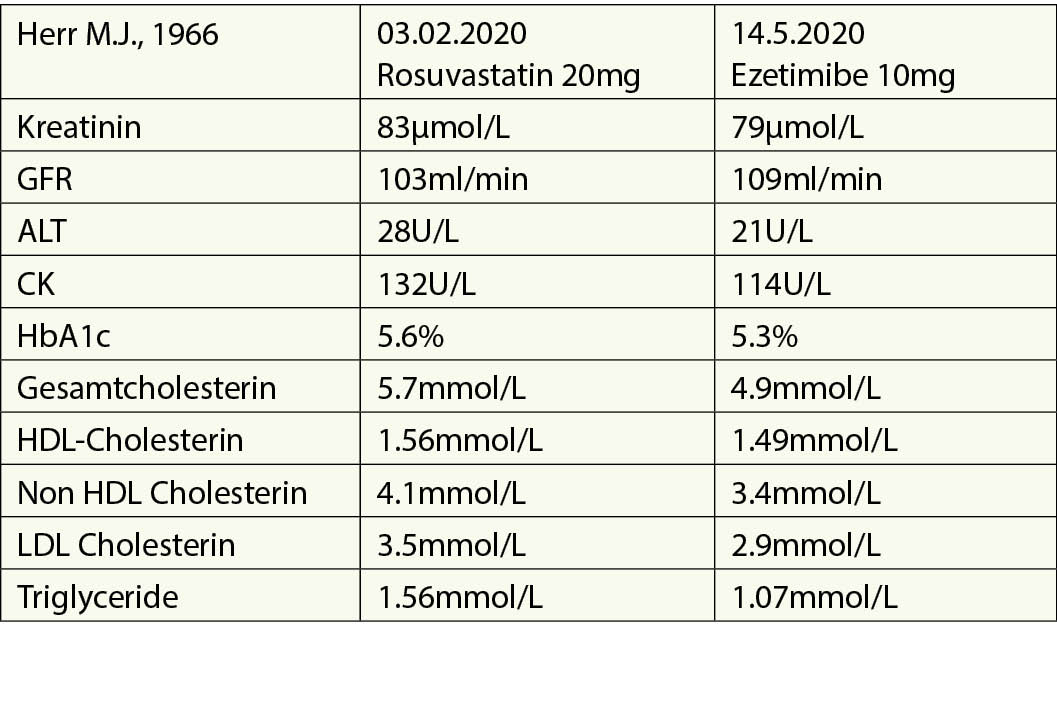
Während des Krankenhausaufenthalts Beginn mit Rosuvastatin 20 mg. Am Ende der stationären Rehabilitation wurde mit Ezetimibe/Rosuvastatin 10/20 mg begonnen.
Die Referentin weist auf die Zielwerte für LDL-Cholesterin entsprechend den verschiedenen Risikokategorein, sehr hohes Risiko, hohes Risiko, moderates Risiko du niedriges Risiko hin.
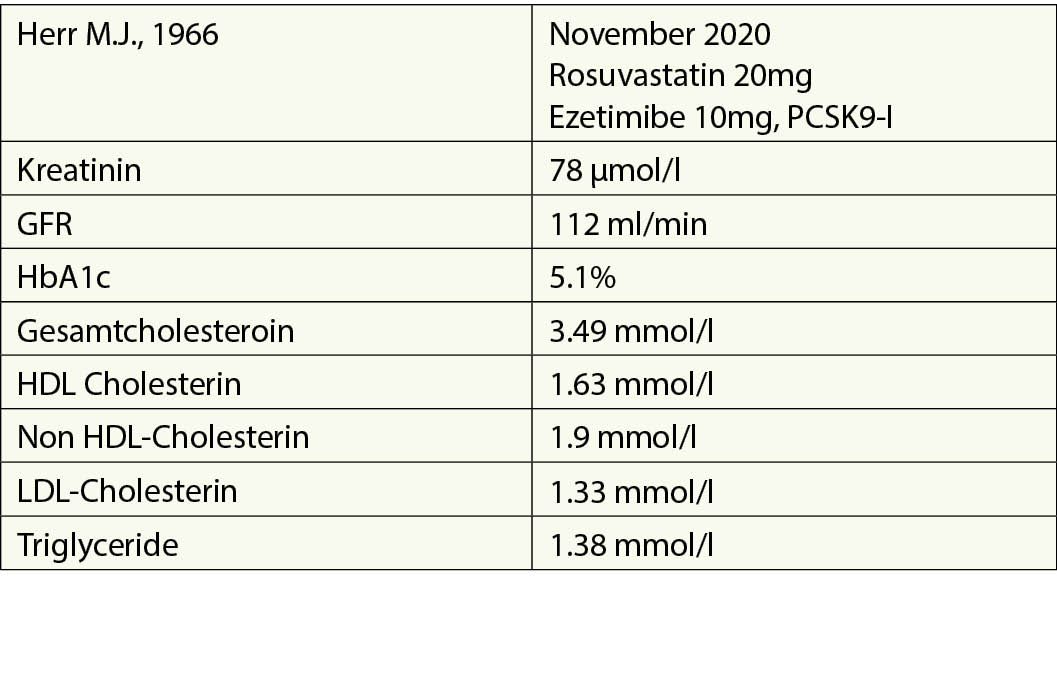
Welche Massnahmen sind im Falle von Herrn M.J. zu treffen?
A) Ich bin mit dieser Reduktion zufrieden.
B) Ich würde ein Fibrat hinzufügen
C) Ich würde einen PCSK9-Inhibitor hinzufügen
D) Ich würde eine hohe Dosis Omega 3 hinzufügen
E) Ich würde Bempedoinsäure hinzufügen
Die Referentin gab dazu den folgenden Kommentar
Fibrate und Omega-3 Fettsäuren sind wirksam zur Triglyceridsenkung, sie haben aber keinen Nutzen bei isolierter Hypercholesterinämie gezeigt.
Die zu treffenden Massnahmen sind entsprechend dem Algorithmus der ESVC Guidelines.
Die Erfassung des kardiovaskulären Gesamtrisikos, die Bestimmung des LDL-Cholesterinbasiswerts, die Beurteilung der Indikation für eine medikamentöse Behandlung, falls eine solche indiziert die Bestimmung des LDL-Cholesterin-Zielwerts, falls keine Indikation zur medikamentösen Therapie, Lebensstilberatung und Lebensstilintervention. Bei medikamentöser Therapie hochpotentes Statin in höchster tolerierter Dosis zur Zielerreichung, falls Ziel erreicht jährliche oder falls notwendig häufigere Überwachung. Falls Ziel nicht erreicht Zugabe von Ezetimibe. Falls Ziel nicht erreicht Zugabe eines PCSK9 Hemmers (bei Sekundärprävention oder Primärprävention bei FH und einem weiteren Hauptrisikofaktor. In der Primärprävention bei Patienten mit sehr hohem Risiko aber ohne FH.
Die PCSK9-Inhibitoren sollen bei Patienten mit sehr hohem Risiko für ASCVD eingesetzt werden, wenn die Zielwerte nicht mit Statinen und Ezetimibe erreicht werden. Allerdings erlauben die Limitationen des Bundesamts für Gesundheit für die Verschreibung von PCSK9-Hemmern in der Schweiz nicht die 1:1-Umsetzung der ESC/EAS-Empfehlungen.
Evolocumab und Alirocumab werden durch die Krankenkasse nur bezahlt, wenn über mindestens drei Monate mit der maximal verträglichen Dosierung einer intensivierten LDL-C-senkenden Therapie mit mindestens zwei verschiedenen Statinen mit oder ohne Ezetimib (oder Ezetimib mit oder ohne weiteren Lipidsenker bei
Statinunverträglichkeit) die folgenden LDL-C-Werte nicht erreicht werden können: In der Sekundärprävention nach einem klinisch manifesten, atherosklerotisch bedingten, ischämischen kardiovaskulären Ereignis, wenn LDL-C trotzdem >2,6 mmol/l beträgt.
In der Primärprävention bei Erwachsenen und Jugendlichen ab einem Alter von 12 Jahren (nur Evolocumab) mit einer schweren heterozygoten oder homozygoten FH und LDL-C >5,0 mmol/l oder >4,5 mmol/l, wenn DM, erhöhtes Lp(a) >50 mg/dl (120 nmol/l) oder ausgeprägte arterielle Hypertonie bestehen.
Evolocumab kann auch bei Erwachsenen und Jugendlichen ab einem Alter von 12 Jahren mit einer homozygoten familiären Hypercholesterinämie eingesetzt werden.
Wenn die Kosten für den Einsatz von PCSK9-Inhibitoren nicht erstattet werden, ist die zusätzliche Gabe von Bempedoinsäure oder eines Gallensäureaustauschharz eine praktikable Alternative für Patienten mit sehr hohem Risiko und hohen LDL-C-Werten, die eine zusätzliche LDL-C-Senkung ermöglicht.
Bempedoinsäure senkt das LDL-Cholesterin um bis zu 18%, in Kombination mit Ezetimibe um ca. 36%. Hs-CRP wird von Bempedoinsäure ebenfalls gesenkt (-31.9%, in Komination mit Ezetimibe um 35.1%).
Auch für Bemedoinsäure (Nilemdo) und Bempedoinsäre-Ezetimibe (Nustendi) gibt es Limitationes:
Nilemdo wird zusätzlich zu einer Diät und in Kombination mit einem Statin, in der maximal verträglichen Dosis, mit oder ohne andere lipidsenkende Therapien angewendet zur Behandlung bei Erwachsenen mit klinisch manifester atherosklerotischer kardiovaskulärer Erkrankung oder heterozygoter familiärer Hypercholesterinämie, die eine zusätzliche LDL-C-Senkung benötigen.
Die Wirkung von Nilemdo auf die kardiovaskuläre Morbidität und Mortalität ist bisher noch nicht bestimmt.
Nustendi ist indiziert begleitend zu einer Diät bei Erwachsenen mit heterozygoter familiärer Hypercholesterinämie oder mit klinisch-manifester atherosklerotischer kardiovaskulärer Erkrankung:
wenn die LDL-C-Ziele mit einer maximal verträglichen Statin-Dosis zusätzlich zu Ezetimibe oder Bempedoinsäure nicht erreicht werden, bei Patienten, die bereits mit der Kombination aus Bempedoinsäure und Ezetimibe als separate Tabletten behandelt werden.
Die Wirkung von Ezetimibe und Bempedoinsäure auf die kardiovaskuläre Morbidität und Mortalität ist nicht bestimmt.
Was ist mit Inclisiran?
Inclisiran ist synthetische kleine interferierende RNA (siRNA), konjugiert mit triantennärem GalNAc-Kohlenhydrat. Inclisiran
nutzt den natürlichen RNA-Interferenz-Mechanismus, um die PCSK9-mRNA abzubauen und ihre Umwandlung in ein Protein zu verhindern. Inclisiran ist die erste siRNA zur Behandlung von Hypercholesterinämie. Mit Inclisiran, welches nur alle 6 Monate subkutan verabreicht wird, wurde in den ORION-Studien eine Senkung des LDL-Cholesterinspiegels um etwa 50 % erreicht.
Inclisiran (Leqvio) ist indiziert bei Erwachsenen mit Hypercholesterinämie (einschliesslich heterozygoter familiärer Hypercholesterinämie) oder gemischter Dyslipidämie begleitend zu einer Diät:
- entweder in Kombination mit einer maximal tolerierten Statin-Dosis mit oder ohne andere lipidsenkende Therapien bei
Patienten, die eine zusätzliche LDL-C-Senkung benötigen, oder - allein oder in Kombination mit anderen lipidsenkenden Therapien bei Patienten, die Statin-intolerant sind oder für die Statine kontraindiziert sind.
Fall 2: Frau J.N., 1948
Familienanamnese: Vater war Raucher, hatte einen hohen Cholesterinspiegel und Bluthochdruck, erlitt im Alter von 67 Jahren einen Herzinfarkt und starb plötzlich im Alter von 72 Jahren.
Mutter mit Bluthochdruck, starb im Alter von 81 J. (ischämischer Schlaganfall).
Ein jüngerer Bruder starb an Prostatakrebs im Alter von 69 Jahren.
Persönliche Vorgeschichte. Raucher (40 J.), hat 1999 mit dem Rauchen aufgehört. Seit der Pensionierung täglicher Spaziergang mit dem Hund (BMI 27,1 kg/m2). Normaler Blutdruck und Blutzucker.
1999: Plaque in der Halsschlagader (30% links und 30% rechts). Keine Symptome. TC 6,8 mmol/L, HDL-C 0,67 mmol/l, non-HDL-C 6,1 mmol/l, LDL-C 5,5 mmol/L, Triglyceride. 1,40 mmol/l
Es wurde eine Therapie mit Atorvastatin 40 mg eingeleitet, und sie hört auf zu rauchen.
2002: Die Therapie mit Atorvastatin wurde in Absprache mit dem Hausarzt wegen SAMS und normaler CK abgesetzt. Zu diesem Zeitpunkt wurde keine weitere Therapie vorgeschlagen.
2004: Plaque in der Halsschlagader (aktuell 50% links und 60% rechts) TC 6,2 mmol/l, HDL 1,32 mmol/l, non-HDL 4,9 mmol/l, LDL 4,6 mmol/l, Trigyceride 0,56 mmol/l
Nutzen und Schaden einer Statintherapie
Nutzen:
Schlaganfallrisiko:16% Risikoreduktion für totalen Schlaganfall, 21% für ischämischen Schlaganfall
Risiko für schwere koronare Ereignisse: 27% Risikoreduktion für nicht tödlichen MI, 20% für Koronartod, 25% Risikoreduktion für Revaskularisierungsprozeduren.
Unerwünschte Effekte (Nat Rev Cardiol 2018;15:757-769)
Kognitive Dysfunktion: keine Evidenz
Risiko für hämorrhagischen Schlaganfall: kleine Zunahme bei Personen mit vorgängigem Schlaganfall
Lebesymptome/-Krankheiten: Klinisch signifikante Erhöhungen der Leberenzyme. Inzidenz für Leberversagen 1:100’000
Inzidenz für neu erworbenen Diabetes: Moderate Statintherapie 0.1%/Jahr, hochintensive Statintherapie 0.2%/Jahr.
Inzidenz von Muskelsymptomen/-Krankheiten: SAMS 10-29% in Beobachtungsstudien und 1-2% in RCTs, Myopathie 1/1000, Rhabdomyolyse 1/10 000.
Erwäge Statin fortfahren/Statin Neubeginn bei Statin-bedingten Muskelsymptomen:
- wenn symptomatisch und CK < 4 x ULN 2-4 Wochen wash out. Wenn die Symptome persistieren Statin-Wiederholungsversuch, Suche nach einem anderen Grund. Wenn die Symptome sich verbessern zweites Statin bei gebräuchlicher oder Startdosis. Wenn die Symptome wiederkehren niedrig dosiertes drittes (potentes) Statin oder wirksames Statin an alternativen Tagen oder ein zweimal pro Woche.
- CK ≥4 x ULN: 6 Wochen wash out und Normalisierung der Symptome niedrig dosiertes drittes potentes Statin oder wirksames Statin mit Alternativ-Tages- oder einmal/zweimal wöchentlicher Behandlungsstrategie
Das Ziel ist die Erreichung des LDL-Cholesterinzieles mit der maximal tolerierten Statindosis. Zugabe von Ezetimibe, Zugabe eines PCSK9 Hemmers (I/A Empfehlung für Patienten in der Sekundärprävention (sehr hohes Risiko). I/C Empfehlung für Primärprävention FH Patienten mit einem weiteren Hauptrisikofaktor (hohes Risiko). IIb/C Empfehlung für Primärprävention Hochrisikopatienten aber ohne FH. Die Gabe eines Gallensäureaustauschharzes kann auch in Betracht gezogen werden (IIb/C Empfehlung).
Der kardiovaskuläre Nutzen einer Langzeit Statintherapie überwiegt die potentiellen Risiken bei weitem.
Frau J.N., 1948
2013 ACS STEMI wegen RCA- und RIVA-Stenose behandelt mit 3 PTCA/Stenting. HbA1c 5.0% TC 6.0 mmol/l, HDL 1.14 mmol/l, non-HDL 4.9 mmol/l, LDL 4.0 mmol/l, Trigl. 2.1 mmol/l. Therapie mit Ezetimibe/Rosuvastatin 10/10 wurde begonnen. Abbruch der Rosuvastatin-Therapie nach 5 Monaten aufgrund von SAMS (CK unbekannt)
2020: Ischämischer Schlaganfall: Monotherapie mit Ezetimibe 10 mg. TC 4,9 mmol/L, HDL 1,39 mmol/l, Nont-HDL 3,3 mmol/l, LDL 2,9 mmol/l, Trigl. 1,04 mmol/l.
Was soll man tun ?
A) Ich würde wieder ein Statin versuchen
B) Ich lasse die Therapie so wie sie ist
C) Ich würde einen PCSK9-Inhibitor hinzufügen
D) Ich würde Bempedoinsäure hinzufügen
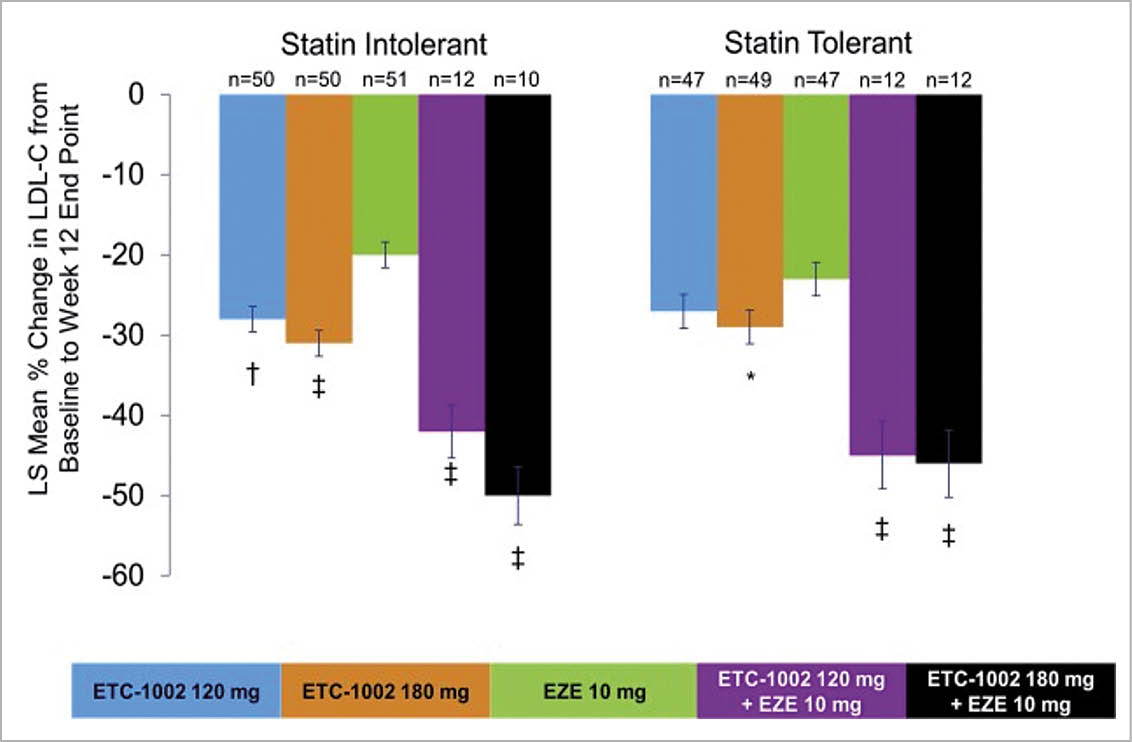
Es stellen sich die gleichen Fragen und Massnahmen wie bei Fall 2. Die Wirkung von Bempedoinsäure bei Statin-Intoleranz und Statin-Toleranz ist in der folgenden Abbildung wiedergegeben (Thompson et al J Clin Lipidol. 2016).
Mit der Kombination von Bempedoinsäure und Ezetimibe (Nustendi) kann selbst bei Statin-Intoleranten eine LDL-Cholesterinsenkung von ca. 50% erreicht werden.
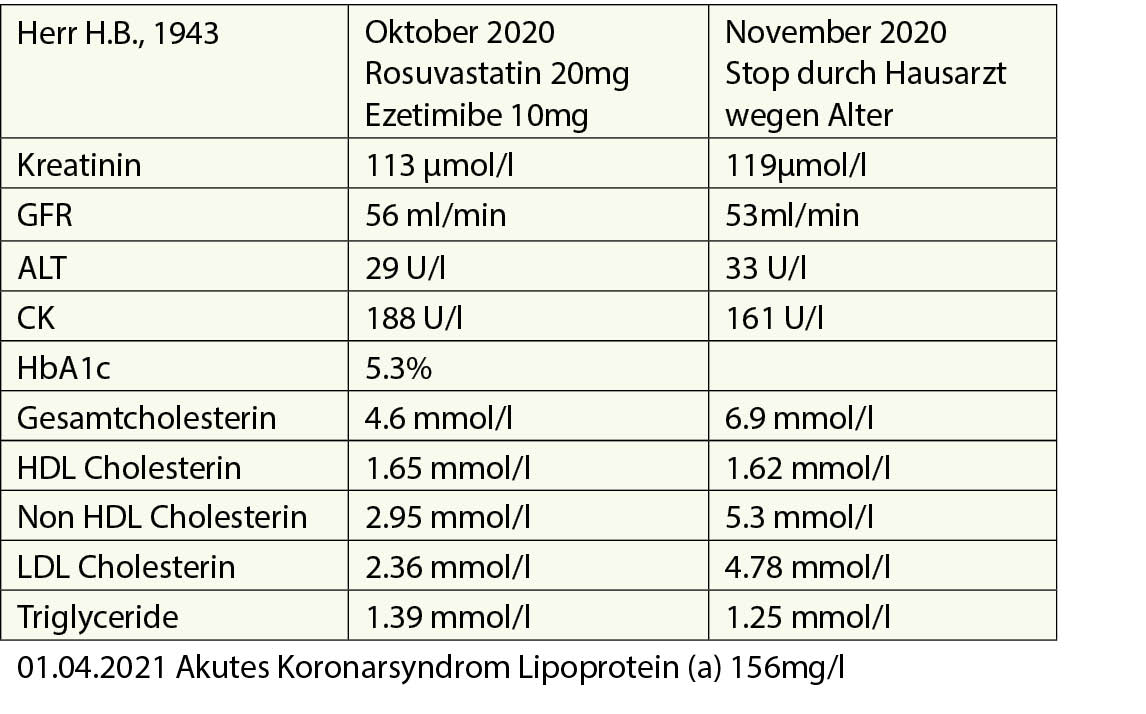
Fall 3: Herr H.B., 1943
Pos. Familienanamnese für vorzeitige ASCVD (Mutter hatte seit jungen Jahren Angina pectoris, behandelt mit PTCA/Stenting im Alter von 47 Jahren und ACBP im Alter von 52 J.)
Rheumatoide Arthritis, Karotis-Atherosklerose (2008 Stent Re bei 85%, symptomatisch, Links 50%). Hat 2008 mit dem Rauchen aufgehört (35 J.). Kein Diabetes, normaler Blutdruck, BMI 28,3 kg/m2, keine körperliche Aktivität. Simvastatin 40 wurde 2010 nach ca.
2 Jahren wegen Myalgien abgesetzt (keine CK-Erhöhung).
Im Jahr 2015 wurde nach einer kardiologischen Untersuchung eine Therapie mit Rosuvastatin 20 mg eingeleitet und gut vertragen. Im Jahr 2019 wurde Ezetimibe 10 mg hinzugefügt.
Breakout Session: Jenseits der Guidelines – Antithrombotische Fälle
Fallbeispiele von Prof. Dr. med. Lucia Mazzolai, Service d’Angiologie, CHUV
Fall 1: Männlicher Patient, 61 Jahre
CAD, PCI RCA 2019, Belastungsecho mit normaler Reaktion, PAD und zunehmende Schmerzen (Claudicatio intermittens) an der rechten unteren Extremität seit einem Jahr, CVD, ATS-Plaques 2019.
Kardiovaskuläre Risikofaktoren: Raucher, Hyperlipidämie, arterielle Hypertonie.
Medikation: Aspirin 100 mg0 –1 -0, Ramipril 5 mg 1 –0 –0, Simvastatin 40 mg 0 – 0 –1
Periphere Impulse wahrgenommen ausser rechts popliteal, rechts anterior pedis, rechter hinterer Tibialis. ABI rechts 80/140 =0.6, ABI links 150/140 =1.1
Laufband: Protokoll für konstante Belastung (3,2 km/h, 12 % Steigung)
Klinisches Symptom: Schmerzen im rechten Bein
Anfängliche Claudicatio-Entfernung: 50 m
Maximale Klaudierungsstrecke: 100 m
Patient mit polyvaskulärer Atherosklerose (CVD, CAD, PAD, mehreren kardiovaskulären Risikofaktoren, Claudicatio intermittens im rechten Unterschenkel, zunehmenden Symptomen seit einem Jahr; kurze schmerzfreie Gehstrecke mit erheblicher Einschränkung in Alltag und Berufsleben
Was würden Sie tun?
PAD ist ein Marker für kardiovaskuläre Morbidität und Mortalität (4-5 Mal höheres Risiko für kardiovaskuläre Ereignisse als Personen ohne PAD). Das Gesamtrisiko muss angesprochen werden und die Symptome der unteren Extremitäten.
Kardiovaskuläre Risikofaktoren
Rauchen: STOP
LDL-Cholesterin Zielwert < 1.4 mmol/L
Arterielle Hypertonie Zielwert < 130/80 mmHg (<65Jahre)
Körperliche Aktivität
Medikation
Aspirin 100 mg 0 –1 –0
Ramipril 5 mg 1 –0 –0
Simvastatin 40 mg 0 – 0 –1
Trotz Therapie bleiben PAD Patientenbei hohem kardialem Risiko und/oder PAD-Risiko (Amputation, periphere Angioplastie, peripheres Bypass Graft Stenting). PAD Patienten bleiben auch trotz optimaler Therapie mit einem kumulativen Risiko für atherothrombotische Ereignisse konfrontiert.
In der WAVE Studie (NEJM 2007;357:217-22/) war die Kombination eines oralen Antikoagulans und Antiplättchen Therapie nicht wirksamer als Antiplättchen Therapie allein, aber die Kombination ging mit einer Zunahme lebensbedrohlicher Blutungen einher.
Ein Paradigmenwechsel stellt der Synergieffekt zur Prävention der Athertothrombose durch Plättchenhemmung und orale antikoagulation mit DOAKS dar. In der COMPASS Studie reduzierte Rivaroxaban 2.5 bid + Aspirin gegenüber Aspirin bei Patienten mit PAD MACE (kardiovaskulären Tod/Schlaganfall/MI) oder MALE inkl. Amputationen um 31.%. Nach einem unerwünschten Ereignis in den Extremitäten (MALE) bleiben Mortalität und Amputationsraten bei PAD Patienten hoch.
Bei Personen mit peripherer arterieller Verschlusskrankheit ist die Entwicklung von MALE mit einer mit einer schlechten Prognose verbunden, weshalb die Prävention von grösster Bedeutung ist. Rivaroxaban 2.5mg + Aspirin ergab eine Reduktion aller peripherer vaskulärer Outcomes um 24%.Die Eur Soc, of Vasc Med. ESVM Guidelines empfehlen zur antithrombotischen Therapie bei symptomatischen PAD Patienten eine kombinierte Therapy mit Aspirin 100mg/ Tag und Rivaroxaban 2 x 2.5mg/Tag (Evidenzgrad IIa/B).
Männlicher Patient, 61 Jahre alt
Wenige Monate später entwickelt der Patient eine tiefe Venenthrombose in der unteren linken Extremität.
Wie würden Sie ihn behandeln?
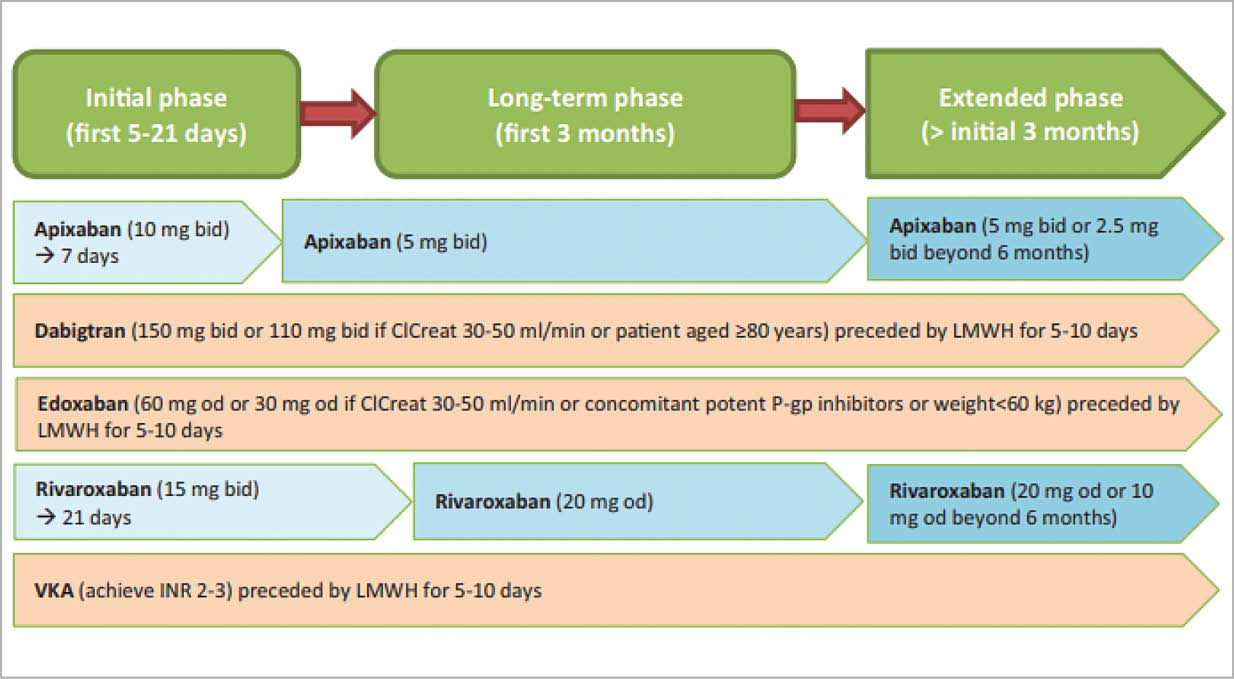
Die Behandlung der tiefen Venenthrombose (nach Mazzolai L et al. EJPC 2020)
Entsprechende Medikation bei unserem Patienten:
Aspirin 100 mg 0 –1 – 0
Rivaroxaban 2.5 mg 1 – 0 –1
Rivaroxaban 15 mg bid for 21 days then 20 mg od for 3 months
Ramipril 5 mg 1 – 0 – 0
Simvastatin 40 mg 0 – 0 –1
Was zu begleitender, antithrombotischer Behandlung?
Evaluation des persönlichen Risikos: Risiko für Rückfall, Risiko für Blutung, Patientenadhärenz, Patientenwahl.
Die Inzidenz für schwere Blutungen is signifikant höher bei Frauen als bei Männern, die mit VKA behandelt werden, bei Patienten über 65 Jahren, Patienten mit Creatininclearance <50ml/min, bei Patienten mit einer Vorgeschichte für Blutungen, bei begleitender Antiplättchentherapie, bei Patienten mit Hämoglobinwerten unter 100g/l. Verlängern der Behandlung über den empfohlenen Zeitraum hinaus verzögert aber verringert das Risiko eines erneuten Auftretens nachdem die Behandlung abgesetzt wird, nicht.
Die Referentin schloss mit der unbeantworteten Frage bei der angiologischen Konsultation nach 3 Monaten: was hat mit der Antikoagulation zu geschehen?
Quelle: AGLA Update Meeting, Breakout Session online, 4. November 2021
riesen@medinfo-verlag.ch
◆ LDL-Cholesterin im Blut: «The lower the better und the earlier
the better»
◆ Statin, Ezetimibe und PCSK9-Hemmer sind die aktuelle Standardtherapie zur Senkung des LDL-Cholesterins und des kardiovaskulären Risikos
◆ Patienten mit hohem und sehr hohem kardiovaskulärem Risiko profitieren von der LDL-Reduktion, die durch die PCSK9-Hemmer erreicht werden kann
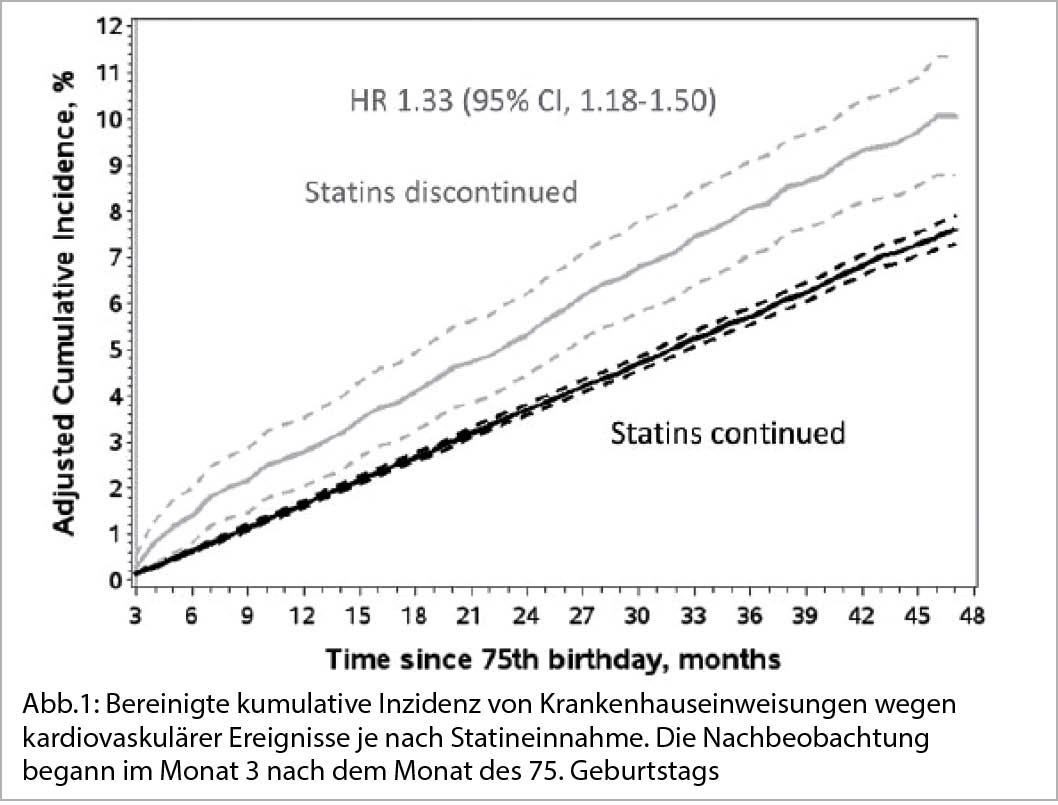
◆ Bei Vorhandensein einer atherothrombotischen Krankheit gibt es keinen Grund die Statintherapie wegen des Alters abzubrechen.
der informierte @rzt
- Vol. 12
- Ausgabe 1
- Januar 2022