- Calprotectin
Erstmalig beschrieben wurde das Calprotectin im Jahre 1980 als Protein L1. Heutzutage ist der aktuell relevanteste fäkale Biomarker aus dem klinischen Alltag des Hausarztes, Internisten und Gastroenterologen kaum mehr wegzudenken. Er wird häufig in Arztpraxen und im Krankenhaus dazu gebraucht, organische von funktionellen gastrointestinalen Erkrankungen abzugrenzen.
Chronisch-entzündliche Darmerkrankungen und das Reizdarmsyndrom
Zwei Krankheitsentitäten, welche es im klinischen Alltag häufig auseinanderzuhalten gilt, sind chronisch-entzündliche Darmerkrankungen (engl. inflammatory bowel disease, IBD) und das Reizdarmsyndrom (engl. irritable bowel syndrome, IBS). IBD sind in westlichen Ländern mit einer Prävalenz von bis zu 0,5% auf dem Vormarsch und das IBS gehört mit einer Prävalenz von bis zu 11,2% zu den sog. Volkskrankheiten.
Da das fäkale Calprotectin eine Entzündung im Gastrointestinaltrakt anzeigt, spielt es eine besondere Bedeutung in der Diagnostik und Therapie der chronisch-entzündlichen Darmerkrankungen – namentlich Morbus Crohn und Colitis ulcerosa. In der Pathophysiologie dieses Krankheitsspektrums geht man von einer fehlgesteuerten Immunantwort in Zusammenhang mit dem intestinalen Mikrobiom aus. Beim Morbus Crohn liegt eine granulomatöse, transmurale Entzündung vor, welche prinzipiell den ganzen Gastrointestinaltrakt (von Mund bis Anus) betreffen kann. Im Falle der Colitis ulcerosa ist lediglich die Mukosa von der Entzündung, welche sich vom Rektum bis zum Zökum ausdehnen kann, betroffen. Prinzipiell kann die Erkrankung in jedem Alter auftreten, der dominante Altersgipfel liegt im jüngeren Erwachsenenalter (15-30 Jahre), wobei auch ein zweiter Peak im Alter (50-80 Jahre) existiert. Bei funktionellen Darmerkrankungen, hierunter stellt IBS die häufigste Entität dar, geht man u.a. von einer Dysregulation der Darm-Hirn-Achse und einer erhöhten Schmerzsuszeptibilität aus. Es handelt sich in der Regel um eine Ausschlussdiagnose, für welche die Rom-IV-Kriterien gelten.
Fäkales Protein, das bestimmten Einflüssen unterliegt
Calprotectin stammt überwiegend aus neutrophilen Granulozyten (weniger auch aus Makrophagen) und macht 60% des zytosolischen Proteins dieser Zellen aus. Es spielt eine Rolle im angeborenen Immunsystem und verfügt sogar über direkte antimikrobielle Effekte. Man kann es in verschiedenen Körperflüssigkeiten abhängig vom Entzündungsausmass nachweisen, wobei im Stuhl eine um bis zu sechsfach höhere Konzentration als im Plasma vorliegt.
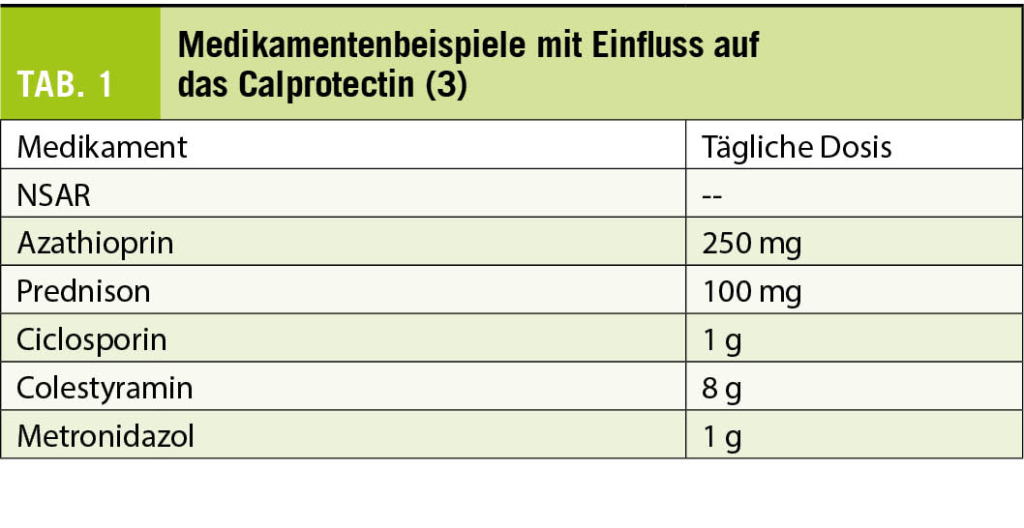
Es sind viele kommerzielle Calprotectin-Assays vorhanden, welche zum Teil eine deutliche Inter-Assay-Variabilität aufweisen (von 5-1000 bis 5-8000 μg/g). Von den meisten Herstellern wird ein Cut-off von 50 μg/g als obere Grenze des normalen Referenzbereichs angegeben. Neuerdings werden bereits point-of-care Tests mit dem Smartphone angeboten. Dies wird in Studien von vielen Patienten als nützliches Eigenmonitoring wahrgenommen und könnte vermutlich gerade in Pandemiezeiten zunehmend an Bedeutung gewinnen. Insgesamt sollte der Kliniker beachten, dass Calprotectin gewissen Einflussfaktoren unterliegen kann: Alter, Medikation, GI-Blutungen und tagesabhängige Variationen gehören dazu. Bei Patienten unter 4 Jahren und denjenigen über 65 Jahren werden in der Literatur höhere Cut-off-Werte vorgeschlagen. Man geht davon aus, dass u.a. altersabhängige Veränderungen des Immunsystems relevant sein könnten. Zu den Medikamenten, die einen Calprotectin-Anstieg zur Folge haben können, gehören insbesondere NSAR (sowohl im Kurzzeit- als auch Langzeitgebrauch). Weitere Medikamente, welche das Calprotectin erhöhen können, sind Tab. 1 zu entnehmen. Auch GI-Blutungen per se scheinen eine Erhöhung des Calprotectins zu bewirken. Obwohl das Protein eine homogene Verteilung im Stuhl aufweist, liegt eine signifikante tageszeitabhängige Variabilität vor: insbesondere je grösser das Stuhlintervall, desto höher der Wert. Dies führte dazu, dass einige Autoren sich in der Vergangenheit für eine Calprotectin-Bestimmung aus dem ersten Stuhlgang des Tages aussprachen, was sich letztlich in Folgestudien nicht bestätigen liess. Dennoch kann es sicherlich nützlich sein, zwei Calprotectin-Messungen vor Therapieanpassung bei IBD-Patienten vorzunehmen (1).
Calprotectin in der (Differential-)Diagnostik gastrointestinaler Erkrankungen
Die Diagnosestellung gastrointestinaler Erkrankungen bleibt selbst für erfahrene Gastroenterologen eine diagnostische Herausforderung. Es ist in vielen Fällen nicht möglich, organische von funktionellen Erkrankungen rein klinisch auf Grundlage der Symptome zu differenzieren. Und laborchemische Untersuchungen (wie CRP und Leukozyten) haben keine ausreichende Sensitivität und Spezifität gezeigt. Daher bedarf es anderer diagnostischer Hilfsmittel. Die Endoskopie hat sich als Goldstandard etabliert, da sie die Vorteile der direkten Visualisierung mit der Möglichkeit der Biopsieentnahme kombiniert. Allerdings benötigt sie Ressourcen und kann unangenehm für den Patienten sein. Daher stellt das Calprotectin im Stuhl als nicht-invasiver fäkaler Biomarker ein sehr hilfreiches diagnostisches Instrument dar. Es eignet sich zur Beurteilung der Krankheitsaktivität und als Marker des mucosal healing. Zudem ist es ein Prädiktor für einen Schub bzw. ein Rezidiv (auch postoperativ). Damit dient es auch der Therapiesteuerung. Im Falle der Colitis ulcerosa hat sich eine enge Korrelation zur klinischen, endoskopischen und histologischen Krankheitsaktivität gezeigt, während es beim M. Crohn weniger mit der klinischen als vor allem mit der endoskopischen und histologischen Aktivität korrelierte.
Wichtig ist immer zu bedenken, dass das Calprotectin Ausdruck einer Entzündungsreaktion des Gastrointestinaltraktes ist und als solcher nicht spezifisch. So können infektiöse Gastroenteritiden genauso wie NSAR-assoziierte Enteropathien erhöhte Werte verursachen. Bei Erkrankungen wie der mikroskopischen Kolitis, Zöliakie, Divertikulitis und Ulzera des oberen GI-Traktes können erhöhte Werte festgestellt werden (2).
Mögliche Calprotectin-Grenzwerte
Die Interpretation der einzelnen Calprotectin-Werte ist aufgrund der eingangs bereits beschriebenen Variabilität oft nicht ganz einfach. Insbesondere diskrete Erhöhungen sind oft schwierig zu interpretieren. Grundsätzlich gilt, dass Calprotectin-Messungen immer im Kontext der Klinik des Patienten interpretiert werden müssen (abdominelle Schmerzen, Stuhlfrequenz und -konsistenz, Blut-oder Schleimauflagerungen, Fisteln, extraintestinale Manifestationen, etc.). Sie sollten nie isoliert betrachtet werden.
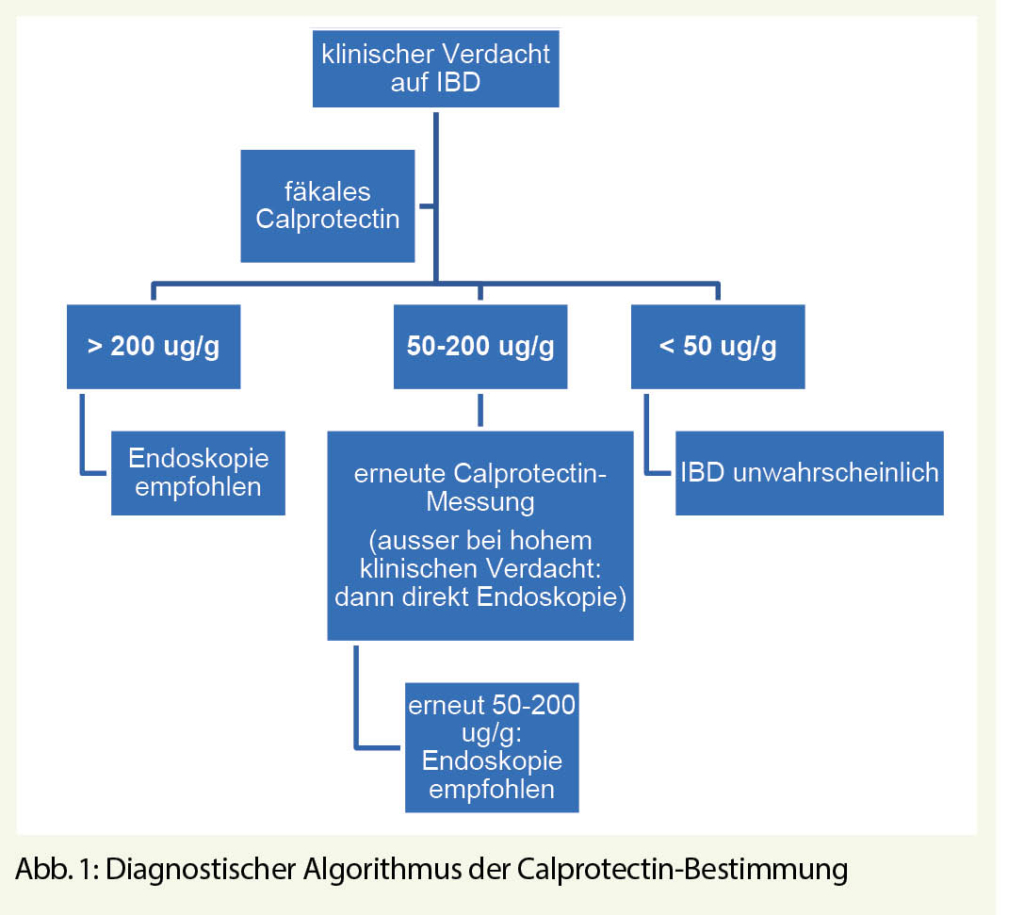
Der gängige Hersteller-Cut-off für das Calprotectin liegt bei 50 μg/g. Dieser Wert hat sicherlich seine Berechtigung als Screening-Verfahren (sehr hohe Sensitivität). Studien haben jedoch gezeigt, dass Werte bis 200 μg/g einen hohen negativ-prädikativen Wert von bis zu 97% aufweisen. Somit scheint es plausibel, diesen Wert als Cut-off für die Differenzierung von IBD und funktionellen Erkrankungen zu verwenden, um die Notwendigkeit einer ergänzenden Endoskopie einzuschätzen. Bei Patienten mit einem Wert zwischen 50 und 200 μg/g sollte allerdings eine zweite Calprotectin-Bestimmung (nach Elimination möglicher Störfaktoren wie NSAR) zur Verifizierung des Befundes erfolgen. IBD-Patienten haben im Gegensatz zu Patienten mit IBS in der Regel eine persistierende Calprotectin-Erhöhung (meist > 200 μg/g). Ein Algorithmus zur sinnvollen Calprotectin-Bestimmung in der Praxis findet sich in Abb. 1.
Ein möglicher Cut-off zur Therapiesteuerung bei IBD ist 250 μg/g, welcher eine Therapieeskalation rechtfertigt. Allerdings bedeutet dieser auch, dass 18% der Patienten ohne Krankheitsaktivität falsch-positiv und 20% mit Krankheitsaktivität falsch-negativ sind. In der STORI-Studie wurde bei Patienten mit initial doppelter Immunsuppression mit Azathioprin und Infliximab letzteres abgesetzt. Hier zeigte sich, dass ein Calprotectin über 300 μg/g ein Risikofaktor für ein Rezidiv war.
Calprotectin bei gastrointestinalen Malignomen
Auch Neoplasien des Gastrointestinaltraktes sind mit einer mukosalen Entzündungsreaktion vergesellschaftet. In Studien zeigte das Calprotectin bei einem Cut-off von 50 μg/g eine Sensitivität von 82% und einen negativ prädikativen Wert von 98%. Diesen Daten zufolge verringert ein negatives Testresultat die Wahrscheinlichkeit einer Neoplasie im GI-Trakt. Hieraus ergeben sich natürlich mögliche Implikationen für die Indikation zur Endoskopie. Es gilt allerdings immer, die Klinik des Patienten und aktuelle Guidelines miteinzubeziehen (kein Ersatz für die Vorsorgekoloskopie ab dem 50. Lebensjahr!). Auch Karzinome des oberen Gastrointestinaltraktes können Calprotectin-Werte erhöhen.
Copyright bei Aerzteverlag medinfo AG
Gastroenterologie und Hepatologie Kantonsspital Luzern
Spitalstrasse
6000 Luzern
houman.azam@luks.ch
Gastroenterologie und Hepatologie Kantonsspital Luzern
Spitalstrasse
6000 Luzern
Die Autoren haben deklariert, in Zusammenhang mit diesem Artikel keine Interessenkonflikte zu haben.
- Das fäkale Calprotectin ist ein Biomarker, welcher eine Entzündungsreaktion des Darms anzeigt und eine Differenzierung zwischen organischen und funktionellen Darmerkrankungen erlaubt.
- Der Wert unterliegt Einflussfaktoren wie Medikation, Abnahmezeitpunkt, GI-Blutung. Daher kann eine zweite Messung vor Ableitung von Konsequenzen sinnvoll sein.
- Ein Cut-off von 200 μg/g erscheint hilfreich, um funktionelle von entzündlichen Darmerkrankungen abzugrenzen. Hierbei gilt es jedoch immer die Klinik und Risikofaktoren des Patienten einzubeziehen.
- In der Therapiesteuerung von IBD scheint ein Cut-off von 250 μg/g als Marker einer relevanten Entzündungsaktivität sinnvoll, um eine Therapieeskalation zu rechtfertigen. Allerdings ist auch hier die Klinik des Patienten entscheidend.
- Calprotectin ist ein unspezifischer Entzündungsmarker. Auch Neoplasien des Gastrointestinaltraktes genauso wie infektiöse Gastroenteritiden, NSAR-assoziierte Enteropathien, Zöliakie, Divertikulitis, mikroskopische Kolitis sowie Ulzera des oberen GI-Traktes können Ursache für eine Erhöhung sein.
1. Ruth MA. Fecal Calprotectin. Adv Clin Chem. 2018; 87: 161 – 190
2. Burri E. The use of fecal calprotectin as a biomarker in gastrointestinal disease. Expert Rev Gastroenterol Hepatol. 2014; 8 (2): 197-210
3. Ton H. Improved assay for fecal calprotectin. Clin Chim Acta. 2000; 25: 41-54
der informierte @rzt
- Vol. 11
- Ausgabe 2
- Februar 2021