- Die nicht-alkoholische Fettleber
Die nicht-alkoholische Fettleber (NAFLD) galt lange als harmlose Wohlstandserscheinung. Tatsächlich ist die NAFLD eine «Wohlstandserscheinung», die sich wie die Adipositas aus den Folgen der Industrialisierung entwickelt hat: Zwar gehen erste Beschreibungen der Fettleber bei Adipositas und Diabetes auf das späte 19. Jahrhundert zurück, der Begriff NAFLD wurde jedoch erst 1980 geprägt (1). Seither nahm die Prävalenz erheblich zu und betrifft heute ca. 25% der Weltbevölkerung. Gleichzeitig wurde nachgewiesen, dass analog zur alkoholischen Fettleber auch ein beachtlicher Teil der Patienten mit NAFLD komplizierte Verlaufsformen entwickeln, die zu Leberkrebs, Leberversagen und einer erhöhten Mortalität infolge kardiovaskulärer Ereignisse führen.
Von «harmlos» kann also nicht gesprochen werden. Insbesondere bei Risikopatienten sollte die NAFLD gesucht und behandelt werden. Der vorliegende Artikel soll die epidemiologischen und pathophysiologischen Zusammenhänge erklären, sowie den aktuellen Stand der Diagnostik und Therapie.
Definitionen
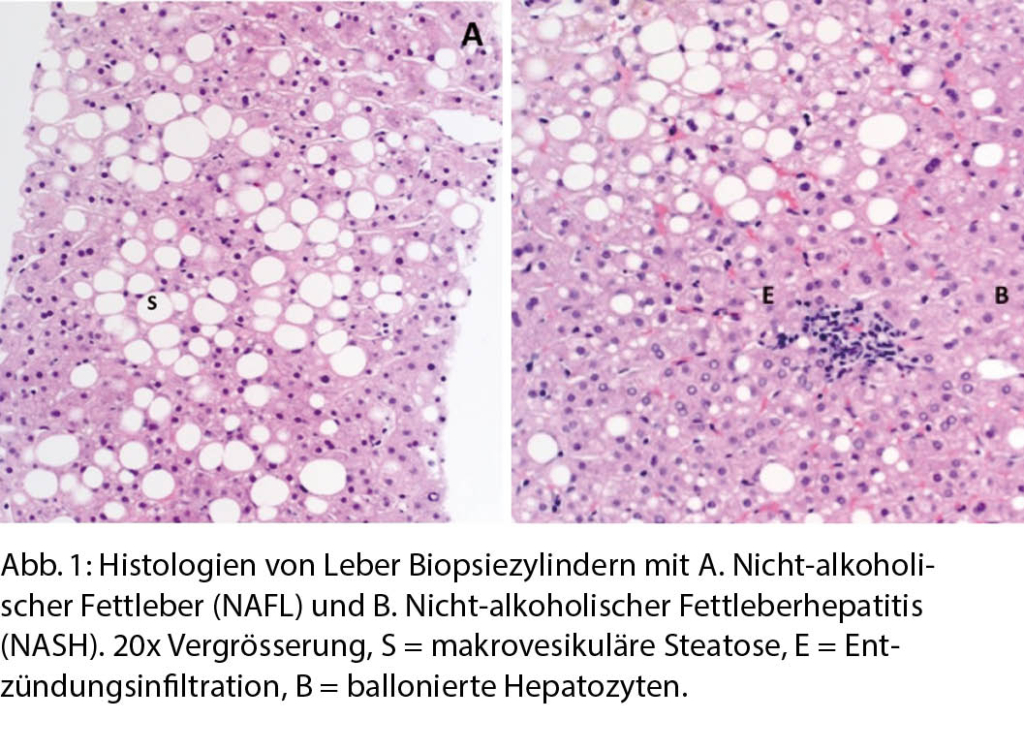
Bei der Fettleber unterscheidet man die alkoholische (Alcoholic-Fatty-Liver-Disease, AFLD) von der nicht-alkoholischen Fettlebererkrankung (NAFLD). Einziges Unterscheidungskriterium ist bis heute der kritische Alkoholkonsum, nach aktueller Definition > 20 g/d für Frauen und > 30 g/d für Männer, ein Biomarker existiert nicht. Die Erkrankung ist histologisch definiert, in beiden Fällen kommt es zu einer makrovesikulären Akkumulation von Fett, genannt Steatose, in > 5% der Hepatozyten. Weiterhin unterscheidet man die reine nicht-alkoholische Fettleber (Non-Alcoholic Fatty-Liver, NAFL) von der Fettleberhepatitis (Non-Alcoholic Steato-Hepatitis, NASH), bei der sich zusätzlich noch Entzündungsinfiltrate, ballonierte Hepatozyten, Mallory-Denk Bodies und andere Charakteristika finden (2, 3) (Abb. 1).
Epidemiologie
Die Prävalenz der NAFLD hat sich in den vergangenen 20 Jahren verdoppelt und betrifft heute ca. 25% der Weltbevölkerung, Europa liegt mit 23.7% im Mittelfeld (4). Diese erhebliche Zunahme geht mutmasslich auf die Zunahme der Prävalenz von Übergewicht / Adipositas (39% der Weltbevölkerung; WHO 2014 (5, 6)) und die verbesserte medizinische Diagnostik zurück. Damit sind auch die NAFLD-assoziierten Gesundheitskosten in den vergangenen Jahren erheblich gestiegen, bisher ohne Einfluss auf die Mortalität (4). Bei Risikogruppen wie Typ-2-Diabetes ist die Prävalenz deutlich höher (65%) (7). Die Studien, die der Abschätzung der Prävalenz zugrunde liegen, beruhen auf bildmorphologischer nicht histologischer Diagnostik, sodass die wahren Prävalenzen der unterschiedlichen Verlaufsformen NAFL und NASH nicht genau bekannt sind.
Pathophysiologie
Pathophysiologisch unterliegt die Regulation des Körpergewichtes und des Fettmetabolismus endokrinen und neurologischen Mechanismen, die allerdings von multiplen Faktoren beeinflusst werden: Umgebungsfaktoren (Schlaf, Arbeitszeit, Temperatur), Diät und Qualität der Nahrung inklusive Alkohol, körperliche und sportliche Aktivität, Medikamente, Mikrobiom, genetische und epigenetische Faktoren. Viele dieser Faktoren haben sich in Folge der Industrialisierung verändert und begünstigen seither die Genese von Adipositas, Metabolischem Syndrom und NAFLD. Die Lipidakkumulation in der Leber ist Folge vermehrter freier Fettsäuren, die durch die Nahrung aufgenommen, aber auch durch Lipolyse aus dem Fettgewebe freigesetzt und neu in der Leber produziert werden. Diese können dann eine niedriggradige systemische Inflammation hervorrufen mit Beteiligung des Fettgewebes und der Leber, welche ferner mit einer Fibroseentwicklung einhergehen kann (8).
Verlauf
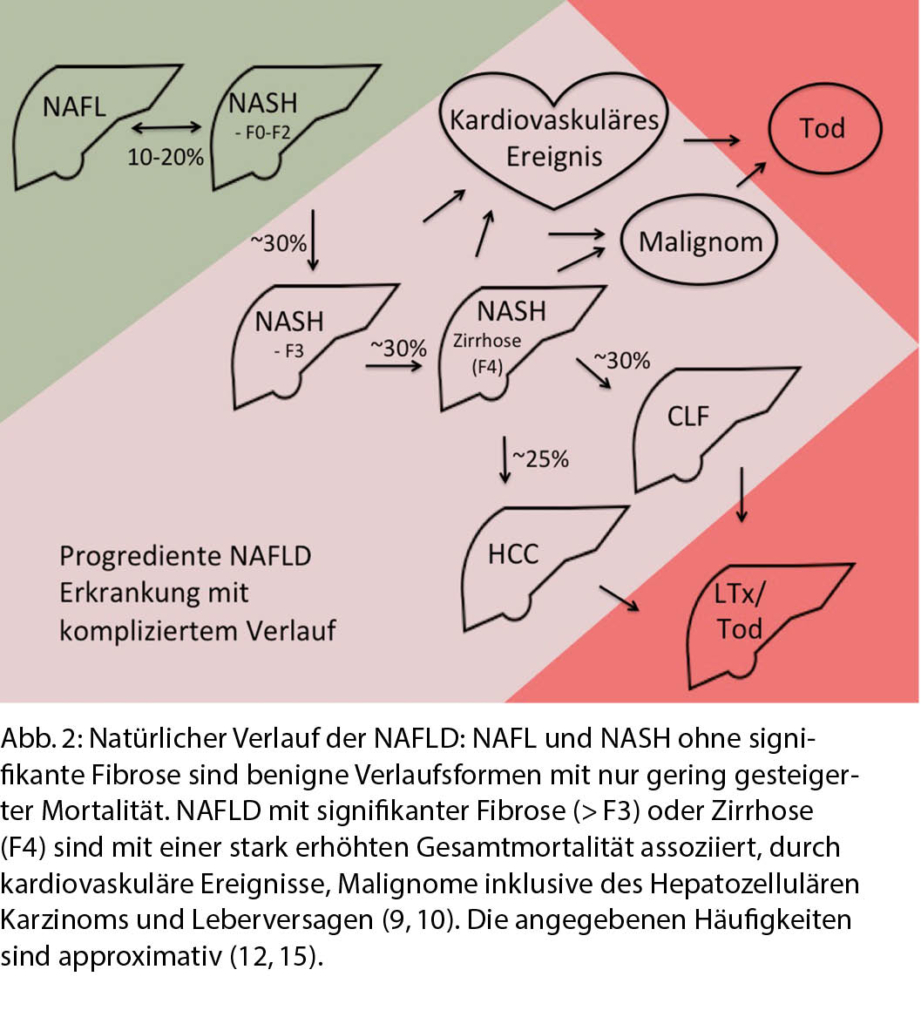
Neben der NAFL und der NASH werden auch die NASH mit und ohne signifikante Fibroseentwicklung unterschieden. Man weiss, dass das Fibrosestadium der beste Prädiktor für die Mortalität bei Patienten mit NASH ist, und bei signifikanter Fibrose (d. h. Fibrosestadium F3 oder F4 nach Metavir) mehr als 3-fach erhöht ist (9–11). Man erwartet, dass etwa ein Drittel aller NAFLD / NASH-Patienten im Verlauf eine signifikante Fibrose entwickeln, von denen ein weiteres Drittel zur Zirrhose fortschreiten wird, verbunden mit erhöhter hepatischer Mortalität entweder durch Entwicklung eines Leberversagens und / oder eines hepatozellulären Karzinoms (12). Bei NASH mit signifikanter Zirrhose ist aber vor allem auch die nicht-hepatische Mortalität erhöht, zum einen durch kardiovaskuläre Ereignisse (13), zum anderen durch extrahepatische Malignome (14) (Abb. 2).
Diagnostik
Die hier folgenden Ausführungen beziehen sich im Wesentlichen auf die aktuell publizierten Richtlinien der European Association for the Study of the Liver (EASL) (16).
1. Anamnese inklusive Alkoholanamnese. Zur Abschätzung der täglich konsumierten Alkoholmenge gilt folgende Faustregel: 10 g Alkohol entsprechen etwa 1dl Wein, 3dl Bier oder 0.3 dl Schnaps.
2. Labordiagnostik (ALT, AST, GGT, AP, Bilirubin, Albumin, INR, Thrombozyten) sollte bei Risikopatienten (z. B. Typ-2-Diabetes, kardiovaskuläre Erkrankungen, Metabolisches Syndrom, Obstruktive Schlafapnoe) bestimmt werden.
3. Hieraus lassen sich nicht-invasive Fibrosemarker berechnen (z. B. der NAFLD Fibrosis Score (17); http://www.nafldscore.com, Fib-4 Score; z. B. http://gihep.com/calculators/hepatology/fibrosis-4-score/).
4. Gleichzeitig sollte eine Sonographie veranlasst werden. Wenn verfügbar, ist die Elastographie (FibroScan®) empfehlenswert. Sie ermöglicht, den Fibrosegrad zu quantifizieren. Diese nicht-invasive Methode weist eine hohe Sensitivität und Spezifität von 75–90% auf (18).
5. Im Fall einer sonographisch detektierten Steatose und erhöhter Leberwerte und / oder erhöhter Fibrosemarker sollte eine Überweisung zum Facharzt für Gastroenterologie & Hepatologie erfolgen. Ziel der fachärztlichen Untersuchung ist es, die Diagnose zu sichern, eventuelle Begleithepatopathien zu suchen und den Schweregrad der Erkrankung festzustellen. Hierfür wird die Indikation zur Leberbiopsie geprüft werden. Die Leberbiopsie ist noch immer der diagnostische Goldstandard, da sie neben der quantitativen Beurteilung der Fibrose (nach Metavir: F0 keine Fibrose bis zu F4 Zirrhose (19)) und des Schweregrades der NAFLD multiple qualitative Merkmale (Steatose, Ballonierung der Hepatozyten, Entzündungsinfiltration, Mallory-Denk Bodies) beschreiben und auch andere Ätiologien abgrenzen kann. Dem gegenüber steht das damit verbundene geringe Blutungsrisiko von ca. 1:5000 (20).
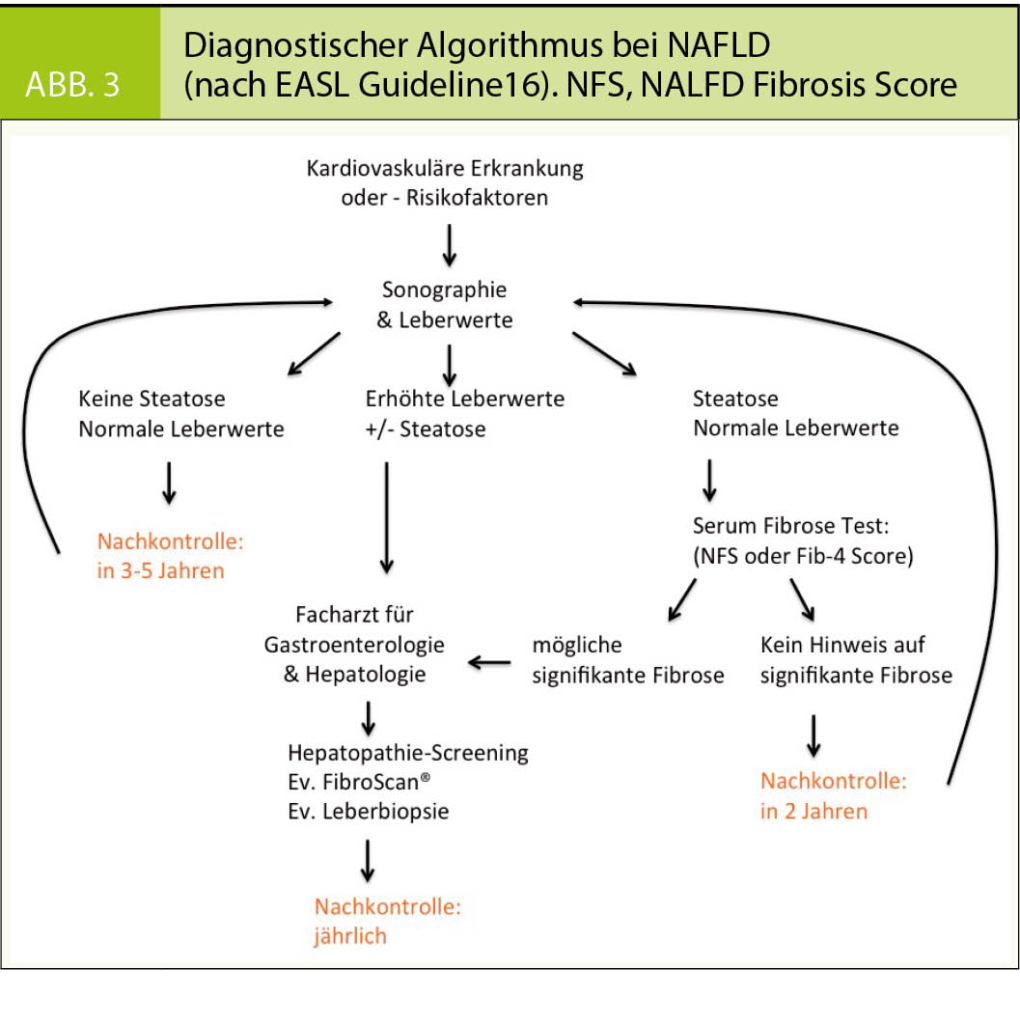
Diese von der EASL empfohlenen Schritte sowie auch die Intervalle der Nachkontrollen werden in Abbildung 3 zusammengefasst.
Therapie
Die Therapie der NAFLD besteht in einer sogenannten «Lifestyle Modifikation». Ziel ist es, das Gewicht um mindestens 8–10% vom Ausgangsgewicht zu reduzieren, welches in zahlreichen Studien zur histologischen Besserung oder gar Heilung von der NAFLD geführt hat (21). Die Therapie beinhaltet 2 Komponenten: Diät und körperliche und sportliche Aktivität. Nachdem man viele Jahre davon ausging, dass der wesentliche Faktor der Diät in der Kalorienrestriktion (Defizit von 500–750 kcal/d) bestehe, modifiziert man heute auch die Komposition im Sinne einer mediterranen Diät (reich an Ballaststoffen, Gemüse, Fisch, Ω-3-Fettsäuren; arm an Zucker, Cholesterin, gesättigten Fettsäuren, Fleisch). Die mediterrane Diät beeinflusst nicht nur kardiovaskuläre Erkrankungen günstig, sondern führte in Studien zur grössten Reduktion der Steatose (21). Ausserdem ist empfohlen, sogenannte «Softdrinks» (z. B. Cola, Eistee, etc.) zu meiden und stattdessen Wasser zu trinken. Diese Getränke enthalten fruktosereiche Zuckerzusätze und sind mit der Entwicklung der NAFLD assoziiert (22–24). Der Alkoholkonsum sollte auf ein Minimum reduziert werden und bei einem Fibrosestadium (F3 oder F4 (Zirrhose)) vollständig gestoppt werden (21). Andererseits wurde in mehreren Studien ein hepatoprotektiver Effekt des Konsums von 2–3 Tassen Kaffee täglich nachgewiesen werden (21).
Die in den vergangenen Jahrzehnten zunehmend «sitzende» Lebens- und Arbeitsweise ist mit einer deutlich erhöhten v. a. kardiovaskulären Morbidität und Mortalität verbunden. Es wird empfohlen, im Alltag möglichst wenig zu sitzen, möglichst viele «normale» Aktivitäten, z. B. Treppen steigen, zu Fuss gehen (statt Lift/Auto benutzen) zu integrieren und sich ≥ 3 Stunden wöchentlich in 3–5 Sitzungen sportlich zu betätigen (21). Andere kardiovaskuläre Erkrankungen oder Risikofaktoren sollten bestmöglich behandelt werden.
Bekannte Medikamente wie z. B. Metformin, Thiazolidinedione (Glitazone), Vitamin E, Ursodesoxycholsäure wurden für die Behandlung der NAFLD geprüft, keines davon ist jedoch hierfür empfohlen oder zugelassen. Zahlreiche neue Medikamente mit verschiedensten Therapieansätzen sind aktuell in klinischer Erprobung. Ziel einer zukünftigen medikamentösen Therapie ist es, das Fortschreiten der NAFLD / NASH und die Entwicklung einer Fibrose zu verhindern.
Danksagung: Die histologischen Abbildungen verdanke ich Herrn Professor Dr. med. Luigi Tornillo, Institut für Pathologie, Universitätsspital Basel.
Gastroenterologie / Hepatologie
Labor für Experimentelle Hepatologie
Kantonsspital St. Gallen
Rorschacherstrasse 95
9007 St. Gallen
christine.bernsmeier@kssg.ch
Die Autorin hat keine Interessenskonflikte im Zusammenhang mit diesem Beitrag deklariert.
- Die NAFLD ist mit einer Prävalenz von 25% der Weltbevölkerung die heutzutage häufigste Hepatopathie.
- Hauptursache ist die pandemische Zunahme von Adipositas und Insulinresistenz.
- Sie ist keine harmlose Erkrankung, denn im fortgeschrittenen Stadium, beim Vorhandensein einer signifikanten Fibrose, ist die Mortalität mehr als 3-fach erhöht.
- Anhand einfach anzuwendender Serum Fibrose Tests (z. B. NAFLD Fibrosis Score, Fib-4 Score) können Patienten mit günstigem Krankheitsverlauf identifiziert werden.
- Eine Überweisung zur fachärztlichen Untersuchung sollte bei allen Patienten mit Steatose und erhöhten Leberwerten und / oder erhöhtem Fibrosemarker erfolgen.
- Die Therapie der NAFLD ist die sogenannte «Life-Style Modifikation». D.h. eine Gewichtsreduktion von 8–10% des Körpergewichtes mittels Umstellung der Diät und Steigerung der körperlichen Aktivität. Medikamente zur eventuellen zukünftigen supportiven Behandlung sind in klinischer Entwicklung.
1. Ludwig J, Viggiano TR, McGill DB, et al. Nonalcoholic steatohepatitis: Mayo Clinic experiences with a hitherto unnamed disease. Mayo Clin Proc 1980;55:434–438.
2. Group AI. Alcoholic liver disease: morphological manifestations. The Lancet 1981;317:707–711.
3. Ratziu V, Bellentani S, Cortez-Pinto H, et al. A position statement on NAFLD/NASH based on the EASL 2009 special conference. J Hepatol 2010;53:372–384.
4. Younossi Z, Henry L. Contribution of Alcoholic and Nonalcoholic Fatty Liver Disease to the Burden of Liver-Related Morbidity and Mortality. Gastroenterology 2016;150:1778–1785.
5. Ng M, Fleming T, Robinson M, et al. Global, regional, and national prevalence of overweight and obesity in children and adults during 1980–2013: a systematic analysis for the Global Burden of Disease Study 2013. The Lancet 2014;384:766–781.
6. González-Muniesa P, Mártinez-González M-A, Hu FB, et al. Obesity. Nat Rev Dis Primer 2017;3:17034.
7. Lonardo A, Nascimbeni F, Mantovani A, et al. Hypertension, diabetes, atherosclerosis and NASH: Cause or consequence? J Hepatol 2017.
8. Marra F, Gastaldelli A, Svegliati Baroni G, et al. Molecular basis and mechanisms of progression of non-alcoholic steatohepatitis. Trends Mol Med 2008;14:72–81.
9. Ekstedt M, Hagström H, Nasr P, et al. Fibrosis stage is the strongest predictor for disease-specific mortality in NAFLD after up to 33 years of follow-up. Hepatology 2015;61:1547–1554.
10. Angulo P, Kleiner DE, Dam-Larsen S, et al. Liver Fibrosis, but No Other Histologic Features, Is Associated With Long-term Outcomes of Patients With Nonalcoholic Fatty Liver Disease. Gastroenterology 2015;149:389–397.e10.
11. Hagström H, Nasr P, Ekstedt M, et al. Fibrosis stage but not NASH predicts mortality and time to development of severe liver disease in biopsy-proven NAFLD. J Hepatol 2017;67:1265–1273.
12. Ekstedt M, Franzén LE, Mathiesen UL, et al. Long-term follow-up of patients with NAFLD and elevated liver enzymes. Hepatology 2006;44:865–873.
13. Targher G, Day CP, Bonora E. Risk of Cardiovascular Disease in Patients with Nonalcoholic Fatty Liver Disease. N Engl J Med 2010;363:1341–1350.
14. Lauby-Secretan B, Scoccianti C, Loomis D, et al. Body Fatness and Cancer — Viewpoint of the IARC Working Group. N Engl J Med 2016;375:794–798.
15. Day CP. Natural history of NAFLD: remarkably benign in the absence of cirrhosis. Gastroenterology 2005;129:375–378.
16. Anon. EASL–EASD–EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. J Hepatol 2016;64:1388–1402.
17. Angulo P, Hui JM, Marchesini G, et al. The NAFLD fibrosis score: A noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology 2007;45:846–854.
18. EASL–ALEH Clinical Pracitce Guidelines: Non-invasive tests for evaluation of liver disease severity and prognosis. J Hepatol 2015.
19. Bedossa P. Intraobserver and Interobserver Variations in Liver Biopsy Interpretation in Patients with Chronic Hepatitis C. Hepatology 1994;20:15–20.
20. Rockey DC, Caldwell SH, Goodman ZD, et al. Liver biopsy. Hepatology 2009;49:1017–1044.
21. Romero-Gómez M, Zelber-Sagi S, Trenell M. Treatment of NAFLD with diet, physical activity and exercise. J Hepatol 2017;67:829–846.
22. Abid A, Taha O, Nseir W, et al. Soft drink consumption is associated with fatty liver disease independent of metabolic syndrome. J Hepatol 2009;51:918–924.
23. Maersk M, Belza A, Stødkilde-Jørgensen H, et al. Sucrose-sweetened beverages increase fat storage in the liver, muscle, and visceral fat depot: a 6-mo randomized intervention study. Am J Clin Nutr 2012;95:283–289.
24. Ma J, Fox CS, Jacques PF, et al. Sugar-sweetened beverage, diet soda, and fatty liver disease in the Framingham Heart Study cohorts. J Hepatol 2015;63:462–469.
der informierte @rzt
- Vol. 8
- Ausgabe 1
- Januar 2018