- Direkte orale Antikoagulanzien in der Geriatrie
Die Geschichte der Antikoagulanzien nahm in den frühen 2000er Jahren eine neue Wendung, als die sog. direkten oralen Antikoagulanzien (DOAK) auf den Markt kamen. Diese neue Medikamentenklasse bietet eine Lösung für einige der Nachteile von Vitamin-K-Antagonisten (VKA) und wird als Erstlinientherapie zur Vorbeugung und Behandlung zahlreicher Herz-Kreislauf-Erkrankungen aufgeführt. Ihre Anwendung bei geriatrischen Patienten, häufig polymediziert und polymorbide, birgt jedoch das hohe Risiko unerwünschter Ereignisse, was eine sorgfältige Risiko/Nutzen Abwägung bei der Verschreibung erforderlich macht.
The history of anticoagulants took a new turn in the early 2000s with the arrival on the market of direct oral anticoagulants (DOACs). This new class of drugs overcomes some of the drawbacks of anti-vitamin K drugs (VKAs) and is one of the first-line treatments for the prevention and treatment of many cardiovascular diseases. However, their use in the geriatric population, which is often multi-mediated and polymorbid, is likely to result in an increased risk of adverse events, requiring a careful assessment of the benefit/risk balance when prescribing these drugs.
Key Words: Anticoagulants oraux directs – interactions médicamenteuses – polymédication – sécurité – Personnes âgées
Einführung
Die direkten oralen Antikoagulanzien Dabigatran (Thrombininhibitor), Rivaroxaban, Apixaban und Edoxaban (Faktor Xa Inhibitoren) werden häufig bei venösen Thromboembolien (VTE) und nicht-valvulärem Vorhofflimmern (1, 2) eingesetzt. Die Einführung der direkten oralen Antikoagulanzien (DOAK) wurde von vielen als ein wichtiger Fortschritt angesehen, da es keine Notwendigkeit mehr gab, die Patienten zu überwachen und auf eine fixe Dosierung zu achten. Grossangelegte Schlüssel-Studien und Metaanalysen zeigten eine mindestens ähnliche Wirksamkeit im Vergleich zu VKA bei zugleich geringerer blutungsbedingter Mortalität. Hauptgrund dafür ist das im Vergleich zu Cumarinpräparaten verminderte Auftreten intrakranieller Blutungen (3-9). Diese Vorteile bewähren sich auch bei geriatrischen Patienten (10). Im Gegensatz dazu sind gastrointestinale Blutungen unter DOAK im Vergleich zu Warfarin häufiger, bei Apixaban hingegen laut Datenlage geringer (11-13).
Variabilität der DOAK-Konzentrationen- eine Herausforderung für die Sicherheit älterer Patienten
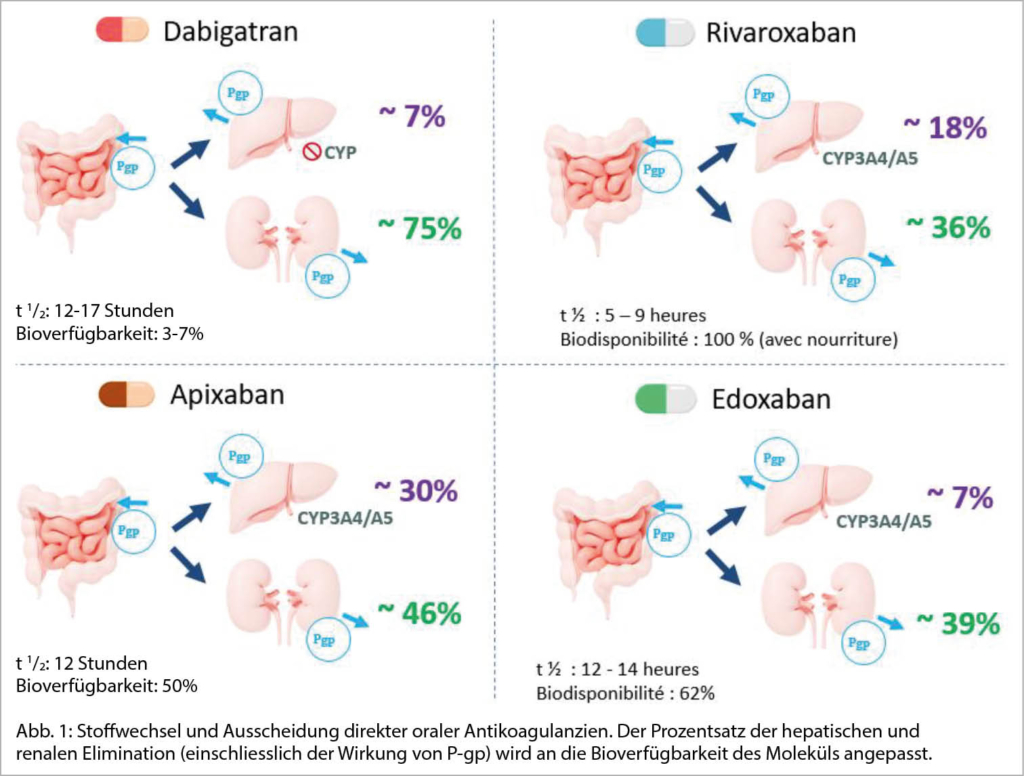
Obwohl diese Medikamente über eine grössere therapeutische Breite verfügen als VKA, gibt es zunehmend Hinweise dafür, dass es einen klaren Zusammenhang zwischen der Höhe der DOAK-Exposition und dem Auftreten von Blutungen gibt (3, 7, 14). Eine solche Korrelation scheint auch für ischämische Ereignisse zu gelten, wobei die Datenlage hier dünn ist (3, 7). In der Tat gibt es eine grosse Variabilität bei den DOAK-Konzentrationen in der Zielbevölkerung, die diese Medikamente erhalten. Grund dafür sind vor allem Niereninsuffizienz, Wechselwirkungen mit anderen Medikamenten, Gewicht und Alter (15-17). Aus pharmakologischer Sicht unterscheiden sich die DOAK in ihrer Metabolisierung und Ausscheidung (Abb. 1). Alle sind Substrate des P-Glykoproteins (P-gp), welches ihre Bioverfügbarkeit beeinflusst (18, 19). Der Haupt-Risikofaktor für eine Überdosierung ist die Niereninsuffizienz (11, 15, 20, 21). Hohes Alter oder starkes Übergewicht (<50 kg oder >120 kg) sind Risikofaktoren in geringerem Masse (3, 22-24). Eine Simulationsstudie, die den Einfluss verschiedener Faktoren auf Arzneimittelkonzentrationen evaluiert, zeigt, dass jeder Faktor für sich genommen die DOAK-Wirkung mässig erhöht, und dass vor allem die Kumulation dieser Risikofaktoren zu einem erheblichen Anstieg der Wirkung dieser Medikamente führen kann (23).
Polymedikation und Risikomanagement
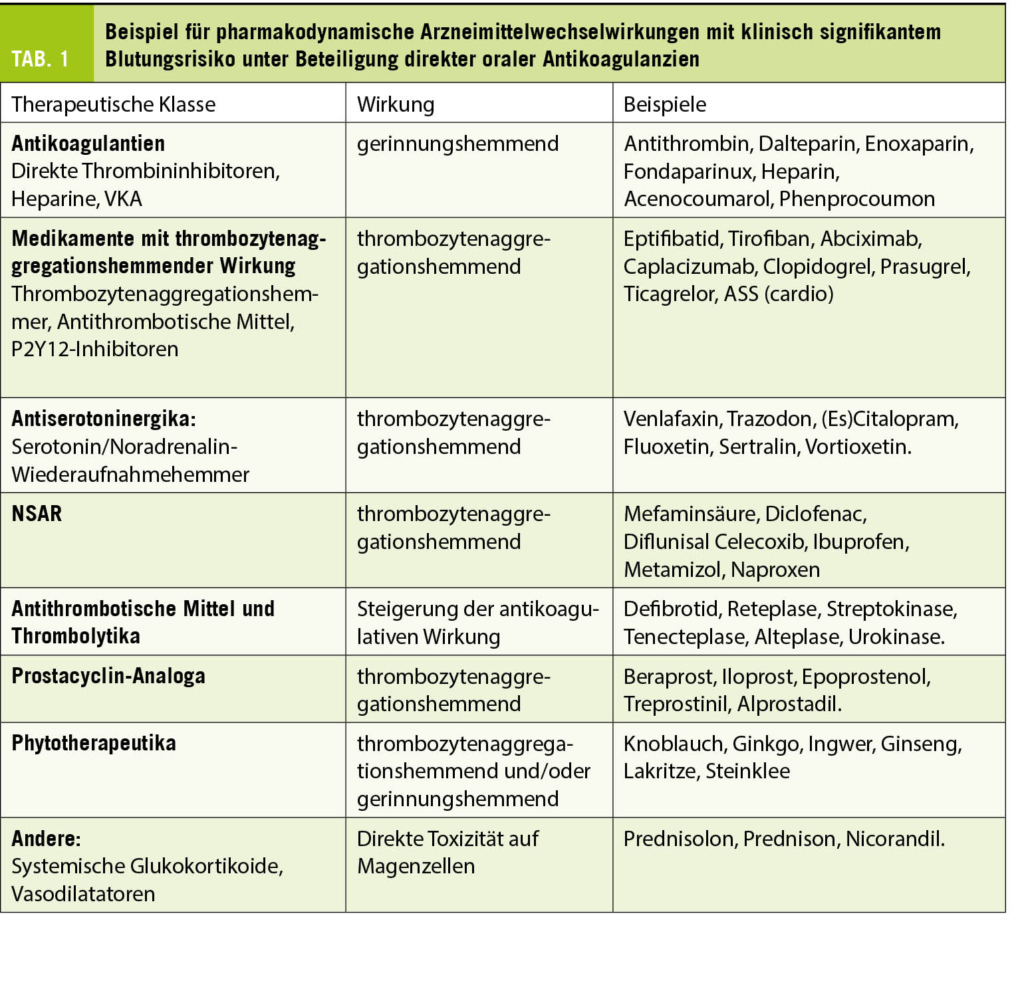
Wechselwirkungen von Medikamenten sind ein wichtiger Faktor für die Konzentrationsvariabilität. Bei älteren Menschen, welche häufig polymediziert und polymorbide sind, kann deren Management komplex sein. Es gibt zwei Arten von Arzneimittelwechselwirkungen. Die pharmakodynamischen Interaktionen werden durch jedes Medikament verursacht, das einen additiven oder antagonistischen Effekt auf das Antikoagulans hat und dessen (therapeutische oder toxische) Wirkung verändert. Dagegen nehmen pharmakokinetische Interaktionen Einfluss auf die Konzentration des Medikamentes (19, 25). Diese Arzneimittelwechselwirkungen können zu einer Über- oder Unterdosierung führen und ein potenzielles unerwünschtes Arzneimittelereignis hervorrufen. Eine Kohortenstudie zeigte einen Anstieg des Blutungsrisikos proportional zur Anzahl der Arzneimittelinteraktionen. Hierbei lag die Odds Ratio bei 1,55 [95% CI: 1,46-1,63] bei gleichzeitiger Einnahme eines DOAK und eines einzigen Inhibitors, und bei 2,60 [95% CI: 2,44-2,77] bei Einnahme von ≥2 Inhibitoren (26). Zum gegenwärtigen Zeitpunkt und mit Ausnahme von Edoxaban gibt es keine validierte Dosisanpassung für DOAK bei Vorliegen einer Arzneimittelinteraktion. Bezüglich Wirkung steigert jede die Hämostase beeinflussende Ko-Medikation das Risiko für Blutungen oder Thrombosen. Die Medikamentenklassen, die klassischerweise im Zusammenhang mit einem hohen Interaktionspotential aufgeführt werden, sind in Tabelle 1 gelistet. Zahlreiche klinische Situationen rechtfertigen den Einsatz von zwei oder mehr zeitgleichen Behandlungsmassnahmen mit Auswirkung auf die Hämostase, sofern die Nutzen-Risiko-Abwägung es erlaubt. In solchen Fällen wird eine engmaschige Überwachung zur frühzeitigen Erkennung von Nebenwirkungen empfohlen.
Pharmakokinetische Wechselwirkungen betreffen modulierende Substanzen mit Wirkung auf Zytochrom P450 3A4 (CYP3A4) und P-gp. Diese werden von der FDA in starke, mässige oder schwache Inhibitoren/Induktoren eingeteilt, je nachdem, ob sie zu einer Erhöhung oder Verringerung der Exposition führen (Fläche unter der Kurve, kurz AUC) (27). Aufgrund der schweren Nebenwirkungen dieser Medikamente werden niedrigere Dosen für DOAK in der Praxis vorgeschlagen.
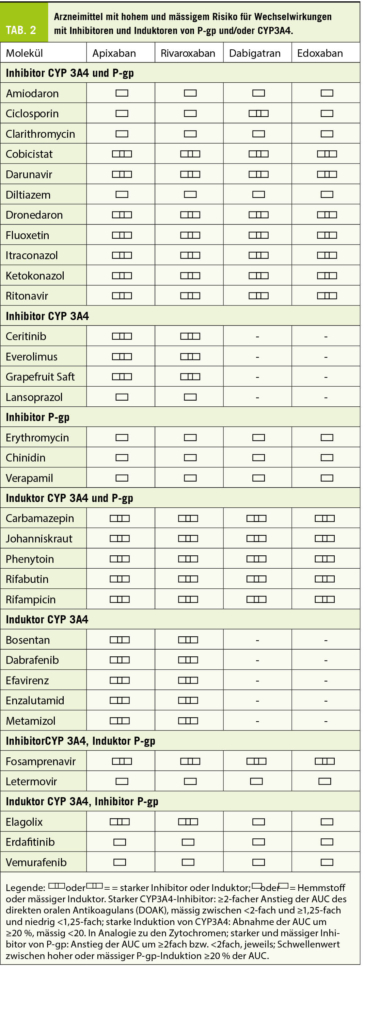
Tabelle 2 listet einige häufig verwendete Medikamente mit einem mässigen bis hohen Risiko für pharmakokinetische Wechselwirkungen. Im Allgemeinen stufen die Europäische Gesellschaft für Rhythmologie (28) und gewisse andere Experten (29) das Risiko einer Arzneimittelinteraktion als hoch ein, wenn diese eine Verdoppelung der AUC eines DOAKs durch einen Inhibitor, respektive eine Abnahme der AUC um mehr als 20 Prozent in Anwesenheit eines Induktors verursacht.
Prinzipiell müssten jedes Mal die Gegebenheiten (Literatur, Arzneimittel-Monographie) geprüft werden, welche darauf hinweisen, dass solche Schwellenwerte in Gegenwart eines Inhibitors/Induktors erreicht werden. Dies gilt vor allem für starke Inhibitoren/Induktoren von P-gp und für mässige Inhibitoren/Induktoren sowohl von CYP3A4 als auch von P-gp. Ein alleiniger starker Inhibitor von CYP3A4 wird nur für Apixaban und Rivaroxaban als hohes Risiko angesehen, welche weitgehend über die Leber via CYP-System eliminiert werden.
Aus praktischer Sicht ist bei einer Wechselwirkung mit einem Inhibitor oder starken Induktor sowohl von P-gp als auch von CYP3A4 ein Therapiewechsel auf VKA in Erwägung zu ziehen, insbesondere bei fehlendem routinemässigem Monitoring der DOAK-Therapie. Wenn eine Hemmung oder Induktion vorliegt, bei der ein moderater Inhibitor/Induktor involviert ist, und zwei oder mehr zusätzliche Risikofaktoren wie z. B. Niereninsuffizienz, starkes Übergewicht oder hohes Alter und/oder eine andere Arzneimittelwechselwirkung bestehen, wird ein Therapiewechsel von Experten (28, 29) empfohlen.
Ausblick und Schlussfolgerung
In der Literatur wird das Anstreben mittlerer Arzneimittelkonzentrationen in der Bevölkerung beschrieben, um das Risiko einer Über- oder Unterdosierung im Verlauf der therapeutischen Nachsorge zu minimieren; ihre Anwendung hängt gleichwohl von der Verantwortung des Verschreibers und der klinischen Situation ab (30). Der Einsatz von DOAK bei geriatrischen Patienten bleibt trotz fehlenden validierten Monitorings sicher und wirksam. Allerdings besteht bei allen DOAK das Risiko von Arzneimittelwechselwirkungen, die zu einer Unter- oder Überdosierung führen und hierdurch zu unerwünschten klinischen Ereignissen führen können, insbesondere im Zusammenhang mit Komorbiditäten wie Niereninsuffizienz, Polymedikation, sehr hohem Alter und starkem Übergewicht. Dies gilt insbesondere für geriatrische Patienten, bei denen die Kumulation dieser Risikofaktoren dazu führen kann, dass der verschreibende Arzt eine Behandlung mit VKA in Erwägung zieht bei Vorhandensein eines Inhibitors/Induktors von CYP450 3A4 und P-gp.
Claire Coumau 1, Apothekerin, Claire.Coumau@chuv.ch
Frederic Gaspar 1, Apotheker, Frederic.Gaspar@chuv.ch
Jean Terrier 2, Apotheker und Arzt, PhD, Jean.Terrier@hcuge.ch
Chantal Csajka 3, Professeure ordinaire, Chantal.Csajka@chuv.ch
1 Centre de Recherche et d’ Innovation en Sciences Pharmaceutiques
Cliniques Centre Hospitalier Universitaire et Université de Lausanne,
Suisse Rue du Bugnon 19, 1011 Lausanne
2 Division de médecine interne générale, Hôpitaux Universitaires de Genève/
Geneva Platelet Group, Faculté de Médecine, Université de Genève/
Service de pharmacologie et de toxicologie clinique, Service d’ anesthésiologie, de pharmacologie et de soins intensifs, Hôpitaux Universitaires de Genève, Suisse Centre Médical Universitaire, 1211 Genève
3 Centre de Recherche et d’ Innovation en Sciences Pharmaceutiques
cliniques Centre Hospitalier Universitaire et Université de Lausanne,
Suisse Rue du Bugnon 19, 1011 Lausanne
Zweitabdruck aus «la gazette médicale» 05-2022
Copyright bei Aerzteverlag medinfo AG
Centre de Recherche et d’ Innovation en Sciences Pharmaceutiques
Cliniques Centre Hospitalier Universitaire et Université de Lausanne,
Suisse Rue du Bugnon 19
1011 Lausanne
Claire.Coumau@chuv.ch
Centre de Recherche et d’ Innovation en Sciences Pharmaceutiques
Cliniques Centre Hospitalier Universitaire et Université de Lausanne
Suisse Rue du Bugnon 19
1011 Lausanne
Frederic.Gaspar@chuv.ch
Centre de Recherche et d’ Innovation en Sciences Pharmaceutiques
cliniques Centre Hospitalier Universitaire et Université de Lausanne
Suisse Rue du Bugnon 19
1011 Lausanne
Chantal.Csajka@chuv.ch
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ DOAK gehören zur Erstlinientherapie zahlreicher Herz-Kreislauf-Erkrankungen und ihr pharmakologisches Profil verleiht ihnen gewisse Vorteile im Vergleich zu VKA.
◆ Obwohl sie mit dem Zielgedanken einer einzigen Dosis für alle vermarktet werden, führt die ausgeprägte interindividuelle Variabilität der Plasmakonzentrationen bei einigen Patienten zu hämorrhagischen und thromboembolischen Risiken im Falle einer Über- oder Unterdosierung.
◆ Hauptsächlich Niereninsuffizienz, Arzneimittelwechselwirkungen und die gleichzeitige Einnahme von Medikamenten, die die Hämostase beeinflussen, gehören zu den am weitesten verbreiteten Faktoren für das Auftreten von Nebenwirkungen dieser Medikamente.
◆ Die Kumulation von Risikofaktoren, die besonders bei geriatrischen polymorbiden und polymedizierten Patienten vorhanden sind, kann zu einer Verschiebung des Nutzen-Risko-Profils zugunsten der VKA führen.
1. Ibáñez L, Sabaté M, Vidal X, Ballarin E, Rottenkolber M, Schmiedl S, et al. Incidence of direct oral anticoagulant use in patients with nonvalvular atrial fibrillation and characteristics of users in 6 European countries (2008-2015): A cross-national drug utilization study. British journal of clinical pharmacology. 2019;85(11):2524-39.
2. Rottenkolber M, Schmiedl S, Ibánez L, Sabaté M, Ballarín E, Vidal X, et al. Prescribers’ compliance with summary of product characteristics of dabigatran, rivaroxaban and apixaban-A European comparative drug utilization study. Basic Clin Pharmacol Toxicol. 2021;128(3):440-54.
3. Reilly PA, Lehr T, Haertter S, Connolly SJ, Yusuf S, Eikelboom JW, et al. The effect of dabigatran plasma concentrations and patient characteristics on the frequency of ischemic stroke and major bleeding in atrial fibrillation patients: the RE-LY Trial (Randomized Evaluation of Long-Term Anticoagulation Therapy). Journal of the American College of Cardiology. 2014;63(4):321-8.
4. Bansilal S, Bloomgarden Z, Halperin JL, Hellkamp AS, Lokhnygina Y, Patel MR, et al. Efficacy and safety of rivaroxaban in patients with diabetes and nonvalvular atrial fibrillation: the Rivaroxaban Once-daily, Oral, Direct Factor Xa Inhibition Compared with Vitamin K Antagonism for Prevention of Stroke and Embolism Trial in Atrial Fibrillation (ROCKET AF Trial). Am Heart J. 2015;170(4):675-82.e8.
5. Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al. Edoxaban versus warfarin in patients with atrial fibrillation. The New England journal of medicine. 2013;369(22):2093-104.
6. Owens RE, Kabra R, Oliphant CS. Direct oral anticoagulant use in nonvalvular atrial fibrillation with valvular heart disease: a systematic review. Clin Cardiol. 2017;40(6):407-12.
7. Eikelboom JW, Quinlan DJ, Hirsh J, Connolly SJ, Weitz JI. Laboratory Monitoring of Non- Vitamin K Antagonist Oral Anticoagulant Use in Patients With Atrial Fibrillation: A Review. JAMA Cardiol. 2017;2(5):566-74.
8. Linkins LA, Choi PT, Douketis JD. Clinical impact of bleeding in patients taking oral anticoagulant therapy for venous thromboembolism: a meta-analysis. Annals of internal medicine. 2003;139(11):893-900.
9. Khan F, Tritschler T, Kimpton M, Wells PS, Kearon C, Weitz JI, et al. Long-Term Risk for Major Bleeding During Extended Oral Anticoagulant Therapy for First Unprovoked Venous Thromboembolism : A Systematic Review and Meta-analysis. Annals of internal medicine. 2021;174(10):1420-9.
10. Sharma M, Cornelius VR, Patel JP, Davies JG, Molokhia M. Efficacy and Harms of Direct Oral Anticoagulants in the Elderly for Stroke Prevention in Atrial Fibrillation and Secondary Prevention of Venous Thromboembolism: Systematic Review and Meta-Analysis. Circulation. 2015;132(3):194-204.
11. Wadsworth D, Sullivan E, Jacky T, Sprague T, Feinman H, Kim J. A review of indications and comorbidities in which warfarin may be the preferred oral anticoagulant. J Clin Pharm Ther. 2021;46(3):560-70.
12. Cuddy S SR, Collis R, Matullah S. 33 Incidence of intracranial haemorrhage associated with antiplatelet and anticoagulant use; referrals to the national neurosurgery referral centre and reports to the health products regulatory authority. Heart (British Cardiac Society) 2015;101:A18-A9.
13. Lip GYH, Keshishian AV, Zhang Y, Kang A, Dhamane AD, Luo X, et al. Oral Anticoagulants for Nonvalvular Atrial Fibrillation in Patients With High Risk of Gastrointestinal Bleeding. JAMA Netw Open. 2021;4(8):e2120064.
14. Ruff CT, Giugliano RP, Braunwald E, Morrow DA, Murphy SA, Kuder JF, et al. Association between edoxaban dose, concentration, anti-Factor Xa activity, and outcomes: an analysis of data from the randomised, double-blind ENGAGE AF-TIMI 48 trial. Lancet (London, England). 2015;385(9984):2288-95.
15. Cirincione B, Kowalski K, Nielsen J, Roy A, Thanneer N, Byon W, et al. Population Pharmacokinetics of Apixaban in Subjects With Nonvalvular Atrial Fibrillation. CPT Pharmacometrics Syst Pharmacol. 2018;7(11):728-38.
16. Liesenfeld KH, Lehr T, Dansirikul C, Reilly PA, Connolly SJ, Ezekowitz MD, et al. Population pharmacokinetic analysis of the oral thrombin inhibitor dabigatran etexilate in patients with non- valvular atrial fibrillation from the RE-LY trial. Journal of thrombosis and haemostasis : JTH. 2011;9(11):2168-75.
17. Willmann S, Zhang L, Frede M, Kubitza D, Mueck W, Schmidt S, et al. Integrated Population Pharmacokinetic Analysis of Rivaroxaban Across Multiple Patient Populations. CPT Pharmacometrics Syst Pharmacol. 2018;7(5):309-20.
18. Heidbuchel H, Verhamme P, Alings M, Antz M, Diener H-C, Hacke W, et al. Updated European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist anticoagulants in patients with non-valvular atrial fibrillation. EP Europace. 2015;17(10):1467-507.
19. Foerster KI, Hermann S, Mikus G, Haefeli WE. Drug-Drug Interactions with Direct Oral Anticoagulants. Clinical pharmacokinetics. 2020;59(8):967-80.
20. Mavrakanas TA, Charytan DM, Winkelmayer WC. Direct oral anticoagulants in chronic kidney disease: an update. Curr Opin Nephrol Hypertens. 2020;29(5):489-96.
21. Kumar S, Lim E, Covic A, Verhamme P, Gale CP, Camm AJ, et al. Anticoagulation in Concomitant Chronic Kidney Disease and Atrial Fibrillation: JACC Review Topic of the Week. Journal of the American College of Cardiology. 2019;74(17):2204-15.
22. Eikelboom JW, Wallentin L, Connolly SJ, Ezekowitz M, Healey JS, Oldgren J, et al. Risk of bleeding with 2 doses of dabigatran compared with warfarin in older and younger patients with atrial fibrillation: an analysis of the randomized evaluation of long-term anticoagulant therapy (RE-LY) trial. Circulation. 2011;123(21):2363-72.
23. Terrier J, Gaspar F, Guidi M, Fontana P, Daali Y, Csajka C, et al. Population Pharmacokinetic Models for Direct Oral Anticoagulants: A Systematic Review and Clinical Appraisal Using Exposure Simulation. Clinical pharmacology and therapeutics. 2022;112(2):353-63.
24. Gong IY, Kim RB. Importance of pharmacokinetic profile and variability as determinants of dose and response to dabigatran, rivaroxaban, and apixaban. Can J Cardiol. 2013;29(7 Suppl):S24-33.
25. Stöllberger C, Finsterer J. Update on drug interactions with non-vitamin-K-antagonist oral anticoagulants for stroke prevention in elderly patients. Expert review of clinical pharmacology. 2021;14(5):569-81.
26. Lee JY, Oh IY, Lee JH, Kim SY, Kwon SS, Yang HJ, et al. The increased risk of bleeding due to drug-drug interactions in patients administered direct oral anticoagulants. Thromb Res. 2020;195:243-9.
27. FDA. Drug Development and Drug Interactions | Table of Substrates, Inhibitors and Inducers 2020 [12.01.2022]. Available from: https://www.fda.gov/drugs/drug-interactions-labeling/drug- development-and-drug-interactions-table-substrates-inhibitors-and-inducers.
28. Steffel J, Collins R, Antz M, Cornu P, Desteghe L, Haeusler KG, et al. 2021 European Heart Rhythm Association Practical Guide on the Use of Non-Vitamin K Antagonist Oral Anticoagulants in Patients with Atrial Fibrillation. Europace : European pacing, arrhythmias, and cardiac electrophysiology : journal of the working groups on cardiac pacing, arrhythmias, and cardiac cellular electrophysiology of the European Society of Cardiology. 2021;23(10):1612-76.
29. Terrier J, Gaspar F, Fontana P, Youssef D, Reny JL, Csajka C, et al. Drug-Drug Interactions with Direct Oral Anticoagulants: Practical Recommendations for Clinicians. Am J Med. 2021;134(8):939-42.
30. Moner-Banet T, Alberio L, Bart PA. Does One Dose Really Fit All? On the Monitoring of Direct Oral Anticoagulants: A Review of the Literature. Hamostaseologie. 2020;40(2):184-200.
der informierte @rzt
- Vol. 13
- Ausgabe 2
- Februar 2023