- Fatigue beim älteren krebsbetroffenen Menschen: Diagnose und Behandlung
Im Rahmen des Geriatrie-Seminars der Barmelweid-Akademie sprach PD Dr. med. Florian Strasser, Cancer Fatigue Clinic (Onkologie Schaffhausen, KS Münsterlingen, Zentrum Radiotherapie Rüti, Zentrum für Integrative Medizin, Kantonsspital St. Gallen) zum Thema Fatigue. Dabei wies der Vorsitzende Dr. med. Matthias Schlögl, Barmelweid, darauf hin, dass Fatigue im klinischen Alltag häufig unterschätzt wird.
Die erste Botschaft des Referenten lautete: Machen Sie das Assessment, verpassen Sie es nicht! Es ist wichtig, zwischen Fatigue im Zusammenhang mit der Krebstherapie und Fatigue im Zusammenhang mit der Krebserkrankung zu unterscheiden. Fatigue ist nicht durch körperliche Aktivität erklärbar und beeinträchtigt auch nicht die gewohnten Funktionen. Ruhe- und Schlafphasen bringen wenig oder keine Erholung.
Krebsbedingte Müdigkeit bei älteren Menschen
Die Erkenntnisse aus dem Jahr 2013 waren:
Inflammation – Zytokine,
Depression, Antikrebs-Therapie Toxizität,
Energie- und Muskel Dysregulation,
Komorbiditäten.
Die Erkenntnisse aus dem Jahr 2023 sind:
Inflammaging, Krebskachexie, Depression, Antikrebstherapie, Toxizität aller Modalitäten
Kognitiv, Mitochondrien
Energie- und Muskeldysregulation
Definition der Krebs-Fatigue
Krebsbedingte Fatigue stellt eine belastende, anhaltende, subjektive Empfindung von physischer, emotionaler und/oder kognitiver Müdigkeit oder Erschöpfung dar, die durch die Krebserkrankung (Cancer disease related) oder durch die Krebsbehandlung (Cancer therapy associated) verursacht wird. Die Fatigue lässt sich nicht durch körperliche Aktivität erklären und beeinträchtigt das gewohnte Funktionieren. Ruhe- und Schlafphasen erweisen sich als wenig oder gar nicht regenerativ.
Tumorkachexie – eine Ursache von Fatigue
Im Kontext einer aktiven Krebserkrankung sind Wahrnehmungen rund um das Essen und körperliche Funktionen verändert. Tumorgewebe ist metabolisch aktiv und verursacht Entzündungen sowie Muskelabbau. In Stress-Situationen werden Hungersignale herunterreguliert. Die verschiedenen Sättigungssignale sind aktiv, jedoch ohne Magenfüllung und trotz eines Energiedefizits. Die Patientin bzw. der Patient erlebt Appetitlosigkeit, frühe Sättigung, Dysgeusie, Verstopfung, Durchfall, Müdigkeit (physisch)/Fatigue, Angst und Ungewissheit.
Tumorkachexie, Malnutrition und Sarkopenie sind überlappende Syndrome.
Malnutrition bezeichnet einen Zustand, bei dem die Nahrungsaufnahme reduziert ist, was zu einem Verlust an Muskelmasse führt.
Sarkopenie bezeichnet den Verlust an Muskelmasse, der durch verschiedene Faktoren bedingt sein kann, darunter Malnutrition, Alter, Kachexie oder Tumorkachexie.
Tumorkachexie bezeichnet ein Spektrum, das sich aus folgenden Kriterien zusammensetzt:
- Präkachexie: Appetitlosigkeit, körperliche Fatigue, CRP > normal
- Kachexie: Gewichtsverlust > 5 % oder BMI < 20 und Gewichtsverlust > 2 %. Sarkopenie und Gewichtsverlust > 2 % oft mit eingeschränkter Nahrungseinnahme/systemischer Inflammation
- Refraktäre Kachexie: variabler Grad an Kachexie. Die Krebserkrankung ist prokatabolisch, wobei sie zudem resistent gegenüber einer onkologischen Therapie ist.
- Der Leistungsstatus ist reduziert (2, 3, 4).
Die Survivorship Fatigue stellt sich zwei Jahre nach einer multimodalen, Krebs-gerichteten Behandlung in kurativer Intention als Cancer Treatment Related Fatigue (CTRF) dar. Das Energielevel liegt bei voller Performance bei 2, bei limitierter Performance bei 3 Stunden.
CtRF (Survivorship Fatigue) Was ist der Mechanismus?
- Reduktion der Mitochondrien (Zahl, Grösse,) im Muskel in astralen Gliazellen, noch experimentell
- Störungen des autonomen Nervensystems: HRV mittels Biofeedback, noch experimentell
- Dysregulation inflammatorischer Zytokine (i. Blut Veränderungen variabel und unter den üblichen Normwerten, z. B. IL-10)
- Störung hypothalamischer, serotoninerger und zirkadianer Regelkreise ( u. a. Melatonin: im ZNS, nur bezüglich Schlafmedizin teilweise therapeutisch verwertbar
- Störungen der neuro-kognitiven Funktion: Neuropsychologische Untersuchung
- Genpolymorphismen für Regulationsproteine führen zu unterschiedliche Veranlagungen für CtRF.
Die Chemotherapie führt zu einer Verringerung der Anzahl und Grösse der Energiekraftwerke (Mitochondrien) in den Muskeln. Dies signalisiert dem Muskel, sich abzubauen (neue Medikamente sind in Entwicklung). Allerdings kann die Chemotherapie den Abbau des Muskels, der durch die Krebserkrankung bedingt ist, bekämpfen. Die Chemotherapie kann somit zu einer Verbesserung des Muskelabbaus führen.
Chemotherapie-assoziierte kognitive Dysfunktion (Chemobrain)
Gegenwärtig wird das glia-zentrische Modell favorisiert.
Es besteht eine Überlappung von CtRF und Chemobrain. Diagnostisch und therapeutisch ähnelt das Vorgehen bei alleiniger CtRF: neurokognitive Untersuchung und multimodales Programm. Alle krebs-spezifischen Therapien können Fatigue verursachen. Die am häufigsten auftretende Ursache ist die Chemotherapie.
In einer im Jahr 2017 veröffentlichten Studie (Kogure E et al. J Phys Ther Sci 2017;29:2004-8) wurden die Veränderungen der körperlichen Funktion und der Müdigkeit untersucht. Die Unterschiede zwischen postoperativen Patienten mit gastroenterologischen Karzinomen, die 65 Jahre oder älter waren, wurden mit solchen unter 64 Jahren verglichen. Zudem wurden die Korrelationen zwischen dem Alter und jeder Bewertung bei den drei Gelegenheiten untersucht. Die 6MWD erwies sich als der Hauptunterschied zwischen der älteren und der jüngeren Gruppe. Dabei zeigte sich, dass die erstere nach der Operation signifikant niedrigere 6MWD-Werte als die letztere aufwies. Das Alter korrelierte positiv mit der 6MWD und Albumin nach der Operation und nach der Entlassung.
Des Weiteren konnte eine negative Korrelation zwischen dem Alter und dem CFS (Cancer Fatigue Scale) nach der Operation sowie nach der Entlassung festgestellt werden. Es wird angenommen, dass ältere Patienten mit höherer Wahrscheinlichkeit eine Abnahme der Belastungstoleranz und eine Zunahme der Müdigkeit erfahren.
Vollnarkosen können kognitive Fatigue verursachen, wobei das Narkosemittel eine Rolle spielt. Diesbezüglich sei auf die Studie von De Bias G et al. (Neurosurgery 2022; 90: 186-191) verwiesen.
Fatigue ist häufig bei allen Tumorarten, vor allem aber bei Mamma- und ZNS-Karzinomen. Die Fatigue stellt eine häufige Langzeit-Nebenwirkung der krebsspezifischen Therapie sowie der Krebserkrankung selbst dar. Von entscheidender Bedeutung ist das systematische (!) Erkennen der Symptomlast sowie der Funktionseinschränkungen, wie der Referent hervorhob. «Welcher Standard ist in Ihrer Klinik bereits implementiert?», fragte er in die Runde.
ESAS oder andere Tools:
Proaktiv, körperlich und psychisch, quantitativ, verbal auch möglich (kein, mittel, stark) – dies ermöglicht die Erfassung des Empfindens von Patienten. Dabei wird oft unterschätzt, dass Angst, Anorexie und Depressionen sowie Fatigue bei Patienten auftreten können. Schwellenwerte: ≥ 4/10 oder individuelles Symptomziel.
Der Schwellenwert für Fatigue liegt bei ≥ 4/10.
Lassen sich Unterschiede bezüglich der Symptomlast bei Depression bzw. Fatigue zwischen älteren und jüngeren Krebsüberlebenden feststellen? Wie ist der Unterschied zwischen Frauen und Männern? Hinsichtlich Depressionen zwischen älteren und jüngeren Erwachsenen wurden keine Unterschiede festgestellt. Frauen berichten jedoch über höhere Raten von Depressionen und höhere Schmerz- und Müdigkeitswerte.
Assessment
Körperlich manifestieren sich die Symptome in Form von Müdigkeit, Erschöpfung, Schwäche, Kraftlosigkeit und einer reduzierten Leistungsfähigkeit. Emotionale Beeinträchtigungen äussern sich in Form von psychischer Erschöpfung, mangelndem Antrieb, Motivationsproblemen, Interessenverlust, Niedergeschlagenheit, Ängsten und Frustration. Kognitive Beeinträchtigungen zeigen sich in Form von Konzentrationsproblemen, Gedächtnisproblemen und Problemen beim Denken.
Im Anschluss erfolgte eine Erörterung des diagnostischen Vorgehens bei Fatigue. Dabei wurden die folgenden Aspekte thematisiert: die Stärke der Müdigkeit, die drei Domänen der Müdigkeit (Müdigkeit „im Kopf“, „keine Freude“, „keine Kraft“) sowie die Verbesserung der Müdigkeit durch Schlaf. Die Bewertung erfolgte jeweils anhand einer Skala von 0 bis 10 Punkten. Ein weiteres Assessment verwendet die Cancer Fatigue Scale (CFS-D: 15 Punkte). Ein weiteres diagnostisches Interview zum Cancer Treatment Related Fatigue Syndrome stellt der Interview-Guide von Alexander Kiss dar. Der Fragebogen umfasst 12 Fragen, die sich auf verschiedene Aspekte der Fatigue beziehen. Dazu zählen Schwäche, Müdigkeit, Konzentration, Gedächtnis, Schlaf, Alltagstätigkeiten und die Belastung durch Fatigue.
Diagnose des krebsassoziierten Fatiguesyndroms
DICRFS: (Diagnostic Interview for Cancer-Related Fatigue) >6/12
Genaue Anamnese: Geschichte der Krebsbehandlung: Ist Fatigue während der Krebsbehandlung aufgetreten?
a) Systemische, (medikamentöse) Krebsbehandlung, typisch G2/3. Fatigue zwischen Tag 4 – 11. Die Schwere der Fatigue nimmt mit der Anzahl der Zyklen zu. Eine Assoziation mit Chemotherapie/induzierter Neuropathie sowie anderen Nebenwirkungen.
Ursachen und deren Abklärung
Körperlich: Malnutrition: Essprotokoll. Albumin, Vitamine (B12, D), Eisenstatus, Zn. Tumorkachexie: Gewichtsverlust, Anorexie, CRP, Tumoraktivität. Sarkopenie (Muskelverlust): Inaktivität, Alter, Kachexie, C-Steroide. Toxizität (Muskel) krebsspezifische Therapie: Anamnese,
Emotional: Angst, Depression: ESAS, HADS, BAI, BDI-II, Trauma: SkPTBS. Ungewissheit: Krankheits- und Prognoseverständnis.
Medikamentös: Anamnese (!) Opiat, Benzodiazepine, Antidepressiva, Krebstherapie-assoziiertes Müdigkeitssyndrom (CtRF).
Kognitiv: Vollnarkosen, kognitive Einschränkungen Schlaganfall, Unfall
Gemischt: Dehydrierung, Anamnese (Urin, Trinken), Haut, Halsvenen
Elektrolyte: Phosphat, Calcium, ev. Na, ev Mg
Organfunktion: Biere, Leber, Herz (NT-proBNP), Lunge (AF, O2-Sättigung)
Entzündung (Tumor)/Infektion): Anamnese, CRP:
Endokrin: TSH, freies Testosteron. (Männer)
Anämie (Hb <10g/dl)
Schlafstörungen (SAS, Beinbewegungen, Störungen): ESS, PSQ)
Atemlosigkeit korreliert mit Fatigue
Atemlosigkeit, die anhand von D-12 und MDP gemessen wurde, war bei älteren Männern mit einer schlechteren Müdigkeit verbunden, und zwar in ähnlicher Weise bei den verschiedenen Dimensionen der Atemlosigkeit (Cristea I et al PLOSone 2023;18:e0296016.
Risikofaktoren für CtRFS
Vorbestehende psychosoziale Belastung, Traumata, körperlich/emotional vorbestehende psychiatrische Krankheit, Unverständnis von Angehörigen, Mitarbeiter/-innen, Stigma Behinderung, chronisches Schmerz-Syndrom,
Fibromyalgie, schwere CIN P. Unzureichende persönliche Ressourcen, um mit Stress umzugehen, die finanzielle oder soziale (Über-)Belastung, die fehlenden körperlichen Aktivitätsgewohnheiten sowie die ungesunden Essgewohnheiten stellen weitere Risikofaktoren dar.
→ Oft «multiple hit»: Anhäufung wiederkehrender
Ursachen-Schädigungen
→ Vulnerabilitäts-Stress-Modell (aus der Psychiatrie)
Parameter eines umfassenden Tumorkachexie-Assessments mit Empfehlungen für Tools
Körpergewicht, Gewichtsverlust (3 Monate)
Die Messung der Nahrungsaufnahme erfolgt anhand des individuellen Bedarfs. Evtl. auch Messung der Muskelmasse (wenn möglich in Klinik; B/A Waage
CRP, Albumin /ev. indirekte Kalorimetrie)
ECOG PS, individuell (z.B. n Stockwerke)
Handkraft (Jamar), FTSTS (Five Times Sitt o Stand Test, praktisch wenig validiert)
ev. 4-Meter gait-speed (1.5-4-1.5m)
Nutritition Impact & GI-Symptome (Checkliste, PG-SGA)
Symptome, Belastung (ESAS, EORTC-QIQ-Cax24)
Onkologische Situation: Tumor behandelbar aktuell?
→ Wichtiger ist «machen» im klinischen Alltag, als das perfekte Instrument finden.
Behandlung
Behandlung von Menschen mit (Survivorship-) Fatigue:
Beginnt mit der Diagnose der Krebserkrankung und der Krebsbehandlung. Regelmässige körperliche Aktivität im Alltag und formelles Ausdauer- & Krafttraining. Eiweissreiche (vorwiegend pflanzliche), entzündungshemmende Ernährung. Umgang mit emotionaler Belastung, Information, Kommunikation. Stärkung von Selbstwirksamkeit und Kohärenz
Die Behandlung ist immer multimodal
- Energiemanagement
- Körperliche Aktivität
- Achtsamkeitsinterventionen, Mind-Body
- Psychologische Begleitung & Behandlung: Energiefresser (emotional, traumat.)
- Ernährung
- Arzneimittel pflanzlich: ev. Mistel, ev. GinsengYoga, ev. Akupunktur, ev. Massagen
- Gemeinschaft (peer-support) ist hilfreich
- CIM-Behandlungen:
Medikamentöse Behandlung von Patient:innen mit Survivorship-Fatigue
«Es gibt nichts»
Methylphenidat (Ritalin) evtl. bei AD(H)S
Antidepressiva: bei Depression (als Co-Faktor), nicht bei CtRF
Kortikosteroide: nicht bei CtRF, nur bei Tumorkachexie (NUR < 2 Wochen!)
Melatonin: RCT negativ
Testosteron: nur bei Hypogonadismus (Männer, nicht Prostata-CA)
Ginseng und Guarana: wenige Studien, unklar
Mistel: nur während Chemotherapie, Bestrahlung und nicht kurativ
Bewegungsrichtlinien für Krebsüberlebende Konsenerklräung eines internationalen multidisziplinären Roundtables
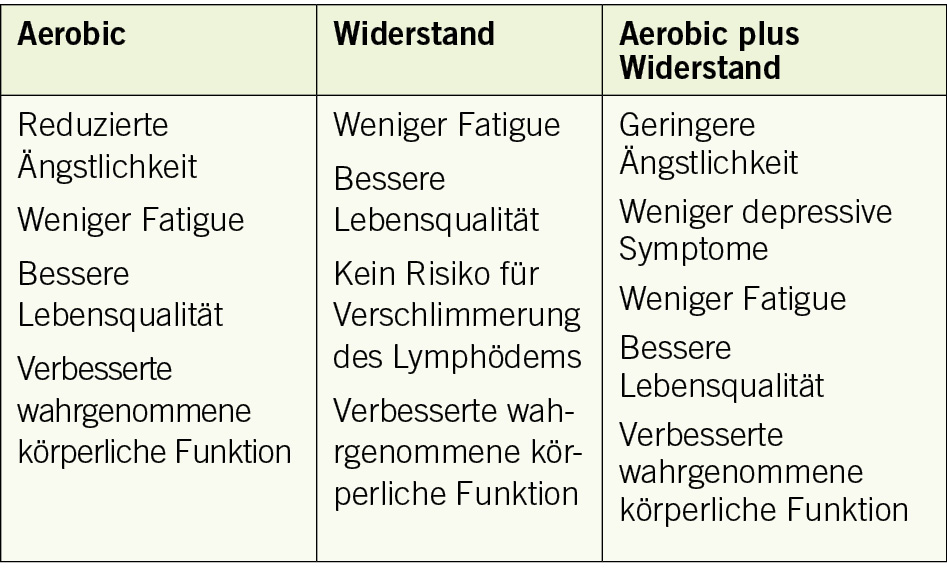
Erwarteter Patientennutzen von Bewegungstraining nach Modus
Der Effekt von Ausdauer- und Krafttraining auf Fatigue ist am besten bei moderater bis energischer Intensität (aerobic) nachgewiesen.
Ausdauertraining (oder Cardio-Kraft) sollte 2-3 x pro Woche (1 h Pause) über einen Zeitraum von 30-40 Minuten durchgeführt werden. Ein fünfminütiges Training (oder High Intensity Intervall Training) mit Überwindung (Borg 5-7/10), Schwitzen sowie erhötem Puls ist empfehlenswert.
Supervidiertes Training hilft, zudem wirkt ein Trainingsprotokoll motivierend (zudem gut für die Kostengutsprache). In einer randomisierten, kontrollierten Studie bei Brustkrebspatientinnen konnte nachgewiesen werden, dass eine pflanzliche, proteinreiche Ernährung während der adjuvanten Chemotherapie die Entwicklung von Fatigue reduzieren kann (Sathiara E. et al. Nutr Cancer 2023;75:848-856).
Des Weiteren konnte in einer Studie nachgewiesen werden, dass eine antientzündliche Ernährung den Ernährungsstatus und die Fatigue im Vergleich zur Kontrollgruppe verbessern kann. Des Weiteren wies der Referent auf die Broschüre der Krebsliga „Fatigue bei Krebs” hin, welche unter anderem folgende Inhalte umfasst: Verständnis von Fatigue, adäquate Diagnostik, angemessene Begleitung, multimodales Interventionsprogramm, Dokumentation für Versicherungen, Energiemanagement, Schlaf, Förderung und Begleitung von Selbstmanagement, auch (geführte) Selbsthilfegruppen.
Information und Motivation sind wesentliche Elemente, um die Betroffenen zu erreichen und zu einer Verhaltensänderung zu motivieren. Dabei ist es wichtig, die individuellen Bedürfnisse und Lebensumstände zu berücksichtigen.
Der Calman-Cap ist ein Messinstrument, das die Lebensqualität als Differenz zwischen Erwartungen und der Realität beschreibt.
Energie-«Management» erlernen
Energie-Level (NRS, Pfeile, …), Energiereserven (Zeit), Müdigkeit: Energie-Fresser und Energie-Quellen beobachten, Reha-Interventionen dokumentieren.
Schlaf
Energie-Fresser: Emotionale Belastung, Erwartungen, Nicht nein-sagen
Energie-Geber/Quellen: Entspannung, Sich was Gutes tun, Reha-Therapien
Im Rahmen der Prioritätensetzung ist zunächst eine Differenzierung zwischen den Bereichen Alltag, Freizeit, Beruf und Reha-Therapien vorzunehmen. Dabei stellt sich die Frage, in welchen Bereichen die eigenen Energiereserven investiert werden und welchen Sinn dies hat.
Im Rahmen einer Studie wurde festgestellt, dass die Durchführung von regenerativem Yoga zu Hause fünf Mal pro Woche für die Dauer von 50 Minuten die Intensität der Fatigue-Symptome sowie die Funktion verbessert und zudem entzündliche Blutmarker reduziert.
Ernährung bei Krebs
Es ist zu eruieren, ob der Patient einem Ernährungsrisiko ausgesetzt ist. Dazu ist eine umfassende Bewertung durchzuführen, welche den Ernährungszustand, den Stoffwechselzustand, den funktionellen Status, die auftretenden Symptome, Schmerzen, Dyspnoe usw. berücksichtigt. Zudem sind die psychische und soziale Belastung sowie die eingenommenen Medikamente zu evaluieren. Basierend auf den eruierten Daten ist eine massgeschneiderte Intervention zu initiieren, welche eine individuelle Ernährungsintervention durch ein ernährungswissenschaftlich geschultes Team, die Linderung/Behandlung von ernährungsbedingten Symptomen beinhaltet.
Des Weiteren ist eine psychologische/soziale Unterstützung sowie ein angeleitetes körperliches Training (Kraft, Ausdauer) indiziert. Zudem ist eine Berücksichtigung von Behandlungsmöglichkeiten erforderlich.
Die Espen-Richtlinien enthalten Empfehlungen zur Ernährung von Krebspatienten. Im Rahmen einer Überarbeitung wurden die Richtlinien gekürzt und die Anwendung in der Praxis vereinfacht. Insgesamt wurden 43 Empfehlungen mit kurzen Kommentaren für das Ernährungs- und Stoffwechselmanagement von Patienten mit neoplastischen Erkrankungen vorgestellt. Den krankheitsbezogenen Empfehlungen sind allgemeine Empfehlungen zur Diagnostik des Ernährungszustandes bei Krebspatienten vorangestellt. Der Leitfaden bietet Gesundheitsdienstleistenden, die an der Behandlung von Krebspatienten beteiligt sind, eine praktische Anleitung für eine optimale Ernährungsversorgung (Mucaritoli M. et al. Clin Nutr. 2021; 40: 2898-2913).
Die Frage, welche Ernährungsweise dazu geeignet ist, das Risiko einer Krebserkrankung zu reduzieren, zu minimieren oder deren Fortschreiten zu verhindern, ist Gegenstand zahlreicher wissenschaftlicher Untersuchungen. Dabei konnte nachgewiesen werden, dass eine mediterrane Ernährung, die reich an ungesättigten Fettsäuren ist, einen positiven Einfluss auf die Gesundheit hat. Auch eine vegetarische oder vegane Ernährungsweise kann das Risiko einer Krebserkrankung reduzieren. Mikrobiom: Erde („Dreck“), Ballaststoffe, geringer Zuckergehalt (Dessert nach Mahlzeiten akzeptabel), Fastenimpulse (Intervall, Tage etc.), keine Nährstoffdefizite
„Welche Ernährungsweise ist empfehlenswert, wenn eine aktive Krebserkrankung vorliegt?“
Eine proteinreiche Ernährung (>1,4 g/kg Körpergewicht), eine adäquate Energiezufuhr (30 kcal/kg Körpergewicht) sowie das Fehlen von Nährstoffdefiziten (Vitamin D, B12, Folsäure u. a.) sind wesentliche Elemente einer solchen Ernährung. Zudem ist eine hohe Frequenz der Mahlzeiten zu beachten.
Ein Grossteil des Fatigue-Managements betrifft Empfehlungen für ein gesundes und selbstwirksames Leben mit und nach Krebs sowie für ein langes Leben.
Die Ernährung ist bewusst, mediterran und beinhaltet Fastenimpulse. Viel Bewegung, viel Gehen, inklusive Treppensteigen. Der Schlaf-Rhythmus und Rituale sind ebenfalls wichtige Elemente. Achtsamkeit im Hier und Jetzt, das Spüren und Atmen sind ebenfalls von Bedeutung. Das „Wozu” des eigenen Lebens, Dankbarkeit und Freude sind ebenfalls wichtige Faktoren. Die Naturverbundenheit ist von Bedeutung.
Bei Leben mit Krebs wird das Leben, Empfinden, die Gefühle und die Liebe oft intensiver, so die Schlussworte des Referenten.
riesen@medinfo-verlag.ch