- Früherkennung von Frailty Geriatrisches Assessment in der Hausarztpraxis
Der demographische Wandel wird sich sehr schnell auch in der hausärztlichen Sprechstunde bemerkbar machen. Die dort gesehenen älteren Patienten sind bereits jetzt zahlreich und werden in Zukunft noch älter und zahlreicher! Für deren adäquate Betreuung wird nicht das chronologische, sondern das biologische Alter (einhergehend mit Gesundheitszustand und vorhandenen funktionellen Reserven) entscheidend sein. Eine auf Alltagsfunktionalität basierte Frailty-Klassifikation (wie z.B. die Frailty-Klassifikation nach Fried) kann hier nicht nur schnell Klarheit schaffen, sondern auch die Indikationsstellung für weitere Diagnostik und Therapie beeinflussen. Ein umfassendes Frailty-Assessment ist sehr zeitaufwändig und im ambulanten Setting meist unrealistisch. Gezielt gewählte kurze geriatrische Assessments können hier ebenso zielführend sein, einen frühen Abbau in den wichtigsten Gesundheitsdimensionen zu identifizieren und entsprechend anzugehen. Frühe Interventionen haben die grösste Chance, Frailty zu verhindern oder zu verzögern und damit die Unabhängigkeit und hohe Lebensqualität von Patienten so lange wie möglich zu sichern.
Demographic change will very quickly make itself felt in GP consultations. The older patients seen there are already numerous and will become even older and more numerous in the future! It is not chronological age, but biological age (together with state of health and existing functional reserves) that will be decisive for their adequate care. A frailty classification based on everyday functionality (such as Fried’s frailty classification) can not only quickly provide clarity here, but also influence the indication for further diagnostics and therapy. A comprehensive frailty assessment is very time-consuming and usually unrealistic in an outpatient setting. Targeted, brief geriatric assessments can be just as effective in identifying and addressing early deterioration in the most important health dimensions. Early interventions have the greatest chance of preventing or delaying frailty and thus ensuring patients’ independence and high quality of life for as long as possible.
Key words: elderly patients, frailty, geriatric assessments
Einleitung
Die von Hausärzten und stationären medizinischen Gesundheitsinstitutionen zu behandelnden hochaltrigen Patienten werden – angesichts der immer noch steigenden Lebenserwartung – nicht nur stetig älter, sie nehmen auch zahlenmässig aus demographischen Gründen zu. Viele Hochaltrige sind heute – im Vergleich zu vor 20 Jahren – in viel besserem, ja ausgezeichnetem Gesundheitszustand. So hat sich z.B. das Durchschnittsalter für operative Wahleingriffe zum Hüftersatz massiv nach oben verschoben. Im Gegensatz zur Altersmedizin und Inneren Medizin, wo invasive diagnostische oder therapeutische Interventionen mit möglichen Zusatzrisiken für den Patientengesamtzustand eher die Ausnahme bilden, sind z.B. Grundversorger bei der Indikationsstellung für chirurgische Eingriffe bei älteren und hochaltrigen Pa-tienten zunehmend gefordert, Eingriffsrisiken hinsichtlich Operationsbenefit und -risiko abzuwägen. Unter den medizinischen (Spezial-)Disziplinen besteht zunehmend Einigkeit, dass hier nicht primär das chronologische Alter, sondern die individuelle Vulnerabilität («Frailty») eines älteren Patienten berücksichtigt werden muss. Dass diese Vulnerabilität für Operations-Outcomes entscheidend ist, wird allgemein nicht bestritten, aber wie diese Vulnerabilität älterer Patienten erkannt respektive definiert werden soll, ist – je nach medizinischer Disziplin und Sichtweise – sehr verschieden. Aus Hausarztperspektive ist neben der bewussten Diagnosestellung einer bereits existierenden «Frailty» für die bewusste Indikationsstellung weiterführender Spezialuntersuchungen/-eingriffe, die frühzeitige Erfassung eines beginnenden Frailty-Prozesses und rechtzeitig eingeleitete Präventivmassnahmen von grösster Bedeutung.
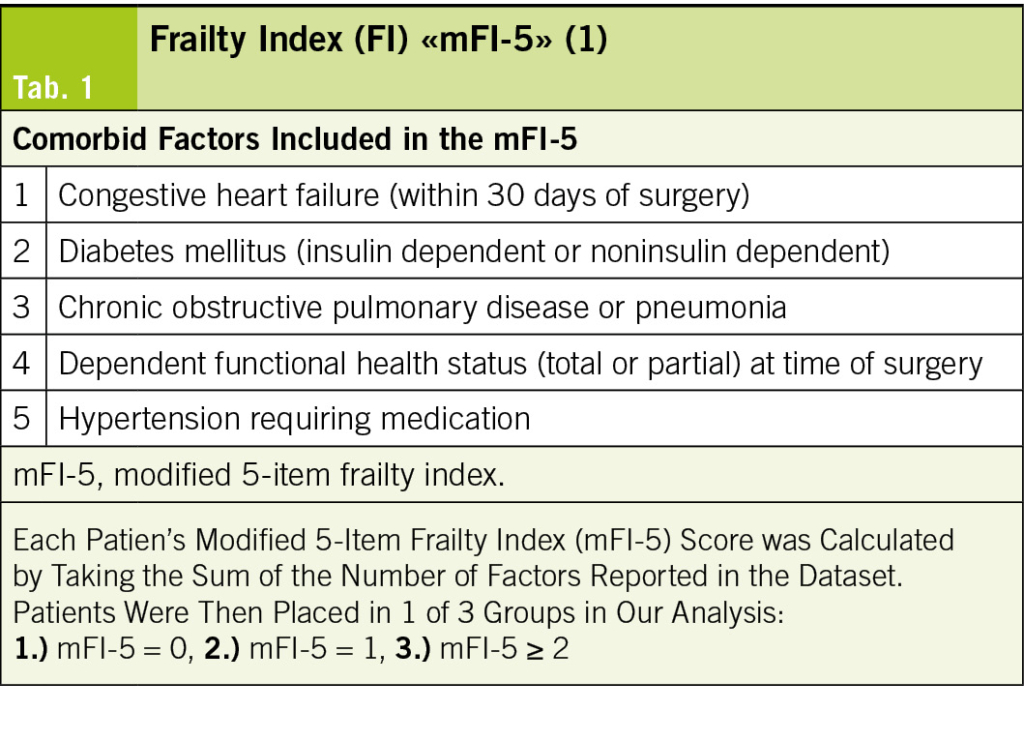
Der vor 2 Jahren publizierte und in chirurgisch behandelten älteren Patienten validierte modifizierte Frailty Index (FI) «mFI-5» basiert auf 5 Komorbiditäts-Risikofaktoren (Herzinsuffizienz, Diabetes mellitus, chronisch obstruktive Lungenerkrankung oder Pneumonie, abhängiger funktioneller Status (total oder partiell) zum Zeitpunkt der Operation, arterielle Hypertonie) (Tab. 1) (1). Im Vergleich zu einer jüngeren Patientenpopulation wurde der «mFI-5» in einer geriatrischen Patientenpopulation als schlechter, aber immer noch effektiver Prädiktor für Mortalität und postoperative Komplikationen befunden.
Der «Study of Osteoporotic Fractures (SOF) frailty index» (2) ist ein weiterer sehr einfach anwendbarer Index, der lediglich aus drei Items besteht: a) Nicht intentionaler Gewichtsverlust von > 5 % binnen des letzten Jahres, b) Verneinung der Frage «Fühlen Sie sich energiegeladen?», c) Unfähigkeit, 5-mal vom Stuhl aufzustehen und sich wieder hinzusetzen. Die Klassifizierung als Frail tritt dann ein, wenn mindestens 2 der 3 genannten Kriterien erfüllt werden. Hierdurch kann es unter medizinischen Akutbedingungen zu systematischen Überschätzungen der Frailtyprävalenz kommen. Dennoch hat sich der SOF als valides Untersuchungsinstrument behauptet und die konvergente Validität zu umfangreicheren anderen FIs bestätigen können.
Mehrere nationale und internationale Empfehlungen, unter anderem die «Entscheidungen über die Zuteilung von Ressourcen in der Notfall- und der Intensivmedizin im Kontext der COVID-19-Pandemie» der Deutschen Interdisziplinären Vereinigung für Intensiv- und Notfallmedizin (DIVI) heben klar die Bedeutung der Verwendung der Clinical Frailty Scale (CFS) / deutsch: Klinischen Frailty Skala hervor. Ziel ist die Identifizierung von Pa-tienten mit einem erhöhten Risiko für einen ausbleibenden Behandlungserfolg, welche nicht von einer intensivmedizinischen Intervention profitieren dürften. Die CFS (deutsch: Klinische Frailty Skala) kann von allen adäquat geschulten Fachkräften im Gesundheits- oder Pflegedienst durchgeführt werden. Die Skala besteht aus 9 Kategorien (Abb. 1) (3).
Frailty: die altersmedizinische Sicht
Das geriatrische Frailty-Konzept basiert auf einer funktionellen Sichtweise und definiert sich als physiologische Vulnerabilität, die durch reduzierte homeostatische Reserven mit daraus resultierender verminderter Stressresistenz zustande kommt (4). Anders als in den obengenannten rein Diagnosen- oder Komorbiditäten-basierten Assessments kommen hier auch funktionelle, am Patienten gemessene Parameter zur Anwendung: Gewichtsverlust, empfundene Erschöpfung, körperliche Aktivität, Ganggeschwindigkeit und Handschlusskraft (Abb. 2). Die erhaltenen Messresultate werden anhand von Normwerten beurteilt. Bei 3 oder mehr positiven Kriterien gilt der Patient als «frail». Dieser Frailty-Phänotyp war in der Originalstudie (auf drei Jahre) unabhängig prädiktiv für Stürze, verschlechterte Mobilität oder eingeschränkte ADLs, Hospitalisation, und Tod mit Risikoassoziationen von 1.82 bis 4.46. Die Studie zeigte auch, dass Frailty weder Synonym für Komorbidität noch körperliche Behinderung war, sondern vielmehr Komorbidität ein ätiologischer Risikofaktor für und Behinderung ein Resultat von Frailty ist! Die Messung der Hirnleistung ist nicht Teil der Fried Frailty Klassifikation. Da eine demenzielle Entwicklung immer auch zu einer Frailty beitragen kann, muss die Fried-Klassifikation immer in Kombination eines kognitiven Assessments erfolgen!
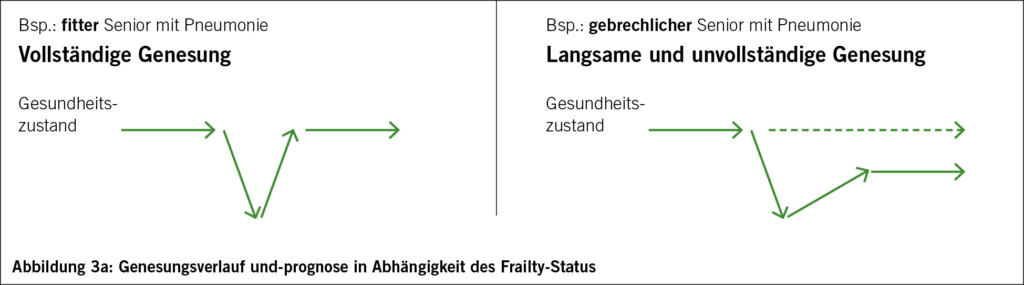
Ob ein Patient als «frail» oder «fit» klassifiziert wird, hat wesentliche Voraussagekraft bei Auftreten von Stressoren wie z.B. Infekten. Ein fitter Patient wird bei einer Pneumonie nach anfänglicher Verschlechterung des Gesundheitszustandes wieder schnell seinen gesundheitlichen Vorzustand erreichen. Anders bei einem fragilen Patienten: Hier wird der Genesungsprozess deutlich länger dauern und – ganz wesentlich – er wird gesundheitsmässig nicht mehr das Niveau seines Vorzustandes erreichen. Im konkreten Beispiel eines hospitalisierten, zuhause lebenden Seniors, der vor einer Pneumonie-Erkrankung bereits einen voll ausgeschöpften Unterstützungsbedarf von drei täglichen SPITEX-Visiten hatte, muss eine Rückkehr nach Hause – nach abgeheilter Pneumonie – bereits bei Spitaleintritt als unrealistisch gesehen werden. Entsprechend gilt es hier, sehr schnell eine Institutionalisierung zu planen (Abb. 3a).
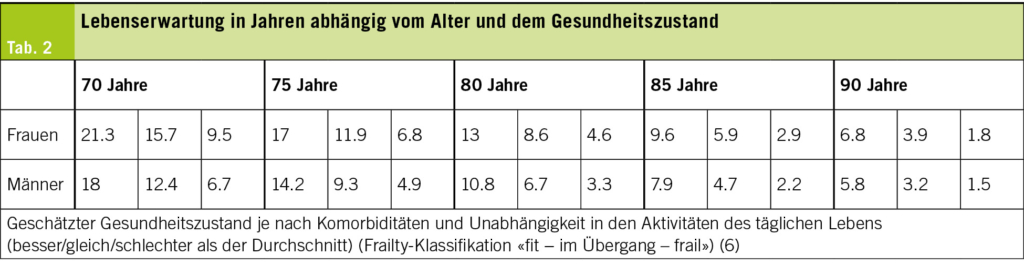
Die Kenntnis des Frailty-Status eines Patienten kann aber auch für andere medizinische Entscheide und Aussagen wesentliche Bedeutung haben. In der Sekundärprävention (z.B. Hypercholesterinämie und Verordnung von Statinen!) ist es bei hochaltrigen Patienten hilfreich, deren mittlere Lebenserwartung zu kennen. Je nach Frailty-Status ist dies bei einem 90-jährigen Mann 5.8 Jahre (fit), 3.2 Jahre (am Übergang zu «frail») oder 1.5 Jahre («frail») (Tab. 2).
Pathophysiologie und klinische Symptome von Frailty
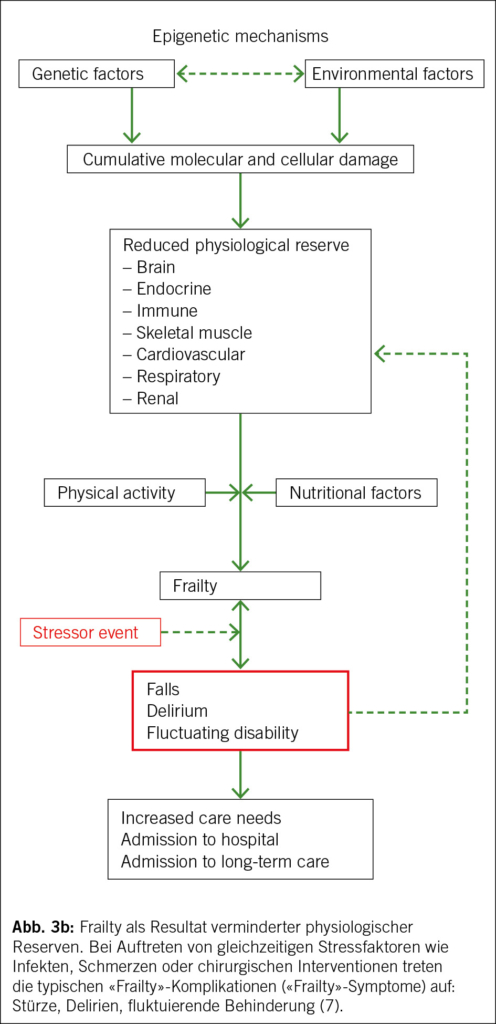
Frailty entsteht durch reduzierte physiologische Reserven in meist mehreren Organsystemen. Die dadurch entstandene verminderte Stressresistenz wird bei plötzlich auftretenden Stressfaktoren wie z.B. Infekten, Schmerzen, Operationen etc. sichtbar mittels drei «stereotyper» Hauptsymptome: Stürze, Delirium oder fluktuierender Behinderung (Abb. 3b) (7).
Das Geriatrische Assessment als Instrument zur Identifizierung von funktionellen Ressourcen
Ein vollumfängliches geriatrisches Assessment eines älteren Patienten (Abb. 4) zeigt nicht nur allfällige Defizite auf, sondern lässt auch sinnvolle und realistische Behandlungsziele für einen besseren Gesundheitsgesamtzustand sichtbar werden. Bei einem elektiv geplanten chirurgischen Eingriff kann dies z.B. eine Möglichkeit sein, den Patienten in einen für die Operation besseren Vorzustand zu bringen. Die Durchführung eines geriatrischen Assessments ist zeitaufwändig und gehört in die Hände eines geriatrischen Spezialisten-Teams. Nicht nur müssen die richtigen Assessment-Instrumente gewählt (zur Vermeidung von Boden- resp. Deckeneffekten), sondern auch die therapierbaren Defizite identifiziert und festgelegt werden. Als stellvertretendes Beispiel für therapeutische Möglichkeiten soll hier die gezielte Behandlung eines Proteindefizits mit Leucin-verstärkten Molkeprotein-Supplementen sein, womit Mobilität und Muskelkraft (ohne Training!) selbst bei Pflegeheimbewohnern substanziell verbessert werden kann (8). Eine derartige Vorbereitung z.B. bei einem chirurgischen Elektiv-Eingriff kann für die postoperative Rekonvaleszenz- und Rehabilitationsphase (und letztlich für das Operationsresultat) entscheidend sein!
Aus obigen Gründen und als Beispiel einer gesamtheitlichen Betreuung älterer Patienten hat sich in den letzten 10 Jahren vielerorts eine enge Zusammenarbeit zwischen Altersmedizin und operativen Disziplinen wie Orthopädie/Traumatologie mit der formalen Gründung von Alters-Traumazentren etabliert (9). Hier werden – unter Einhaltung von Qualitätsstandards – ältere Patienten entsprechend ihrer Gesamtbedürfnisse vor und nach der Operation interdisziplinär behandelt.
Der «Timed Up & Go Test» als modernes und schnelles Screening für Mobilität und Kognition
Um sich – auch ohne direkten Einbezug eines Geriaters – schnell und informativ zu Mobilität und kognitiver Fitness eines Patienten ein Bild machen zu können, gibt es einfache Screening-Tests, die sich ohne grosse Kosten oder Platzbedürfnisse auch in der hausärztlichen Praxis durchführen lassen.
Mobilität und «Frailty»: Für den Timed Up & Go Test (Abb. 5) (10) braucht es z.B. lediglich einen Stuhl mit Armlehnen und ein drei Meter davor aufgestelltes Ziel (Verkehrskonus, Flasche etc.), sowie eine Stopp-Uhr. Der Patient nimmt im Stuhl Platz. Auf das Kommando «Los» (Beginn der Zeitmessung) soll er aufstehen (normal, keine Kompetition, wenn nötig mit Gehhilfe!), nach vorne und um den Verkehrskonus herumgehen und sich wieder im Stuhl niedersetzen. Berührt sein Gesäss die Stuhlfläche, ist die Zeitmessung beendet. Braucht der Patient dafür länger als 10 Sekunden, steht eine mögliche «Frailty» im Raum (11). Ab 13.5 Sekunden besteht ein erhöhtes Sturzrisiko (12), mit für den Alltag relevanten Mobilitätsproblemen ist ab 20 Sekunden zu rechnen (10, 12).
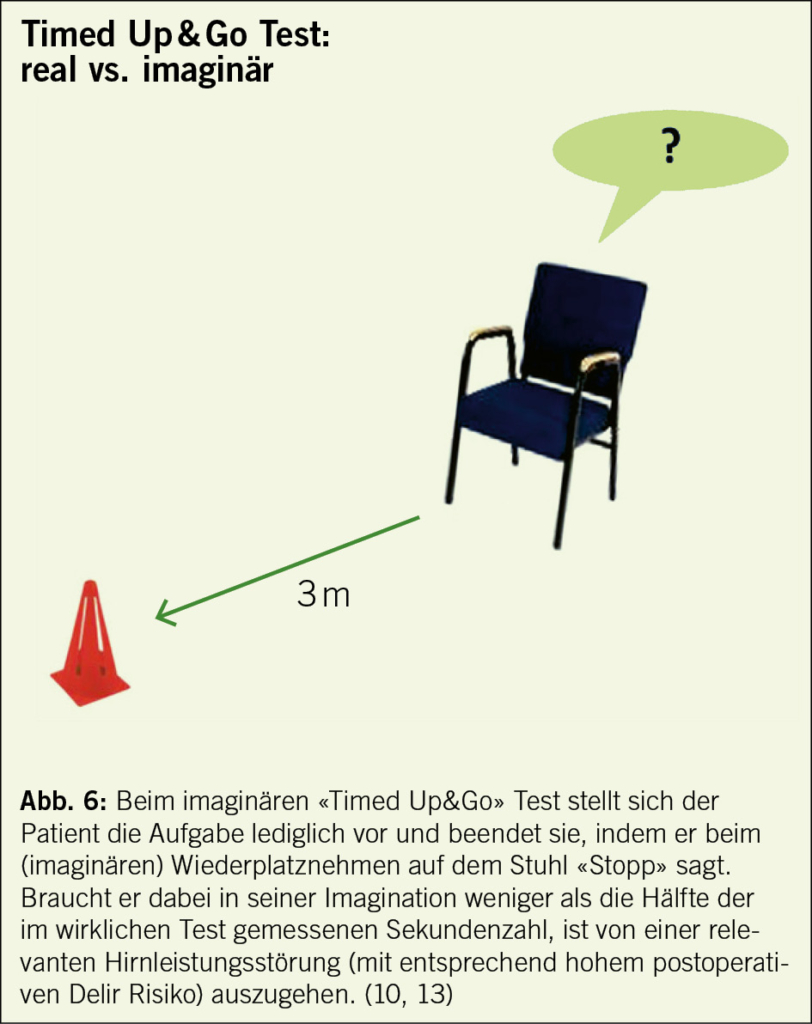
Motorisch-kognitives Dual-Tasking (Exekutivfunktion): Ein weiter entwickelter «Imagined Timed Up&Go» (13) kann auch sehr schnell über die kognitive Fitness (Exekutivfunktion) eines Patienten Auskunft geben: Dazu lässt man den Patienten – nach Durchführung des obigen Testablaufs – im Stuhl die gleiche Aufgabe nochmals durchführen, allerdings nur in seiner Vorstellung. Auf das Kommando «Los» macht er sich – in seiner Vorstellung – nochmals auf denselben Parcours und sagt «Stopp», wenn er sich wieder auf dem Stuhl zurückbefindet. Braucht der Patient für diese imaginäre Aufgabe weniger als halb so lang wie in Wirklichkeit, ist von einer erheblichen Hirnleistungsstörung (mit z.B. potentiellem postoperativem Delir-Risiko!) auszugehen (Abb. 6)!
Kognition und Emotion
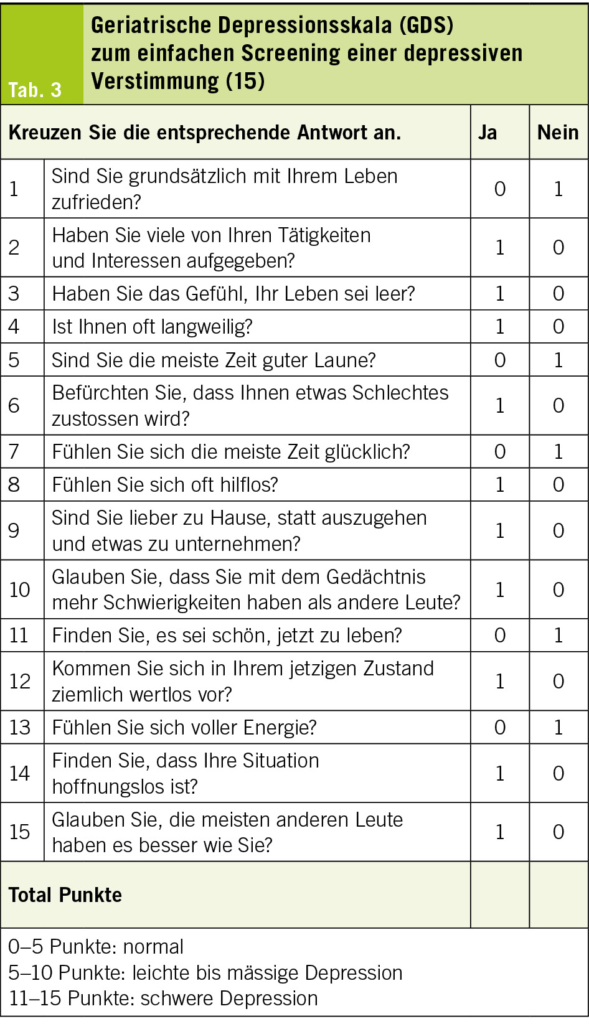
Ist der «Imagined Timed Up&Go» Test pathologisch, lohnt es sich allenfalls, einen «BrainCheck» durchzuführen. Hier kann mittels drei einfacher Fragen an den Patienten, 7 Fragen an den nächsten Angehörigen und einem Uhrentest in 90 % Sicherheit zwischen «normal» oder «weiter abklärungsbedürftig» unterschieden werden (14, https://braincheck.ch/de). Nicht selten kann auch eine depressive Verstimmung (im Alter am häufigsten verpasste psychiatrische Diagnose) die Hirnleistung verschlechtern. Hier lohnt sich die Durchführung eines kurzen Screenings mittels «Geriatric Depression Scale» (GDS) (Tab. 3, (15)).
Sarkopenie und Malnutrition
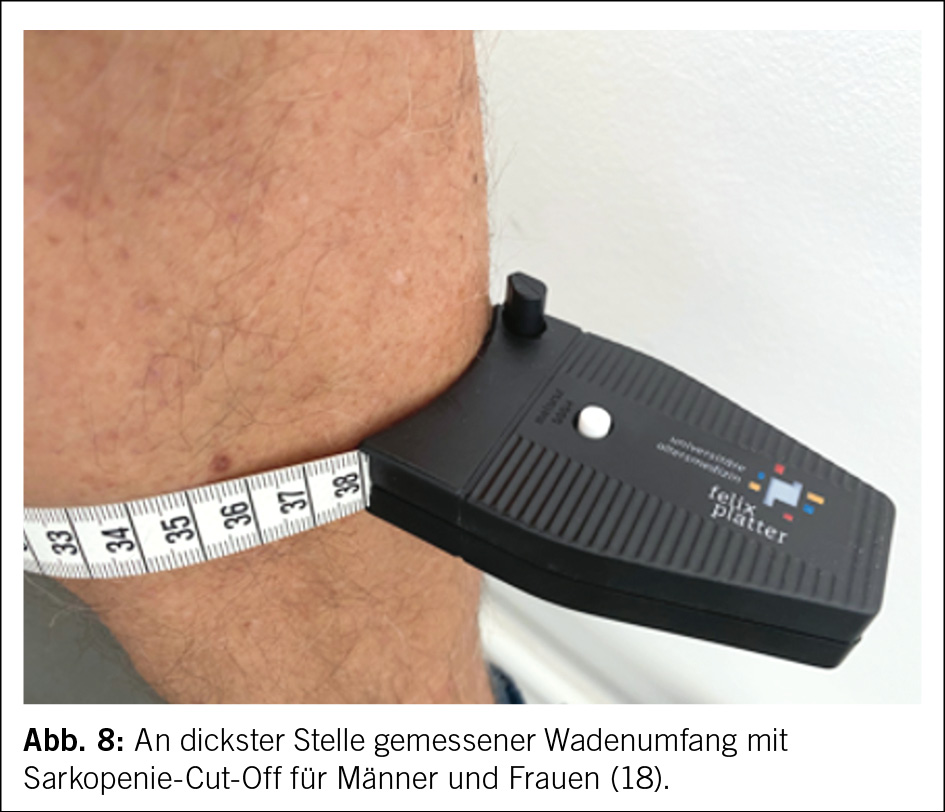
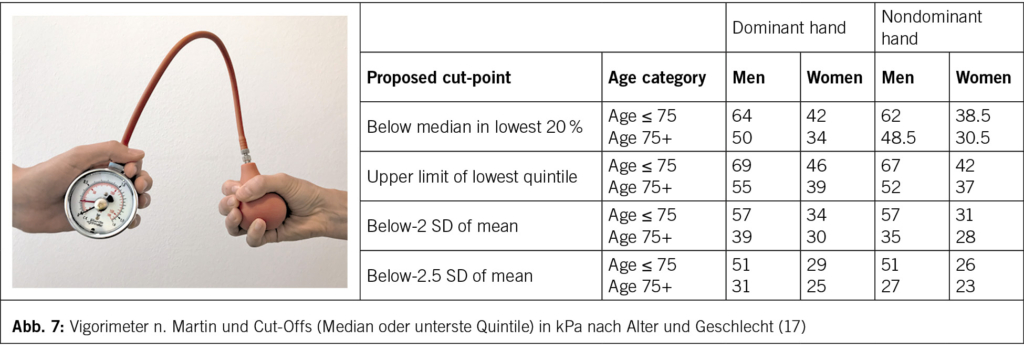
Dass ältere Menschen zum Erhalt ihrer Muskelmasse und -kraft sich nicht nur bewegen, sondern auch mehr Proteine essen müssen als jüngere Erwachsene, ist mittlerweile bekannt (16). Die frühe Identifizierung einer beginnenden Sarkopenie/Malnutrition hat – insbesondere auch angesichts der hier verfügbaren und therapeutisch sehr wirksamen Leucin-angereicherten Molkeprotein-Supplementen – für den Erhalt von Mobilität und funktioneller Unabhängigkeit entscheidende Bedeutung. Zur klinischen Diagnosestellung reicht meist die Bestimmung der Handschlusskraft (Vigorimetrie nach Martin, Abb. 7 (17)). Noch einfacher: auch die Messung des Wadenumfangs (Abb 8, (18)) kann hier schnell richtungsweisend sein.
Copyright
Aerzteverlag medinfo AG
Ärztlicher Direktor & Klinischer Professor für Geriatrie
Universitäre Altersmedizin FELIX PLATTER & Universität Basel
Burgfelderstrasse 101
4002 Basel
RetoW.Kressig@felixplatter.ch
Der Autor hat keinen Interessenkonflikt im Zusammenhang mit diesem Artikel deklariert.
Ein kurzes, klinisch orientiertes geriatrisches Assessment in der Hausarztpraxis kann Patienten mit beginnender oder bereits etablierter Frailty identifizieren, gleichzeitig aber auch allfällig vorhandene therapeutisch nutzbare Ressourcen aufzeigen. Dies kann einerseits für die sinnhafte Indikationsstellung weiterer Untersuchungen/Interventionen hilfreich sein, aber auch Hinweise auf mögliche therapeutische/präventive Massnahmen zur Verbesserung/Verzögerung von Frailty geben.
1. Subramanian S, Aalberg JJ, Soriano RP, Divino CM. The 5-Factor Modified Frailty Index in the Geriatric Surgical Population. The American Surgeon 2021;87:1420-1425.
2. Ensrud KE, Ewing SK, Taylor BC et al. Comparison of 2 frailty indexes for prediction of falls, disability, fractures, and death in older women. Arch Intern Med 2008;168:382–9.
3. Rockwood K, Song X, MacKnight C, Bergman H, Hogan DB, McDowell I, Mitnitski A. A global clinical measure of fitness and frailty in elderly people. CMAJ. 2005 Aug 30;173(5):489-95. doi: 10.1503/cmaj.050051. PMID: 16129869; PMCID: PMC1188185.
4. Fried LP et al. Cardiovascular Health Study Collaborative Research Group. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci 2001;56:M146-56.
5. Benzinger P, Eidam A, Bauer JM. Klinische Bedeutung der Erfassung von Frailty [Clinical importance of the detection of frailty]. Z Gerontol Geriatr 2021;54(3):285-296. German. doi: 10.1007/s00391-021-01873-z. Epub 2021 Mar 29. PMID: 33782735; PMCID: PMC8006639.
6. Walter LC, Covinsky KE. Cancer screening in elderly patients: a framework for individualized decision making. JAMA.2001;285(21):2750-6. doi: 10.1001/jama.285.21.2750. PMID: 11386931.
7. Clegg A, Young J, Iliffe S, Rikkert MO, Rockwood K. Frailty in elderly people. Lancet. 2013 Mar 2;381(9868):752-62. doi: 10.1016/S0140-6736(12)62167-9. Epub 2013 Feb 8. Erratum in: Lancet 2013;382(9901):1328. PMID: 23395245; PMCID: PMC4098658.
8. Bauer JM, Verlaan S, Bautmans I, Brandt K, Donini LM, Maggio M, McMurdo ME, Mets T, Seal C, Wijers SL, Ceda GP, De Vito G, Donders G, Drey M, Greig C, Holmbäck U, Narici M, McPhee J, Poggiogalle E, Power D, Scafoglieri A, Schultz R, Sieber CC, Cederholm T. Effects of a vitamin D and leucine-enriched whey protein nutritional supplement on measures of sarcopenia in older adults, the PROVIDE study: a randomized, double-blind, placebo-controlled trial. J Am Med Dir Assoc 2015;16(9):740-7. doi: 10.1016/j.jamda.2015.05.021. Epub 2015 Jul 10. PMID: 26170041.
9. https://www.bv-geriatrie.de/images/INHALTE/Qualitaet/1406_Anforderungskatalog_atz.pdf
10. Podsiadlo D, Richardson S. The timed „Up & Go“: a test of basic functional mobility for frail elderly persons. J Am Geriatr Soc 1991;39(2):142-8. doi: 10.1111/j.1532-5415.1991.tb01616.x. PMID: 1991946.
11. Turner G, Clegg A; British Geriatrics Society; Age UK; Royal College of General Practioners. Best practice guidelines for the management of frailty: a British Geriatrics Society, Age UK and Royal College of General Practitioners report. Age Ageing 2014;43(6):744-7. doi: 10.1093/ageing/afu138. PMID: 25336440.
12. Shumway-Cook A, Brauer S, Woollacott M. Predicting the probability for falls in community-dwelling older adults using the Timed Up & Go Test. Phys Ther 2000;80(9):896-903. PMID: 10960937.
13. Bridenbaugh SA, Beauchet O, Annweiler C, Allali G, Herrmann F, Kressig RW. Association between dual task-related decrease in walking speed and real versus imagined Timed Up and Go test performance. Aging Clin Exp Res 2013;25(3):283-9. doi: 10.1007/s40520-013-0046-5. Epub 2013 May 17. PMID: 23740587.
14. Ehrensperger MM, Taylor KI, Berres M, Foldi NS, Dellenbach M, Bopp I, Gold G, von Gunten A, Inglin D, Müri R, Rüegger B, Kressig RW, Monsch AU. BrainCheck – a very brief tool to detect incipient cognitive decline: optimized case-finding combining patient- and informant-based data. Alzheimers Res Ther 2014;6(9):69. doi: 10.1186/s13195-014-0069-y. PMID: 25422675; PMCID: PMC4241397.
15. Yesavage JA, Brink TL, Rose TL, Lum O, Huang V, Adey M, Leirer VO. Development and validation of a geriatric depression screening scale: a preliminary report. J Psychiatr Res 1982-1983;17(1):37-49. doi: 10.1016/0022-3956(82)90033-4. PMID: 7183759.
16. Ernährungsempfehlungen für Seniorinnen und Senioren, BLV 2022; https://www.blv.admin.ch/blv/de/home/lebensmittel-und-ernaehrung/ernaehrung/empfehlungen-informationen/lebensphasen-und-ernaehrungsformen/ernaehrung-fuer-aeltere-menschen.html
17. Gagesch M, Wieczorek M, Abderhalden LA, Lang W, Freystaetter G, Armbrecht G, Kressig RW, Vellas B, Rizzoli R, Blauth M, Orav EJ, Egli A, Bischoff-Ferrari HA. Grip strength cut-points from the Swiss DO-HEALTH population. Eur Rev Aging Phys Act 2023;20(1):13. doi: 10.1186/s11556-023-00323-6. PMID: 37543639; PMCID: PMC10403936.
18. Kiss CM, Bertschi D, Beerli N, Berres M, Kressig RW, Fischer AM. Calf circumference as a surrogate indicator for detecting low muscle mass in hospitalized geriatric patients. Aging Clin Exp Res 2024;36(1):25. doi: 10.1007/s40520-024-02694-x. PMID: 38321234; PMCID: PMC10847205.
der informierte @rzt
- Vol. 14
- Ausgabe 5
- Mai 2024