- Impfung bei chronischen Lungenerkrankungen
In der Schweiz wird Patient/-innen mit chronischen Lungenerkrankungen die Impfung gegen Influenza, COVID-19, S. pneumoniae und Varizella-Zoster-Virus (VZV) empfohlen. Trotz wirksamer Pneumokokken-Impfstoffe sind die Impfraten niedrig. Die Influenza-Impfraten sind höher und hochdosierte Impfstoffe steigern die Wirksamkeit in Jahren mit geringer Stammübereinstimmung. Die COVID-19-Mortalität ist zurückgegangen, doch ohne variantenangepasste Impfstoffe haben Patient/-innen mit Lungenerkrankungen weiterhin ein erhöhtes Exazerbationsrisiko. VZV- und Pertussis-Impfungen konnten die Reaktivierungs- bzw. Infektionsraten senken, jedoch ist die Pertussis-Impfung durch ihren raschen Wirkverlust limitiert. Ein Blick in die Zukunft lässt vermuten, dass breitere Impfungen gegen S. pneumoniae eingeführt werden, während erste Impfstoffe gegen das Respiratorische Synzytial Virus (RSV) auf den Schweizer Markt kommen. Dieser Artikel fasst die Impfempfehlungen für Patient/-innen mit chronischen Lungenerkrankungen zusammen.
In Switzerland, vaccinations against influenza, COVID-19, S. pneumoniae, and varicella zoster virus (VZV) are recommended for patients with chronic lung diseases. High-valency S. pneumoniae vaccines have been developed, but vaccination rates remain low. Influenza vaccination rates are higher, with high-dose vaccines improving efficacy in years of low strain matching. COVID-19 mortality has decreased, but patients with chronic lung disease remain at increased risk for exacerbation, unless vaccinated with variant-adjusted vaccines. VZV and pertussis vaccinations have reduced reactivation and infection rates, respectively. However, pertussis vaccination is still limited by its fast waning. A glimpse into the future presumes the introduction of new higher-valence vaccinations against S. pneumoniae, and several types of Respiratory Syncytial Virus (RSV) vaccines are currently entering the Swiss market. This review aims to summarize recommended vaccinations for patients with chronic lung diseases.
Key words: Vaccine efficacy, chronic lung diseases, viral infections, exacerbation prevention
Einleitung
Chronische Lungenerkrankungen stellen eine erhebliche gesundheitliche und wirtschaftliche Belastung dar. Die Inzidenz chronischer Lungenkrankheiten wie Asthma und COPD nimmt zu, während COPD bereits die vierthäufigste Todesursache in der Schweiz ist (1–3). Exazerbationen dieser chronischen Erkrankungen bergen ein hohes Risiko, da sie zu Funktionseinschränkungen, schweren Pneumonien und Krankenhausaufenthalten bis hin zum Tod führen können (3). Ein Grossteil der akuten Exazerbationen wird durch Infektionen verursacht, insbesondere durch Viren, mit Virusnachweisraten von 22–64 % (4–6). Rhinoviren sind die am häufigsten nachgewiesenen viralen Auslöser (bis zu 60 %), gefolgt von Influenza (bis zu 36 %) und Respiratorischem Synzytial-Virus (RSV; bis zu 28 %) (6). Die Vorbeugung von Infektionen durch Impfungen ist daher eine tragende Säule zur Reduktion akuter infektionsbedingter Exazerbationen und der damit verbundenen Verschlechterung chronischer Lungenerkrankungen (7). Aktuelle internationale Richtlinien sowie der Schweizer Impfplan empfehlen für diese Patientengruppe bereits Impfungen gegen Influenza, Pneumokokken und SARS-CoV-2 (7–9). Da auch RSV zu Exazerbationen beitragen kann und ähnliche oder sogar höhere Sterblichkeitsraten als die Influenza aufweist, empfiehlt die Global Initiative for Chronic Obstructive Lung Disease (GOLD) und seit Kurzem auch das Schweizer Bundesamt für Gesundheit (BAG) eine Impfung gegen RSV bei Patient/-innen mit COPD (9–12). Dieser Artikel fasst Daten zur Impfeffizienz (vaccine efficacy, VE) verfügbarer Impfstoffe zusammen und gibt einen Ausblick auf künftige Impfmöglichkeiten für Risikopersonen.
Pneumokokken-Impfung
S. pneumoniae verursacht Infektionen des Lungenparenchyms und der unteren Atemwege und ist eine der Hauptursachen für die ambulant erworbene Pneumonie (13). Zwei Drittel der Pneumokokken-Erkrankungen treten bei 25 % der Bevölkerung mit hohem Risiko auf (13, 14). Dies ist besorgniserregend, da eine gleichzeitige Pneumonie bei Exazerbation einer chronischen Lungenerkrankung ein schlechteres Outcome für Patient/-innen birgt (15). Dennoch sind die Pneumokokken-Impfraten in der Schweiz immer noch niedrig: bei Personen mit chronischen Lungenerkrankungen wurde sie für 2020 auf etwa 14.8 % geschätzt, und erreichte bei den 65- bis 85-Jährigen nur 9.6 % (16).
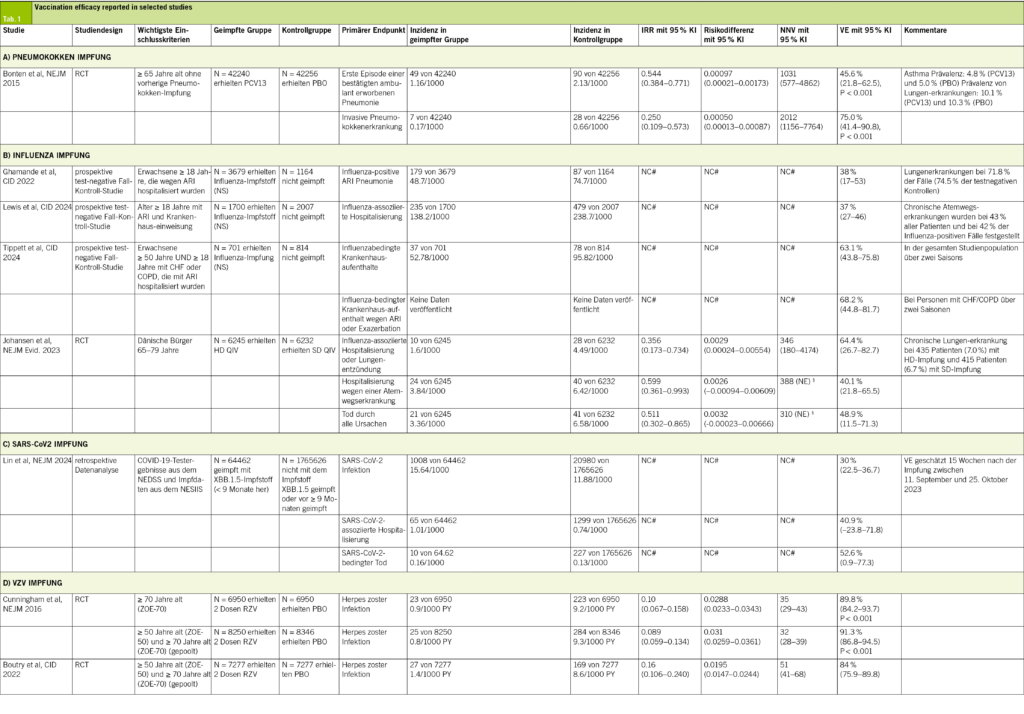
Seit 2023 wird die Impfung mit einem Pneumokokken-Konjugat-Impfstoff (PCV) für alle Personen ≥ 65 Jahre (zusätzlich zu Kindern und Erwachsenen mit Risikofaktoren) vom BAG und von internationalen Richtlinien empfohlen (VE siehe Tab. 1A) (8, 9, 17). Höhervalente Impfstoffe wie PCV15 (Vaxneuvance®) (18) und PCV20 (Prevenar 20®) (19) wurden kürzlich in der Schweiz eingeführt und für die Anwendung bei Personen ≥ 65 Jahre zugelassen (17). Die höhere Serotypenabdeckung ist wichtig, da das sogenannte Serotypen-Replacement durch nicht in den Impfstoffen enthaltene Serotypen in den letzten Jahren zu einer zunehmenden Häufigkeit von Pneumokokken-Infektionen geführt hat (20). In der Tat variierte im Jahr 2023 die Serotypen-Abdeckung der verfügbaren Impfstoffe stark: 31 % für PCV13, 40 % für PCV15 und 68 % für PCV20 (21). Die Kosten für die Impfung werden derzeit nur für Risikopersonen < 5 Jahre und für Erwachsene > 65 Jahre rückerstattet (17).
Influenza-Impfung
Das Influenzavirus infiziert jedes Jahr etwa 10–20 % der Weltbevölkerung, verursacht jährlich 3–5 Millionen Krankenhausaufenthalte und birgt eine hohe Mortalität vor allem bei Risikopersonen (22). Für Patient/-innen mit COPD zeigte eine Influenzaimpfung langfristige Vorteile in Bezug auf influenzabedingte Atemwegsinfektionen, Anzahl der Exazerbationen, Hospitalisierungsrate, Gesamtmortalität und Mortalität durch Atemwegserkrankungen (23). Zudem reduzierte sie die Zahl der Krankenhausaufenthalte aufgrund von Pneumonie und Influenza bei Personen ≥ 65 Jahre um 8.5 % und bei Personen im Alter von 50–64 Jahren um 12.4 % (24, 25). Aktuelle Studien aus den USA verzeichneten VEs von 37–38 % gegen influenzabedingte Krankenhausaufenthalte (Tab. 1B) (26, 27). Eine prospektive Studie berichtete sogar von einer VE von 63.1 %. Bei Personen mit Herzinsuffizienz oder COPD war die VE mit 68.2 % hinsichtlich Krankenhausaufenthalten aufgrund von Exazerbation oder akuter Atemwegsinfektion sogar noch höher (28). Die aktuellen Schweizer Empfehlungen betonen die Relevanz der Influenzaimpfung bei Risikopersonen, einschliesslich solcher mit chronischen Lungenkrankheiten (29). In der Schweiz sind die quadrivalenten inaktivierten Impfstoffe (quadrivalent inactivated vaccine, QIV) Fluarix Tetra® (30) und Vaxigrip Tetra® (31) für Personen ≥ 65 Jahre und für alle mit mindestens einem Risikofaktor verfügbar und werden erstattet (29). Aufgrund der höheren VE ist die hochdosierte Efluelda® Impfung (32) in der Schweiz für Personen ≥ 65 Jahre verfügbar und wird für alle Personen ≥ 75 Jahre oder ≥ 65 Jahre mit mindestens einem Risikofaktor erstattet (29). Die Influenza-Impfquote bei Personen mit chronischen Lungenkrankheiten in der Schweiz liegt bei 21.6 % in allen Altersgruppen und bei 49.85 % in der Altersgruppe ≥ 65 Jahre (33). Für die Influenzasaison 2024/2025 haben die USA beschlossen, auf einen trivalenten Impfstoff umzusteigen, da der in QIVs enthaltene B/Yamagata-Stamm nicht mehr zirkuliert (34).
SARS-CoV-2-Impfung
Trotz gesunkenem Medieninteresse an SARS-CoV-2 sind die Raten des zirkulierenden Virus im Jahr 2024 immer noch hoch (35). Schwere COVID-19-Fälle sind in der Omikron-Ära zurückgegangen, aber Studien zeigen, dass Personen mit Asthma und COPD noch immer ein deutlich erhöhtes Risiko für schwere Verläufe haben (HR: 1.31 bzw. HR: 1.36) (36). Die Verabreichung von ≥ 3 Impfdosen kann dieses Risiko jedoch reduzieren (OR: 0.35) (37).
Im Allgemeinen zeigten XBB.1.5-Impfstoffe gegen Omikron-Subvarianten eine begrenzte Dauer zur Verhinderung von Infektionen, mit einer VE von 52.2 % nach 4 Wochen und 32.6 % nach 10 Wochen (Tab. 1C). Die Wirksamkeit bezüglich der Reduktion von Krankenhausaufenthalten und Todesfällen blieb jedoch über einen längeren Zeitraum aufrechterhalten (38). Entsprechend empfiehlt das BAG eine SARS-CoV-2-Impfung für alle Risikopersonen, und derzeit sind die mRNA-Impfstoffe Comirnaty® (39) und Spikevax® (40) in der Schweiz verfügbar und zugelassen (8). Die Verwendung eines mRNA-Impfstoffs, der auf aktuelle SARS-CoV-2-Varianten abzielt, wird unabhängig von früheren Impfungen empfohlen (41).
VZV-Impfung
VZV verursacht Windpocken, die sich typischerweise als hoch ansteckender Ausschlag in der Kindheit manifestieren, und Herpes zoster, das durch Reaktivierung latenter VZV auftritt (42, 43). Weltweit sind jährlich fast 84 Millionen Menschen betroffen und leiden unter der hohen Krankheitslast des Virus (43). Das Risiko, an Herpes zoster zu erkranken, ist bei Patient/-innen mit Asthma um 24 % und bei COPD um 41 % erhöht (44). Eine Exazerbation der COPD scheint zudem mit dem Auftreten von Herpes zoster einherzugehen, und das Risiko für assoziierte Komplikationen ist bei COPD ebenfalls erhöht (44). Dank der Impfung mit Subunit-Impfstoffen hat sich die Krankheitslast stetig verringert (43, 45). Aus klinischen Studien geht hervor, dass zur Vorbeugung einer Reaktivierung bei ≥ 70-jährigen Patient/-innen 35 Individuen geimpft werden müssen (number needed to vaccinate, NNV), und bei ≥ 50-jährigen 32 Individuen (Tab. 1D) (46). Ein 7-Jahres-Follow-up der Kohorte von ≥ 50-Jährigen ergab eine NNV von 51 (47). Im Gegensatz dazu nahm der Schutz des abgeschwächten Lebendimpfstoffs in diesem Zeitraum ab (48). In der Schweiz wird die Impfung mit dem rekombinanten Subunit-Impfstoff Shingrix® (49) für Personen ≥ 65 Jahre, für Personen ≥ 50 Jahre mit schwerem Asthma, COPD oder Immundefizienz sowie für Personen ≥ 18 Jahre mit schwerer Immunsuppression empfohlen (8).
Pertussis-Impfung
Jedes Jahr erkranken etwa 50 Millionen Menschen an Keuchhusten, wobei jährlich 300 000 Menschen daran sterben (50). Die Inzidenz bei gesunden Menschen liegt bei 0.5 pro 100 000 und ist bei Patient/-innen mit COPD und Asthma deutlich erhöht (2.47 und 3.35 pro 100 000) (50). Es gibt immer noch Ausbrüche der Krankheit (51), was möglicherweise auf den schnell abnehmenden Schutz der azellulären Dreifachimpfstoffe (Tetanus, Diphtherie, Pertussis) Boostrix® (52) und Adacel® (53) zurückzuführen ist. Während die VE im ersten Jahr bei 75.3 % liegt, sinkt sie innerhalb von 4–5 Jahren auf 11.9 % (54).
Das BAG empfiehlt eine Grundimmunisierung gegen Pertussis bei Säuglingen und Auffrischungen im Kindes- und Jugendalter. Darüber hinaus wird eine Auffrischungsimpfung mit Boostrix® (52) oder Adacel® (53) für Erwachsene empfohlen, die mit Säuglingen und Schwangeren in Kontakt kommen. Es gibt jedoch keine spezielle Empfehlung für Patient/-innen mit chronischen Lungenerkrankungen (8). (Tab. 1)
Zukunftsaussichten in der Schweiz
Neue Pneumokokkenimpfungen
Derzeit wird in der Schweiz der Einsatz von PCV15 und PCV20 empfohlen (17). Die US-amerikanische Arzneimittelbehörde (Food and Drug Administration, FDA) hat kürzlich PCV21 für Menschen im Alter von ≥ 65 Jahren zugelassen, welches bis zu 85 % der Serotypen in dieser Altersgruppe abdeckt (55, 56). Diese Zulassung basiert auf kürzlich veröffentlichten Daten, die ein gutes Sicherheitsprofil von PCV21 bewiesen, während die Reaktogenität auf alle eingeschlossenen Serotypen im Vergleich zu niedrigen valenten PCV-Impfungen nicht unterlegen war (57). Darüber hinaus laufen Studien zu einem 24-valenten PCV, mit dem die Abdeckung der Serotypen noch weiter erhöht werden soll (58).
RSV-Impfungen
RSV ist ein RNA-Virus, das Atemwegsinfektionen bis hin zur Pneumonie verursachen kann. Schwere Fälle betreffen vor allem Säuglinge, Kleinkinder und ältere Menschen, und RSV ist im Vergleich zu Influenza oder SARS-CoV-2 mit schwereren Krankheitsverläufen verbunden (59–61). Darüber hinaus wurde ein 2- bis 4-fach erhöhtes Risiko für RSV-bedingte Krankenhausaufenthalte bei Erwachsenen mit COPD und ein 1.5- bis 3-fach erhöhtes Risiko bei Erwachsenen mit Asthma festgestellt (62).
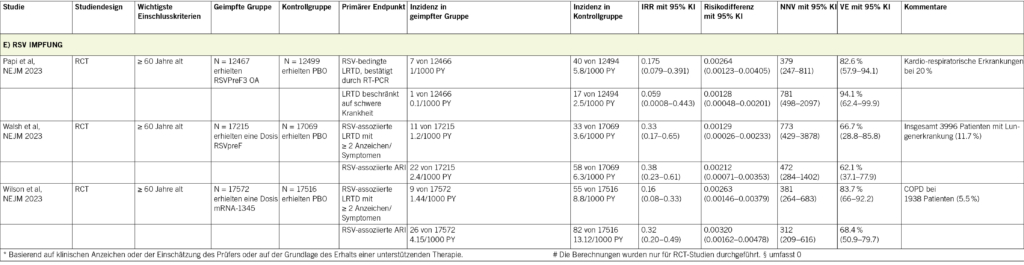
In den letzten Jahren wurden Impfungen gegen das RSV-Fusionsprotein F in klinischen Studien untersucht (63). Die NNVs für den AS01E-adjuvanten RSV-Impfstoff, den bivalenten und den mRNA-Impfstoff betrugen 379, 772 und 381, um eine RSV-bedingte Erkrankung der unteren Atemwege zu verhindern (Tab. 1E) (64–66). Die Wirksamkeit der Impfung liess sich über einen Zeitraum von mindestens zwei bis drei Saisonen aufrechterhalten, aber die Daten hinsichtlich der Verhinderung von Krankenhausaufenthalten sind noch begrenzt (67, 68). In den USA sind jeweils ein Impfstoff mit Adjuvans, ein bivalenter und ein mRNA-Impfstoff für Erwachsene ≥ 60 Jahre zugelassen, und kürzlich wurden die ersten Sicherheitsdaten vorgelegt: Die geschätzten Raten für das Guillain-Barré-Syndrom (GBS) waren für den bivalenten Impfstoff höher (4.4 pro 1 Million verabreichter Dosen) als für den Impfstoff mit Adjuvans (1.8 pro 1 Million verabreichter Dosen) (69). In der Schweiz sind die beiden Protein-basierten RSV-Impfstoffe Abrysvo® und Arexvy® (70, 71) zugelassen, und ein mRNA-basierter Impfstoff befindet sich derzeit im Zulassungsverfahren. Kürzlich hat das BAG Impfempfehlungen für ältere Menschen und Patient/-innen mit hohem Komplikationsrisiko, darunter solche mit chronischen Lungenerkrankungen, veröffentlicht (72).
Diskussion
Der schweizerische Impfplan enthält spezifische Empfehlungen für die Impfung von Risikopersonen, darunter Patient/-innen mit chronischen Lungenkrankheiten (8). Dennoch sind die Impfraten, insbesondere gegen S. pneumoniae, in der Schweiz nach wie vor niedrig und Empfehlungen zur Impfung mit höhervalenten Impfstoffen sollten Einzug finden (16, 20). In der Schweiz wurden kürzlich zwei RSV-Impfstoffe für Erwachsene ≥ 60 Jahre auf den Markt gebracht (72). Während die GOLD-Leitlinien bereits früher RSV- und Pertussis-Impfungen für Patient/-innen mit COPD empfohlen haben, wurden die Empfehlungen bezüglich RSV erst kürzlich auch in der Schweiz verankert (8, 9, 12). Im Zusammenhang mit der RSV-Impfung sind noch einige wichtige Fragen offen, wie z.B. die Dauer des Impfschutzes, die Notwendigkeit einer wiederholten Impfung, und vor allem die Wirksamkeit in Bevölkerungsgruppen mit Komorbiditäten (73). Darüber hinaus werden Sicherheit und Immunogenität der gleichzeitigen Verabreichung mit z.B. Influenzaimpfstoffen derzeit noch untersucht (74). Auch wenn die RSV-Impfung mit bestimmten Risiken wie GBS verbunden ist, werden diese durch die erfolgreiche Prävention von Exazerbationen und kardiovaskulären Ereignissen bei Risikopersonen aufgewogen (75).
Bei diesem Artikel handelt es sich nicht um eine systematische Übersichtsarbeit und Metaanalyse, da lediglich ausgewählte Studien zur Bewertung des NNV und VE verschiedener Impfstoffe (empfohlen für Patient/-innen mit chronischen Lungenerkrankungen) einbezogen wurden. Ausserdem wurden die meisten dieser Impfstudien nicht explizit bei Personen mit chronischen Lungenerkrankungen durchgeführt. Im Allgemeinen konzentrieren sich viele Impfempfehlungen für chronische Lungenkrankheiten auf die COPD (9). Zwar gibt es einige Studien über die Rolle infektionsbedingter Exazerbationen bei Asthma, doch es liegen nur wenige Daten über die Auswirkungen von Atemwegsinfektionen auf interstitielle Lungenerkrankungen vor (76).
Zusammenfassend ist eine höhere Impfrate bei Personen mit chronischen Lungenerkrankungen entscheidend, um Exazerbationen und damit Morbidität und Mortalität in dieser gefährdeten Bevölkerungsgruppe zu verhindern. Daher wird die Einführung neuer und wirksamerer Impfstoffe in der Schweiz mit ständigen Variantenanpassungen von zentraler Bedeutung sein. Zu den Strategien zur Verbesserung der Impfraten gehören die Ermittlung von Faktoren und Hindernissen, um fundierte Entscheidungen treffen zu können, sowie die Aufklärung der Patient/-innen und die Schulung von Gesundheitsdienstleistern und nationalen Behörden (77).
VZV-Impfung
VZV verursacht Windpocken, die sich typischerweise als hoch ansteckender Ausschlag in der Kindheit manifestieren, und Herpes zoster, das durch Reaktivierung latenter VZV auftritt (42, 43). Weltweit sind jährlich fast 84 Millionen Menschen betroffen und leiden unter der hohen Krankheitslast des Virus (43). Das Risiko, an Herpes zoster zu erkranken, ist bei Patient/-innen mit Asthma um 24 % und bei COPD um 41 % erhöht (44). Eine Exazerbation der COPD scheint zudem mit dem Auftreten von Herpes zoster einherzugehen, und das Risiko für assoziierte Komplikationen ist bei COPD ebenfalls erhöht (44). Dank der Impfung mit Subunit-Impfstoffen hat sich die Krankheitslast stetig verringert (43, 45). Aus klinischen Studien geht hervor, dass zur Vorbeugung einer Reaktivierung bei ≥ 70-jährigen Patient/-innen 35 Individuen geimpft werden müssen (number needed to vaccinate, NNV), und bei ≥ 50-jährigen 32 Individuen (Tab. 1D) (46). Ein 7-Jahres-Follow-up der Kohorte von ≥ 50-Jährigen ergab eine NNV von 51 (47). Im Gegensatz dazu nahm der Schutz des abgeschwächten Lebendimpfstoffs in diesem Zeitraum ab (48). In der Schweiz wird die Impfung mit dem rekombinanten Subunit-Impfstoff Shingrix® (49) für Personen ≥ 65 Jahre, für Personen ≥ 50 Jahre mit schwerem Asthma, COPD oder Immundefizienz sowie für Personen ≥ 18 Jahre mit schwerer Immunsuppression empfohlen (8).
Dr. med. Maria Bösing 1,2
Prof. Dr. med. Werner Albrich 3
Prof. Dr. med. Pierre-Olivier Bridevaux 4,5
Dr. med. Florian Charbonnier 6
Prof. Dr. med. Christian Clarenbach 7
Prof. Dr. med. Jean-Marc Fellrath 8
Dr. med. Pietro Gianella 9
Dr. med. Lukas Kern 10
PD Dr. med. Tsogyal Latshang 11
Dr. med. Nikolay Pavlov 12
Prof. Dr. med. Michael Osthoff 13
Prof. Dr. med. Claudia Steurer-Stey 14
Prof. Dr. med. Christophe von Garnier 15
Prof. Dr. med. Jörg D. Leuppi 1,2
1 Universitäres Zentrum Innere Medizin, Kantonsspital Baselland, Liestal
2 Medizinische Fakultät, Universität Basel, Basel
3 Abteilung für Infektiologie, Infektionsprävention und Reisemedizin, HOCH Health Ostschweiz, Kantonsspital St. Gallen, St. Gallen
4 Service de pneumologie, Centre Hospitalier du Valais Romand, Hôpital du Valais, Sitten
5 Faculté de médecine, Université de Genève, Genf
6 Service de pneumologie, Hôpitaux universitaires de Genève, Genf
7 Abteilung für Pneumologie, Universitätsspital Zürich, Zürich
8 Service de pneumologie, Réseau hospitalier neuchâtelois, Neuenburg
9 Ente Ospedaliero Cantonale, Lugano
10 Abteilung für Pneumologie, Kantonsspital St. Gallen, St. Gallen
11 Abteilung für Pneumologie, Kantonsspital Graubünden, Chur
12 Universitätsklinik für Pneumologie, Allergologie und klinische Immunologie, Inselspital, Universitätsspital Bern, Universität Bern
13 Abteilung für Innere Medizin, Kantonsspital Winterthur, Winterthur
14 Universität Zürich, Zürich
15 Abteilung für Pneumologie, Department Medizin, Centre Hospitalier Universitaire Vaudois (CHUV) und Universität Lausanne (UNIL), Lausanne
Abkürzungen
ARI akute Atemwegserkrankung
BAG Bundesamt für Gesundheit
CHF kongestive Herzinsuffizienz
COPD chronisch obstruktive Lungenerkrankung
COVID-19 Coronavirus Erkrankung 2019
FDA Food and Drug Administration
GOLD Global Initiative for Chronic Obstructive Lung Disease
HD hohe Dosis
HR Hazard Ratio (Risikoverhältnis)
IRR Inzidenzratenverhältnis
KI Konfidenzintervall
LRTD Erkrankung der unteren Atemwege
mRNA-1345 mRNA-basierter RSV-Impfstoff, der das stabilisierte RSV-Präfusions-F-Glykoprotein kodiert
NC nicht berechenbar
NE nicht schätzbar
NEDSS Nebraska Electronic Disease Surveillance System
NESIIS Nebraska State Immunization Information System
NNV number needed to vaccinate (Zahl der erforderlichen Impfungen, auf Einheit gerundet)
NS keine Angabe
OR Odds Ratio (Chancenverhältnis)
PBO Placebo
PCV Pneumokokken-Konjugatimpfstoff
PY Personenjahre
QIV quadrivalenter Grippeimpfstoff
RCT randomisierte kontrollierte Studie
RSV Respiratorisches Synzytialvirus
RSVpreF bivalenter RSV-Präfusionsimpfstoff auf F-Protein-Basis
RSVPreF3 OA AS01E-adjuvierter RSV-Präfusionsimpfstoff auf F-Protein-Basis
RZV Glykoprotein E (gE)-basierter adjuvanter rekombinanter Zoster-Impfstoff
SARS-CoV-2 Severe Acute Respiratory Syndrome Coronavirus 2
SD Standarddosis
VE vaccine efficacy (Impfeffizienz)
VZV Varizella-Zoster-Virus
Finanzierung
Das Manuskript wurde finanziell von GSK AG Schweiz und Moderna AG Schweiz unterstützt. Die Sponsoren hatten keinen Einfluss auf den Inhalt der wissenschaftlichen Übersichtsarbeit.
Copyright
Aerzteverlag medinfo AG
– Universitäres Zentrum Innere Medizin, Kantonsspital Baselland, Liestal
– Medizinische Fakultät, Universität Basel, Basel
Jörg D. Leuppi hat nicht zweckgebundene Förderungen von AstraZeneca Schweiz, GSK Schweiz, OM Pharma Schweiz und Sanofi Schweiz erhalten. Werner Albrich erhielt Förderungen von der Swiss National Science Foundation (33IC30_201300), dem Kantonsspital St. Gallen, OM Pharma, FUNGINOS, Gilead, und erhielt Zahlungen an seine Institution für Vorträge und Präsentationen von Pfizer, GSK, MSD, Gilead. Zudem erhielt er Zahlungen für Reisen zu Tagungen, die an seine Institution gezahlt wurden, von Pfizer, GSK und Gilead, und war Mitglied in den Beiräten von MSD, Sanofi, Pfizer, GSK, OM Pharma, Moderna, Aurovir Pharma und Janssen.
1. Bundesamt für Gesundheit (BAG). Chronische Atemwegserkrankungen. https://www.bag.admin.ch/bag/de/home/krankheiten/krankheiten-im-ueberblick/chronische-atemwegserkrankungen.html#-876619191; letzter Zugriff Januar 2025.
2. McLean, S., et al., Projecting the COPD population and costs in England and Scotland: 2011 to 2030. Sci Rep, 2016. 6: p. 31893.
3. Britto, C.J., et al., Respiratory Viral Infections in Chronic Lung Diseases. Clin Chest Med, 2017. 38(1): p. 87-96.
4. Kherad, O., et al., Upper-respiratory viral infection, biomarkers, and COPD exacerbations. Chest, 2010. 138(4): p. 896-904.
5. Bridevaux, P.O., et al., Incidence and outcomes of respiratory viral infections in lung transplant recipients: a prospective study. Thorax, 2014. 69(1): p. 32-8.
6. Ritchie, A.I. and J.A. Wedzicha, Definition, Causes, Pathogenesis, and Consequences of Chronic Obstructive Pulmonary Disease Exacerbations. Clin Chest Med, 2020. 41(3): p. 421-438.
7. Simon, S., et al., The role of vaccination in COPD: influenza, SARS-CoV-2, pneumococcus, pertussis, RSV and varicella zoster virus. Eur Respir Rev, 2023. 32(169).
8. Bundesamt für Gesundheit (BAG). Impfplan 2024. https://www.bag.admin.ch/bag/de/home/gesund-leben/gesundheitsfoerderung-und-praevention/impfungen-prophylaxe/schweizerischer-impfplan.html; letzter Zugriff Januar 2025.
9. Global Initiative for Chronic Obstructive Lung Disease; GOLD Report 2024. https://goldcopd.org/2024-gold-report/; letzter Zugriff Januar 2025.
10. Hedberg, P., et al., Outcomes of SARS-CoV-2 Omicron Variant Infections Compared With Seasonal Influenza and Respiratory Syncytial Virus Infections in Adults Attending the Emergency Department: A Multicenter Cohort Study. Clin Infect Dis, 2024. 78(4): p. 900-907.
11. National Library of Medicine (NIH). https://clinicaltrials.gov/study/NCT01255410; letzter Zugriff Januar 2025.
12. Bundesamt für Gesundheit (BAG). Impfempfehlungen gegen Erkrankungen mit dem Respiratorischen Synzytial-Virus (RSV). BAG Bulletin, 47/2024. Available at https://www.bag.admin.ch/dam/bag/de/dokumente/mt/i-und-b/richtlinien-empfehlungen/empfehlungen-spezifische-erreger-krankheiten/rsv/impfempfehlungen-rsv-bulletin-47-24.pdf.download.pdf/impfempfehlungen-rsv-bulletin-47-24-de.pdf
13. Parks, T., L. Barrett, and N. Jones, Invasive streptococcal disease: a review for clinicians. Br Med Bull, 2015. 115(1): p. 77-89.
14. Pelton, S.I., et al., Rethinking risk for pneumococcal disease in adults: the role of risk stacking. Open Forum Infect Dis, 2015. 2(1): p. ofv020.
15. Søgaard, M., et al., Incidence and outcomes of patients hospitalized with COPD exacerbation with and without pneumonia. Int J Chron Obstruct Pulmon Dis, 2016. 11: p. 455-65.
16. Zens, K.D., et al., Pneumococcal Vaccination Coverage and Uptake Among Adults in Switzerland: A Nationwide Cross-Sectional Study of Vaccination Records. Front Public Health, 2021. 9: p. 759602.
17. Bundesamt für Gesundheit (BAG). Pneumokokken-Impfung neu für alle Personen ab dem Alter von 65 Jahren als ergänzende Impfung empfohlen. BAG Bulletin, 2024.
18. Aktuelle Fachinformation von Vaxneuvance® (PCV15) abrufbar unter www.swissmedicinfo.ch.
19. Aktuelle Fachinformation von Prevenar 20® (PCV20) abrufbar unter www.swissmedicinfo.ch.
20. Ouldali, N., et al., Invasive pneumococcal disease incidence in children and adults in France during the pneumococcal conjugate vaccine era: an interrupted time-series analysis of data from a 17-year national prospective surveillance study. Lancet Infect Dis, 2021. 21(1): p. 137-147.
21. University of Bern. Annual Report of the National Center for invasive Pneumococci (NZPn), 2023. Abrufbar unter: https://www.ifik.unibe.ch/unibe/portal/fak_medizin/ber_vkhum/inst_infekt/content/e39965/e39976/e1098920/e1565106/NZPn_Jahresbericht2023_ger.pdf; letzter Zugriff Januar 2025.
22. Sellers, S.A., et al., The hidden burden of influenza: A review of the extra-pulmonary complications of influenza infection. Influenza Other Respir Viruses, 2017. 11(5): p. 372-393.
23. Bekkat-Berkani, R., et al., Seasonal influenza vaccination in patients with COPD: a systematic literature review. BMC Pulm Med, 2017. 17(1): p. 79.
24. Baxter, R., G.T. Ray, and B.H. Fireman, Effect of influenza vaccination on hospitalizations in persons aged 50 years and older. Vaccine, 2010. 28(45): p. 7267-72.
25. Fireman, B., et al., Influenza vaccination and mortality: differentiating vaccine effects from bias. Am J Epidemiol, 2009. 170(5): p. 650-6.
26. Ghamande, S., et al., Vaccine Effectiveness Against Acute Respiratory Illness Hospitalizations for Influenza-Associated Pneumonia During the 2015-2016 to 2017-2018 Seasons: US Hospitalized Adult Influenza Vaccine Effectiveness Network (HAIVEN). Clin Infect Dis, 2022. 74(8): p. 1329-1337.
27. Lewis, N.M., et al., Vaccine Effectiveness Against Influenza A-Associated Hospitalization, Organ Failure, and Death: United States, 2022-2023. Clin Infect Dis, 2024. 78(4): p. 1056-1064.
28. Tippett, A., et al., Influenza Vaccine Effectiveness Pre-pandemic Among Adults Hospitalized With Congestive Heart Failure or Chronic Obstructive Pulmonary Disease and Older Adults. Clin Infect Dis, 2024. 78(4): p. 1065-1072.
29. Bundesamt für Gesundheit (BAG). Saisonale Grippe (Influenza). https://www.bag.admin.ch/bag/de/home/krankheiten/krankheiten-im-ueberblick/grippe.html; letzter Zugriff Januar 2025.
30. Aktuelle Fachinformation von Fluarix Tetra® abrufbar unter www.swissmedicinfo.ch.
31. Aktuelle Fachinformation von VaxigripTetra® abrufbar unter www.swissmedicinfo.ch.
32. Aktuelle Fachinformation von Efluelda® abrufbar unter www.swissmedicinfo.ch.
33. Zürcher, K., et al., Losing ground at the wrong time: trends in self-reported influenza vaccination uptake in Switzerland, Swiss Health Survey 2007-2017. BMJ Open, 2021. 11(2): p. e041354.
34. Centers for Disease Control and Prevention (CDC). Influenza (Flu). https://www.cdc.gov/flu/spotlights/2023-2024/trivalent-vaccines-2024-2025.htm; letzter Zugriff Januar 2025.
35. Eawag aquatic research. SARS-CoV-2 in Wastewater. https://sensors-eawag.ch/sars/overview.html; letzter Zugriff Januar 2025.
36. Wee, L.E., et al., A Nationwide Cohort Study of Delta and Omicron SARS-CoV-2 Outcomes in Vaccinated Individuals With Chronic Lung Disease. Chest, 2024.
37. Solera, J.T., et al., Longitudinal outcomes of COVID-19 in solid organ transplant recipients from 2020 to 2023. Am J Transplant, 2024. 24(7): p. 1303-1316.
38. Lin, D.Y., et al., Durability of XBB.1.5 Vaccines against Omicron Subvariants. N Engl J Med, 2024. 390(22): p. 2124-2127.
39. Aktuelle Fachinformation von Comirnaty® abrufbar unter www.swissmedicinfo.ch.
40. Aktuelle Fachinformation von Spikevax® abrufbar unter www.swissmedicinfo.ch.
41. Bundesamt für Gesundheit (BAG). Covid-19. https://www.bag.admin.ch/bag/de/home/krankheiten/krankheiten-im-ueberblick/coronavirus/covid-19.html; letzter Zugriff Januar 2025.
42. Pan, C.X., M.S. Lee, and V.E. Nambudiri, Global herpes zoster incidence, burden of disease, and vaccine availability: a narrative review. Ther Adv Vaccines Immunother, 2022. 10: p. 25151355221084535.
43. Huang, J., et al., The global disease burden of varicella-zoster virus infection from 1990 to 2019. J Med Virol, 2022. 94(6): p. 2736-2746.
44. Safonova, E., et al., Risk factors for herpes zoster: should people with asthma or COPD be vaccinated? Respir Res, 2023. 24(1): p. 35.
45. Kawai, K., et al., Increasing Incidence of Herpes Zoster Over a 60-year Period From a Population-based Study. Clin Infect Dis, 2016. 63(2): p. 221-6.
46. Cunningham, A.L., et al., Efficacy of the Herpes Zoster Subunit Vaccine in Adults 70 Years of Age or Older. N Engl J Med, 2016. 375(11): p. 1019-32.
47. Boutry, C., et al., The Adjuvanted Recombinant Zoster Vaccine Confers Long-Term Protection Against Herpes Zoster: Interim Results of an Extension Study of the Pivotal Phase 3 Clinical Trials ZOE-50 and ZOE-70. Clin Infect Dis, 2022. 74(8): p. 1459-1467.
48. Tseng, H.F., et al., Declining Effectiveness of Herpes Zoster Vaccine in Adults Aged ≥ 60 Years. J Infect Dis, 2016. 213(12): p. 1872-5.
49. Aktuelle Fachinformation von Shingrix® abrufbar unter www.swissmedicinfo.ch.
50. Chen, J., et al., Incidence and Healthcare Burden of Pertussis among Older Adults with and without Pre-Existing Chronic Obstructive Pulmonary Disease or Asthma in South Korea. Copd, 2023. 20(1): p. 126-134.
51. Domenech de Cellès, M. and P. Rohani, Pertussis vaccines, epidemiology and evolution. Nat Rev Microbiol, 2024.
52. Aktuelle Fachinformation von Boostrix® abrufbar unter www.swissmedicinfo.ch.
53. Aktuelle Fachinformation von Adacel® abrufbar unter www.swissmedicinfo.ch.
54. Koepke, R., et al., Estimating the effectiveness of tetanus-diphtheria-acellular pertussis vaccine (Tdap) for preventing pertussis: evidence of rapidly waning immunity and difference in effectiveness by Tdap brand. J Infect Dis, 2014. 210(6): p. 942-53.
55. Gierke, R., Current Epidemiology of Pneumococcal Disease among Adults, United States. Presented at the Advisory Committee on Immunization Practices (ACIP) Meeting on February 29, 2024.
56. Centers for Disease Control and Prevention (CDC). Pneumococcal Disease. https://www.cdc.gov/pneumococcal/hcp/vaccine-recommendations/index.html; letzter Zugriff Januar 2025.
57. Platt, H., et al., Safety, tolerability, and immunogenicity of a 21-valent pneumococcal conjugate vaccine, V116, in healthy adults: phase 1/2, randomised, double-blind, active comparator-controlled, multicentre, US-based trial. Lancet Infect Dis, 2023. 23(2): p. 233-246.
58. Wassil, J., et al., Evaluating the safety, tolerability, and immunogenicity of a 24-valent pneumococcal conjugate vaccine (VAX-24) in healthy adults aged 18 to 64 years: a phase 1/2, double-masked, dose-finding, active-controlled, randomised clinical trial. Lancet Infect Dis, 2024. 24(3): p. 308-318.
59. Piralla, A., Z. Chen, and H. Zaraket, An update on respiratory syncytial virus. BMC Infect Dis, 2023. 23(1): p. 734.
60. Du, Y., et al., Global burden and trends of respiratory syncytial virus infection across different age groups from 1990 to 2019: A systematic analysis of the Global Burden of Disease 2019 Study. Int J Infect Dis, 2023. 135: p. 70-76.
61. Surie, D., et al., Disease Severity of Respiratory Syncytial Virus Compared with COVID-19 and Influenza Among Hospitalized Adults Aged ≥ 60 Years–IVY Network, 20 U.S. States, February 2022-May 2023. MMWR Morb Mortal Wkly Rep, 2023. 72(40): p. 1083-1088.
62. Osei-Yeboah, R., et al., Respiratory Syncytial Virus-Associated Hospitalization in Adults With Comorbidities in 2 European Countries: A Modeling Study. J Infect Dis, 2024. 229(Supplement_1): p. S70-s77.
63. Ramilo, O., R. Rodriguez-Fernandez, and A. Mejias, Respiratory Syncytial Virus Infection: Old Challenges and New Approaches. J Infect Dis, 2023. 228(1): p. 4-7.
64. Papi, A., et al., Respiratory Syncytial Virus Prefusion F Protein Vaccine in Older Adults. N Engl J Med, 2023. 388(7): p. 595-608.
65. Walsh, E.E., et al., Efficacy and Safety of a Bivalent RSV Prefusion F Vaccine in Older Adults. N Engl J Med, 2023. 388(16): p. 1465-1477.
66. Wilson, E., et al., Efficacy and Safety of an mRNA-Based RSV PreF Vaccine in Older Adults. N Engl J Med, 2023. 389(24): p. 2233-2244.
67. Falsey, A.R., et al., Long-term efficacy and immunogenicity of Ad26.RSV.preF-RSV preF protein vaccine (CYPRESS): a randomised, double-blind, placebo-controlled, phase 2b study. Lancet Infect Dis, 2024.
68. Ison, M.G., et al., Efficacy and Safety of Respiratory Syncytial Virus (RSV) Prefusion F Protein Vaccine (RSVPreF3 OA) in Older Adults Over 2 RSV Seasons. Clin Infect Dis, 2024. 78(6): p. 1732-1744.
69. Hause, A.M., et al., Early Safety Findings Among Persons Aged ≥ 60 Years Who Received a Respiratory Syncytial Virus Vaccine–United States, May 3, 2023-April 14, 2024. MMWR Morb Mortal Wkly Rep, 2024. 73(21): p. 489-494.
70. Aktuelle Fachinformation von Abrysvo® (bivalent) abrufbar unter www.swissmedicinfo.ch.
71. Aktuelle Fachinformation von Arexvy® (RSVPreF3-Antigen) abrufbar unter www.swissmedicinfo.ch.
72. Bundesamt für Gesundheit (BAG). Respiratorisches-Synzytial-Virus (RSV). https://www.bag.admin.ch/bag/de/home/krankheiten/krankheiten-im-ueberblick/rsv.html; letzter Zugriff Januar 2025.
73. Moreira, A.C., et al., Efficacy of anti-RSV vaccination in preventing respiratory syncytial virus disease and severe illness in older adults: a systematic review of randomized controlled trials. Eur Geriatr Med, 2024.
74. Centers for Disease Control and Prevention (CDC). New Respiratory Syncytial Virus (RSV) Vaccines for Adults: General Information and Clinical Guidance. Current Issues in Immunization Webinar, August 30th, 2023.
75. Rademacher, J., et al., Association of respiratory infections and the impact of vaccinations on cardiovascular diseases. Eur J Prev Cardiol, 2024. 31(7): p. 877-888.
76. Shah Gupta, R., et al., Incidence and prevalence of interstitial lung diseases worldwide: a systematic literature review. BMJ Open Respir Res, 2023. 10(1).
77. World Health Organisation (WHO). Increasing and sustaining acceptance of and demand for vaccination. https://www.who.int/europe/activities/increasing-and-sustaining-acceptance-of-and-demand-for-vaccination; letzter Zugriff Januar 2025.
der informierte @rzt
- Vol. 15
- Ausgabe 3
- März 2025