- KHM Kongress 2023
Alt und herzinsuffizient – wie findet man die optimale Behandlung?
Die Lebenserwartung in der Schweiz ist hoch. Im Jahre 2018 betrug sie bei Geburt für Männer 81,7 Jahre, für Frauen 85,4 Jahre.
Die Anzahl von Patienten mit Herzinsuffizienz steigt ab 65 Jahren bei beiden Geschlechtern stark an. Sie ist bei Frauen mit einem Mittelwert von fast 3500 über die letzten 5 Jahre höher als bei Männern, mit fast 2500 Fällen pro Jahr, berichteten Frau Dr. med. Renate Albrecht, Zürich und Dr. med. Stefan Christen, Zürich.
Die moderne Herzinfarkttherapie ist eine Erfolgsgeschichte. Das kardiovaskuläre und das pulmonale System verändern sich indessen mit dem Alter. Herzinsuffizienz und Multimorbidität sind häufig und treten in Clustern auf. Bei Patienten, die mit Herzinsuffizienz hospitalisiert werden, haben solche aus dem gesamten EF-Spektrum ein ähnlich schlechtes 5-Jahres-Überleben mit einem erhöhten Risiko für kardiovaskuläre Erkrankungen und Herzinsuffizienz-Hospitalisierung. Diese Ergebnisse unterstreichen die Notwendigkeit einer Verbesserung der Behandlung.
Die klassischen Symptome und klinischen Zeichen im Alter sind Dyspnoe, schnelle Ermüdbarkeit und Ödeme. Unspezifische Symptome sind Schwäche, Müdigkeit, Kachexie, Verwirrtheit und Gebrechlichkeit.
Gemäss den ESC-Guidelines von 2021 sollen vier prognostisch und symptomatisch wirksame Medikamente (ACE-Hemmer, Beta-Blocker, MRA, Dapagliflozin,/Empagliflozin, Loop Diuretika (Klasse Ia)) möglichst früh kombiniert in tiefen Dosierungen eingesetzt werden. Aufdosierung im Verlauf je nach Klinik (Cave: Alter, Gebrechlichkeit), Schleifendiuretika nur zur Volumenkontrolle. Die Polypharmazie stellt ein wichtiges Problem dar. Beim Absetzen berichteten in einer Studie 88% über besseres Allgemeinbefinden und 2/3 über eine Verbesserung der kognitiven Leistungsfähigkeit (Garfinkel D et al. Isr Med Assoc. 2007:9:430). Das Vorgehen geht nach dem Prinzip «Less is more» als oberstes Credo beim Teaching auf der täglichen Visite: 1. Vollständige Medikamentenliste, 2. Kein Medikament ohne Diagnose, 3. Was ist symptomatisch, was ist prognostisch? 4. Welche Medikamente stellen wir in Frage? 5. Dialog zwischen Patient, Angehörige, Hausarzt. 6. Absetzen. Die Referenten stellen ihre persönliche Favoritenliste vor: PPI, Statine, Allopurinol, Betablocker, Antihypertensiva, Nitrate, Aspirin, insbesondere Kombinationen mit OAK, Amiodarone, Antidementiva, Vitaminpräparate und andere Nahrungsergänzungsmittel, Insulin, NSAR, Benzodiazepin, Stark anticholinergische Substanzen (Anti-Parkinson, Spasmo-Urogenin), Sulfonylharnstoffe.
Niere und Herzinsuffizienz – das Duo infernale
Ein weiteres Thema war der Zusammenhang zwischen Niere und Herzinsuffizienz. Eine Verschlechterung der Nierenfunktion ist häufig, wofür es zahlreiche Gründe gibt: Venöser Nierenstau, arterielle Minderperfusion, Volumenmangel/zu viel Diuretika, zu starke Vasodilatation, Medikamente (+30% Kreatinin unter ACE-Hemmer normal), Infekte, interstitielle Nephritis. Wenn die Verschlechterung nur vorübergehend ist, besteht kein relevanter Einfluss auf die Prognose.
Diagnose des Volumenstatus: Anamnese/Klinik (Zunahme der Anstrengungsdyspnoe, Orthopnoe, Gewichtsverlauf, Blutdruck und Puls in Selbstmessung durch Patienten, klinische Zeichen der Hypovolämie: Oedeme peripher, Halsvenenstauung, Rasselgeräusche und/oder Dämpfung pulmonal (Pleuraergüsse). Technische Untersuchungen: EKG, Labor, insbesondere Kreatinin, Elektrolyte und proBNP, insbesondere Verlauf), Thoraxbild (nur stehend von Nutzen), Bedside-Sonographie der Pleuraergüsse und der Cava inferior.
Behandlung der Hypervolämie (Vorschlag der Guidelines geht nur stationär). Ambulant: Verdoppelung orale Dosis Torasemid, Gewicht, BD/P durch Patient monitorisieren lassen, Kontrolle nach 2-3 Tagen inkl. Kreatinin, Elektrolyte, falls kein Effekt einmal Verdoppelung der oralen Dosis Torasemid oder falls Torasemid 100mg bereits erreicht, zusätzlich Metolazon 2,5mg 20-30 min vor Torasemid p.o., Verlaufskontrolle in 2-3 Tagen, dabei enge Zusammenarbeit mit Kardiologen in der Praxis oder am Spital suchen.
Hypotonie – wie damit umgehen? To do bei BD <90mmHg und/oder symptomatischer Hypotonie klinisch oder Kreatinin-Anstieg): 1. Überprüfen von allen Medikamenten, 2. Überprüfen des Volumenstatus (klinisch, BNP, Kreatinin, allenfalls Sonographie),
3. Reduktion und/oder bessere Verteilung der Herzinsuffizienzmedikamente, 4. Engmaschisches Monitoring (klinisch, Labor).
Patientenprofile und massgeschneiderte Herzinsuffizienztherapie: «Tailored to patient concept». Der ideale Patient hat eine Herzfrequenz von 60-70/min, eine normale Nierenfunktion und keine Hyperkaliämie, Blutdruck >90/60mmHg, kein Vorhofflimmern und all dies unter der Maximaldosis der Fantastic 4 (SGLT2-Hemmer, Beta-Blocker, ACB/ARB/ARNI, MRA, Diuretika).
End Stage Herzinsuffizienz – Palliation
Bei der Herzinsuffizienz ist die langsame Dynamik, und dass das Endstadium schwierig zu finden ist, besonders. Symptomatische Therapien, Medikamente: Diuretika, Opiate, Benzodiazepine, O2, anti-ischämisches Medikament, aber auch Beta-Blocker, SGLT2-Hemmer, ACE-Hemmer. Spironolacton, ARNI, und viele mehr.
Symptomatische Therapie invasiv: TAVI und Mitra-Clip, Pacemaker, CRT-P (Resynchronisation), Revaskularisation.
Ein spezieller Fokus ist auf folgendes zu legen: Patientenverfügung früh machen lassen, immer wieder IPS ja/nein, Rea-Status, Diskussion über invasive Möglichkeiten (CRT-P, Mitra-Clip, TAVI, Revaskularisation, Symptomkontrolle Fokus Dyspnoe, Angst, Leistungsfähigkeit, Vermeidung von Hospitalisationen, Abschalten ICD/PM? Palliativ-Spitex, Behandlungs-/Notfallplan.)
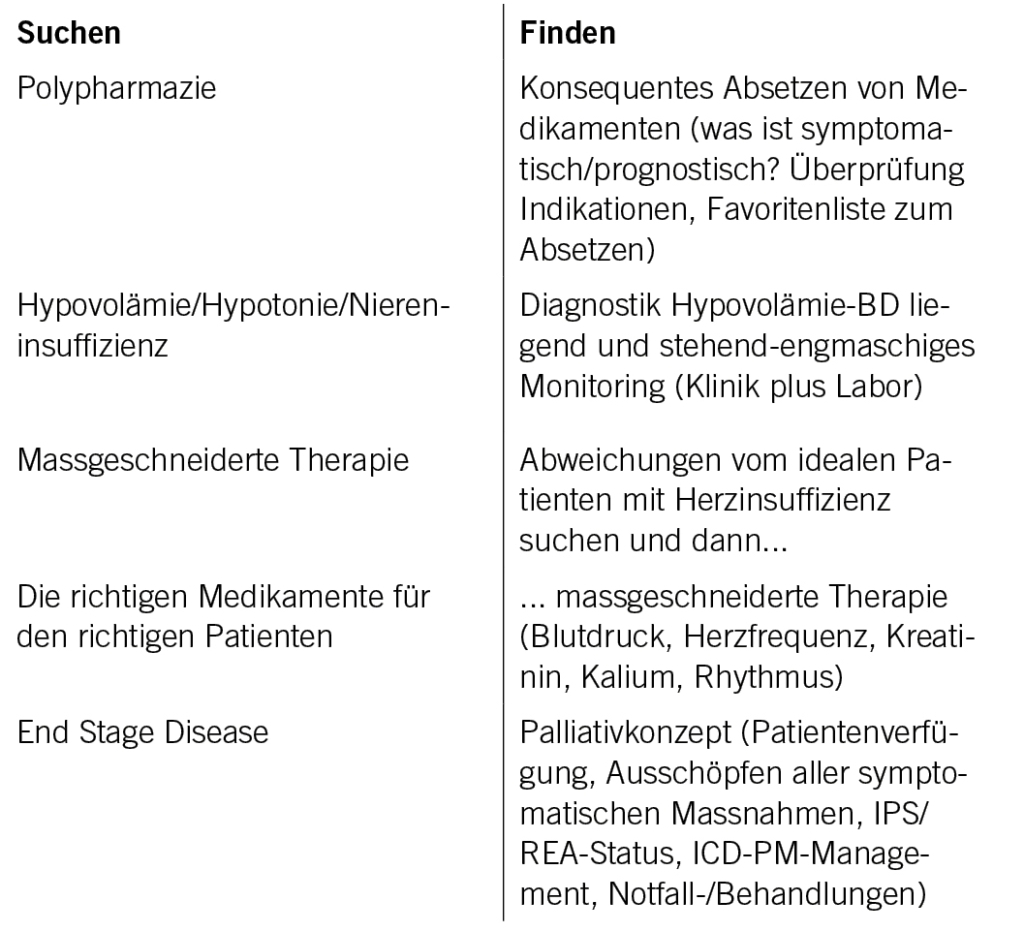
Die Referenten schlossen mit den folgenden Gegensätzen (in Analogie zum Hauptthema der Tagung)
 Diagnose und Behandlung von Eisenmangel bei Patienten mit Herzinsuffizienz: Was der behandelnde Arzt wissen sollte
Diagnose und Behandlung von Eisenmangel bei Patienten mit Herzinsuffizienz: Was der behandelnde Arzt wissen sollte
Am KHM Kongress 2023 sprach Prof. Dr. med. Roger Hullin, CHUV Lausanne, zum Thema Eisenmangel, einer häufigen und relevanten Komorbidität bei Patienten mit Herzinsuffizienz. Die Definitionen des Eisenmangels in der Herzinsuffizienz sind die Folgenden:
Anämie
Mann: <130gHämoglobin/l
Frau: <120g Hämogobin/l
Eisenmangel
Absoluter Eisenmangel Ferritin < µ100g/l
Funktioneller Eisenmagel
Ferritin 100-299µg/l + Transferrinsättigung <20%
Die Prävalenz des Eisenmangels bei Herzinsuffizienz betrage in der Schweiz und Deutschland 54%, so der Referent. Eisenmangel (Ferritin <100): kommt bei 33% der Patienten mit Herzinsuffizienz vor, Eisenmangel (Ferritin 100-300 + Transferrinsättigung <20%) bei 21% und kein Eisenmangel bei 45%.
Der natürliche Verlauf von Eisenmangel und Anämie bei ambulanten chronischen Herzinsuffizienz-Patienten zeigte zu Beginn der Studie bei 10% eine Anämie ohne ID, bei 23% einen Eisenmangel ohne Anämie, 20% hatten beides und 47% hatten keines von beidem. Die Prozentsätze änderten sich im Laufe eines Jahres kaum, aber bei 30% der Patienten trat ein neuer Eisenmange auf, bei 16% eine neue Anämie, während sich der Eisenmangel bei 44% und die Anämie bei 23% auflöste. Im Vergleich zu denjenigen, die eisenreich blieben (Eisen >13 µmol/L), war die Sterblichkeit bei denjenigen mit persistierendem oder neu auftretendem Eisenmangel nach einem Jahr höher [Hazard Ratio (HR) 1,81 (1,23-2,67) bzw. HR 1,40 (0,91-2,14)] in multivariablen Modellen (P = 0,02). Im Vergleich zum persistierenden Eisenmangel war die Auflösung des Eisenmangels mit einer geringeren Mortalität verbunden [HR 0,61 (0,44-0,86); P = 0,004]. Veränderungen des nach FAIR-HF-Kriterien definierten Eisenmangels waren nicht in gleicher Weise mit der Sterblichkeit verbunden. Eine Anämie war mit einem schlechten Ergebnis assoziiert, selbst wenn sie sich auflöste.
Die Behandlung einer Anämie mit Darbepoetin alfa verbesserte die klinischen Ergebnisse bei Patienten mit eingeschränkter linksventrikulärer Pumpfunktion nicht, wie die RED-HF-Studie zeigte. Eisenmangel ist ein unabhängiger Prädiktor für Belastungsintoleranz bei Patienten mit systolischer Herzinsuffizienz. Eisenmangel in Kardiomyozyten beeinträchtigt die mitochondriale Atmung und die Anpassung an eine akute und chronische Zunahme der Arbeitsbelastung. Eine Eisensupplementierung stellt die Energiereserven und die Funktion des Herzens in eisenarmen Herzen wieder her.
Eisenmangel-Behandlung: oral oder intravenös?
In der Herzinsuffizienz ist die Eisenresorption durch ein Ödem der gastrointestinalen Mukosa beeinträchtig. Zudem ist in der Herzinsuffizienz die intestinale Eisenaufnahme durch eine 30-40% Verminderung des Blutflusses in der gastrointestinalen Mukosa beeinträchtigt. Die Eisenresorption kann ebenfalls durch gleichzeitige Einnahme von Medikamenten wie zum Beispiel H2-Blocker oder durch eine diabetische Gastroparese verschlechtert werden. In der Studie IRONOUT (Lewis et al. Circ Heart Fail 2016;9:300 ergab die orale Substitution nach 16 Wochen eine leichte Zunahme des Ferritins von 11ng/ml und der Transferrinsättigung von 3%, während in der FAIR-HF Stuide (Anker et al NEJM 2009;36:2436-4) eine Zunamhe des Ferritins mit intravenöser Substitution von 238ng/ml und eine Zunahme der Transferrinsättigung von +12% registriert wurde.
Welche Behandlung des Eisenmangels und wie? In der EFFECT-HF Studie (van Veldhuisen et al. Circulation 2017;139:1374-1383) ergab sich nach 24 Wochen Behandlung eine Differenz zwischen Behandlung mit Eisencarboxymaltose zur Standard of Care von Ferritin um +188,7ng/ml, der Transferrinsättigung von +4,7% und des Hämoglobins um + 0,74g/l. Klinisch äusserte sich die orale Behandlung in der IRONOUT-Studie in einer nicht signifikanten Zunahme des VO2 Peaks um 0,30 ml/kg/min (p=0.30). Die intravenöse Eisensubstitution ergab in EFFECT-HF eine signifikante Zunahme des VO2-Peaks. Die Studien-Autoren bewerteten die IRONOUT-Studie wie folgt «Die Ergebnisse dieser Studie zeigen, dass orale Eisensubstitution bei Herzinsuffizienz-Patienten mit reduzierte Pumpfunktion ohne Wirkung ist». EFFECT-HF: Intravenöse Eisensubstitution mit Eisencarboymaltose verbessert die maximale VO2 um 7.5% (1.o4ml O2/min/kg). Dies kann die Morbidität und Mortalitat verringern, da 6% Zunahme des peak VO2 mit einer 5% verringerten Inzidenz für Gesamtmortalität und Hospitalisierung einhergeht.
Guidelines ESC 2021: Eisenmangel
Es wird empfohlen, dass alle Patienten mit Herzinsuffizienz periodisch auf Anämie und Eisenmangel mit einem vollständigen Blutbild, Serumferritin-Konzentration und Transferrinsättigung gescreent werden (I/C).
Die intravenöse Eisensubstitution mit Eisencarboxymalfose sollte für symptomatische Patienten mit LVEF <45% und Eisenmangel, definiert als Serumferritin <100ng/ml oder Serumferritin 100-299 ng/ml mit Transferrinsättigung <20% in Betracht gezogen werden zur Linderung der Herzinsuffizienz-Symptome, Verbesserung der körperlichen Leistungsfähigkeit und der Lebensqualität (IIa/A).
Bei Patienten mit Eisenmangel und einer linksventrikulären Auswurffraktion von weniger als 50 %, die nach einer akuten Herzinsuffizienz stabilisiert wurden, war die Behandlung mit Eisen(III)-carboxymaltose sicher und verringerte das Risiko von Krankenhausaufenthalten wegen Herzinsuffizienz, ohne erkennbare Auswirkungen auf das Risiko eines kardiovaskulären Todes.
Studien mit intravenöser Behandlung mit Eisencarboxymaltose
Die Resultate der AFFIRM-HF Studie ergab, dass bei Patienten mit Eisenmangel und einer linksventrikulären Auswurffraktion von weniger als 50 %, die nach einer akuten Herzinsuffizienz stabilisiert wurden, die Behandlung mit Eisen(III)-Carboxymaltose sicher war und das Risiko von Krankenhausaufenthalten wegen Herzinsuffizienz verringerte, ohne erkennbare Auswirkungen auf das Risiko eines kardiovaskulären Todes. (Ponikowski et al Lancet 2020; 396: 1895-1904).
Eine weitere Studie, die den Nutzen einer Eisensubstitution bei Herzisuffizienz zeigte, ist die IRONMAN-Studie mit intravenöser Gabe von Eisenderisomaltose. Diese Studie zeigte, dass bei einem breiten Spektrum von Patienten mit Herzinsuffizienz, verminderter linksventrikulärer Ejektionsfraktion und Eisenmangel die intravenöse Verbareichung von Eisen(III)-Derisomaltose mit einem geringeren Risiko von Krankenhauseinweisungen wegen Herzinsuffizienz und kardiovaskulärem Tod verbunden, was den Nutzen der Eisenergänzung in dieser Bevölkerungsgruppe weiter untermauert.
In einer diesjährigen Metaanalyse von zwölf randomisierten und kontrollierte Studien wurden 2381 Patienten einbezogen (Sindone et al ESC Geart Failure 2023;10:44-56). Die Mehrheit (90,8 %) der Patienten, die eine IV-Eisenkohlenhydrattherapie erhielten, bekamen Eisencarboxymaltose (FCM) verabreicht; 7,5 % erhielten Eisensaccharose und 1,6 % Eisenisomaltosid. Eine IV-Eisenkohlenhydrattherapie reduzierte signifikant die Hospitalisierung wegen einer Verschlechterung der HF [0,53 (0,42-0,65); P < 0,0001] und die erste Hospitalisierung wegen einer Verschlechterung der HF oder Tod [0,75 (0,59-0,95); P = 0,016], ie Therapie hatte aber keinen signifikanten Einfluss auf die Gesamtmortalität im Vergleich zur Kontrollgruppe. Eine intravenöse Eisen-Kohlenhydrat-Therapie verbesserte die funktionelle und körperliche Leistungsfähigkeit im Vergleich zur Kontrollgruppe signifikant. Es gab keinen signifikanten Unterschied zwischen den Ergebnissen der IV-Eisenkohlenhydratformulierungen, wenn ähnliche Endpunkte gemessen wurden. Es wurde kein signifikanter Unterschied bei den unerwünschten Ereignissen zwischen den Behandlungsgruppen festgestellt. Die IV-Eisenkohlenhydrat-Therapie führte zu Verbesserungen bei einer Reihe klinischer Ergebnisse und zu einer Steigerung der funktionellen und körperlichen Leistungsfähigkeit, während sich die unerwünschten Ereignisse zwischen den IV-Eisenkohlenhydrat- und Placebo-/Standardbehandlungsgruppen nicht signifikant unterschieden.
Abschliessend zeigte der Referent einen Behandlungsalgorithmus für Eisenmangel (Gstrein C et al. Swiss Med Wkly 2017;147:w14453), sowie die Anzahl der intravenöser Eisensubstitutionen, die erforderlich sind bei 711 Patienten aus der gleichen Studie , nämlich 168 (23.6%) eine Substitution, 50 (7.0%) zwei Substitutionen und 15 (2,%) drei oder mehr Substitutionen.
Fazit
Patienten mit Herzinsuffizienz sollen regelmässig auf einen Eisenmangel und eine Anämie gescreent werden.
Die frühzeitige Korrektur eines Eisenmangels durch intravenöse Substitution kann Krankenhauseinweisungen wegen Verschlechterung der Herzinsuffizienz vorbeuge.
riesen@medinfo-verlag.ch