- Kognitive Störungen im Alter
Kognitive Störungen im Alter sind häufig und können – wenn früh und richtig diagnostiziert – mit heute vorhandenen medikamentösen und nicht-medikamentösen Massnahmen entscheidend beeinflusst werden. Die Abklärung wie auch die Therapie sind auf den einzelnen Patienten abgestimmt und hängen wesentlich von dessen Einverständnis, Gesundheitszustand und den sozialen Lebensumständen ab.
Mit Patientenklagen über kognitive Störungen können wir bei jüngeren Erwachsenen, aber ganz speziell im 3. und 4. Lebensalter konfrontiert werden. In jedem Fall müssen solche Klagen ernst genommen werden, da bei richtiger Diagnosestellung und frühzeitiger Einleitung von therapeutischen Massnahmen der weitere Verlauf massgeblich beeinflusst werden kann. Obwohl es seit Einführung der DSM-5 den Begriff «Demenz» eigentlich nicht mehr gibt, ist dieses im Alter häufige Krankheitsbild (jeder 3. über 85-Jährige betroffen!) natürlich nicht verschwunden. Zwar hat die Demenz-Inzidenz infolge deutlich besserer Behandlung von vaskulären Risikofaktoren in den letzten 20 Jahren bis zu 50% abgenommen – doch, der demographische Wandel hat diesen medizinischen Fortschritt zahlenmässig praktisch neutralisiert. Das moderne Management von kognitiven Störungen bei dementieller Entwicklung fusst auf 4 Pfeilern (Abb. 1): Frühe und präzise Diagnostik, medikamentöse Therapie, nicht-medikamentöse Therapiemassnahmen und gezielte Unterstützung/Begleitung der Angehörigen und Betreuer (1).
Gibt es im Alter «normale» kognitive Störungen?
Patienten – wie wir Ärzte – haben Tendenz, bei vermehrter Vergesslichkeit und anderen «kleinen» Hirnfehlleistungen das Älterwerden oder das Alter im Allgemeinen dafür verantwortlich zu machen. Die Tatsache ist eine andere. Die normale Hirnalterung ist wissenschaftlich sehr gut untersucht und ist lediglich mit einer diskreten Verlangsamung von Denk- und Reaktionsprozessen verbunden. Kann also ein Name nicht sofort, aber nach einer gewissen Zeit erinnert werden, ist dies noch «normal». Wenn man immer schon ein schlechtes Namensgedächtnis hatte, darf man im Alter keine diesbezügliche Verbesserung erwarten! Ist die Vergesslichkeit aber neu und der dadurch verursachte subjektive Leidensdruck der Patienten vorhanden (selbst bei neuropsychologischer Untersuchung mit Normalbefund), dann ist dies nach neuesten Erkenntnissen als «Subjective Cognitive Decline» zu werten, der in 25% der Fälle innerhalb von 6 Jahren zu einer Demenz führt (2). Leider werden Hirnleistungsstörungen von vielen immer noch primär auf Gedächtnis und Vergesslichkeit reduziert. Unser Hirn leistet jedoch viel mehr! Viele dementielle Prozesse beginnen denn auch in anderen Hirnleistungsbereichen, wo Verschlechterungen (bei erhaltener Gedächtnisleistung) primär über ein anderes Verhalten (z.B. mehr Probleme mit komplexen Aufgaben wie Management von finanziellen Angelegenheiten oder auch das Kochen von komplizierteren Menus!) sichtbar werden. Solche Veränderungen sind nicht normal und müssen abgeklärt werden!
Abgrenzung von «Normal» versus «Pathologisch»
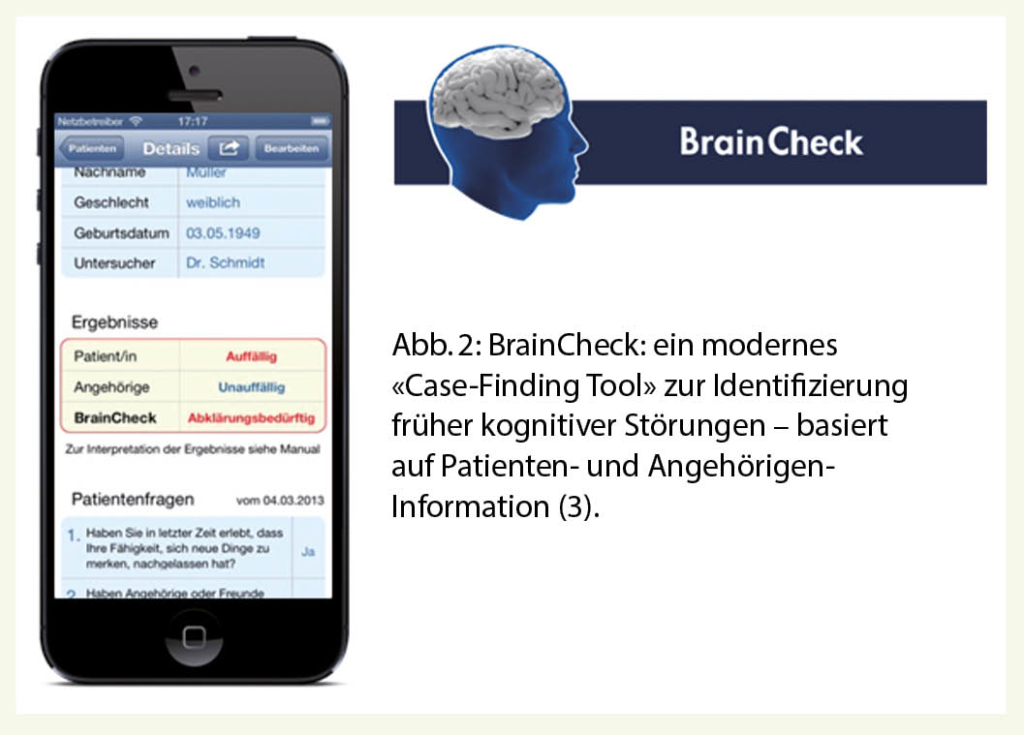
Im Praxisalltag muss schnell und mit wenig Zeitaufwand entschieden werden können, ob kognitive Störungen schnell weiter abgeklärt werden müssen, ob weiter beobachtet werden muss oder kein weiterer Handlungsbedarf besteht! Das frühere (zeitaufwändige) Screening von kognitiven Störungen mittels MMSE und Uhrentest wurde in den letzten Jahren vom sensitiveren und gezielten «Case Finding» mittels «App» abgelöst (Abb. 2). Die von den «Swiss Memory Clinics» und Schweizer Hausärzten entwickelte kostenpflichtige «App» «BrainCheck» trennt in wenigen Minuten «Normal» von «Pathologisch» mit einer Trennschärfe von 90% (3).
Dazu muss der Patient drei einfache Fragen beantworten und einen Uhrentest absolvieren. Gleichzeitig werden seinem engsten Angehörigen/Partner 7 kurze Fragen gestellt. Alle Resultate können sofort in der App erfasst und beurteilt werden. Die Kurzabklärung kann als PDF-File einfach in die elektronische Krankengeschichte integriert werden!
Bei bestehender weiterer Abklärungsbedürftigkeit muss zusammen mit dem Patienten und seinen Angehörigen entschieden werden, wie die Diagnostik weiter vorangetrieben werden soll. Als erster Schritt ist hier sicherlich der (einfache) Ausschluss von schnellbehandelbaren Ursachen ein absolutes «Muss». Eine Schilddrüsenstörung kann mittels TSH Bestimmung ausgeschlossen werden, eine Depression mittels Geriatric Depression Scale (GDS) und eine psychosoziale Belastungssituation (Stressbelastung) mit einer sorgfältigen Anamnese erkannt und im positiven Fall mit entsprechenden Gegenmassnahmen angegangen werden. Bei anamnestisch begründbarem Verdacht, kann auch ein Vitamin-B-Status und eine Lues-Serologie weiterführend sein. Wird man in den genannten Bereichen fündig und entsprechend therapie-aktiv, empfiehlt es sich, rund 6 Monate später die Kognition mittels BrainCheck nachzukontrollieren.
Abklärungsbedürftige kognitive Störungen
Die Art der weiteren Abklärung von kognitiven Störungen ist sehr individuell und hängt vom Einverständnis, dem Gesundheitszustand/Lebenserwartung und den sozialen Lebensumständen des Patienten ab. Bei jüngeren und fitteren Senioren sollte immer eine spezialisierte Abklärung bei einem Demenzspezialisten oder einer Memory Clinic erfolgen. Diese umfasst neben einer medizinischen Untersuchung mit Labor und Biomarkern eine neuropsychologische Abklärung mit Hirnbildgebung (MRI). Bei sehr hochaltrigen und fragilen Patienten kann auch eine verkürzte kognitive Abklärung (z.B. mittels MoCa-Assessment (4)) erfolgen. Diese kann – mit etwas Erfahrung – in der hausärztlichen Praxis durchgeführt und diagnostisch ausgewertet werden. Dazu gehört auch hier imperativ eine Hirnbildgebung (MRI oder CT), um den wahrscheinlichsten neuropathologischen Grund der dementiellen Entwicklung festzulegen. Dies ist entscheidend für die Art der einzuleitenden Therapie.
Kognitive Störungen: Therapeutische Optionen
Handelt es sich gemäss DSM-5 um «milde» kognitive Störungen, befinden sich diese innerhalb von zwei Standardvariationen eines kognitiven Normalbefundes. Therapeutisch stehen hier neben medikamentösen (Ginkgo Biloba 240mg/d und Vitamin D (24 000 Einheiten pro Monat) v.a. nicht medikamentöse Massnahmen im Vordergrund: regelmässige körperliche und soziale (kognitive) Aktivität, gesunde altersgerechte Ernährung (regelmässig und genügend Protein (1.2g/kg Körpergewicht pro Tag; mediterrane Diät mit genügend Omega-3-Fettsäuren) und eine gute hausärztliche Kontrolle von vaskulären Risikofaktoren (art. Hypertonie, Diabetes, Hypercholesterinämie). In der finnischen FINGER Studie (5) konnten allein mit diesen Lebensstilmassnahmen nach 2 Jahren signifikante kognitive Verbesserungen erzielt werden!
Medikamentöse Optionen
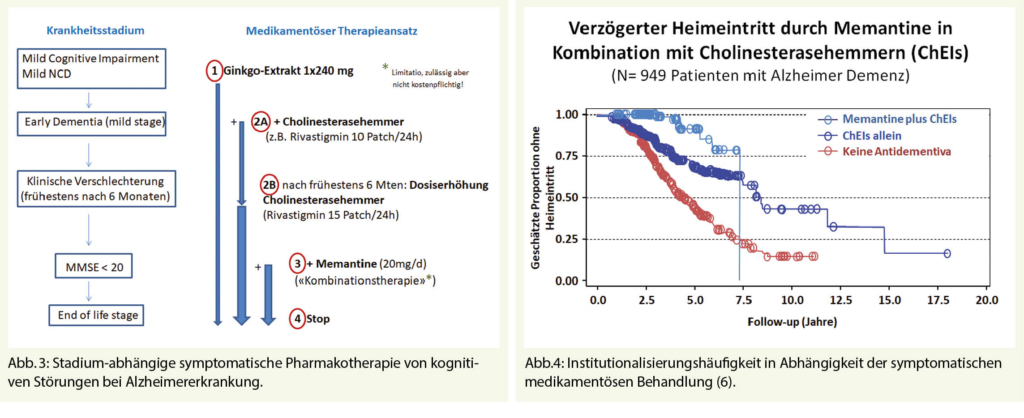
Bevor neue Medikamente zum Einsatz kommen, gilt es grundsätzlich, eine bereits vorhandene allfällige Polypharmazie auf kognitiv beeinträchtigende anticholinerge Substanzen zu überprüfen. Handelt es sich gemäss DSM-5 um «major» kognitive Störungen (Demenz), ist für die Festlegung der medikamentösen Therapie (meist mittels Bildgebung und/oder Biomarker) die dem Prozess zugrundeliegende Neuropathologie entscheidend. Handelt es sich um einen neurodegenerativen Prozess (Alzheimer-Erkrankung), sind abhängig vom Stadium Ginkgo, Cholinesterasehemmer und Memantine Mittel der ersten Wahl (Abb. 3). Bei dieser symptomatischen Therapie wird (bei frühzeitigem Beginn) der Verlauf der Krankheit bzgl. Funktionalitäts- und Selbständigkeitserhalt massgeblich verbessert. Diese Medikamente wirken ausgesprochen langsam, sind aber dank einer «Number Needed to Treat» (NNT) von unter 10 (für alle drei Substanzklassen!) mit einer hohen Responder-Rate versehen. Im Vergleich zu nicht-behandelten Kontrollpopulationen treten erste klinische Differenzen jedoch erst nach einem Jahr Behandlung auf; diese werden in den weiteren Jahren aber sehr relevant, da die Behandlung zu eindrücklich weniger Pflegeheimeintritten führt (6) (Abb. 4). Hier hat sich v.a. auch die Kombinationstherapie von Memantine mit Cholinesterasehemmer (bei MMSE < 20) als sehr erfolgreich erwiesen. Diese ist in der Schweiz jedoch nur off-label-mässig möglich und wegen einer Limitatio nicht voll von der Grundversicherung übernommen. Trotzdem: viele Patienten tragen (angesichts stark gefallener Antidementiva-Preise) die paar Hundert Franken pro Jahr gerne selber, wenn damit finanziell viel höhere Kosten einer Institutionalisierung gespart werden können. Neben der durch Antidementiva länger erhaltenen Alltagsfunktionalität treten unter dieser Therapie auch signifikant weniger demenz-assoziierte Verhaltensauffälligkeiten auf (Aggression, Schreien, motorische Unruhe etc.).
Ist die der dementiellen Entwicklung zugrundeliegende Pathologie rein vaskulär, sind obige Antidementiva (ausser Ginkgo) nicht wirksam und entsprechend nicht indiziert. Hier gilt es mit allen Mitteln, mit Lebensstilmassnahmen und der Beherrschung von vaskulären Risikofaktoren das weitere Fortschreiten der Erkrankung zu verlangsamen. Bei gemischten vaskulär-neurodegenerativen Demenzformen können Antidementiva eingesetzt werden. Bei selteneren Demenz-Pathologien wie Lewis-Body Krankheit, Parkinson- oder Frontotemporal-Demenz lohnt sich eine Rücksprache mit entsprechenden Spezialisten.
Nicht-medikamentöse Optionen
Nicht-medikamentöse Interventionen bei Demenzkranken werden von grossen Fachgesellschaften und Expertengruppen – ausser bei Notfallsituationen – in erster Linie und als primärer Approach bei demenzassoziierten psycho-sozialen Verhaltensauffälligkeiten (BPSD) empfohlen (7). Gemäss Cohen-Mansfield (8) sind die meisten Ärzte für die Medikamentenverschreibung bei BPSD geschult und ausgebildet, jedoch nur die wenigsten verfügen über Kenntnisse zu diesbezüglichen nicht-medikamentösen Therapiemassnahmen und deren Wirkungserfolg. Entsprechend häufig werden deshalb antipsychotische Medikamente eingesetzt, bevor nichtmedikamentöse Interventionen versucht werden.
Im Gegensatz zu den bei Demenz bereits früh eingeschränkten oder verlorenen kognitiven Fähigkeiten sind die emotionalen und psychosozialen Kompetenzen bis in späte Demenzkrankheitsstadien weit weniger vom Abbau betroffen. Hier setzen nicht-medikamentöse Interventionen an, indem sie – weg vom Defizit-Fokus – auf vorhandene Hirnleistungs-Ressourcen zugreifen, diese gezielt nutzen und fördern. Körperliche Aktivität, musikbasierte Aktivitäten sowie proteinreiche, mit Vitamin D ergänzte Ernährung zum Erhalt der Muskelgesundheit bei Demenz haben sich am erfolgreichsten gezeigt (9). Spannend und immer wieder Gegenstand von Forschungen ist die Hirnwirkung von mit Musik kombinierten Bewegungsaktivitäten wie Tanz und Rhythmik. In der «Einstein-Aging» Kohortenstudie wurde regelmässiges Tanzen als Freizeitbeschäftigung mit einem bis zu 80% erniedrigten späteren Demenzrisiko assoziiert (10). In einer Interventionsstudie mittels Rhythmik nach Dalcroze konnte das motorisch-kognitive Dual-Task Vermögen von zuhause lebenden Senioren verbessert und das Sturzrisiko um über 50% reduziert werden (11). Bei fortgeschrittenen Demenzstadien scheint die Dalcroze Rhythmik neben der positiven Beeinflussung von BPSD-Symptomen vor allem die sprachlichen Fähigkeiten zu fördern (12). Nicht-pharmakologische Interventionen bei Demenzerkrankten sind ein wesentlicher Bestandteil des modernen 4-Säulen-Demenz-Managements. Die zu erwartende Hauptwirkung solcher Massnahmen besteht in der positiven und nebenwirkungsfreien Beeinflussung von BPSD. Körperliche Aktivitätsprogramme zeigen zusätzliche Vorteile für die Alltags-Funktionalität, die insbesondere bei gleichzeitiger proteinreicher Ernährung und Vitamin- D-Supplementation deutlich länger erhalten werden kann. Musik und musikbasierte Bewegungsprogramme wie Tanz und Rhythmik scheinen besonders geeignet, Hirnreserven zu mobilisieren und damit die Kognition signifikant zu verbessern.
Bei diesem Artikel handelt es sich um einen Zweitabdruck des in info@herz+gefäss 2019:9(5);10-12 erschienen Originalartikels.
Ärztlicher Direktor & Klinischer Professor für Geriatrie
Universitäre Altersmedizin FELIX PLATTER & Universität Basel
Burgfelderstrasse 101
4002 Basel
RetoW.Kressig@felixplatter.ch
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Beitrag deklariert.
- Die nicht-medikamentöse und medikamentöse symptomatische Therapie bei kognitiven Störungen ist lediglich ein Bestandteil im multifaktoriellen 4-Säulen Management der Demenzerkrankung.
- Nicht-medikamentöse Ansätze zeigen marginale bis nicht nachweisbare kognitive Effekte, sind aber wirksam bei Verhaltensstörungen, psychiatrischen Symptomen und Betreuerbelastung.
- Bei der pharmakologischen Therapie gilt es, eine vorhandene Polymedikation soweit wie möglich zu reduzieren und potentiell schädliche Substanzen (Priscus-Liste) abzusetzen.
- Zum heutigen Zeitpunkt gibt es keine rationalen Gründe, die heute zur Verfügung stehenden symptomatisch wirkenden Antidementiva (Cholinesterasehemmer, Memantine und Ginkgo Extrakt) nicht einzusetzen.
- Bei klinisch relativ gering ausfallenden Sofortwirkungen bei Therapiebeginn stehen hier vor allem Vorteile im Langzeitverlauf (um Jahre verzögerte Institutionalisierung, signifikant weniger Verhaltensstörungen) im Vordergrund.
1. Kressig RW. Aktuelle Pharmakotherapie der Alzheimer Demenz. der informierte Arzt 2015;10:30-33
2. Wolfsgruber S, et al. AgeCoDe Study Group. Differential Risk of Incident Alzheimer’s Disease Dementia in Stable Versus Unstable Patterns of Subjective Cognitive Decline.J Alzheimers Dis. 2016;54:1135-1146
3. Ehrensperger MM, et al. BrainCheck – a very brief tool to detect incipient cognitive decline: optimized case-finding combining patient- and informant-based data. Alzheimers Res Ther. 2014;6:69
4. Nasreddine ZS, et al. The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc. 2005;53:695-99
5. Kivipelto M et al. The Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability (FINGER): study design and progress. Alzheimers Dement. 2013;9:657-65.
6. Lopez OL et al. Long-term effects of the concomitant use of memantine with cholinesterase inhibition in Alzheimer disease. J Neurol Neurosurg Psychiatry. 2009 Jun;80(6):600-7
7. Savaskan E et al. Recommendations for diagnosis and therapy of behavioral and psychological symptoms in dementia (BPSD).Praxis (Bern 1994). 2014;103:135-48
8. Cohen-Mansfield J. Nonpharmacologic interventions for inappropriate behaviors in dementia: a review, summary, and critique. Am J Geriatr Psychiatry. 2001;9:361-81
9. Kressig RW. Non-pharmacological interventions in dementia. Internistische Praxis 2017;58:1-7
10. Verghese J et al. Leisure activities and the risk of dementia in the elderly. N Engl J Med. 2003;348:2508-16
11. Trombetti A et al. Effect of music-based multitask training on gait, balance, and fall risk in elderly people: a randomized controlled trial. Arch Intern Med. 2011 Mar 28;171:525-33.
12. Winkelmann A et al. La rythmique Jacques-Dalcroze. Une activité physique novatrice pour les personnes agées. Gériatrie Pratique 2005;3:52-55
der informierte @rzt
- Vol. 8
- Ausgabe 11
- November 2019