- Kryoglobulinämie und erhöhte Kreatinkinase
Am 6. Januar fand ein Online-Workshop zu rheumatologischen Themen unter der Leitung von Prof. Dr. med. Oliver Distler, Klinikdirektor der Klinik für Rheumatologie am USZ, statt. Die Themen waren Kryoglobulinämie-Vaskulitis, MR-Neurographie, Abklärung von Creatinkinase-Erhöhungen, «Reaktive» Arthritis und Fasciitis plantaris. Dieser Bericht fasst die Referate über die Kryoglobulinämie und die Differentialdiagnose von Creatinkinase-Erhöhungen zusammen.
Kryoglobulinämie-Vaskulitis
Kryoglobuline sind Immunkomplexe, Verbindungen aus (Auto)-Antikörpern und Antigenen. Die Kryoglobulinämie ist eine Verbindung von Kryoglobulin und Antigen, z.B. HCV-Proteine. Kryoglobuline sind Antikörper, die bei Kälte ausfallen und In-vivo-Immunkomplexe bilden. Bei der rheumatoiden Arthritis sind es Rheumafaktoren und andere Antikörper. Diese Komplexe lagern sich an den Wänden kleiner Gefässe ab und führen zur Entzündung, im Gegensatz zu keinen oder kaum nachweisbaren Immunkomplexen, ANCA-assoziierten Vaskulitiden (sog. Pauci-immun-Vaskulitiden). Davon müssen die Kälteagglutinine unterschieden werden. Sie bestehen v.a. aus IgM (Auto-)-Antikörpern, die Erythrozyten binden (agglutinieren) und zur Hämolyse (bei 15-18 °C) führen (Mykoplasmen, EBV, HIV, B-NHL). Nach dieser Einführung ins Thema Kryoglobulinämie-Vaskulitis übergab Prof. Distler das Wort dem Referenten, Dr. med. Mike Becker, Oberarzt an der Klinik für Rheumatologie des USZ.
Die kryoglobulinämische Vaskulitis gehört zu den Vaskulitiden kleiner Gefässe, erklärte Dr. med. Mike Becker, Oberarzt Klinik für Rheumatologie USZ. Der Referent unterschied 3 Typen von Kryoglobulinen. Typ I: monoklonales Immunglobulin, tritt bei B-Zell-lymphoproliferativen Krankheiten auf; Typ II: monoklonales Ig + polyklonales Ig und Typ III: polyklonales Ig. «Die gemischten Kryoglobulinämien vom Typ II und Typ III treten bei chronischen Infekten – vor allem Hepatitis-C-Virus, bei B-Zell-lymphoproliferativen und Autoimmunkrankheiten – und als «essentielle» Kryoglobulinämien auf», ergänzte Dr. Becker.
Fallbeispiel: 51-jähriger Patient, wegen V.a. Kollagenose nach Ischämie Dig. III re. zugewiesen. ANA pos., RF neg.
2019 Diagnose einer demyelinisiernden PNP/c. 01/2020 Diagnose kryoglobulinämische Vaskulitis Typ II nach Brouet (IgM Kappa), keine Hepatitis, Quantiferon neg., Lues neg. Immunfixation neg., Patient möchte keine Therapie.
05/2020 Zuweisung Neurologie wg. Verschlechterung PNP (u.a. Grosszehenerhebung M1 li.) Therapie Rituximab – zwischenzeitlich krit. Ischämie re. Fuss → PTA
Fallbeispiel: 48-jähriger Patient, Hepatitis C (1b) ED12/2018 bei St.n. Polytrauma als Kind mit Transfusion (Mitbeurteilung aus Gastroenterologie).
Symmetrische, axonale PNP seit 2015, 4/2019 progredient; Gelenkschmerzen und Morgensteifigkeit, bei Erstvorstellung abgeblasste Purpura an den Beinen. Zunächst Therapie mit Maviret (Glecaprevir/Pibrentasvir) 8 Wochen, dann zeigt sich laborchemisch eine Remission.
Therapie der Kryoglobulinämie
Therapiestrategie bei gemischten kryoglobulinämischen
Vaskulitiden:
- Mild bis moderat: Arthralgien, Purpura, Polyneuropathie
HCV neg.: Kortikosteroide? Azathioprin? Rituximab?
HCV pos.: Antivirale Therapie - Schwer: Nierenbeteiligung, Mononeuritis multiplex, Hautnekrosen
HCV neg.: Rituximab, Kortikosteroide, Ilomedin®
HCV pos.: Antivirale Therapie - Katastrophal: Rapid-progressive Glomerulonephritis, ZNS-
gastrointestinale, Herz- oder Lungenbeteiligung
HCV neg.: Rituximab, Plasmaaustausch vs. Kortikosteroide
HCV pos.: Antivirale Therapie
Optionen für die Zukunft sind: Belimumab, Ibrutinib, Daratumumab/ Bortezomib/ Lenalidomid.
Erhöhte Kreatininkinase (CK): Abklärungen
Welches sind die ersten Überlegungen bei der Feststellung einer erhöhten Kreatinkinase? Die Referentin, Frau Dr. med. Katja Göhner, Oberärztin an der Klinik für Rheumatologie des USZ, empfahl ihrem Publikum, bei betroffenen PatientInnen wie folgt nachzufragen: Muskuläre Anstrengungen am Vortag? (Arbeit auf Baustelle? Marathonlauf? Gartenarbeit?); Grippeimpfung intramuskulär vorgestern? Drogen? Klinische Abklärung mittels ENMG oder Operation letzte Woche? Die Kreatinkinase kann elektrophoretisch in drei Isoenzyme aufgeteilt werden, CK-MM, CK-MB und CK-BB. Häufig begleitend mit CK sind AST, ALT und LDH. CK-MB ist ein Marker für Myokardschaden, allerdings sind die kardialen Troponine spezifischer und sensitiver. Eine weitere Ursache für erhöhte Kreatinkinase ist die Makro-CK, eine Komplexbildung mit Immunglobulin. Man kann sie elektrophoretisch aufgrund des höheren Molekulargewichts unterscheiden.
Erhöhte Kreatinkinase: Differentialdiagnose Teil 1
1. Anstrengende körperliche Aktivität v.a. exzentrisch
2. Trauma (EMG, i.m. Injektionen), Operationen, epileptischer Anfall
3. Medikamente
4. Toxine (Alkohol, Heroin, Kokain)
5. Endokrinoloisch (Hypothyreose, Hypoparathyreoidismus,
Akromegalie)
6. Virusinfektionen
7. Metabolische Störungen (Hypokaliämie, Hyponatriämie)
8. Geschlecht, Herkunft, idiopathisch
9. Obstruktive Schlafapnoe
10. Chronische Kardiopathie
11. Makro-CK
12. Malignes Hyperthermiesyndrom
Medikamente, die mit CK-Erhöhung einhergehen
Statine, Fibrate, Colchicin, Anti-Psychotika (eingeschlossen Malignes Neuroleptika-Syndrom), Zidovudine, Beta-Blocker, Isoretinoin, Antimalaria, Penicillamin, u.a.
Anti-HMGCR-assoziierte immunmediierte Myopathie
Therapie: Prednison mit jeweils deutlicher Verbesserung. MTX/AZA nicht vertragen, Privigen, RTX abgelehnt wegen Sorge vor
Nebenwirkungen.
Statin-assoziierte immunvermittelte nekrotisierende Myopathie (IMNM)
Prävalenz 2-3/100’000, proximale Muskelschwäche +/- Schmerzen und stark eröhte CK (zumeist über 5000U/l). Beschwerden und CK bleiben nach Sistieren des Statins. Meist kein zusätzlicher Organbefall. Mittlere Dauer der Statinexposition betrug in einer Fallkontrollstudie 38 Monate. HMG-CoA-Reduktase-Autoantikörper sind in der Regel positiv.
Histopathologische Muskelbiopsie: prominente Muskelnekrose und Zeichen der Regeneration mit sehr wenig Entzündungszellen/Infiltraten. Aufregulation der MHCI-Expression.
Therapie: Steroide, MTX, AZA oder MMF, in schweren Fällen IVIG oder RTX. Eher schlechtes Ansprechen.
Erhöhte Kreatinkinase: Differentialdiagnose Teil 2
Entzündliche Myopathien
- PM, DM, IMHM, juvenile Myositis
Begleitmyositis
bei Sjögren-Syndrom, Lupus, SS, RA
bei Sarkoidose/M. Behçet/Vaskulitiden - Dystrophinopathien
Duchenne, Becker, Fazio-scapulo-humeral
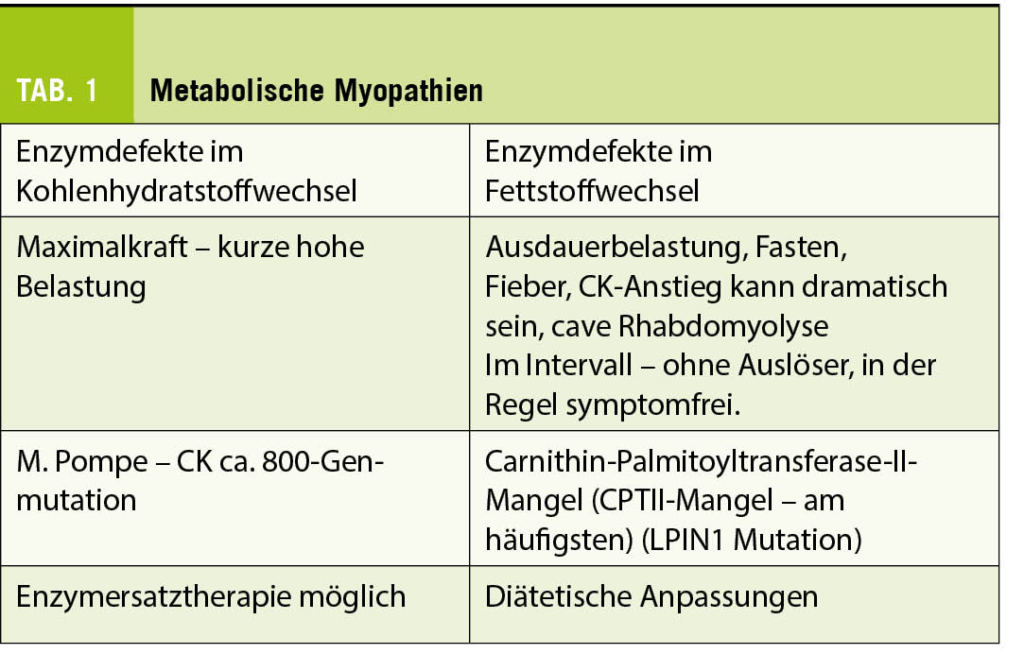
Limb-Girdle, Myotone Dystrophie - Metabolische Myopathien
Enzymmangel im KH-Lipid-Purin-Metabolismus - Motoneuronenerkrankungen
Amyotrophe Lateralsklerose, spinale Muskelatrophie
Polymyositis/Dermatomyositis. Abklärung nach Anamnese und Klinik: Untersuchung Integument, Kapillarmikroskopie, erweiterte Laboranalyse mit Antikörperprofil, MRI Myositis Protokoll, ENMG, Muskelbiopsie. Bei der Polymyositis ist die Kreatinkinase i.d.R deutlich erhöht. Die Höhe variiert jedoch beträchtlich. Bei der Dermatomyositis ist eine amyopathische DM möglich oder DM sine Myositis Einschlusskörperchenmyositis: oft erhöhte CK, aber milde, nicht über 1000U/l.
Klassifikationskriterien für adulte und juvenile, idiopathische, inflammatorische Myopathien und Hauptsubgruppen (www.imm.ki.se/biostatistics/calculators/iim).
Fallbeispiel: 68-jährige Patientin mit Adipositas, Diabetes mellitus Typ 2. HbA1c 8.8%, hohe Insulindosen, Osteoporose, Atorvastatin. Multilokuläre Muskelschmerzen, Probleme beim Treppensteigen und Greifen/Halten von Gegenständen (Mutilation der Hände bei Nabelschnurvorfall).
Labor: CK 800U/l, Myoglobin 260µg/l, Troponin T 159mg/l. ANA und Differenzierung, Myositis Screen negativ.
Bisherige Therapie: Prednison 10-20mg – Besserung subjektiv
Ganzkörper-MRI: Ödeme M. vastus medialis links, keine Atrophien.
CT Hals/Thorax/Abdomen unauffällig, keine Hinweise auf Neoplasien.
MRI Herz: keine Hinweise auf Myokarditis, keine Narbe oder Fibrose des LV-Myokards.
Adenosin-Kardio-MRI 04/2020 (extern): keine Hinweise auf Myokarditis, keine Ischämie.
Kapillarmikroskopie 07/20: unauffällig. Antikörper CN-1A-AK 5.4 (<1) deutlich erhöht.
Biopsie M. vastus medialis links 07/20: CD-8 Infiltration, MHC-I Aufregulierung, deutliche mitochondriale Pathologie, pTOP43 und p62 positiv.
Einschlusskörperchenmyositis (IBM)
Charakteristische Klinik: Langsam progrediente zumeist schmerzlose Schwäche besonders der Knieextensoren und Fingerflexoren.
Labor: milde CK-Erhöhung in ca. 80%. Anti-CN-1A (90-95% spezifisch, 40-70% sensitiv)
Muskelbiopsie: Endomysiale lymphozytäre Infiltrationen (CD 8 T-Zellen), mitochondriale Abnormalitäten, Proteinaggregate, Rinmed Vacuoles.
MRI: z.B. Ödeme im Bereich Knieextensoren
Therapieoptionen: keine evidenzbasierte wirksame Therapie. Steroide verbessern allein die CK, MTX und IVIG (insbesondere bei Schluckproblemen).
Fazio-Scapulohumerale Dystrophie
(kommerzieller Gentest – wie in 95% der Fälle – war positiv)
Dritthäufigste Muskeldystrophie ca. 1:20’000, autosomal dominant vererbt, 30% Spontanmutationen.
Muskeldystrophien: Defekte/Fehlen bestimmter Muskelproteine. Beginn häufig um das 20. Lebensjahr, langsam progredient. Bis zu 50% entzündliche Infiltrate in der Biopsie.
Quelle: Online-Rheumaworkshop USZ, 06.01.2022
riesen@medinfo-verlag.ch