- Nahrungsergänzung bei Hämodialyse
In der Schweiz gibt es etwa 5000 Dialysepatienten. Es handelt sich dabei um eine gefährdete und zunehmend ältere Bevölkerungsgruppe. Dialysepatienten weisen häufig mehrere Komorbiditäten auf, weshalb Pflegefachpersonen verschiedener Disziplinen regelmässig mit diesen Patienten konfrontiert sind. Dies erfordert spezifische Kenntnisse, auch in Bezug auf ihre Ernährung. In diesem Artikel werden mögliche Nährstoffdefizite und -überschüsse bei Dialysepatienten sowie die neuesten Therapieempfehlungen zu deren Behebung erläutert.
There are about 5000 dialysis patients in Switzerland. They represent a vulnerable and increasingly elderly population. Dialysis patients often have multiple co-morbidities; therefore, caregivers from different disciplines are regularly confronted with these patients, which requires specific knowledge, also with regard to their nutrition. In this review, we will discuss possible dietary deficits and excesses in hemodialysis patients and the latest therapeutic recommendations.
Key Words: hemodialysis, co-morbidities, dietary, nutritional supplements, vitamins
Dialysepatienten in der Schweiz: eine gefährdete Bevölkerungsgruppe
Gemäss dem Schweizer Dialyseregister «SRRQAP» (Swiss renal registry and quality assessment program) gibt es in der ganzen Schweiz rund 5000 Dialysepatienten. Dieses Register erfasst seit 2014 auch die klinischen Merkmale dieser Patientengruppe. Bei 90 % der Patienten kommt die Hämodialyse (HD) zum Einsatz, bei 10 % die Peritonealdialyse. In beiden Fällen handelt es sich um eine langwierige Behandlung. Bei der HD müssen durchschnittlich drei Dialyse-Sitzungen pro Woche absolviert werden, wobei jede drei bis vier Stunden dauert. Patienten, die mit Peritonealdialyse behandelt werden, müssen sich 2 bis 5 Behandlungszyklen à 30 Minuten pro Tag unterziehen.
Die Zahl der Dialysepatienten steigt langsam, aber stetig um 1-2 % pro Jahr. Weltweit gibt es derzeit etwa 2 Millionen Dialysepatienten. Dies ist vor allem auf die Diabetes-Epidemie, Hauptursache für terminale Niereninsuffizienz, zurückzuführen, aber auch auf die Alterung der Bevölkerung. Das Medianalter der Dialysepatienten liegt bei 72 Jahren, wobei 20 bis 25 % ≥ 80 Jahre alt sind (SRRQAP-Daten). Die Dialyse-Sitzungen und die Einschränkungen bei der Ernährung, die zur Aufrechterhaltung der Homöostase erforderlich sind, stellen die die betroffenen Patienten auf eine harte Probe bezüglich ihrer Ernährungsgewohnheiten. Häufig sind diese schon dadurch geschwächt, dass sie aufgrund der Niereninsuffizienz weniger Appetit haben. Es besteht das Risiko sowohl einer Unterernährung als auch eines Überangebots an bestimmten Nahrungsstoffen. Der Grat zwischen diesen beiden Zuständen ist schmal. Aus diesem Grund ist es wichtig, dass die Ernährung dieser Bevölkerungsgruppe genau überwacht wird, am besten durch spezialisierte Ernährungsberaterinnen.
Die in diesem Artikel besprochenen Empfehlungen gelten im Grossen und Ganzen auch für Peritonealdialyse-Patienten, deren genaueren Betrachtung den Rahmen dieses Artikels sprengen würde.
Technischer Hintergrund
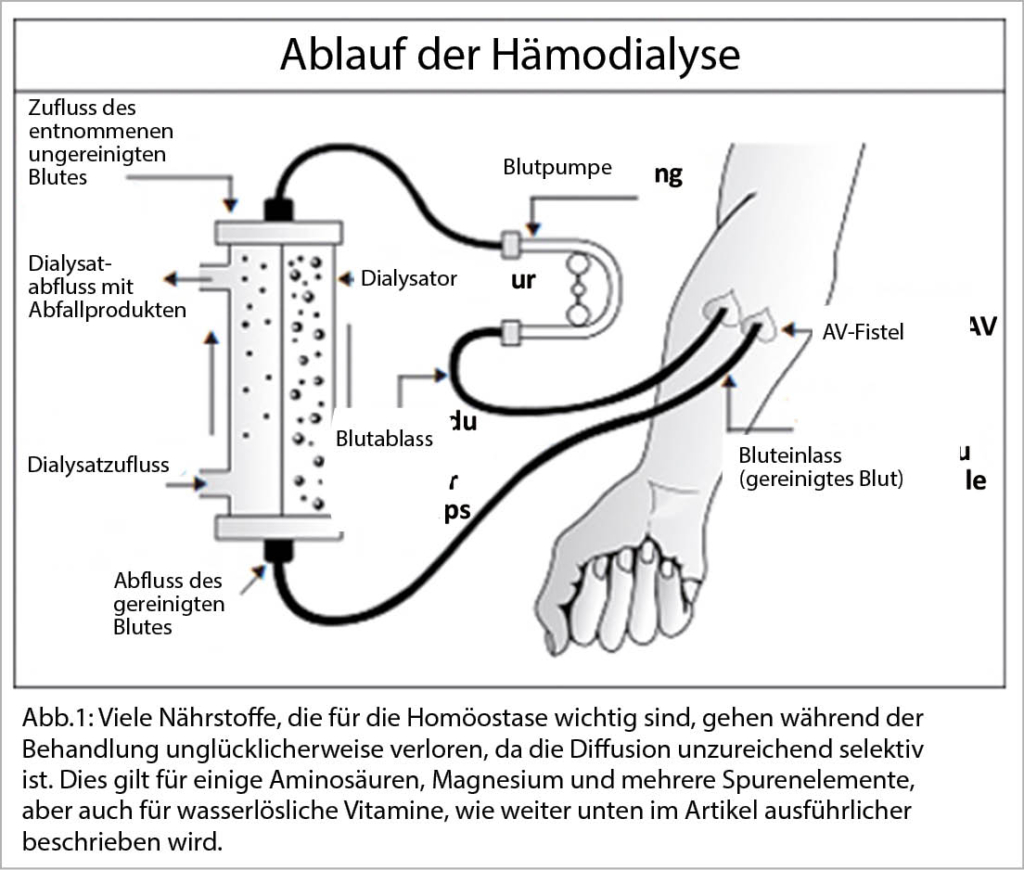
Die Hämodialyse (HD) ist ein hochtechnischer Vorgang, bei der semipermeable Filtersysteme, hochreines Wasser, eine Mischung aus Elektrolyten und ein extrakorporales Kreislaufsystem zur Reinigung des Blutes eingesetzt werden (Abb. 1). Obwohl es sich um ein sehr leistungsstarkes System handelt, beträgt die erreichte Clearance von Schlüsselsubstanzen wie Harnstoff und Kreatinin nicht mehr als 15 ml/min. Die HD ersetzt also bei weitem nicht alle Funktionen der Niere. Dies hat zur Folge, dass die Patienten viele Medikamente einnehmen und Einschränkungen bei der Ernährung in Kauf nehmen müssen. Darüber hinaus entwickeln die meisten Patienten eine Oligurie oder Anurie und müssen zudem eine Flüssigkeitsrestriktion einhalten.
Die Blutreinigung erfolgt nach dem Diffusionsprinzip. Während einer Hämodialyse-Sitzung kommt das Blut des Patienten mit einem Filter, dem Dialysator (einer künstlichen, halbdurchlässigen Membran) in Kontakt. Wenn das Blut und die Dialyselösung eine unterschiedliche Molekülkonzentration aufweisen, diffundieren die Moleküle durch die Membran in Richtung der niedrigeren Konzentration. Dies ist zum Beispiel bei Kalium (Konzentration im Dialysat: 2-4 mmol/l), Harnstoff und Phosphat (Konzentration im Dialysat: 0 mmol/l) der Fall. Ihre Konzentration nimmt während jeder Dialysesitzung stark ab, um sich dann in den folgenden Stunden und Tagen bis zur nächsten Sitzung wieder zu stabilisieren.
Der alte Dämon ist noch nicht tot: Kalium
Die wahrscheinlich am meisten gefürchtete Elektrolytstörung bei Dialysepatienten, die zu zahlreichen Einschränkungen bei der Ernährung führt, ist die Hyperkaliämie. Die Hyperkaliämie ist grösstenteils auf die Anreicherung von Kalium aus der Nahrung (Obst, Gemüse, Kartoffeln) zurückzuführen.
Weniger bekannt ist, dass auch Verstopfung eine Hyperkaliämie auslösen oder verschlimmern kann. Die Ausscheidung von Kalium über den Dickdarm ist bei Hämodialyse-Patienten dreimal so hoch wie bei Gesunden. Dies ist wahrscheinlich auf eine kompensatorisch erhöhte Leitfähigkeit der Kaliumkanäle in den Epithelzellen des Dickdarms zurückzuführen (1). Daher ist es wichtig, Verstopfung zu vermeiden und/oder zu behandeln, am besten mit einer ballaststoffreichen Diät und/oder osmotischen Abführmitteln wie Lactulose oder Polyethylenglycol (2).
Ein gewisser Grad an Hyperkaliämie wird bei Dialysepatienten häufig toleriert. Dies zeigen Beobachtungsstudien, bei denen das Mortalitätsrisiko nur bei einem Kaliumwert von >5,6 mmol/l steigt (3). In solchen Fällen wird der Nephrologe zunächst versuchen, durch Dialysesitzungen das Kalium herauszufiltern, bevor er dem Patienten eine strengere Nahrungsrestriktion nahelegt. Die National Kidney Foundation empfiehlt für alle Dialysepatienten eine Kaliumaufnahme von <3g (<77 mmol) pro Tag. Um dieses Ziel zu erreichen, ist es häufig nötig, den Verzehr von kaliumreichen Lebensmitteln wie bestimmten Früchten (Bananen, Aprikosen) und Gemüse (Spinat, Avocados, Bohnen, Kartoffeln) einzuschränken. Kaliumreiche Lebensmittel sind auch reich an Ballaststoffen, so dass eine Einschränkung das Risiko von Verstopfung erhöhen und zu einem Teufelskreis führen kann.
Um dies zu verhindern, ist die Verwendung von Kalium Chelatoren theoretisch eine interessante Lösung. Die in der Schweiz erhältlichen Chelatbildner sind Natrium-Polystyrolsulfonat (Resonium®), Calcium-Polystyrolsulfonat (Sorbisterit®) und seit kurzem auch Patiromer (Veltassa®). Hierbei handelt es sich um Harze oder Polymere (Veltassa®) in Pulverform, die mit Wasser verdünnt werden. Im Dickdarm wird Kalium in den Verbindungen gegen Natrium oder Kalzium ausgetauscht, die dann mit dem Stuhl ausgeschieden werden. Leider können Sorbisterit® und Resonium® in seltenen Fällen zu Nekrosen und/oder Perforation des Dickdarms führen (Inzidenz 0,27 %), insbesondere in der postoperativen Phase (4). Aus diesem Grund sollte ihre Verschreibung zeitlich begrenzt werden. Im Gegensatz dazu wurde diese Nebenwirkung bei Veltassa® nicht beschrieben. Es wird derzeit untersucht, ob die langfristige Einnahme von Veltassa® dazu beiträgt, eine Ernährung mit mehr Obst, Gemüse und Ballaststoffen aufrechtzuerhalten.
Mangelernährung, Proteine und Aminosäuren
Mangelernährung gilt als eine der Hauptkomplikationen der Hämodialyse. In der englischsprachigen Literatur als «Protein-Energy Wasting (PEW)» bezeichnet, ist Unterernährung die Folge eines über den Anabolismus hinausgehenden Katabolismus von Körperprotein. PEW tritt besonders häufig bei Hämodialyse-Patienten auf, und zwar aufgrund der Proteinverluste im Dialysat, der diätetischen Einschränkungen zur Eindämmung der Hyperphosphatämie und der urämischen Anorexie (durch die Urämie bedingten Appetitlosigkeit), die trotz der Dialysesitzungen bestehen bleiben kann. Bei Patienten mit fortgeschrittener Niereninsuffizienz, die (noch) nicht dialysepflichtig sind, ist eine zu proteinreiche Ernährung jedoch mit einem schnelleren Rückgang der glomerulären Filtrationsrate (GFR) verbunden. Grund dafür ist eine Hyperfiltration in den verbleibenden in ihrer Anzahl bereits reduzierten Nephronen, bedingt durch die proteinreiche Ernährung.
Im Allgemeinen wird eine Aufnahme von 0,6 bis 0,8 g/kg/d empfohlen, wenn die GFR unter 45 ml/min liegt (5). Hämodialyse-Patienten sollten idealerweise 1,0 bis 1,2 g/kg/d Protein zu sich nehmen. Der Übergang zur Dialyse erfordert daher eine deutliche Erhöhung der Proteinzufuhr, ohne dass der Phosphatspiegel “explodiert”. Auch hier ist die Einbeziehung von Ernährungsberaterinnen für eine optimale Behandlung von entscheidender Bedeutung.
In Anbetracht der Aminosäureverluste während der Hämodialyse, kam der letzte Konsensus der ISRNM (International Society of Renal Nutrition and Metabolism) zu dem Schluss, dass Mahlzeiten und Nahrungsergänzungsmittel allen Patienten ohne Kontraindikationen während der Hämodialyse angeboten werden sollten. Dieser Konsensus basiert auf Studien, die den Nutzen für den Ernährungszustand und das Potenzial zur Verbesserung anderer wichtiger Ergebnisse (z.B. Lebensqualität, Patientenzufriedenheit, Überleben) belegen (6).
Laut KDOQI-Empfehlungen 2020 (Kidney Disease Outcome Quality Initiative) sollen Erwachsene mit terminaler Niereninsuffizienz und manifester oder drohender Protein-Energie- Unterernährung, orale Nahrungsergänzungsmittel zu sich nehmen. Dies würde ihren Ernährungszustand verbessern, falls die diätetische Beratung allein nicht ausreicht, um eine dem Grundbedarf entsprechende Protein-Energiezufuhr zu erreichen. Bei Patienten, die trotz oraler Nahrungsergänzungsmittel chronisch unterversorgt sind, ist es sinnvoll, einen Versuch mit enteraler Sondenernährung in Betracht zu ziehen (5).
Vitamine
Hämodialyse-Patienten haben ein erhöhtes Risiko für Vitaminmangel. Zu den Ursachen für Vitaminmangel gehören (a) die Verordnung einer kalium- und phosphatarmen Diät, die den Verzehr von frischem Obst und Gemüse, Milchprodukten und anderen vitaminreichen Produkten einschränkt; (b) ein veränderter Stoffwechsel, wie bei Pyridoxin und möglicherweise Folat; (c) eine veränderte Synthese (z. B. von 1,25-Dihydroxy-Vitamin D); (d) eine möglicherweise verminderte intestinale Absorption (z.B. wurde eine verminderte Aufnahme von Riboflavin, Folat und Vitamin D bei Ratten mit chronischer Niereninsuffizienz festgestellt); und (e) Verluste von wasserlöslichen Vitaminen im Dialysat aufgrund ihres niedrigen Molekulargewichts (<1 kDa) (7).
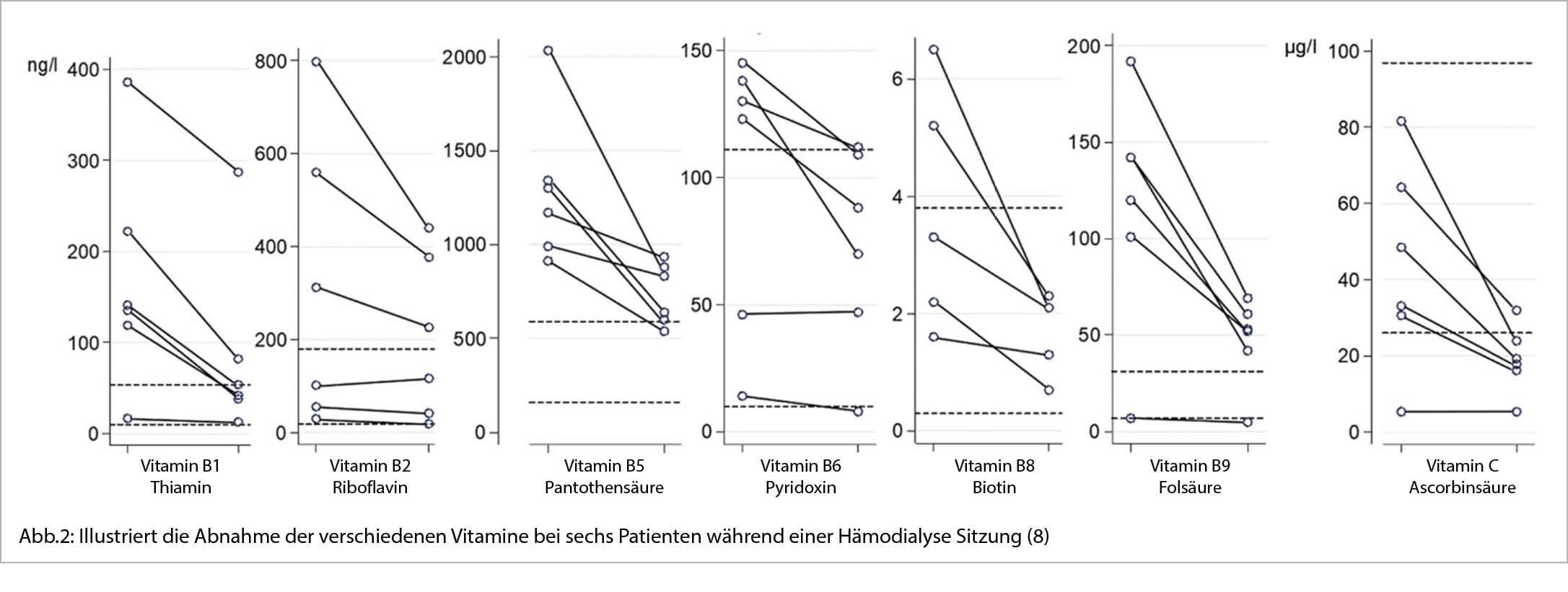
In den letzten Jahrzehnten wurden mehrere technische Fortschritte und Änderungen bei der Hämodialyse in der klinischen Praxis umgesetzt, darunter die Verwendung von Hochflussmembranen (high-flux) und die Einführung der Hämodiafiltration (HDF) (2). Eine kürzlich in Lausanne durchgeführte Studie zeigt, dass die Vitaminverluste bei HDF noch höher sind als bei HD, insbesondere bei Vitamin C (Abb. 2) (8). Die Supplementierung mit wasserlöslichen Vitaminen nach jeder Dialysesitzung ist bei chronischen Hämodialyse-Patienten üblich und gleicht die Verluste aus. Die am häufigsten verschriebenen Präparate sind Dialvit® (mit 50mg Vit B1, 10mg Vit B2, 40mg Vit B6, 3mg Folsäure und 200mg Vit C) oder eine Kombination aus Becozyme forte®, Folsäure und Vitamin C. Zusätzlich erhalten die meisten Patienten regelmässig Vitamin-D-Präparate (Cholecalciferol, Calcitriol).
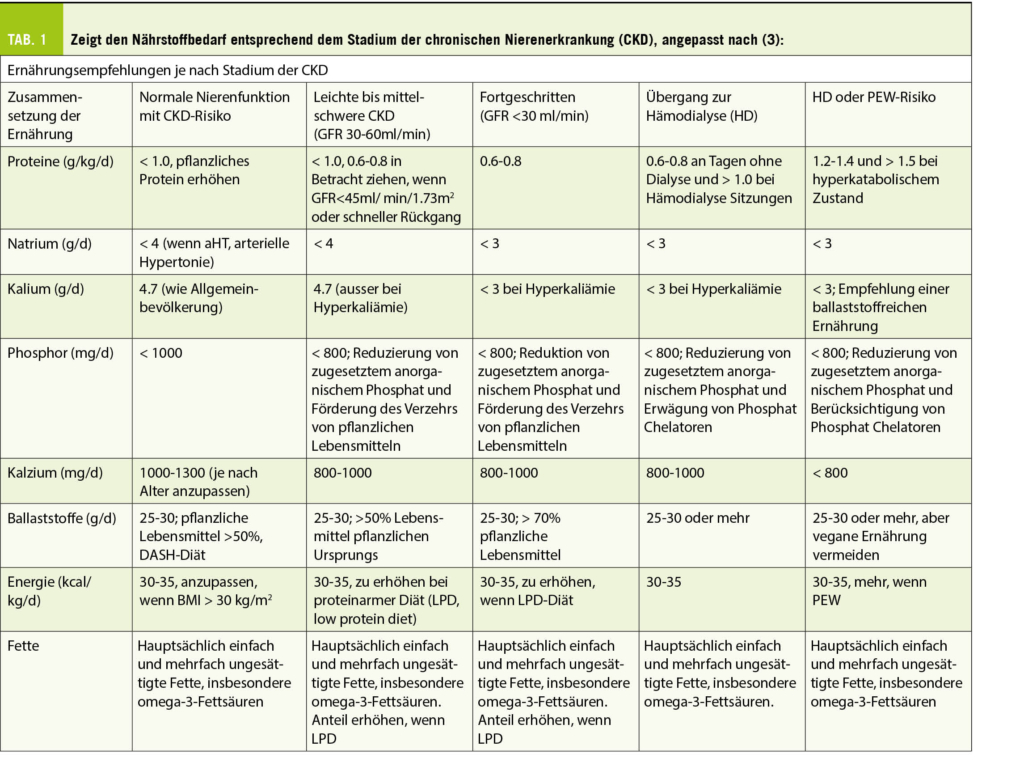
Zusammenfassend lässt sich sagen, dass Hämodialyse-Patienten mehrere Stoffwechselveränderungen, Elektrolytstörungen sowie ein erhöhtes Risiko für Vitaminmangel und Protein-Energie-Unterernährung aufweisen. Eine ausführliche Betrachtung aller Aspekte würde den Rahmen dieses Artikels sprengen, aber die verschiedenen Ernährungsempfehlungen sind in Tabelle 1 zusammengefasst.
Zukunft: Eine Rolle für die Mikrobiota?
Die intestinale Mikrobiota, definiert als die Gesamtheit der Mikroorganismen im Darm, war in den letzten zehn Jahren Gegenstand zahlreicher Forschungsarbeiten. Es wurde deutlich, dass die Mikrobiota viele nützliche Funktionen intestinal und systemisch ausübt, darunter die Synthese von Vitamin K, den Abbau von Oxalat und die Reifung des Immunsystems. Bei Patienten mit chronischer Nierenerkrankung ist ihre Zusammensetzung wahrscheinlich als Reaktion auf Urämie, häufige Antibiotikaverschreibung und Ernährungsumstellung verändert. Die veränderte Mikrobiota führt zu einer vermehrten Produktion von Molekülen wie p-Cresylsulfat und Indoxylsulfat, die entzündungsfördernde und kalzifizierende Effekte haben (9). Die Hämodialyse wiederum wird mit einer vorübergehenden Erhöhung der Durchlässigkeit der Darmbarriere und einem Anstieg der zirkulierenden Zytokinspiegel in Verbindung gebracht. Derzeit laufen mehrere Studien, um zu untersuchen, ob die regelmässige Einnahme von Probiotika (lebende Mikroorganismen, die positive Auswirkungen auf die Gesundheit haben) oder Präbiotika (unverdauliche Nahrungsbestandteile, die eine positive Wirkung auf die Zusammensetzung oder die Aktivität der intestinalen Mikrobiota haben) die Zusammensetzung der Mikrobiota verändern und den Trend von PEW und Muskelabbau verzögern oder umkehren kann.
Schlussfolgerungen:
Nierenversagen führt zu grossen Veränderungen des Metabolismus und des inneren Milieus der Patienten. Dazu gehören nicht nur Elektrolytstörungen, Vitaminmangel und ein erhöhtes Risiko für Unterernährung, sondern auch eine Protein-Energie-Unterernährung. Die Hämodialyse kann den Mangel an Vitaminen und Aminosäuren aufgrund der Verluste, die durch die hochdurchlässigen Filter verursacht werden, noch verstärken. Die Ernährungsberatung und -kontrolle nimmt heute einen wichtigen Platz in der Behandlung von Hämodialyse-Patienten ein. Dies gilt umso mehr, als die Kenntnisse auf diesem Gebiet ständig zunehmen und neue Strategien zur Erreichung eines angemessenen homöostatischen Gleichgewichts bei Dialysepatienten ermöglichen.
Eine enge Zusammenarbeit zwischen Nephrologen, Ernährungsberatern, Allgemeinmedizinern, Endokrinologen und Internisten ist für die optimale Betreuung dieser besonders gefährdeten Patientengruppe von entscheidender Bedeutung. Die Zukunft wird zeigen, ob sich die Manipulation von Mikrobiota als neues Instrument im täglichen Kampf gegen die Protein-Energie-Unterernährung durchsetzen wird.
Übersetzung aus «la gazette médicale» 01-2023
Copyright bei Aerzteverlag medinfo AG
Abteilung für Nephrologie und Hypertonie
Universitätsklinik und Hochschule Lausanne
Rue du Bugnon 17
1011 Lausanne
Abteilung für Nephrologie und Hypertonie
Universitätsklinik und Hochschule Lausanne
Rue du Bugnon 17
1011 Lausanne
menno.pruijm@chuv.ch
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Hyperkaliämie kann durch Verstopfung ausgelöst oder verschlimmert werden; bei anhaltender Hyperkaliämie ist eine Beschränkung auf <3g/d durch die Nahrung erforderlich. Kalium Chelatoren (mit Ausnahme von Patiromer) können wegen des Risikos einer Dickdarmperforation nicht über einen längeren Zeitraum verschrieben werden.
◆ Die Proteinzufuhr spielt eine wichtige Rolle für die Prognose von Patienten mit Nierenerkrankungen und sollte an das Stadium ihrer Erkrankung angepasst werden.
◆ Eine optimale Einstellung der Ernährung bei Hämodialyse-Patienten erfordert eine spezialisierte und multidisziplinäre Betreuung.
1. Hayes CP, Jr., McLeod ME, Robinson RR. An extravenal mechanism for the maintenance of potassium balance in severe chronic renal failure. Trans Assoc Am Physicians. 1967;80:207-16.
2. Cupisti A, Kalantar-Zadeh K. Management of natural and added dietary
phosphorus burden in kidney disease. Semin Nephrol. 2013;33(2):180-90.
3. Kalantar-Zadeh K, Fouque D. Nutritional Management of Chronic Kidney Disease. N Engl J Med. 2017;377(18):1765-76.
4. Bansal S, Pergola PE. Current Management of Hyperkalemia in Patients on
Dialysis. Kidney Int Rep. 2020;5(6):779-89.
5. Ikizler TA, Burrowes JD, Byham-Gray LD, Campbell KL, Carrero JJ, Chan W,
et al. KDOQI Clinical Practice Guideline for Nutrition in CKD: 2020 Update.
Am J Kidney Dis. 2020;76(3 Suppl 1):S1-S107.
6. Kistler BM, Benner D, Burrowes JD, Campbell KL, Fouque D, Garibotto G, et al. Eating During Hemodialysis Treatment: A Consensus Statement From the International Society of Renal Nutrition and Metabolism. J Ren Nutr. 2018;28(1):4-12.
7. Kendrick J, Chonchol M. The role of phosphorus in the development and
progression of vascular calcification. Am J Kidney Dis. 2011;58(5):826-34.
8. Schwotzer N, Kanemitsu M, Kissling S, Darioli R, Benghezal M, Rezzi S, et al. Water-Soluble Vitamin Levels and Supplementation in Chronic Online Hemodiafiltration Patients. Kidney Int Rep. 2020;5(12):2160-7.
9. Ghajarzadeh-Wurzner A, Berney M, Teta D, Genton L, Pruijm M. [Gut microbiota and kidney diseases : dangerous liaisons?]. Rev Med Suisse. 2018;14(595):422-5.
der informierte @rzt
- Vol. 13
- Ausgabe 1
- Januar 2023