- Neue Antikörper in der Migräneprophylaxe – wann und wie einsetzen?
Die CGRP-Antikörper wirken spezifisch auf das Trigeminus-Schmerzsystem und ermöglichen ein selektives Targeting. In den aktuellen Leitlinien der European Headache Federation werden die monoklonalen Antikörper als prophylaktische Medikamente zur Vorbeugung von episodischen und chronischen Migräneanfällen vorgeschlagen und empfohlen.
Migräne ist gemäss Global Burden of Disease Study die zweithäufigste neurologische Erkrankung weltweit. Sie ist für mehr Behinderungen verantwortlich als alle anderen neurologischen Erkrankungen zusammen (1). Trotzdem nehmen in Europa schätzungsweise nur 2-14 % der in Frage kommenden Patienten präventive Medikamente gegen Migräne ein (2).
Migräne manifestiert sich klinisch in Form von wiederkehrenden mittelschweren bis schweren Kopfschmerzattacken, die von Übelkeit, Erbrechen, Phonophobie und/oder Photophobie begleitet werden und 4 bis 72 Stunden andauern (3).
Betreffend der Pathophysiologie wird allgemein angenommen, dass eine periphere und zentrale Aktivierung des trigeminovaskulären Systems zugrunde liegt (4). Umfangreiche Forschungen in den letzten drei Jahrzehnten haben gezeigt, dass das Calcitonin-Gene-related Peptid (CGRP) eine wichtige Rolle bei dieser Aktivierung spielt. CGRP ist ein potenter Vasodilatator sowie ein Neurotransmitter, der auch eine wichtige Rolle bei der Homöostase des gastrointestinalen und kardiovaskulären Systems spielt. Das 37-Aminosäuren-Neuropeptid kommt in zwei Isoformen vor, als α-CGRP vor allem im peripheren und zentralen Nervensystem und als β-CGRP bei der enterischen Übertragung. CGRP vermittelt seine Wirkungen hauptsächlich durch seine Interaktionen mit dem CGRP-Rezeptor (5).
Die klassische prophylaktische Behandlung umfasst eine Vielzahl von Medikamenten, darunter β-Blocker (Metoprolol, Propranolol*), Antiepileptika (z.B. Topiramat*), Ca-Antagonisten (Flunarizin*), Sartane (Candesartan) und andere Antihypertensiva sowie verschiedene Antidepressiva. Erst in den letzten 10-20 Jahren wurden jedoch neue Antimigräne-Medikamente (Gepante und monoklonale Antikörper) entwickelt, die auf das CGRP oder dessen Rezeptor abzielen.
Gepante
Die ersten spezifischen CGRP-Antagonisten, die sogenannten Gepante, zeigten Wirksamkeit bei akuten Migräneattacken. Telcagepant zeigte in der Phase III eine gute Wirksamkeit mit geringen Nebenwirkungen. Bei dauerhafter und täglicher Anwendung zeigte sich jedoch eine Hepatotoxizität, sodass die Entwicklung eingestellt wurde (5). Zwei neu entwickelte Vertreter dieser Klasse, Rimegepant und Ubrogepant zeigten keine relevante Lebertoxizität und wurden von der FDA für die Therapie von Migräneattacken zugelassen. Inzwischen wurde auch das Potential der Substanzklasse als prophylaktische Therapie erkannt. Die FDA hat kürzlich Atogepant speziell für die vorbeugende Behandlung von Migräne zugelassen (6). Derzeit wird auch die prophylaktische Wirkung von Rimegepant in einer klinischen Studie untersucht (7).
CGRP-Antikörper
Aufgrund ihrer langanhaltenden Wirkung (Halbwertszeit ca. 30 Tage) werden CGRP-monoklonale Antikörper zur spezifischen Prophylaxe bei häufiger episodischer Migräne und chronischer Migräne eingesetzt. Die Wirkung zielt darauf ab, die Frequenz und/oder die Intensität von Migräneanfällen sowie die Begleitsymptome der Migräne zu reduzieren. CGRP- Antikörper passieren die Blut-Hirn-Schranke nicht, was auf einen peripheren Ort der therapeutischen Wirkung bei Migräne hinweist (5).
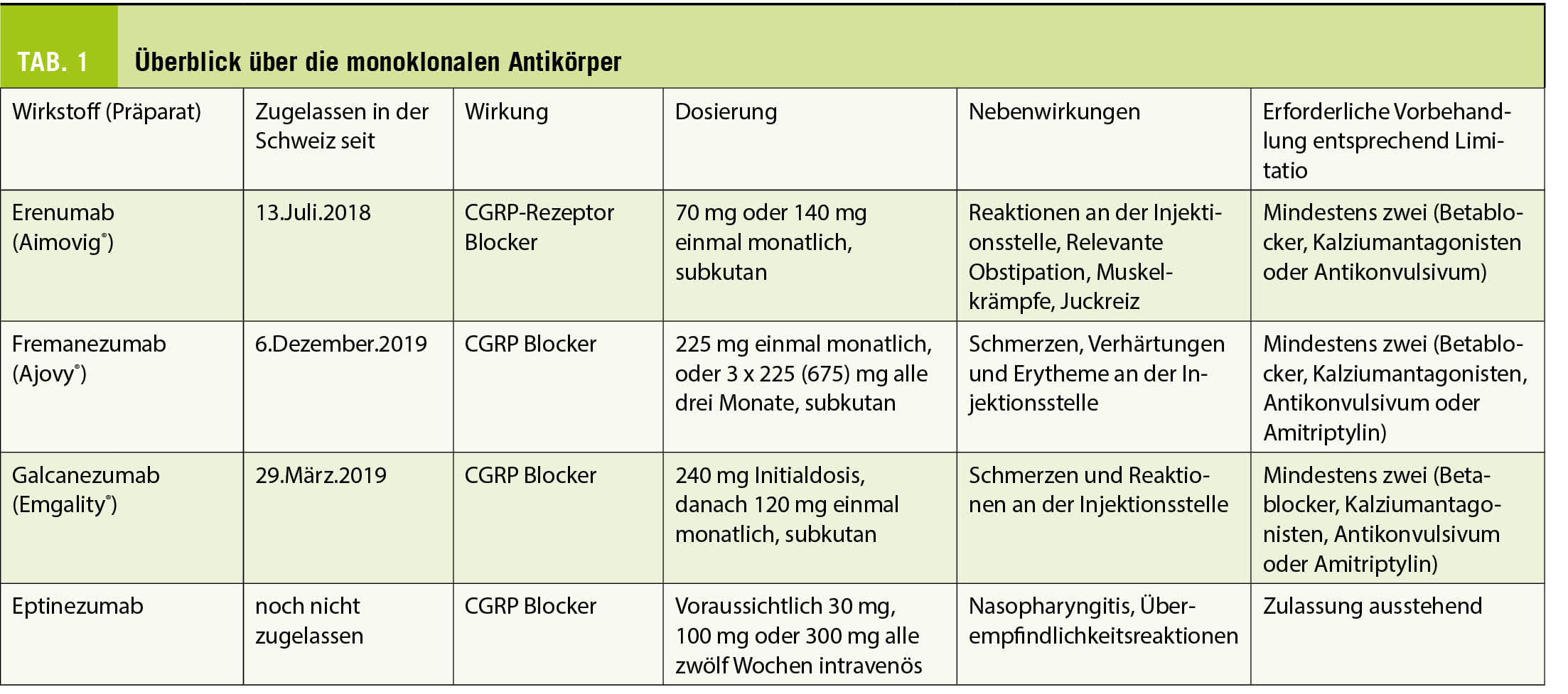
In der neuen Konsenserklärung, die von der European Headache Federation und der European Academy of Neurology unterstützt wird, werden die vier monoklonalen Antikörper Erenumab, Fremanezumab, Galcanezumab und Eptinezumab als präventive Drittlinienbehandlung eingestuft (8). Eine Übersicht gibt Tabelle 1.
Ein Vorteil der monoklonalen CGRP-Antikörper im Vergleich mit den klassischen Prophylaktika ist ihr schneller Wirkungseintritt: innerhalb der ersten Woche bei Erenumab, Galcanezumab und Fremanezumab (9,10,11) und nach einem Tag bei Eptinezumab (12). Die potenzielle Lebertoxizität der Gepante und hepatische Arzneimittelinteraktionen wurden bei den Antikörpern nicht beobachtet (5).
Erenumab und Fremanezumab waren auch bei Patienten mit Migräne wirksam, bei denen 2 bis 4 vorherige präventive Behandlungen erfolglos waren (13,14). Ausserdem sind sie auch bei Patienten mit chronischer Migräne und Medikamentenübergebrauch von Nutzen (11,15,16).
Seit 2018 wurden in der Schweiz drei Antikörper zugelassen, die im Folgenden vorgestellt werden. Für alle drei Präparate gilt eine Limitatio (17), die den Einsatz von mindesten 2 klassischen Migräneprophylaxen vorschreibt (Betablocker, Kalziumantagonisten, Antikonvulsiva bzw. bei Fremanezumab und Galcanezumab auch Amitriptylin). Alle CGRP-Antikörper können nur von Neurologen verschrieben werden.
- Erenumab (Aimovig®) zielt auf den CGRP-Rezeptor selbst ab. In zwei klinischen Phase-III-Studien- ARISE (18) und STRIVE (19) wurde eine Verringerung der Anzahl der monatlichen Kopfschmerztage erreicht. Inzwischen konnte in einer offenen Nachbeobachtungsstudie die langfristige Wirksamkeit (Verringerung der Migränehäufigkeit und Verbesserung der gesundheitsbezogenen Lebensqualität) und Sicherheit von Erenumab bei der Migräneprophylaxe über 5 Jahre gezeigt werden (20). Die häufigsten Nebenwirkungen sind Reaktionen an der Injektionsstelle, Obstipation, Muskelkrämpfe, Juckreiz (21). Die jüngste Zusammenfassung der Produktmerkmale von Erenumab wurde aktualisiert, um die Ärzte zu informieren und die Patienten vor mässiger bis schwerer Obstipation zu warnen, die mit Krankenhausaufenthalten assoziiert waren. Im Rahmen der post-marketing-Überwachung fanden sich Hinweise auf Fälle von erhöhtem Blutdruck als Nebenwirkung (22). Erenumab wird einmal monatlich 70 mg als subkutane Injektion verabreicht. Mit der angepassten Limitatio kann bei ungenügendem Ansprechen auch eine Dosis von 140 mg monatlich verordnet werden (21).
- Fremanezumab (Ajovy®). In der multizentrischen randomisierten doppelblinden Parallelgruppenstudie FOCUS erzielte Fremanezumab eine klinisch bedeutsame Reduktion an Migränetagen auch bei Patienten mit schwierig zu behandelnder episodischer und chronischer Migräne (14). Auch bei hochfrequenter episodischer Migräne ist es wirksam, reduziert Begleitsymptome und den Einsatz der Bedarfsmedikation (23). Die häufigsten Nebenwirkungen in Studien waren Schmerzen, Verhärtungen und Erytheme an der Injektionsstelle. Seit November 2020 steht in der Schweiz neben der Fertigspritze auch ein Fertigpen zur Verfügung. Der Patient kann wählen zwischen einer Monatsdosierung von 225 mg oder einer Quartalsdosierung: 3 x 225 mg (drei Fertigpens). Die Applikation erfolgt subkutan (21). Die Limitatio wurde zum 1. November 2021 angepasst.
- Galcanezumab (Emgality®). In zwei klinischen Phase-III-Studien (EVOLVE-1 und EVOLVE-2) führten monatliche Injektionen von Galcanezumab über 6 Monate zu einer im Placebo-Vergleich signifikanten Reduktion der monatlichen Migräne-Kopfschmerztage. Galcanezumab konnte die Migräne-Kopfschmerztage sowohl in der Gruppe der niedrigfrequenten als auch der hochfrequenten episodischen Migräne signifikant reduzieren (10). Die in Studien untersuchten Dosierungen unterschieden sich nicht in der Wirksamkeit (24,25). In der EVOLVE-2-Studie schienen jedoch unerwünschte Wirkungen im 240-mg-Behandlungsarm etwas häufiger aufzutreten (25). Die häufigsten Nebenwirkungen gemäss Zulassungsstudien sind Schmerzen und Reaktionen an der Injektionsstelle. Galcanezumab wird einmal monatlich 120 mg als subkutane Injektion appliziert. Zu Beginn der Behandlung ist eine einmalige Anfangsdosis von 240 mg (2 Injektionen) zu verabreichen (21).
- Eptinezumab ist in der Schweiz noch nicht zugelassen. Dies ist der einzige intravenös verabreichte humanisierte monoklonale Antikörper, der CGRP direkt blockiert. Es wird alle 3 Monate als intravenöse Infusion verabreicht. Eptinezumab wurde von der FDA zugelassen (Februar 2020), Zulassungsanträge werden aktuell von EMA und Swissmedic geprüft (26). In einer randomisierten, placebo-kontrollierten Studie (PROMISE -1) war die einmalige Gabe von 100 und 300 mg Eptinezumab intravenös über einen Zeitraum von 12 Wochen signifikant wirksamer als Placebo für die Prophylaxe der episodischen Migräne. Eptinezumab wurde gut vertragen (12). Bei Erwachsenen mit Migräne bestand ein günstiges Sicherheits- und Verträglichkeitsprofil. Nasopharyngitis und Überempfindlichkeitsreaktionen sind die häufigsten unerwünschten Ereignisse (27).
Circa 20-30% der Patienten sprechen auf die Therapie nicht an. Neutralisierende Antikörper wurden in geringen Prozentsätzen bei Patienten in den aktiven Gruppen in Studien gefunden, scheinen jedoch keinen Einfluss auf das klinische Ergebnis zu haben, da ihre Titer sehr niedrig waren (28).
Trotz des generell schnellen Wirkeintritts sollten die Antikörper mindestens drei bis sechs Monate lang in maximal verträglicher Dosierung angewendet werden, um die Wirksamkeit richtig beurteilen zu können. Die Quantifizierung des Behandlungserfolgs kann durch Berechnung der prozentualen Verringerung der monatlichen Migränetage oder der monatlichen Kopfschmerztage von mittlerer bis schwerer Intensität (8) erfolgen. In der Schweiz folgt auf eine 12-monatige Behandlung gemäss Limitatio eine Therapiepause. Eine längerdauernde Unterbrechung, wie sie initial vorgesehen war, wird durch aktuelle Studien nicht unterstützt (29).
Schlussfolgerung und Ausblick: Alle monoklonalen CGRP-Antikörper hatten in klinischen Studien gute Wirksamkeit und Verträglichkeit und ein günstiges Sicherheitsprofil. Zum jetzigen Zeitpunkt gibt es keine Hinweise auf eine Überlegenheit eines
einzelnen Antikörpers gegenüber den anderen für Patienten mit episodischer oder chronischer Migräne. Aktuelle Studien weisen auf eine Wirksamkeit dieser Medikamentenklasse bei der Behandlung weiterer Kopfschmerztypen, wie dem Medikamentenübergebrauchs-, Cluster-Kopfschmerz, aber auch posttraumatischen Kopfschmerzen hin.
Copyright bei Aerzteverlag medinfo AG
Neurologie & Neurorehabilitation, ZURZACH Care
Quellenstrasse 34
5330 Bad Zurzach
galina.stoyanova@zurzachcare.ch
Facharzt Neurologie
Neurologie am Untertor
Erachfeldstrasse 2
8180 Bülach
www.neurologie-untertor.ch
andreas.gantenbein@zurzachcare.ch
RehaClinic Bad Zurzach und Universität Zürich
Schweiz
GS-P hat Reisestipendien von Teva erhalten.
◆ Patienten mit einer hohen Frequenz bzw. Intensität von Migräneanfällen oder chronischer Migräne benötigen eine prophylaktische Migränetherapie. Klassische, zur Prophylaxe eingesetzte Medikamente sind nur bei einem eher geringen Teil der Patienten wirksam.
◆ In der Schweiz sind bereits drei monoklonale Antikörper zur Prophylaxe der episodischen (8 und mehr Migränetagen pro Monat) oder chronischen (15 und mehr Migränetagen pro Monat) Migräne bei Erwachsenen verfügbar. Die Kopfschmerztage müssen für die Kostenerstattung über mindestens 3 Monate mit einem Tagebuch dokumentiert werden. Limitationskriterien müssen erfüllt sein.
◆ Der Einsatz von Erenumab, Galcanezumab und Fremanezumab kann vorerst nur nach dokumentiertem Versagen von mindestens zwei anderen Arzneimittel zur Migräneprophylaxe oder bei deren Unverträglichkeit erfolgen.
◆ Die Verordnung und Verlaufskontrolle der monoklonalen Antikörper müssen gemäss Limitatio durch einen Facharzt für Neurologie erfolgen.
◆ Bei der Auswahl der Antikörperpräparate können Patientenpräferenzen hinsichtlich Nebenwirkungen und Applikationshäufigkeit berücksichtigt werden.
1. GBD 2016 Neurology Collaborators. Global, regional, and national burden of neurological disorders, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2019; 18:459–480.
2. Katsarava Z, Mania M, Lampl C, et al. Poor medical care for people with migraine in Europe – evidence from the Eurolight study. J Headache Pain. 2018 Feb 1;19(1):10.
3. Headache Classification Committee of the International Headache Society. The international classification of headache disorders, 3rd edition. Cephalalgia. 2018;38:1–211.
4. Ashina M, Hansen JM, Do TP, et al. Migraine and the trigeminovascular system-40 years and counting. Lancet Neurol. 2019 Aug;18(8):795-804.
5. Edvinsson L, Warfvinge K. Recognizing the role of CGRP and CGRP receptors in migraine and its treatment. Cephalalgia. 2019 Mar;39(3):366-373.
6. https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2021/215206Orig1s000ltr.pdf
7. NCT0372368. Efficacy and safety trial of rimegepant for migraine prevention in adults. Available from: https:// clinicaltrials.gov/ct2/show/NCT03732638
8. Eigenbrodt AK, Ashina H, Khan S, et al. Diagnosis and management of migraine in ten steps. Nat Rev Neurol. 2021 Aug;17(8):501-514.
9. Schwedt T, Reuter U, Tepper S, et al. Early onset of efficacy with erenumab in patients with episodic and chronic migraine. J Headache Pain. 2018 Oct 1;19(1):92.
10. Silberstein SD, Stauffer VL, Day KA, et al. Galcanezumab in episodic migraine: subgroup analyses of efficacy by high versus low frequency of migraine headaches in phase 3 studies (EVOLVE-1 & EVOLVE-2). J Headache Pain. 2019 Jun 28;20(1):75.
11. Silberstein S, Ashina S, Katsarava Z, et al. The impact of fremanezumab on medication overuse in patients with chronic migraine. Neurology. 2019;92 (15 Suppl):P1.10-026.
12. Ashina M, Saper J, Cady R, et al. Eptinezumab in episodic migraine: A randomized, double-blind, placebo-controlled study (PROMISE-1). Cephalalgia. 2020 Mar;40(3):241-254.
13. Goadsby PJ, Reuter U, Lanteri-Minet M, et al. Long-Term Efficacy and Safety of Erenumab: Results From 64 Weeks of the LIBERTY Study. Neurology. 2021 Apr 28;96(22):e2724–35.
14. Ferrari MD, Diener HC, Ning X, et al. Fremanezumab versus placebo for migraine prevention in patients with documented failure to up to four migraine preventive medication classes (FOCUS): a randomised, double-blind, placebo-controlled, phase 3b trial. Lancet. 2019 Sep 21;394(10203):1030-1040.
15. Tepper SJ, Diener HC, Ashina M, et al. Erenumab in chronic migraine with medication overuse: Subgroup analysis of a randomized trial. Neurology. 2019 May 14;92(20):e2309-e2320.
16. Dodick DW, Doty EG, Aurora SK, et al. Medication overuse in a subgroup analysis of phase 3 placebo-controlled studies of galcanezumab in the prevention of episodic and chronic migraine. Cephalalgia. 2021 Mar;41(3):340-352.
17. www.spezialitaetenliste.ch
18. Dodick DW, Ashina M, Brandes JL, et al. ARISE: A Phase 3 randomized trial of erenumab for episodic migraine. Cephalalgia. 2018 May;38(6):1026-1037.
19. Goadsby PJ, Reuter U, Hallström Y, et al. Controlled Trial of Erenumab for Episodic Migraine. N Engl J Med. 2017 Nov 30;377(22):2123-2132.
20. Ashina M, Goadsby PJ, Reuter U, et al. Long-term efficacy and safety of erenumab in migraine prevention: Results from a 5-year, open-label treatment phase of a randomized clinical trial. Eur J Neurol. 2021 May;28(5):1716-1725.
21. www.compendium.ch
22. Saely S, Croteau D, Jawidzik L, et al. Hypertension: A new safety risk for patients treated with erenumab. Headache. 2021 Jan;61(1):202-208.
23. Brandes JL, Kudrow D, Yeung PP, et al. Effects of fremanezumab on the use of acute headache medication and associated symptoms of migraine in patients with episodic migraine. Cephalalgia. 2020 Apr;40(5):470-477.
24. Stauffer VL, Dodick DW, Zhang Q, et al. Evaluation of Galcanezumab for the Prevention of Episodic Migraine: The EVOLVE-1 Randomized Clinical Trial. JAMA Neurol. 2018 Sep 1;75(9):1080-1088.
25. Skljarevski V, Matharu M, Millen BA, et al. Efficacy and safety of galcanezumab for the prevention of episodic migraine: Results of the EVOLVE-2 Phase 3 randomized controlled clinical trial. Cephalalgia. 2018 Jul;38(8):1442-1454.
26. https://www.swissmedic.ch/dam/swissmedic/de/dokumente/stab/journal/swissmedic-journal-052020.pdf.download.pdf/Swissmedic%20Journal%2005-2020.pdf
27. Smith TR, Spierings ELH, Cady R, et al. Safety and tolerability of eptinezumab in patients with migraine: a pooled analysis of 5 clinical trials. J Headache Pain. 2021 Mar 30;22(1):16.
28. Martinez JM, Hindiyeh N, Anglin G, et al. Assessment of immunogenicity from galcanezumab phase 3 trials in patients with episodic or chronic migraine. Cephalalgia. 2020 Aug;40(9):978-989.
29. Gantenbein AR, Agosti R, Gobbi C, Fet al. Impact on monthly migraine days of discontinuing anti-CGRP antibodies after one year of treatment – a real-life cohort study. Cephalalgia. 2021 May 17:3331024211014616.
der informierte @rzt
- Vol. 11
- Ausgabe 11
- November 2021