- Neue Schweizerische Empfehlungen zur Therapie des Typ 2 Diabetes mellitus 2023
Viele Ärzte werden sich fragen, wieso gibt es schon wieder neue Empfehlungen? Die Antwort ist einfach: Seit den letzten Empfehlungen von 2020 gab es viele kardiovaskuläre Endpunktstudien, welche eingeordnet werden müssen. Daneben gibt es einige neue Medikamente, welche 2023 eingeführt wurden oder werden, die noch nicht berücksichtigt wurden. Daneben gibt es zwar die europäischen und amerikanischen Leitlinien zu Diabetes, die aber unserer Meinung nach für den Allgemeininternisten und Hausarzt zu kompliziert sind. Das Ziel der Schweizerischen Arbeitsgruppe war es, einfache Schritt für Schritt Empfehlungen zu erarbeiten, welche von allen Ärzten gut implementiert werden können (1).
Many physicians will ask themselves, why are there already new recommendations? The answer is simple: since the last recommendations of 2020, there have been many cardiovascular endpoint studies that need to be classified. In addition, there are some new drugs that have been or will be introduced in 2023 that have not yet been considered. In addition, there are the European and American guidelines on diabetes, but in our opinion they are too complicated for the general internist and GP. The goal of the Swiss working group was to develop simple step-by-step recommendations that can be easily implemented by all physicians (1).
Key words: Diabetes, Diabetes mellitus Typ 2, Endokrinologie
Therapieempfehlungen in der Schweiz
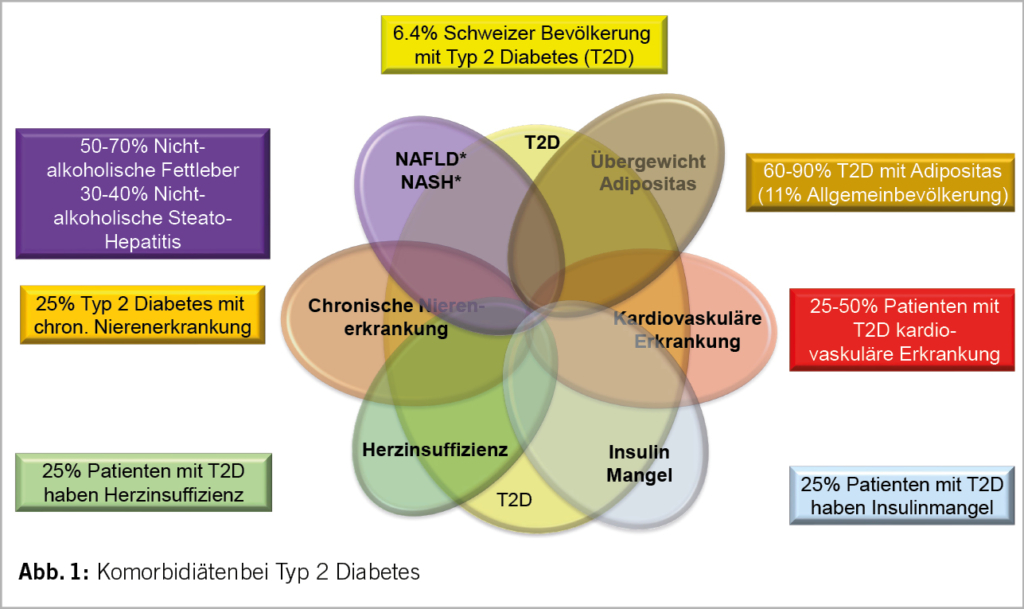
In der Abbildung 1 werden die häufigsten Komorbiditäten bei Typ 2 Diabetes mellitus in der Schweiz mit den Prävalenzen zusammengefasst. Bei allen Komorbiditäten gab es in den letzten Jahren wesentliche Fortschritte und neue Erkenntnisse. Die einzige und bei Diabetes sehr häufige Komorbidität, bei der es noch keine allgemeingültigen Therapieempfehlungen gibt und wo noch ein grosse Forschungsarbeit benötigt wird, ist die nicht-alkoholische Fettleber (NAFLD), die heute auch als metabolisch assoziierte Fettleber (MAFLD) bezeichnet wird, da diese Form sehr häufig mit metabolischem Syndrom, Adipositas und Diabetes vergesellschaftet ist (50-70%). Der Begriff nicht-alkoholisch wurde ersetzt, da ein leichter bis mässiger Alkoholgenuss bei dieser Bevölkerungsgruppe doch recht häufig ist. Was man bereits weiss, ist, dass v.a. GLP-1 RA und GLP-1/GIP RA die Leberverfettung und auch die Progression zur Fibrose reduzieren können und auch SGLT-2 Hemmer einen positiven Effekt haben, wobei wahrscheinlich der Gewichtsverlust den wichtigsten Faktor darstellt.
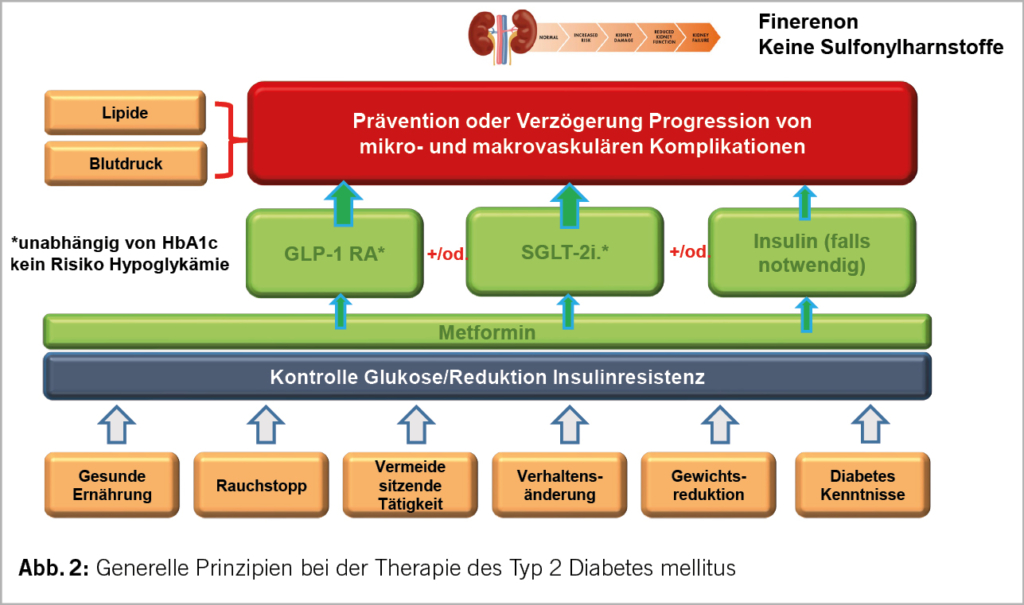
Abbildung 2 fasst die allgemeinen Therapieprinzipien zusammen, wobei hier zu beachten ist, dass eben auch Lipide und Blutdruck mitberücksichtigt werden sollen und dass der Einsatz von GLP-1 RA und SGLT-2 Hemmern unabhängig vom HbA1c erfolgen sollte.
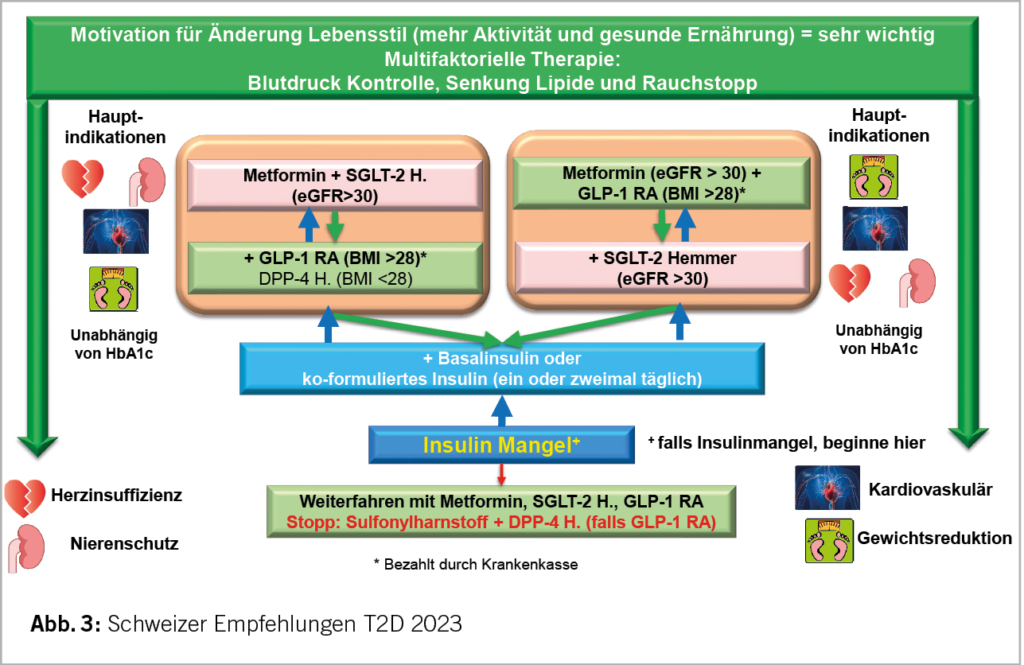
Abbildung 3 stellt eine Schritt für Schritt Anleitung dar, wie der Typ 2 Diabetes behandelt werden sollte. Der erste Schritt definiert die Hauptindikation für den Einsatz der modernen Antidiabetika. Liegt der Schwerpunkt auf der Behandlung der chronischen Nierenerkrankung oder aller Formen der Herzinsuffizienz, soll eine initiale Kombinationstherapie mit Metformin und SGLT-2 Hemmern in Betracht gezogen werden. Ist die Hauptindikation der Gewichtsverlust und der kardiovaskuläre Schutz (insbesondere auch die Prävention der Apoplexie) soll die Kombination Metformin und GLP-1 RA favorisiert werden. GLP-1 RA funktionieren auch bei einem BMI <28. Das Bundesamt für Gesundheit hat diese Einschränkung eingeführt, um die Häufigkeit der Verschreibung zu reduzieren. Die Frage taucht manchmal auf, warum Metformin immer noch eingesetzt wird? Metformin ist das einzige Medikament, welches die hepatische Glukoneogenese deutlich hemmt und es wurde bei allen kardiovaskulären Endpunktstudien als Erstlinientherapie eingesetzt. Darüber hinaus zeigte eine grosse Metaanalyse aus über 40 Studien und über 1 Million Patienten mit Diabetes mellitus und einer koronaren Herzkrankheit eine signifikante Senkung von kardiovaskulärem Tod und der Gesamtmortalität von 19, resp. 33% und auch die kardiovaskulären Ereignisse wurden signifikant um 17% gesenkt (2).
Der zweite Schritt ist dann die Kombination von SGLT-2 Hemmern mit GLP-1 RA unabhängig vom HbA1c. Diese Tripelkombination stellt die ideale Therapie des Typ 2 Diabetes mellitus dar, indem sie alle Vorteile der beiden Substanzgruppen vereint: Reduktion von 3-Punkte MACE, nicht-tödlicher Apoplexie, kardiovaskulären Tod, Herzinsuffizienz, Nephroprotektion und Senkung der Gesamtmortalität. Ein neues Medikament, welches im Herbst 2023 auf den Schweizer Markt kommen wird, ist der duale GLP-1/GIP RA Tirzepatid (Mounjaro®), welcher für den Typ 2 Diabetes zugelassen ist und in einer Dosis von 5-15 mg angewandt wird. Die Wirkungen auf HbA1c und Gewicht sind mit Semaglutid (1.0 resp. 2.4 mg (Wegovy® zugelassen für Adipositas)) vergleichbar. Es gibt aber erst einen direkten Vergleich mit 1 mg Semaglutid vs. 5-15 mg Tirzepatid, wobei Tirzepatid bezüglich Gewichtsreduktion und HbA1c-Senkung überlegen war.
DPP-4 Hemmer werden eigentlich nur eingesetzt, wenn der BMI <28 ist oder GLP-1 RA aufgrund von gastrointestinalen Nebenwirkungen nicht eingesetzt werden können.
Das Hauptproblem bei der Tripelkombination ist die Vergütung der Kosten durch die Krankenkassen. Wenn mit dem teureren Medikament, dem GLP-1 RA, begonnen wird, bezahlt die Krankenkasse praktisch immer den SGLT-2 Hemmer, der gleich teuer wie ein DPP-4 Hemmer ist. Falls man mit der Kombination von SGLT-2 Hemmer und Metformin beginnt, braucht es aktuell beim Einsatz eines GLP-1 RA meist eine Kostengutsprache. Dies kann man umgehen, indem man die Indikation für den SGLT-2 Hemmer entweder für die chronische Nierenerkrankung oder für jede Form der Herzinsuffizienz stellt. Die Herzinsuffizienz mit erhaltener Auswurffraktion (>40%) ist die vorherrschende Form beim Typ 2 Diabetes (3/4 aller Fälle) und SGLT-2 Hemmer sind die einzige erfolgreiche Therapie für die HFpEF. Die Indikation für den GLP-1 RA wäre demnach die Diabetestherapie. Bestrebungen aller beteiligten Pharmafirmen laufen, um diese Limitationen durch das BAG zu beseitigen, weil die Tripelkombination die national und international bevorzugte Therapieoption darstellt.
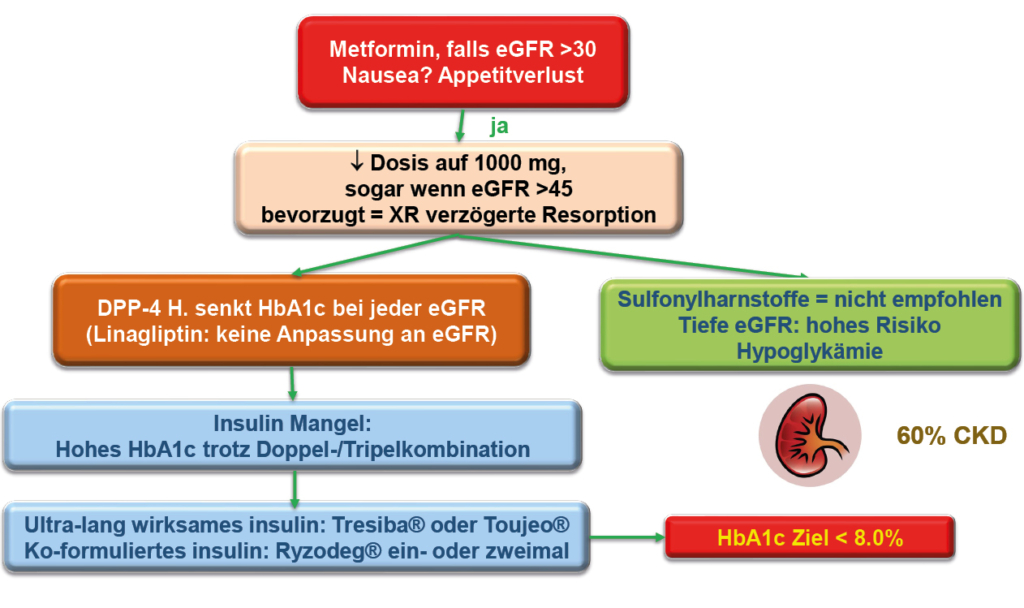
Schritt 3 folgt, wenn das HbA1c trotz Tripeltherapie nicht im Zielbereich liegt, dann wird Insulin eingesetzt (Insulinmangel bei 25% aller Patienten mit Typ 2 Diabetes mellitus). Die einfachste Form ist die einmal tägliche Verabreichung eines ultralang wirksamen Basalinsulins wie Glargin 300 oder Insulin Degludec (Toujeo® oder Tresiba®). Man beginnt meist mit 10 E pro Tag oder 0.2 E/kg und steigert einmal pro Woche um 2 Einheiten. Die Alternative wäre, v.a. wenn der Blutzucker nach einer oder zwei Hauptmahlzeiten stark ansteigt, ein ko-formuliertes Insulin wie Ryzodeg® zu geben, welches aus 30% kurzwirksamem NovoRapid® und 70% Tresiba® besteht. Dieses Insulin kann ein- oder zweimal pro Tag zu den Mahlzeiten mit dem höchsten Kohlenhydratanteil gegeben werden oder zu der Mahlzeit, bei der der postprandiale Blutzucker am meisten ansteigt. Es wurde im Direktvergleich mit einem Basis-Bolus System bei Typ 2 Diabetes gezeigt, dass das gleiche HbA1c erreicht werden kann, aber mit weniger Hypoglykämien mit dem zweimal täglich applizierten Insulin Ryzodeg®.
HbA1c Ziel bei Typ 2 Diabetes mellitus
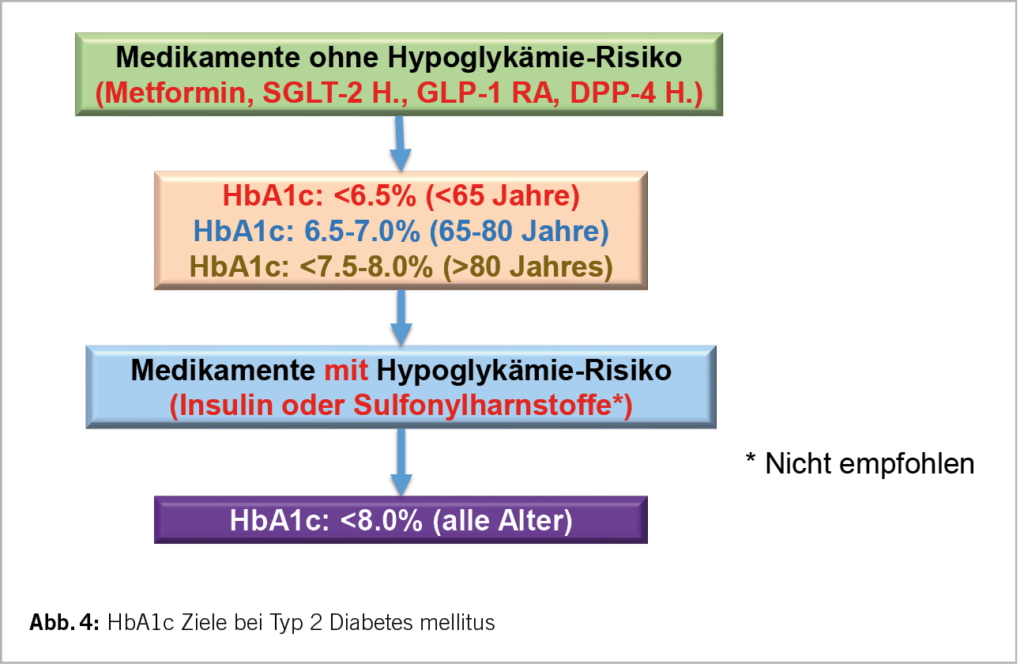
Da mit einer Doppel- oder Tripelkombination (Metformin, SGLT-2 Hemmer, GLP-1 RA oder DPP-4 Hemmer) keine Hypoglykämiegefahr besteht, ist das Ziel HbA1c <6.5% oder so nahe am Normalen wie möglich bei allen Personen unter 65 Jahren. Bei einem Alter >65 oder 80 Jahren kann man etwas nachsichtiger sein. Die Abbildung 4 verdeutlicht diese Empfehlungen. Nur bei einer Therapie mit Insulin oder Sulfonylharnstoffen, wobei letztere nicht mehr empfohlen werden, möchte man kein zu tiefes HbA1c erreichen, wegen der Hypoglykämiegefahr. Das HbA1c sollte aber bei allen Altersgruppen auch bei einer Insulintherapie immer <8.0% sein.
Spezielle Situationen: Chronische Nierenerkrankung, Herzinsuffizienz und alte, gebrechliche Patienten
Etwa 25% aller Schweizer Patienten mit Typ 2 Diabetes haben eine chronische Nierenerkrankung. Leider werden viele nicht diagnostiziert, weil die Bestimmung der Albuminurie in weniger als 30% der Patienten vorgenommen wird. Bei der chronischen Nierenerkrankung sind SGLT-2 Hemmer die bevorzugte Medikamentengruppe gefolgt von GLP-1 RA, welche bis zu einer eGFR von 15 ml/min gegeben werden können. Ein neues Medikament, welches seit dem 1. Juni 2023 auf dem Markt ist, ist ein neuer nichtsteroidaler Mineralokortikoidrezeptor Antagonist, Fineronon (Kerendia®). Dieses neue Medikament ist bei einer CKD mit einer eGFR von 25-59 ml und einer Mikroalbuminurie und einer eGFR von 25-75 ml/min und einer Makroalbuminurie indiziert und kann zusammen mit SGLT-2 Hemmern eingesetzt werden.
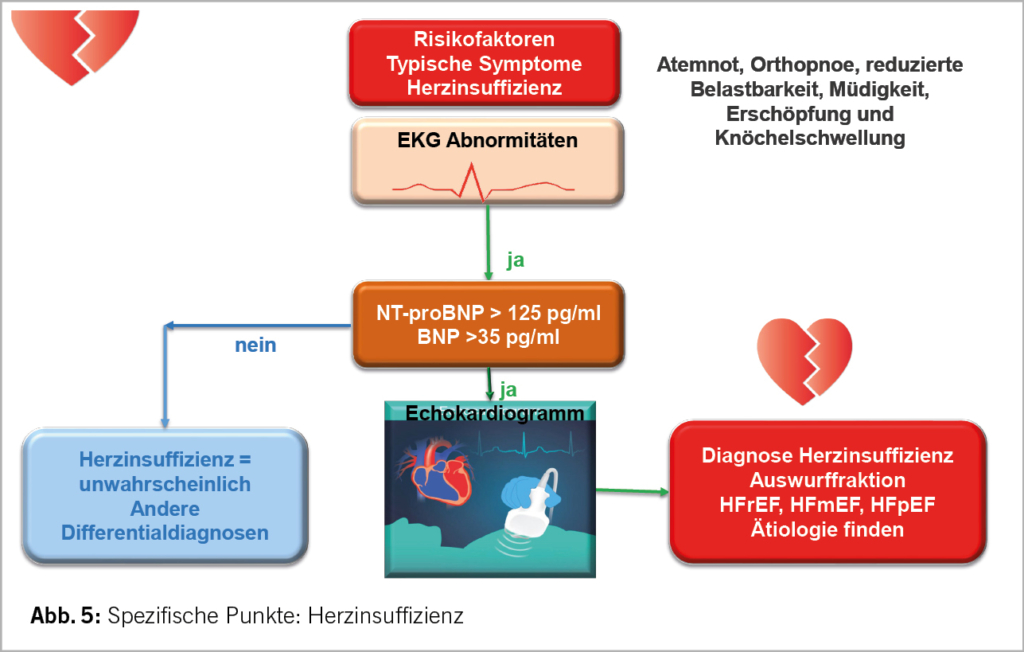
Für die frühzeitige Erkennung der Herzinsuffizienz wird empfohlen bei allen Patienten die typischen Symptome zu erfragen (Atemnot, Orthopnoe, reduzierte Belastbarkeit, Müdigkeit, Knöchelödeme). Falls eines oder mehrere Symptome vorhanden sind und/oder EKG Abnormitäten vorliegen, sollen NT-proBNP oder BNP bestimmt werden. Sind die Werte erhöht, sollen die Patienten einem Kardiologen zur Echokardiografie zugewiesen werden. Mit dieser Untersuchung kann die Herzinsuffizienz diagnostiziert und gemäss systolischer Auswurffraktion in HFrEF, HFmEF oder HFpEF eingeteilt werden. Abbildung 5 veranschaulicht den Ablauf dieser Abklärung. Neben der etablierten Therapie für HFrEF (ACE-Hemmer/Sartane, Diuretika, Betablocker, Aldosteron-Antagonisten) werden für die erhaltene und reduzierte Auswurffraktion SGLT-2 Hemmer empfohlen. SGLT-2 Hemmer sind die einzige Medikamentengruppe mit einer signifikanten Reduktion der Hospitalisation wegen Herzinsuffizienz bei der erhaltenen Auswurffraktion (HFpEF).
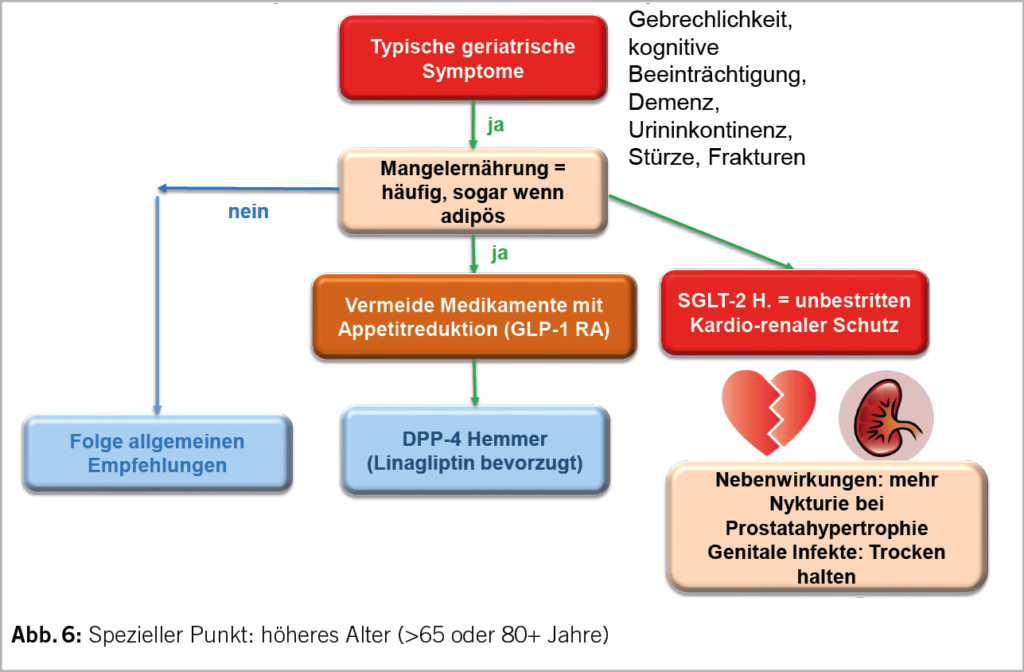
Patienten >65 Jahre leiden oft an typischen geriatrischen Krankheiten und haben häufig, auch wenn sie adipös sind, eine Mangelernährung (Abbildungen 6 und 7). Bei diesen Patienten möchte man die appetithemmende Wirkung von GLP-1 RA vermeiden und man bevorzugt DPP-4 Hemmer. Bevorzugt wird Linagliptin (Trajenta®), da die Dosis nicht an die eGFR angepasst werden muss. Der renokardioprotektive Effekt von SGLT-2 Hemmer ist auch bei dieser Gruppe unbestritten.
Copyright bei Aerzteverlag medinfo AG
UniversitätsSpital Zürich
Rämistrasse 100
8091 Zurich
Roger.Lehmann@usz.ch
Der Autor deklariert Teilnahme an Advisory Boards und Referentenhonorare von Novo Nordisk, Sanofi, MSD, Boehringer Ingelheim, Servier und Astra Zeneca.
- In einer Kurzversion wurden die modernsten und einfachsten
Empfehlungen zur Behandlung des Typ 2 Diabetes mellitus vorgestellt. - Im Unterschied zu früheren Empfehlungen beruhen die aktuellen Empfehlungen alle auf zahlreichen kardiovaskuläre Endpunkstudien, welche diese Schritte dokumentieren.
- Der holistsche Therapieansatz beruht aber immer auf der individuellen Einschätzung des Patienten und der Akzeptanz der Therapie durch den Patienten. Der vorgeschlagene Therapiealgorithmus soll eine einfach zu befolgende Hilfe darstellen.
1. Giacomo Gastaldi, Barbara Lucchini , Sebastien Thalmann, Stephanie Alder,
Markus Laimer, Michael Brändle, Peter Wiesli. Roger Lehmann; Working group of the SGED/SSED, Swiss recommendations of the Society for Endocrinology and Diabetes (SGED/SSED) for the treatment of type 2 diabetes mellitus (2023), Swiss Med Wkly 2023;153;40060 doi.org/10.57187/smw.2023.40060
2. Han Y, Xie H, Liu Y, Gao P, Yang X, Shen Z. Effect of metformin on all-cause and cardiovascular mortality in patients with coronary artery diseases: a systematic review and an updated meta-analysis. Cardiovasc Diabetol. 2019 Jul 30;18(1):96. doi: 10.1186/s12933-019-0900-7. PMID: 31362743; PMCID: PMC6668189.
der informierte @rzt
- Vol. 13
- Ausgabe 8
- August 2023