- Non-CF-Bronchiektasen – Ursachen, Abklärung, Therapie
Eine Bronchiektasen-Erkrankung liegt vor bei chronisch produktivem Husten, Atemnot oder einer Vorgeschichte mit Exacerbationen im Zusammenhang mit dem Nachweis von Bronchiektasen im CT-Thorax. Die Prävalenz von Bronchiektasen nimmt seit einigen Jahren zu, so dass diese Patienten nicht mehr nur von Pneumologen betreut werden. Kenntnisse über zugrundeliegende Erkrankungen, die therapeutischen Möglichkeiten und potentielle Komplikationen gehören unterdessen in das Repertoire von Grundversorger/-innen. Es werden CF-Bronchiektasen (Bronchiektasen bei Patienten mit zystischer Fibrose) und Non-CF-Bronchiektasen unterschieden. Weiter gibt es Traktionsbronchiektasen, welche im Zusammenhang mit fibrotischen Lungenparenchymveränderungen auftreten, klinisch aber ohne Relevanz sind. In diesem Artikel wird nur auf die Non-CF-Bronchiektasen eingegangen.
A diagnosis of bronchiectasis is considered in patients with chronic productive cough, shortness of breath, and a history of exacerbations along with the detection of bronchiectasis on a chest CT scan. The prevalence of bronchiectasis has been increasing, meaning that these patients are no longer only treated by pulmonologists. Knowledge about the underlying conditions, therapeutic options, and potential complications has become essential for general practitioners too. There are CF (cystic fibrosis) bronchiectasis and non-CF bronchiectasis. Additionally, there are traction bronchiectasis, which occur in the context of fibrotic changes in the lung parenchyma but are clinically irrelevant. This article focuses only on non-CF bronchiectasis.
Key words: Non-CF Bronchiectasis, Etiology, Mucociliary Clearance, Exacerbations, Secretion Management, Therapeutic Approaches
Einleitung
Non-CF-Bronchiektasen können als alleinstehendes Krankheitsbild oder im Rahmen einer Grunderkrankung auftreten. Die Entstehung wird als Folge einer Wechselwirkung zwischen gestörter mukoziliärer Clearance, Infekt, Entzündung und destruierter Bronchialwand gesehen. Es entsteht ein Teufelskreis, welcher zur Erkrankung führt (1). Die Prävalenz in Europa liegt je nach untersuchter Population zwischen 67 und 500 Patienten pro 100 000 Einwohner.
Ursachen der Bronchiektasen
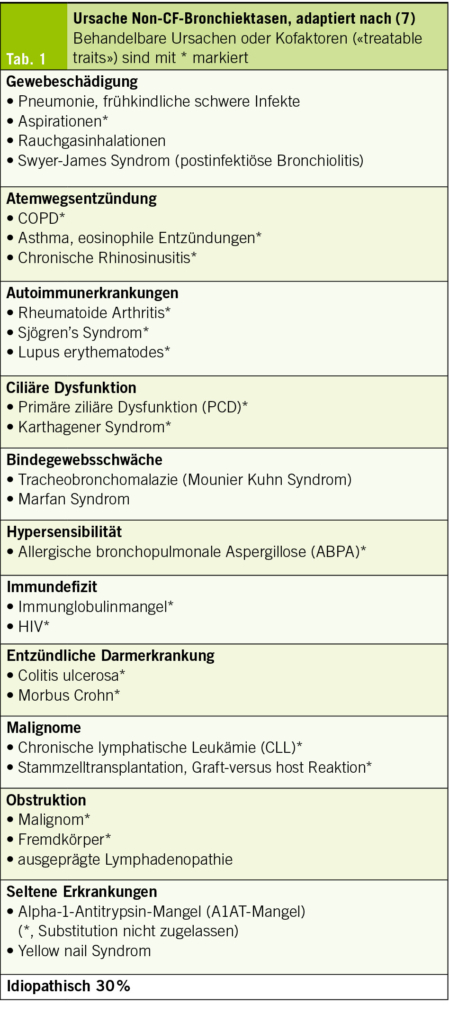
Am häufigsten sind postinfektiöse Bronchiektasen. Bronchiektasen können auch im Zusammenhang mit COPD oder Asthma auftreten und den Krankheitsverlauf komplizieren. COPD-Patienten mit Bronchiektasen haben beispielsweise häufiger Exacerbationen. Eine Immunsuppression oder aber eine überschiessende Immunreaktion (z. B. Autoimmunerkrankungen oder allergische bronchopulmonale Aspergillose (ABPA)) können ebenfalls zu Bronchiektasen führen. Bei rund einem Drittel der Bronchiektasien bleibt die Ursache auch nach einer systematischen Abklärung offen. Sie fallen in die Gruppe der idiopathischen (oder kryptogenen) Bronchiektasen. Eine umfassende Zusammenstellung der Ursachen entnehmen Sie der Tab. 1.
Bronchiektasen-Erkrankung
Die typischen Symptome von Bronchiektasen sind ein produktiver Husten (chronisch oder nur intermittierend) und Dyspnoe. Oft haben Patienten eine Vorgeschichte mit Exacerbationen oder Haemoptoe. Vor allem im Zusammenhang mit Exacerbationen bestehen eine Malaise und ein Gewichtsverlust, selten Thoraxschmerzen. Das Ausmass der Beschwerden variiert stark, oft ist die Lebensqualität aber in relevantem Masse eingeschränkt.
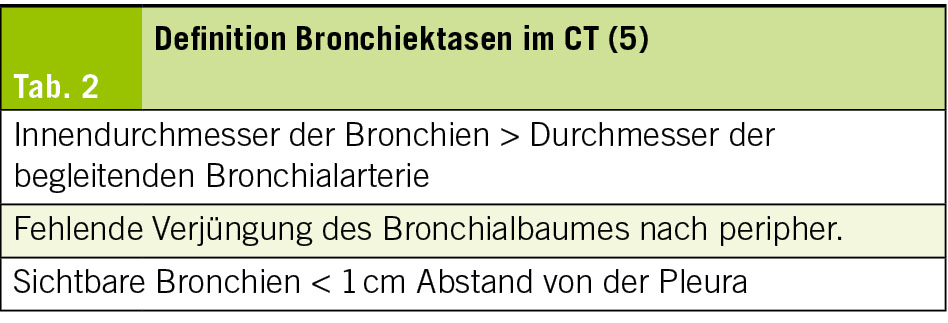
Die radiologische Definition von Bronchiektasen im CT-Thorax ist in der Tab. 2 aufgeführt. Nur wenn Bronchiektasen von typischen Symptomen begleitet werden, liegt eine Bronchiektasen-Erkrankung vor. Ein Zufallsbefund im CT-Thorax ohne Beschwerden und ohne Vorgeschichte mit Exacerbationen hat klinisch keine Relevanz und muss in der Regel nicht abgeklärt werden.
Abklärungen
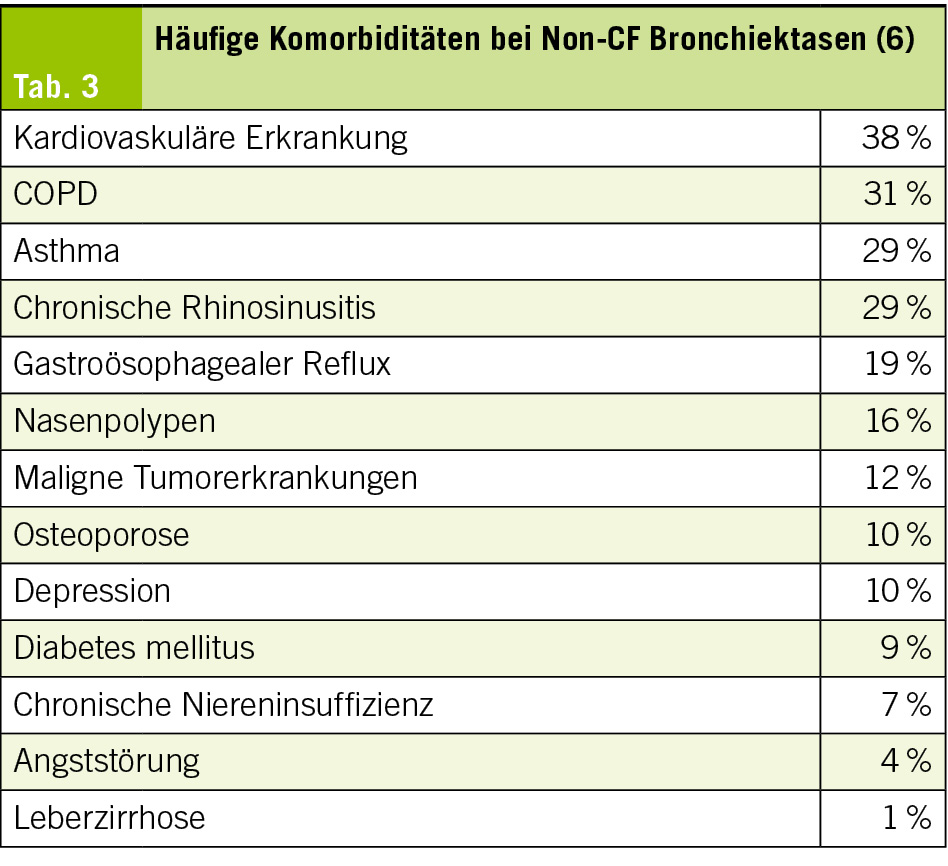
Die Abklärung von Bronchiektasien hat zum Ziel, eine behandelbare Ursache («treatable traits») zu finden und /oder häufige Komorbiditäten zu identifizieren. Siehe dazu Tab. 3. Die Komorbiditäten müssen nicht zwingend die Ursache der Bronchiektasen darstellen, sie verstärken aber die Symptome und komplizieren den Verlauf.
Die Basisdiagnostik besteht aus Laboruntersuchungen, Sputumanalyse und einer Lungenfunktion. Je nach der klinischen Einschätzung folgen weitere Spezialuntersuchungen. Vergleiche hierzu Abb. 1. Es sei auch auf ausführliche Guidelines hingewiesen, z. B. die soeben aktualisierte Leitlinie der DGP (2).
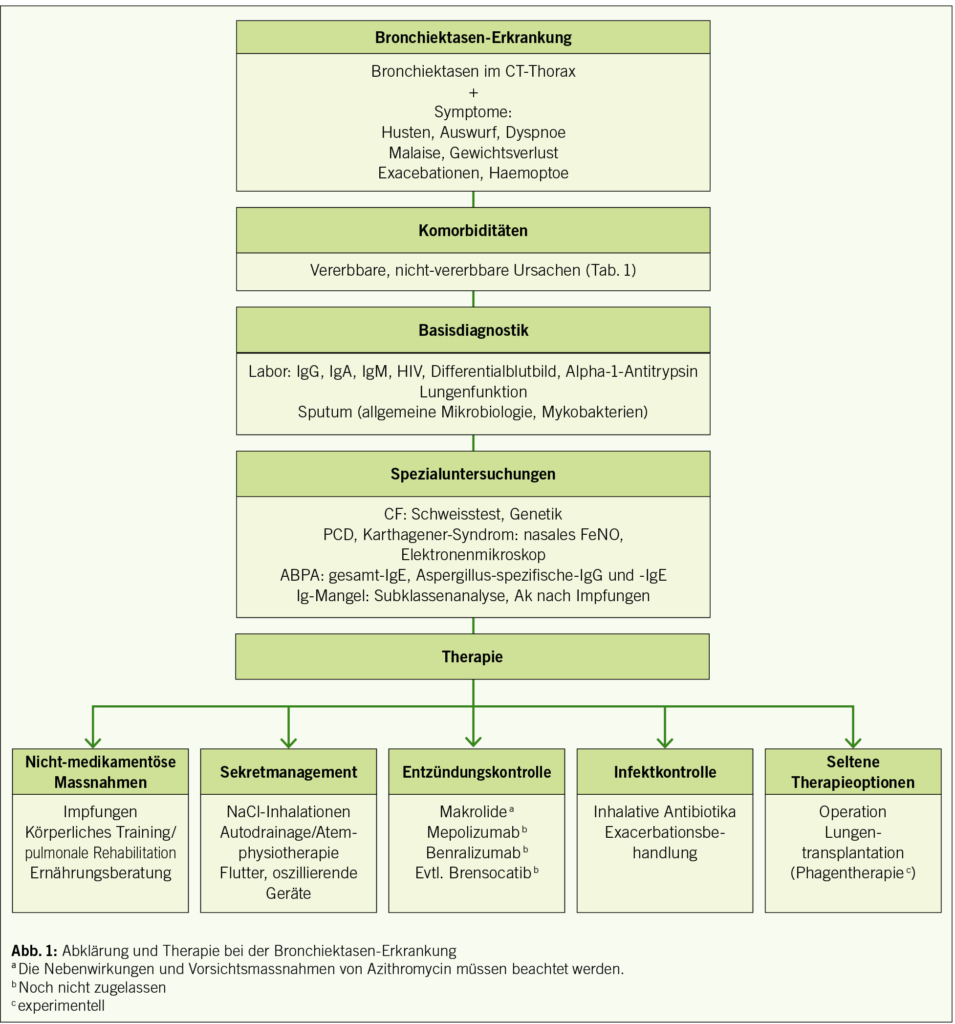
Therapie
Die Ziele der Therapie sind die Symptomkontrolle, der Erhalt der Lungenfunktion und das Verhindern von Komplikationen. Bisher gibt es keine zugelassene spezifische Therapie für Non-CF-Bronchiektasen. Alle hier angegebenen Therapien entsprechen einem Off-Label-Use.
Am Anfang steht die Behandlung der Grunderkrankung, falls eine solche gefunden werden konnte. Die Eckpfeiler der Behandlung der Bronchiektasen bestehen aus:
1. Allgemeinmassnahmen wie Impfungen, Rauchstopp, körperliche Aktivität und pulmonale Rehabilitation,
2. dem Sekretmanagement und
3. der Kontrolle der Entzündung und Infektion. Siehe auch die Abb 1.
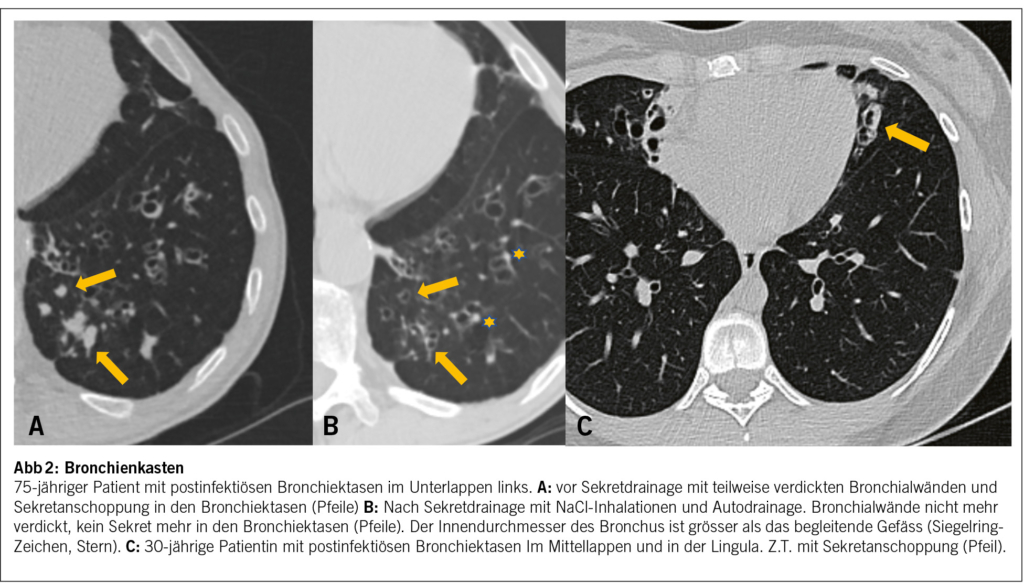
Das Sekretmanagement hat zum Ziel, die mukoziliäre Clearance zu verbessern. Dies geschiet mit regelmässiger Inhalation von hochprozentiger NaCl-Lösung und anschliessendem Abhusten des gelösten Sekretes (Autodrainage). Eine effiziente Autodrainage kann bei einer spezialisierten Physiotherapie erlernt werden. Der zeitliche Aufwand für das Sekretmanagement ist beträchtlich.
Exacerbation
Eine Exacerbation liegt vor, wenn der Husten und die Dyspnoe zunehmen, das Sputum putrider wird oder zusätzlich eine Haemoptoe vorliegt. Die Präsentation kann sehr unterschiedlich sein, oft sind Malaise und Gewichtsverlust assoziiert.
Exacerbationen nehmen eine besondere Stellung ein und sind charakteristisch für die Bronchiektasen-Erkrankung. Sie beeinflussen die Lebensqualität, den Verlauf der Lungenfunktion, den Bedarf an medizinischen Ressourcen und die Prognose. Eine Exacerbation wird mit Antibiotika während 10–14 Tagen behandelt. Die Antibiotikawahl stützt sich auf die letzte verfügbare Sputummikrobiologie. Falls keine vorliegt, erfolgt die Therapie empirisch. Die häufigsten Keime sind Haemophilus influenzae, Enterobacterioceae, Staphylococcus aureus, Pneumokokken oder aber Pseudomonas aeruginosa und auch Viren. Mit zunehmendem Antibiotikabedarf steigen die Resistenzen, eine orale Antibiotikatherapie ist dann nicht mehr möglich.
Ein Phänotyp ist der «frequent exacerbator». Diese Patienten haben pro Jahr mindestens zwei behandlungsbedürftige Exacerbationen oder eine Exacerbation mit Hospitalisationspflicht. Es sind die Patienten mit dem schwersten Krankheitsverlauf. Sie qualifizieren für eine langdauernde Immunmodulation mit Azithromycin oder aber eine inhalative Antibiotikatherapie über mehrere Monate, gelegentlich gar unbefristet. Die Reduktion der Exacerbationen durch diese zwei Massnahmen ist signifikanter bei chronischer Infektion mit Pseudomonas aeruginosa.
Beim Erstnachweis von Pseudomonas aeruginosa ist eine Eradikationstherapie empfohlen. Es gibt verschiedene Kombinationsmöglichkeiten aus oralen, intravenösen und inhalativen Antibiotika, siehe hierzu die Empfehlungen der European Respiratory Society (ERS) (3). Die Erfolgschance einer anhaltenden Eradikation nach 12 Monaten liegen um 50 %.
Etwas komplexer wird die Behandlung bei multiresistenten Keimen oder Keimen mit einem anspruchsvollen Therapieschema, wie es bei nichttuberkulösen Mykobakterien der Fall ist. Diese Patienten gehören in eine spezialisierte Sprechstunde.
Bei fehlendem Ansprechen auf die Antibiotikatherapie muss differentialdiagnostisch an neue Resistenzen, neue Keime wie NTM, eine fehlende Therapieadhärenz, an Komplikationen wie ein Empyem oder an eine alternative Diagnose wie z. B. an eine ABPA gedacht werden.
Es ist wichtig, die Patienten über das Krankheitsbild mit chronischem Verlauf aufzuklären und die Therapieansätze zu erläutern. Ein Krankheitsverständnis verbessert die Therapieadhärenz auch langfristig. Es ist zudem wichtig, dass Patienten eine Exacerbation erkennen und sich rechtzeitig ärztlich vorstellen.
Komplikationen
Die häufigsten Komplikationen sind Haemoptoe, Lungenabszess, Pleuraempyem, Pneumothorax, eine ventilatorische Insuffizienz oder ein Cor pulmonale. Nur in ausgewählten Situationen hat ein operatives Vorgehen oder eine Lungentransplantation einen Stellenwert.
Ausblick
Die Prävalenz wird weiter steigen. Umso wichtiger ist es, dass die Patienten früh erkannt werden und eine Basistherapie erhalten. Es gibt mehrere europäische Kohorten mit Non-CF-Bronchiektasen, welche neue Erkenntnisse und Therapieansätze liefern werden. Es zeichnet sich ab, dass der eosinophile Endotyp auch bei Non-CF-Patienten eine gewisse Relevanz hat; Studien mit spezifischen Antikörpertherapien wie Mepolizumab und Benralizumab sind unterwegs. Aber auch die neutrophile Entzündungskaskade ist ein neuer Angriffspunkt: Brensocatib, ein oraler Antikörper gegen die neutrophile Elastase, dürfte bald die Zulassung erhalten bei Non-CF-Bronchiektasen. Studien zeigten eine signifikante Reduktion von Exacerbationen (4). Es wäre das erste zugelassene spezifische Medikament für Non-CF-Bronchiektasen.
Abkürzungen
ABPA: allergische bronchopulmonale Aspergillose (endobronchiale Hypersensibilisierung auf Aspergillen)
CF: Cystische Fibrose
NTM: nichttuberkulöse Mykobkterien
PCD: primäre Ziliendysfunktion
Copyright Aerzteverlag medinfo A
Chefarzt Pneumologie / Schlafmedizin
Luzerner Kantonsspital
Spitalstrasse
6000 Luzern
Der Autor hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
Die Bedeutung von Non-CF-Bronchiektasen in der Grundversorgung nimmt zu. Die Abklärung einer möglichen Ursache beinhaltet die Bestimmung von Immunglobulinen, HIV, Alpha-1-Antitrypsin, Rheumaserologien und eine Sputumuntersuchung. Die Therapieziele sind die Symptomkontrolle, der Erhalt der Lungenfunktion und das Verhindern von Komplikationen wie Infektektexacerbationen und Haemoptoe. Dies wird erreicht mit der Behandlung der Grunderkrankung, der Sekretdrainage und einem gezielten Einsatz von Antibiotika. Neuere Therapieansätze, welche auf die neutrophile und eosinophile Entzündungskaskade abzielen, sind in greifbarer Nähe.
1. O’Donnell. Bronchiectasis – A Clinical Review. NEJM 2022;387:533-45
2. S2k-Leitlinie Management erwachsener Patientinnen und Patienten mit Bronchiektasen-Erkrankung. Version 1.2 – Mai 2024. AWMF Online
3. Polverino. European Respiratory Society guidelines for the management of adult bronchiectasis. Eur Respir J. 2017 Sep 9;50(3):1700629.
4. Chalmers. Dipeptidyl peptidase 1 inhibition as a potential therapeutic approach in neutrophil-mediated inflammatory disease. Front Immunol. 2023 Dec 14:14:1239151.
5. Aliberti. Criteria and definitions for the radiological and clinical diagnosis of bronchiectasis in adults for use in clinical trials: international consensus recommendations. Lancet Respir Med. 2022 Mar;10(3):298-306.
6. Quellhorst L, Barten-Neiner G, de Roux A et al. Psychometric Validation of the German Translation of the Quality of Life Questionnaire-Bronchiectasis (QOL-B)-Data from the German Bronchiectasis Registry PROGNOSIS. J Clin Med 2022; 11
7. Pasteur MC. Pasteur. An Investigation into Causative Factors in Patients with Bronchiectasis. Am J Crit Care Med 2000 Oct;162(4 Pt 1):1277-84.
der informierte @rzt
- Vol. 14
- Ausgabe 9
- September 2024