- Schilddrüsenknoten
Schilddrüsenerkrankungen sind im klinischen Alltag verbreitet. Patienten mit sicht- und tastbaren Schilddrüsenknoten oder einer veränderten Stoffwechsellage werden idealerweise frühzeitig in der hausärztlichen Praxis identifiziert und abgeklärt. Schilddrüseninzidentalome sollten ebenfalls systematisch aufgearbeitet werden. In diesem Artikel sind die wichtigsten Punkte der Diagnostik und Therapie, aber auch der Nachsorge von Schilddrüsenknoten zusammengefasst.
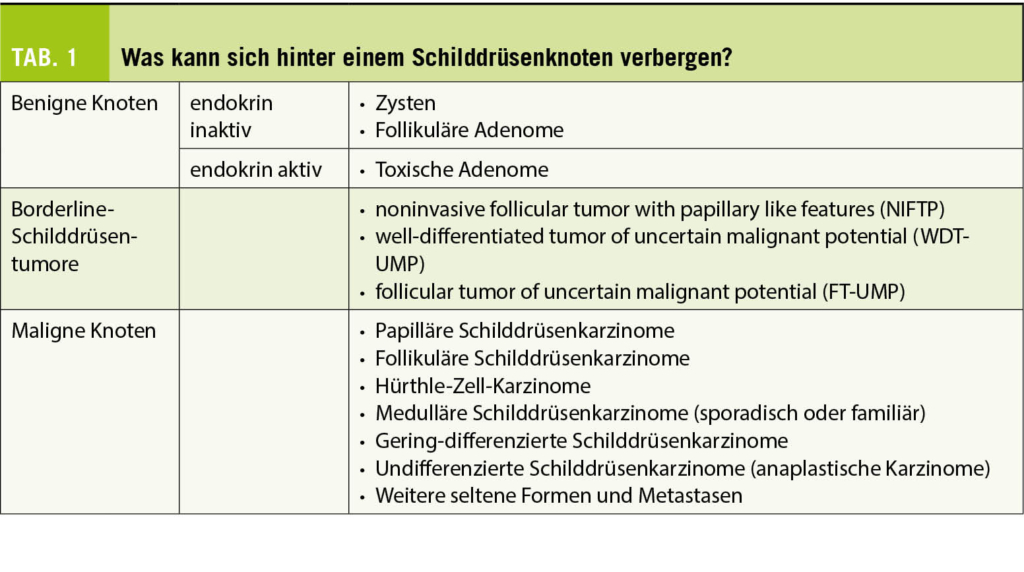
Die Diagnostik, die Patientenberatung und die Festlegung und Durchführung einer definitiven Therapie von Schilddrüsenknoten erfolgen im interdisziplinären Kontext. Evidenzbasierte Algorithmen beschleunigen die Diagnosefindung und ermöglichen eine effektive und ressourcenschonende Therapie. Die Bandbreite der möglichen Schilddrüsenknoten ist gross (Tab. 1). Bei der Behandlung von Schilddrüsenknoten kommen medikamentöse Therapien, Radiojodtherapie, Thermoablation und gezielte chirurgische Eingriffe zum Einsatz. Bei der Verlaufsbeobachtung und der Nachsorge sichert der enge Dialog zwischen Grundversorgern und spezialisierten Kollegen langfristig den Behandlungserfolg.
Basisdiagnostik bei der Erstdiagnose eines Schilddrüsenknotens
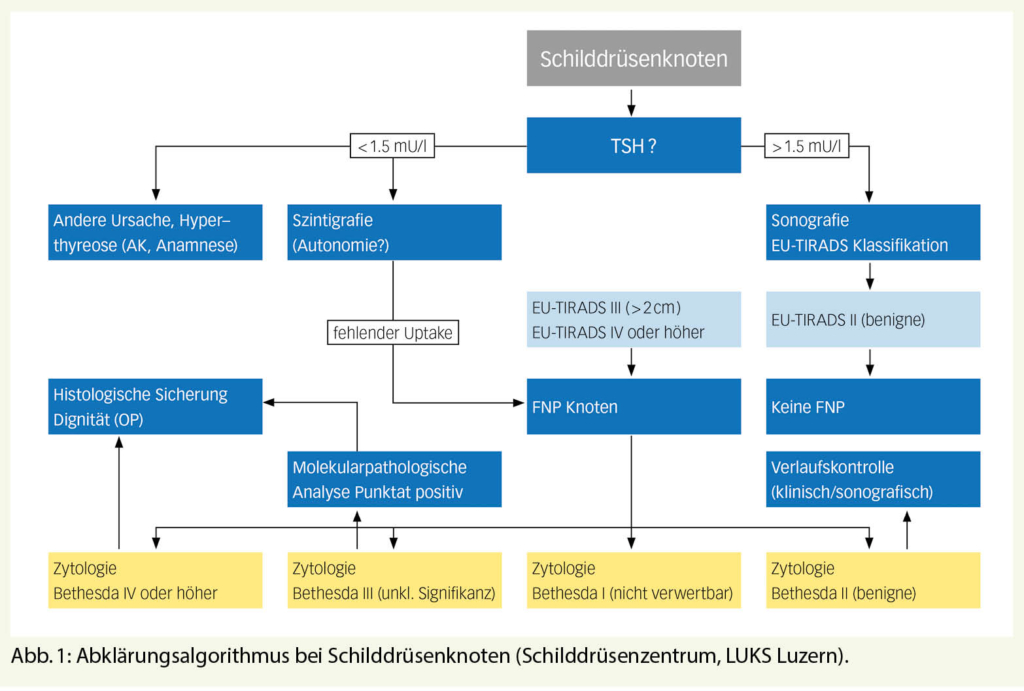
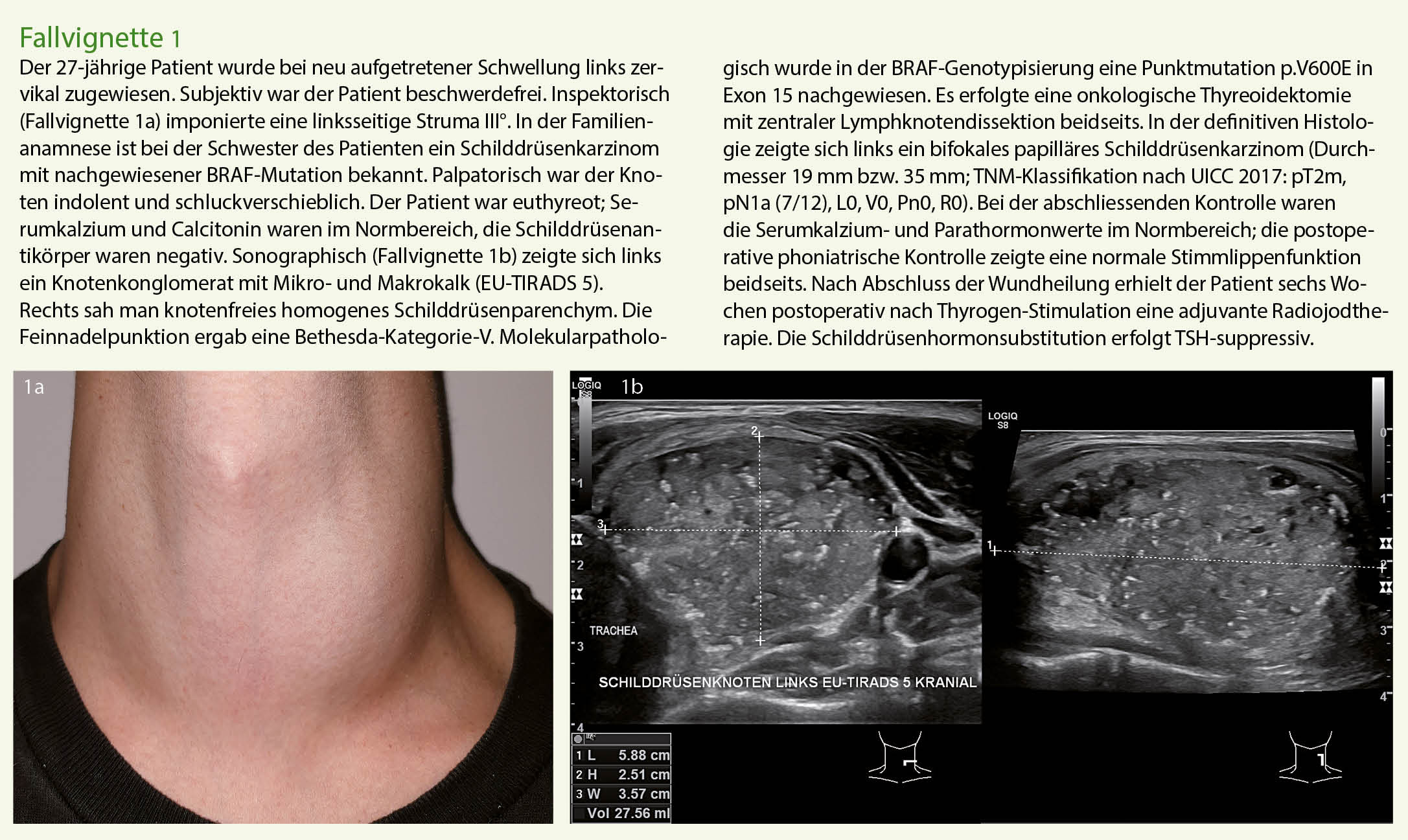
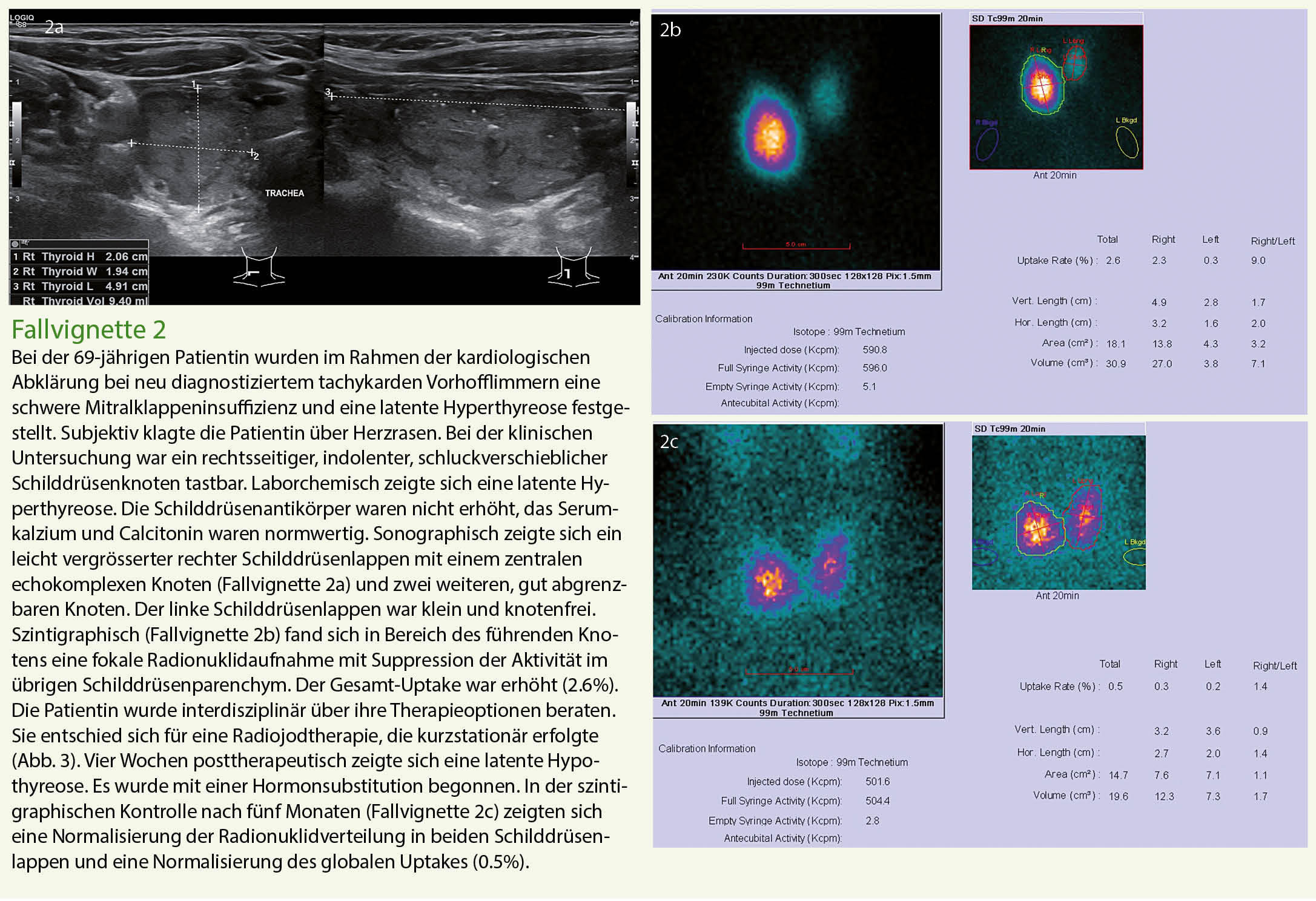
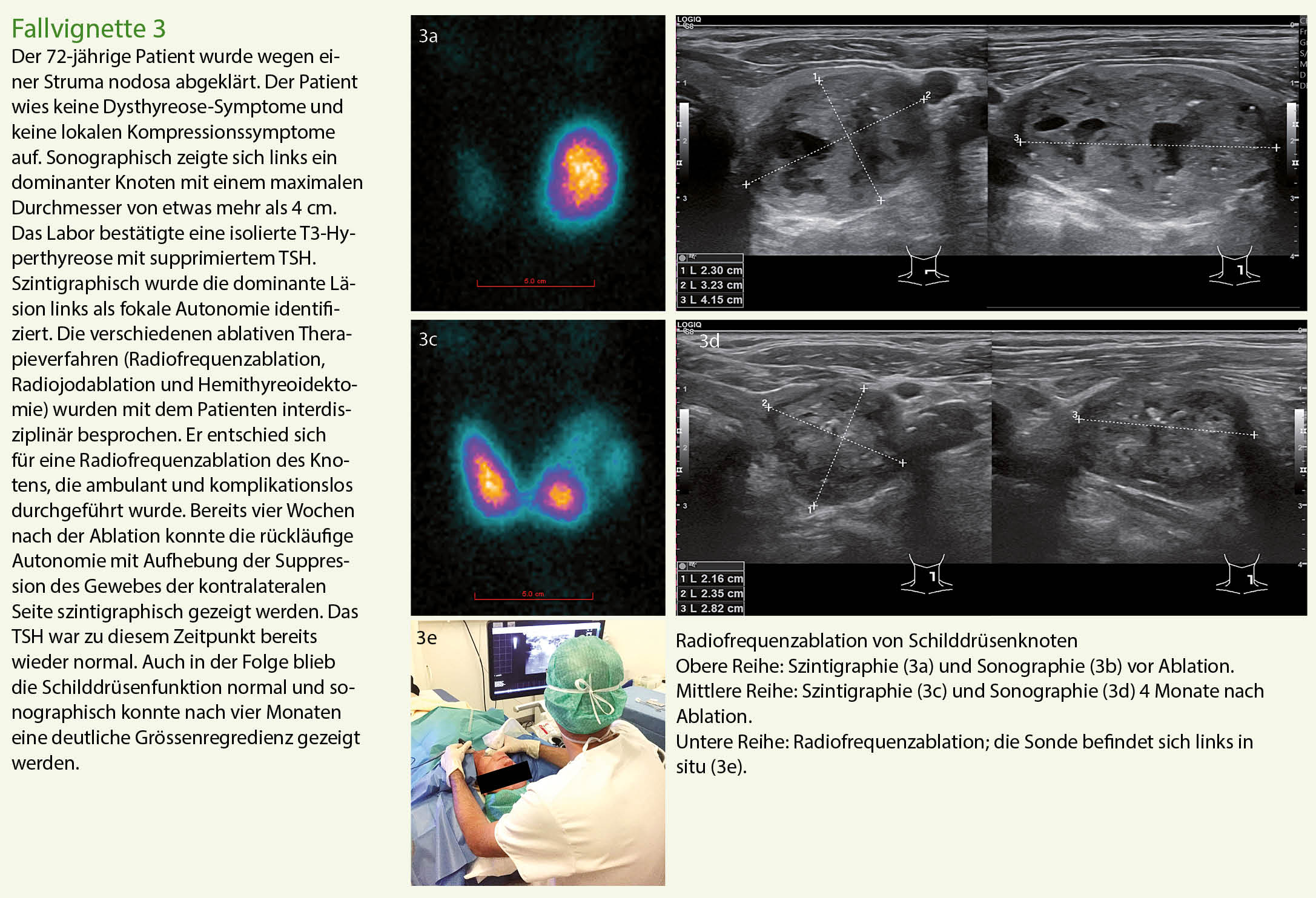
Die Basisabklärung von Schilddrüsenknoten umfasst eine detaillierte Anamnese, die körperliche Untersuchung, die laborchemische Kontrolle der Schilddrüsenfunktion und die Sonographie. Die Abklärung erfolgt standardisiert und evidenzbasiert (Abb. 1). Die Fallvignetten 1-3 zeigen exemplarisch drei aktuelle Fälle, die uns zugewiesen wurden.
Anamnese
Eine genaue Anamnese gibt wertvolle Hinweise zur Wachstumsdynamik, zur Funktion und zum Risikoprofil von Schilddrüsenknoten. Patienten berichten bei langsam wachsenden Knoten häufig erst auf gezieltes Nachfragen von lokalen mechanischen Symptomen wie Räusperzwang, Dyspnoe oder Dysphagie. Diese Symptome können lageabhängig sein, ihre Ausprägung variiert individuell. Hypo- bzw. Hyperthyreosesymptome variieren ebenfalls und müssen spezifisch erfragt werden. Wichtige Informationen ergeben sich aus der Familienanamnese bezüglich Schilddrüsen- und Nebenschilddrüsenerkrankungen und der Frage nach Ernährungsgewohnheiten und Noxen.
Anamnestisch wichtige Risikofaktoren für Malignität sind:
- Bestrahlung von Kopf und Hals in der Anamnese
- junges und fortgeschrittenes Alter
- rasches Knotenwachstum, wenig schluckverschiebliche Knoten, zervikale Lymphknotenvergrösserung
- neu aufgetretene Heiserkeit
- männliches Geschlecht
- positive Familienanamnese für Schilddrüsenmalignome
Körperliche Untersuchung
Die Tastbarkeit eines Knotens hängt von seiner Grösse, seiner Lage am Hals, der Physiognomie des Patienten und der Erfahrung des Untersuchers ab. Das frühzeitige Erkennen klinisch bedeutsamer Kompressionssymptome ist wichtig. Retrosternal gelegene Knoten können bei der körperlichen Untersuchung nicht zuverlässig erfasst werden.
Laborchemische Basisdiagnostik
Die Euthyreose wird durch TSH-Bestimmung gesichert. Die Kenntnis von TSH und fT3/fT4 ermöglicht die Einteilung in normale bzw. Unter- und Überfunktion und die Quantifizierung der Störung (subklinisch vs. manifest). Die Schilddrüsenfunktion variiert über die Lebenszeit (1). Ein Grossteil der Patienten mit Schilddrüsenknoten ist euthyreot. Ein synchron vorliegender Hyperparathyreoidismus sollte durch die Bestimmung des Serumkalziums ausgeschlossen werden.
Sonographie
Die Sonographie ist der Goldstandard in der bildmorphologischen Beurteilung von Schilddrüsenknoten und sollte immer erfolgen. Dabei werden die Grösse der Schilddrüsenlappen, die Echogenität des Parenchyms, die Knotencharakteristika (Grösse, Form und Randbildung, Lage, Echogenität, Vaskularisation und ggf. Elastizität) beschrieben und bilddokumentiert. Die Klassifizierung der Schilddrüsenknoten erfolgt standardisiert und ist gleichzeitig die Grundlage für die Indikationsstellung zur Feinnadelpunktion (2). Unscharf begrenzte Knoten, hypoechogene Knoten, Knoten, die die Schilddrüsenkapsel durchbrechen und/oder die Nachbarstrukturen infiltrieren, Mikrokalzifikationen, verstärkte Vaskularisation, pathologische Lymphknoten, PET-CT-Positivität sind wesentliche Indikatoren für Malignität. Die Sonographie umfasst auch die Beurteilung der Halslymphknoten und der Nebenschilddrüsen bei synchronem Hyperparathyreoidismus. Es erfolgt eine klinisch differenzierte Auswahl der zu punktierenden Knoten. Die Sonographie ist limitiert beim Erkennen von retrosternal gelegenen Schilddrüsenanteilen.
Spezielle Diagnostik bei der Erstdiagnose eines Schilddrüsenknotens
Weiterführende Laborchemie
Die Messung der Schilddrüsen-Antikörper ergänzt die Diagnostik zum Ausschluss einer Autoimmunthyreoiditis. Das seltene, medulläre Schilddrüsenkarzinom wird bei knotiger Schilddrüse durch die Calcitonin-Bestimmung ausgeschlossen.
Erweiterte Bildgebung Szintigraphie
Die Szintigraphie erlaubt eine «Funktionstopographie» der Schilddrüse. Sie ermöglicht bei vorliegendem Ultraschall eine Differenzierung zwischen hyper- und hypofunktionellen Knoten, die Unterscheidung zwischen fokaler und disseminierter Autonomie und das Erkennen von extrazervikalem Schilddrüsengewebe (3).
Die ideale Zuweisung zur Szintigraphie umfasst eine problemorientierte Anamnese, ein aktuelles TSH und aktuelle Ultraschallbilder.
Schilddrüsenknoten mit einem erhöhten Uptake in der Schilddrüsenszintigraphie sind selten maligne.
Schnittbildgebung
Eine Computertomographie des Halses und Thorax ohne jodhaltiges intravenöses Kontrastmittel oder eine Magnetresonanztomographie kommen bei der Beurteilung des oberen Mediastinums zum Einsatz. Die intrathorakale Knotenausdehnung und die Gefässversorgung können damit ergänzend beurteilt werden. Selten muss bei erforderlicher chirurgischer Therapie die Zervikotomie durch eine Sternotomie erweitert werden.
Feinnadelpunktion
Die ultraschallgesteuerte Feinnadelpunktion hat eine hohe Sensitivität und Spezifität, wenn sie von geübter Hand durchgeführt und mit grosser zytopathologischer Erfahrung beurteilt wird. Entscheidend ist die Gewinnung von repräsentativem Punktionsmaterial mit ausreichend Thyreozyten.
Bei der Beurteilung der Ergebnisse der Feinnadelpunktion sollte das Bethesda-System verwendet werden. Es dient der Risikoabschätzung einer potenziellen Malignität und ist eine wichtige Entscheidungshilfe bei der Therapieplanung und auch bei der Festlegung des Operationsausmasses (4). Wird eine Probe als nicht repräsentativ (Bethesda-Kategorie-I) eingestuft, erfolgt die Repunktion. Die Risikobewertung der sechs existierenden Bethesda-Kategorien wurde über die Zeit angepasst (5). Neue vergleichende Untersuchungen internationaler Registerstudien zeigen, dass die prognostische Aussagekraft der zytopathologischen Befunde immer wieder kritisch hinterfragt werden muss. Die Zytopathologie ist nur ein Element bei der interdisziplinären Entscheidungsfindung und der individuellen Therapieempfehlung (6). Sowohl bei der sonographischen als auch bei der zytopathologischen Risikostratifizierung bleibt der mittlere Bereich der Bereich mit der grössten Unschärfe. Gerade hier profitiert der Patient von einer interdisziplinären Beratung im Expertenteam.
Einsatz molekularpathologischer Zusatzuntersuchungen
Zur genaueren Differenzierung von Knoten mit intermediärem Risikoprofil können molekularpathologische Zusatzuntersuchungen erfolgen. Um bei der Planung der weiteren Therapie entscheidend zu sein, muss die Molekularpathologie zuverlässige prognostische Informationen liefern. Die Validierung, die Analyse des Nutzen-Risiko-Verhältnisses und die Kosteneffizienz der molekulargenetischen Untersuchungen stehen noch aus.
Therapieoptionen bei Schilddrüsenknoten
Nach Abschluss der Basisdiagnostik und der speziellen Diagnostik können folgende Therapiemöglichkeiten offenstehen:
- Verlaufsbeobachtung mit klinischer, laborchemischer und sonographischer Kontrolle
- Medikamentöse Therapie
- Operation
- Radiojodtherapie
- Thermoablation
Patientenpräferenzen spielen bei der Festlegung der Therapie eine wesentliche Rolle. Von Patienten häufig genannte Aspekte bei der Entscheidungsfindung sind der Wunsch nach Unabhängigkeit von Medikamenten, keine langwierigen Verlaufsbeobachtungen, zügige Therapieentscheide, komplikationsarme klinische Verläufe, Rezidivfreiheit. Der Patient wird bei seiner informierten Entscheidung im interdisziplinären Team gestärkt.
Verlaufsbeobachtung mit Kontrolle
Asymptomatische Schilddrüsenknoten ohne Malignitätszeichen in einer euthyreoten Schilddrüse können klinisch, laborchemisch und sonographisch beobachtet werden.
Medikamentöse Therapie
Die thyreostatische Therapie mit Carbimazol (Néo-Mercazole®) kann initial oder auch überbrückend bei fokaler Autonomie zum Einsatz kommen. Propylthiouracil (Propycil®) wird nur in Reservefällen (z. B. Behandlung im ersten Trimenon der Schwangerschaft) und bei Unverträglichkeiten eingesetzt. Bei fokalen Autonomien ist die medikamentöse Therapie nicht kurativ, d.h. ein Absetzen der Behandlung führt zum Wiederauftreten der Schilddrüsenüberfunktion.
Die Operation
In der Schweiz werden jährlich etwa 3600 Operationen an der Schilddrüse vorgenommen. Die medizinische Praxis richtet sich nach europäischen und amerikanischen Leitlinien. Die häufigsten Indikationen zur Schilddrüsenresektion sind Kompressionssymptome, Malignitätsausschluss und Malignität sowie Schilddrüsenüberfunktion (7). Im Schilddrüsenzentrum, LUKS Luzern, wurden im Jahr 2019 150 primäre Operationen an der Schilddrüse durchgeführt; die meisten Operationen erfolgten bei Kompressionssymptomen (58/150). 50/150 Operationen wurden zum Ausschluss vermuteter Malignität vorgenommen und von diesen wurde der Malignitätsverdacht in 52% der Fälle bestätigt. Bei 10/150 Patienten war die Malignitätsdiagnose bereits präoperativ gesichert. Bei 32/150 Patienten bestand eine klinisch manifeste Hyperthyreose (Abb. 2).
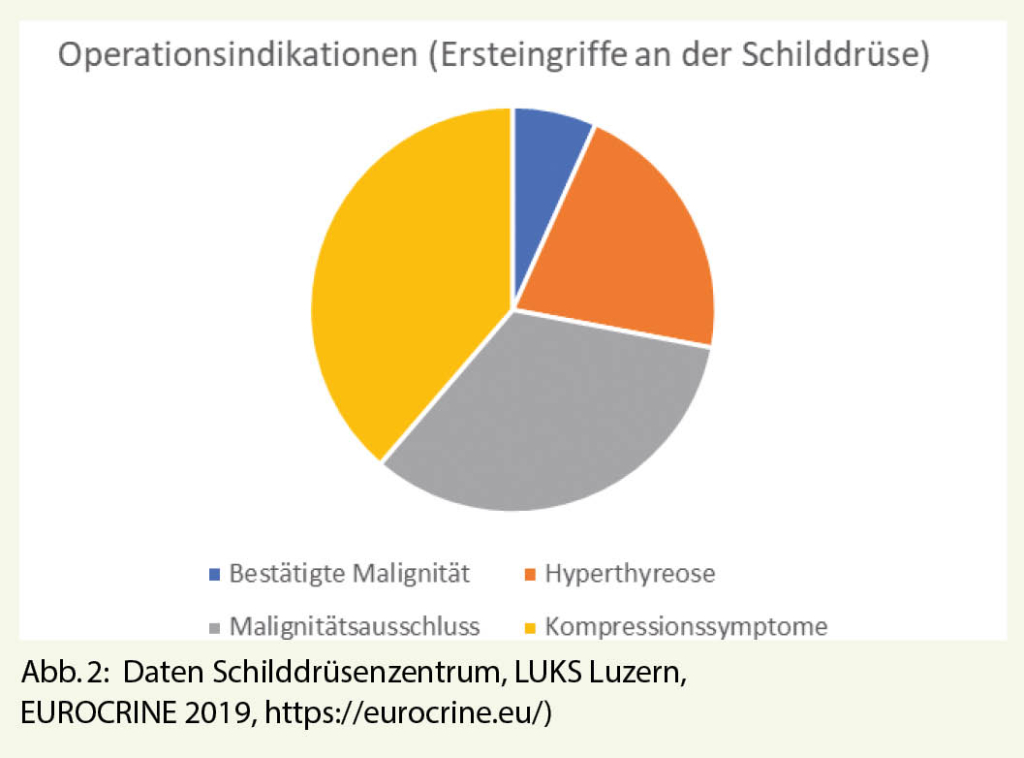
Die chirurgische Strategie ist fallbezogen und individuell. Es erfolgt eine lappengetrennte Indikationsstellung. Die befunddominante Seite wird zuerst operiert. Alle Operationen erfolgen mit Lupenbrille. Der Einsatz des intraoperativen Neuromonitorings schützt den N. laryngeus recurrens (8). Einzeitige Operationen werden angestrebt. Der intraoperative Gefrierschnellschnitt kommt dabei zum Einsatz. Rezidive sind bei benignen und malignen Schilddrüsenerkrankungen zu vermeiden. Individualisierte, risikoadaptierte Operationen an erfahrenen Zentren mit hohem Operationsvolumen senken das Operationsrisiko für den einzelnen Patienten. Eingriffe durch «high-volume» endokrine Chirurgen haben ein besseres Outcome. Dies gilt sowohl für eingriffsspezifische Komplikationen (Nachblutung, postoperativer Hypoparathyreoidismus und N. recurrens-Läsionen) als auch für die 30-Tage-Morbidität (Infektionen, Operationsdauer und Spitalaufenthalt).
Die Radiojodtherapie
Bei autonomen Knoten kann die Radiojodtherapie bei manifester oder latenter Hyperthyreose zum Einsatz kommen. Faktoren, die bei der Beratung des Patienten für eine Radiojodtherapie sprechen, sind Voroperationen an der Schilddrüse und ein erhöhtes Operationsrisiko bei Begleiterkrankungen. Die wichtigsten Kontraindikationen sind eine Schwangerschaft und die Stillzeit. Vor jeder Radiojodtherapie soll auf Jod-Zufuhr verzichtet werden. Die Therapie wird individuell berechnet und hängt von der Grösse der Schilddrüse, dem Joduptake (wird durch eine geringe Menge Testdosis von Jod-131 ermittelt) und der angestrebten Zieldosis ab. Bei unifokaler und multifokaler Autonomie kommt ein funktionsoptimiertes Therapiekonzept zur Anwendung mit dem Ziel, die Hyperthyreose zu beseitigen, die Funktion der Schilddrüse jedoch zu erhalten. Neben der Normalisierung der Stoffwechsellage kann eine erfolgreiche Radiojodtherapie auch das Volumen des hyperaktiven Schilddrüsenknotens reduzieren.
Die Thermoablation
Die ablative Behandlung von unifokalen Autonomien durch Thermoablation mit monopolaren oder bipolaren Sonden stellt ein neueres, minimalinvasives Verfahren dar, das im ambulanten oder kurzstationären Setting durchgeführt wird. Der Vorteil der Methode liegt darin, dass das hyperfunktionelle Gewebe organerhaltend reduziert wird. Die Thermoablation kann zu einer Volumenreduktion von 65-80% führen. Die therapeutische Erfolgsrate in Bezug auf die Normalisierung der Schilddrüsenfunktion reicht von 50 bis fast 90% (9). Die Indikation zur Thermoablation wird in unserem Schilddrüsenzentrum interdisziplinär gemeinsam mit dem Patienten gestellt. Für die Qualitätssicherung werden die Patienten vor und nach dem Eingriff engmaschig kontrolliert (Sonographie, postinterventionelle Szintigraphie zur Beurteilung des Ablationserfolges, prä- und postablationelle phoniatrische Prüfung der Stimmbandfunktion).
Nachsorge und Qualitätssicherung
In der Nachsorge kommen ‒ in Analogie zur Basisabklärung von Schilddrüsenknoten ‒ die detaillierte Anamnese, die körperliche Untersuchung, die laborchemischen Kontrollen und die Sonographie erneut zum Einsatz. Das TSH-Monitoring nimmt in der Nachsorge einen wichtigen Stellenwert ein. Schwankende Compliance und Dosisanpassungen der Schilddrüsenhormonersatztherapie erfordern engmaschigere Laborkontrollen. Nach Anpassungen der medikamentösen Therapie erfolgt die TSH-Kontrolle in 4-6-wöchigem Abstand. Die angestrebten TSH-Werte variieren je nach Erkrankung, definitiver histologischer Diagnose und dem Therapieansprechen. Sie können sich zwischen Zielwerten im Normbereich, im unteren Normbereich und TSH-suppressiven Werten bewegen.
Durch eine regelmässige Nachsorge kann die Therapietreue der Patienten zuverlässig gewahrt bleiben. Rezidive können frühzeitig erkannt werden. Rezidivierende Erkrankungen bei Schilddrüsenknoten können sich klinisch, laborchemisch und sonographisch bemerkbar machen durch neu aufgetretene Kompressionssymptome, dysthyreote Symptome, sicht- und/oder tastbare Schilddrüsenknoten, zervikale Lymphadenopathie oder laborchemische Auffälligkeiten. Sie bedürfen in Analogie zur Erstdiagnose einer strukturierten Abklärung.
Eine systematische Qualitätssicherung in Datenbanken mit Benchmarking ist integraler Bestandteil der Patientenversorgung. In der Langzeitbetreuung wird klinisch, laborchemisch und sonographisch der therapeutische Erfolg dokumentiert.
Ausblick
Schilddrüsenknoten bleiben häufig. Schilddrüsenkarzinome haben weltweit eine steigende Inzidenz (10). Die Diagnose eines Schilddrüsenknotens unklarer Dignität und die damit verbundenen Verlaufsuntersuchungen sind für viele Patienten belastend. Die diagnostisch eindeutige und zeitnahe Abklärung kann auch für das Behandlungsteam eine Herausforderung sein. Der Patient und das Behandlungsteam profitieren von einer strukturierten und einheitlichen Diagnostik. Neueste wissenschaftliche Erkenntnisse verbessern die Diagnostik- und Therapieabfolge. Bei der individualisierten Therapieempfehlung wird die Kompetenz und Erfahrung der unterschiedlichen Fachdisziplinen gebündelt. Die enge Zusammenarbeit mit den Kollegen in der Praxis sichert für den Patienten auch langfristig den Therapierfolg.
Lukas Scheuble, 1
Dr. med. Stefan Fischli, 2,1
Dr. med. Maria del Sol Pérez Lago, 3,1
Dr. med. Walter Arnold, 4,1
PD Dr. med. Corinna Wicke, 1
Schilddrüsenzentrum1, Endokrinologie und Diabetologie2, Radiologie und Nuklearmedizin3, Pathologie4, Luzerner Kantonsspital, Luzern
Luzerner Kantonsspital, Spitalstrasse, 6000 Luzern 16
Copyright bei Aerzteverlag medinfo AG
Schilddrüsenzentrum
Luzerner Kantonsspital
Spitalstrasse
6000 Luzern 16
corinna.wicke@luks.ch
Die Autoren haben in Zusammenhang mit diesem Artikel keine Interessenkonflikte deklariert.
- Schilddrüsenknoten sind im Praxisalltag häufig – nur ein kleiner Anteil aller Knoten ist maligne.
- Klar definierte Algorithmen beschleunigen die Diagnosefindung und die Therapieempfehlung.
- Die sonographisch-gesteuerte Feinnadelpunktion erfasst das Malignitätspotential eines Knotens.
- Jeder Patient wird über seine Behandlungsoptionen (Beobachtung, medikamentöse Therapie, Operation, Radiojodbehandlung oder Thermoablation) individuell beraten.
- Eine konsequente Nachsorge optimiert den Behandlungserfolg.
1. Franceschi C, Ostan R, Mariotti S, Monti D, Vitale G. The Aging Thyroid: A Reappraisal Within the Geroscience Integrated Perspective. Endocr Rev. 2019;40(5):1250-70.
2. Russ G, Bonnema SJ, Erdogan MF, Durante C, Ngu R, Leenhardt L. European Thyroid Association Guidelines for Ultrasound Malignancy Risk Stratification of Thyroid Nodules in Adults: The EU-TIRADS. Eur Thyroid J. 2017;6(5):225-37.
3. Giovanella L, D’Aurizio F, Campenni A, Ruggeri RM, Baldari S, Verburg FA, et al. Searching for the most effective thyrotropin (TSH) threshold to rule-out autonomously functioning thyroid nodules in iodine deficient regions. Endocrine. 2016;54(3):757-61.
4. Cibas ES, Ali SZ, Conference NCITFSotS. The Bethesda System For Reporting Thyroid Cytopathology. Am J Clin Pathol. 2009;132(5):658-65.
5. Pusztaszeri M, Rossi ED, Auger M, Baloch Z, Bishop J, Bongiovanni M, et al. The Bethesda System for Reporting Thyroid Cytopathology: Proposed Modifications and Updates for the Second Edition from an International Panel. Acta Cytol. 2016;60(5):399-405.
6. Inabnet WB, 3rd, Palazzo F, Sosa JA, Kriger J, Aspinall S, Barczynski M, et al. Correlating the Bethesda System for Reporting Thyroid Cytopathology with Histology and Extent of Surgery: A Review of 21,746 Patients from Four Endocrine Surgery Registries Across Two Continents. World J Surg. 2020;44(2):426-35.
7. Patel KN, Yip L, Lubitz CC, Grubbs EG, Miller BS, Shen W, et al. The American Association of Endocrine Surgeons Guidelines for the Definitive Surgical Management of Thyroid Disease in Adults. Ann Surg. 2020;271(3):e21-e93.
8. Staubitz JI, Watzka F, Poplawski A, Riss P, Clerici T, Bergenfelz A, et al. Effect of intraoperative nerve monitoring on postoperative vocal cord palsy rates after thyroidectomy: European multicentre registry-based study. BJS Open. 2020;4:821-29.
9. Dobnig H, Amrein K. Monopolar Radiofrequency Ablation of Thyroid Nodules: A Prospective Austrian Single-Center Study. Thyroid. 2018;28(4):472-80.
10. Cabanillas ME, McFadden DG, Durante C. Thyroid cancer. Lancet. 2016;388(10061):2783-95.
der informierte @rzt
- Vol. 10
- Ausgabe 12
- Dezember 2020