- Strategien zur Verbesserung der Prognose des Darmkrebses
Kolorektale Karzinome (KRK) zählen mit Brust- und Prostata- sowie Bronchialkarzinomen zu den häufigsten Krebsursachen in der Schweiz. Das Risiko, im Laufe des Lebens an Darmkrebs zu erkranken, beträgt in der Schweiz für Männer ca. 6% und für Frauen ca. 3,7% (1). Vor allem nach dem 50. Lebensjahr steigt das Risiko für das Auftreten von kolorektalen Adenomen deutlich an. Der Artikel stellt die aktuellen Massnahmen zur Verbesserung der Prognose dieser individuell und volkswirtschaftlich bedeutenden Krankheit dar.
Die Risikofaktoren für die Entwicklung eines KRK sind in Tabelle 1 aufgeführt. Durch die Resektion kolorektaler Adenome während einer Screeningkoloskopie kann die Inzidenz des kolorektalen Karzinoms um 70–80% und die krebsbedingte Mortalität um bis zu 90% reduziert werden (2, 3). Erfolgt die Koloskopie hingegen erst wegen typischer Alarmsymptome wie Stuhlunregelmässigkeiten, Gewichtsverlust, Schmerzen oder Blut im Stuhl, so liegt nur in knapp 20% der Fälle mit kolorektalem Karzinom ein UICC-Stadium 1, in 33% aber bereits ein Stadium 2 und bei jeweils knapp 24% der Fälle ein UICC-Stadium 3 bzw. 4 vor (2). Bei Koloskopien im Rahmen eines schweizerischen Screening-Programms in den Kantonen Uri und Glarus lag der Anteil kolorektaler Karzinome im UICC-Stadium 1 demgegenüber bei über 70% (2). Die Erkennung kolorektaler Karzinome in einem frühen Stadium ist insofern relevant, da die 5-Jahres-Überlebensrate mit einer Therapie in kurativer Absicht im UICC-Stadium 1 bei > 90% liegt, diese sich in den Stadien 2, 3 und 4 aber erheblich reduziert (60–85%, 25–65% und 5–7%) (4).
Strategien zur Verbesserung der Prognose kolorektaler Karzinome setzen daher an 3 Hebeln an:
1. Änderung beeinflussbarer Risikofaktoren bzw. Lifestylemassnahmen
2. Verbesserung der Früherkennung und Vorsorge durch qualitativ hochwertige Screeningmassnahmen
3. Optimierung der Therapie in Bezug auf Qualität in zertifizierten Darmkrebszentren.
Lifestylemassnahmen und Reduktion beeinflussbarer Risikofaktoren
Beeinflussbare Risikofaktoren umfassen die Empfehlung eines Rauchstopps, die Reduktion von Übergewicht bzw. des Bauchumfangs sowie regelmässige körperliche Bewegung oder Sport von mindestens 30 Minuten / Tag und diätetische Massnahmen wie das Meiden von rotem Fleisch und Alkohol sowie die vermehrte Zufuhr von Obst oder Gemüse. So konnte in einer prospektiven Kohortenstudie an 55 487 Männern und Frauen in Dänemark über eine mediane Nachbeobachtungszeit von knapp 10 Jahren gezeigt werden, dass die positive Beeinflussung bereits eines Risikofaktors jeweils zu einer Risikoreduktion um 11% führt (5). Umgekehrt sind ca. 13% aller kolorektalen Karzinome auf die fehlende Einhaltung nur einer dieser Empfehlungen zur gesunden Lebensführung zurückzuführen. Werden hingegen alle Empfehlungen umgesetzt, könnten 23% aller kolorektalen Karzinome verhindert werden. Das bedeutet konkret, dass sich die Anzahl der neu auftretenden kolorektalen Karzinome bei Männern von 60 auf 46 und bei Frauen von 37 auf 29 (jeweils pro 1000 Personen) reduzieren oder anders ausgedrückt durch Änderung des Lebensstils bei Männern 14 und bei Frauen 8 Darmkrebs-Neuerkrankungen pro 1000 verhindern liessen. Darüber hinaus gibt es Anhaltspunkte dafür, dass sich durch eine langfristige Einnahme von Aspirin (≥ 5 Jahre) das Karzinomrisiko um 27% reduziert (6). Da dies aber auch zu einer erhöhten Rate schwerer Blutungen führt, kann die präventive Einnahme von Aspirin zur Reduktion der Inzidenz des kolorektalen Karzinoms weiterhin nicht empfohlen werden.
Verbesserung der Darmkrebs-Vorsorge und -Früherkennung durch qualitativ hochwertige Screeninguntersuchungen
Eine sehr wirksame und kosteneffiziente Strategie zur Verbesserung der Prognose des kolorektalen Karzinoms stellen Vorsorge- und Früherkennungsuntersuchungen dar. Screeningtests basieren auf den Erkenntnissen der Tumorbiologie und der Erforschung der sogenannten Adenom-Karzinom-Sequenz, der zufolge sich Karzinome über Jahre bis Jahrzehnte aus zunächst dysplastisch veränderten Adenomen entwickeln (2, 7, 8).
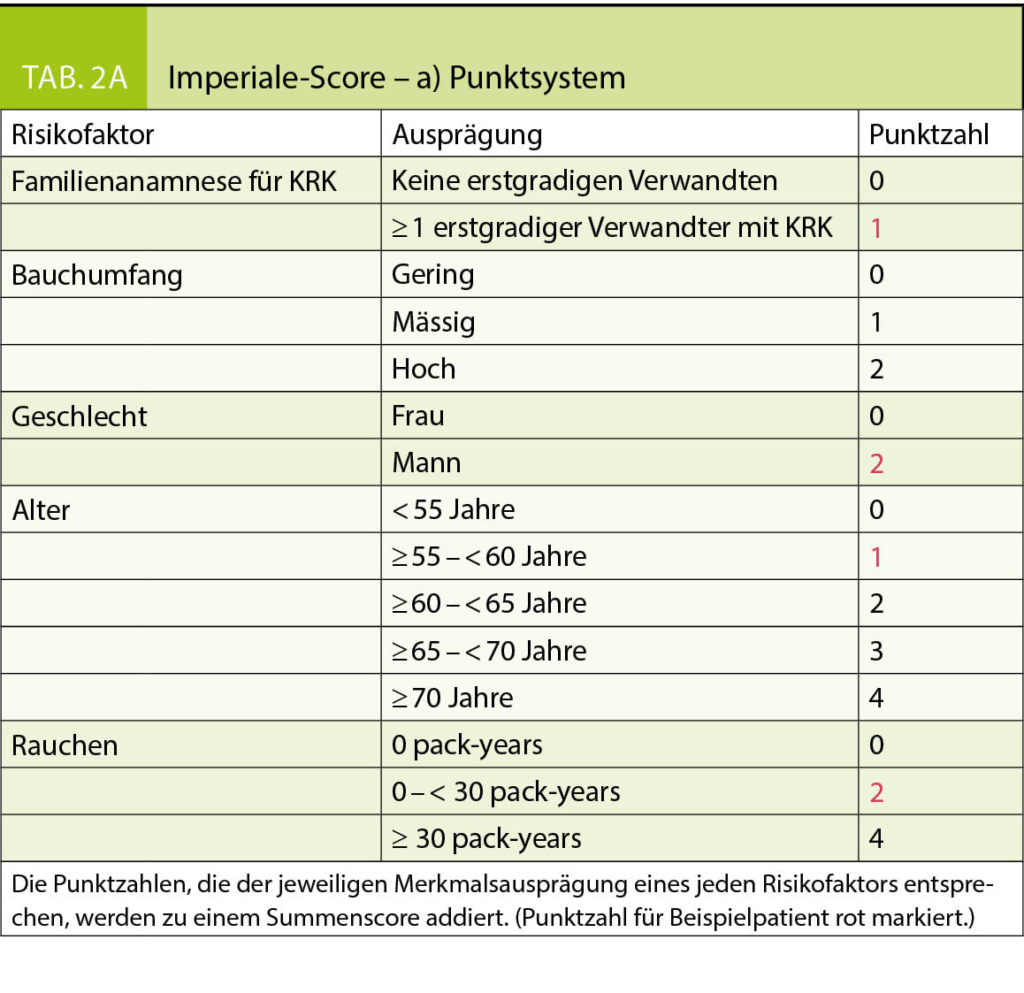
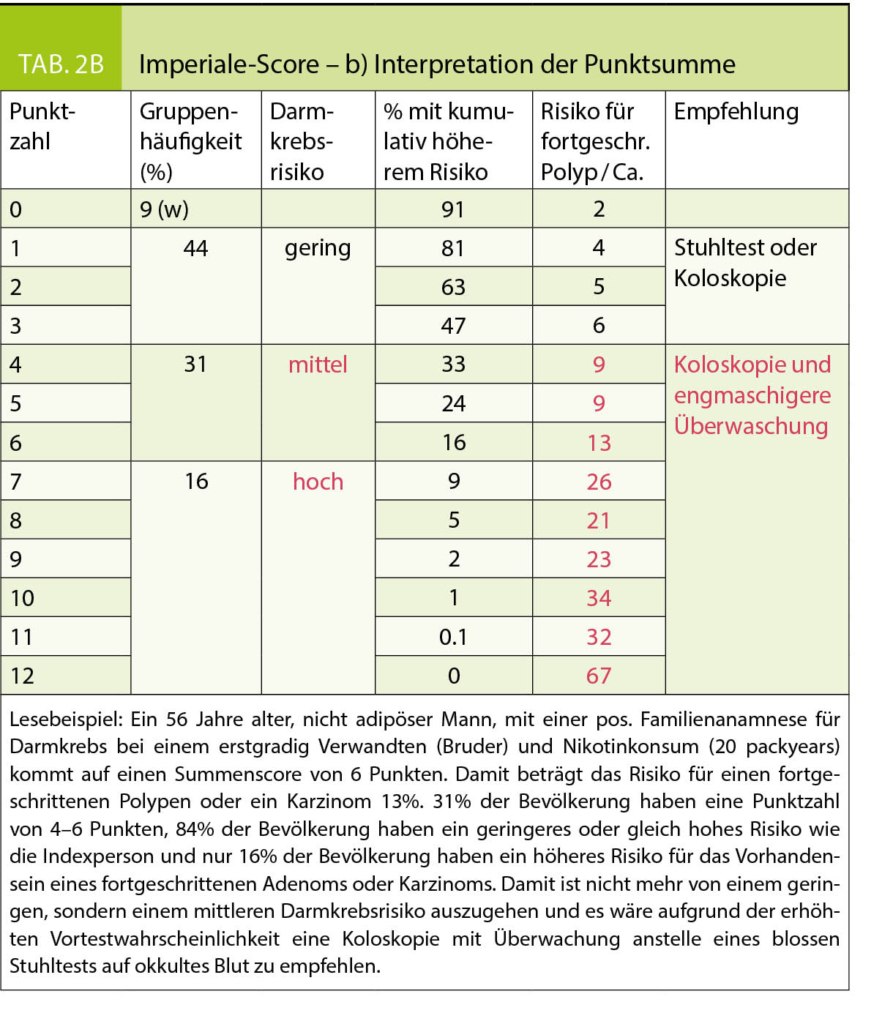
Die verschiedenen Screeningverfahren unterscheiden sich in Bezug auf Sensitivität, Spezifität und Akzeptanz. Bei der Wahl des Untersuchungsverfahrens sollten nicht nur die testspezifischen Vor- und Nachteile gegeneinander abgewogen, sondern dieses auch mit dem vorbestehenden individuellen Risiko in Einklang gebracht werden. Dieses lässt sich anhand des sogenannten Imperiale-Scores erfassen (9). Dabei werden für verschiedene Risikofaktoren je nach Merkmalsausprägung 0 bis max. 4 Punkte vergeben und aufaddiert (Tab. 2A). Mit dem Summenscore (0–12 Punkte) kann das individuelle Risiko für das Vorhandensein eines fortgeschrittenen Polypen oder Karzinoms und die Gruppenhäufigkeit bzw. die Perzentile des Individuums in der Grundgesamtheit abgeschätzt werden. Daraus lässt sich dann eine Empfehlung für die Wahl des Screeningverfahrens ableiten (Tab. 2B).
Testverfahren
Zur Darmkrebsvorsorge können indirekte oder direkte Screeningtests eingesetzt werden. Die indirekten Tests dienen zum Nachweis von okkultem, d.h. mit blossem Auge nicht sichtbarem Blut im Stuhl, wie es bei fortgeschrittenen Adenomen oder vor allem Karzinomen häufig, aber keineswegs immer auftreten kann. Bei den strukturellen Untersuchungen wird die direkte Visualisierung von Adenomen mittels Koloskopie oder CT-Kolonographie («virtuelle Koloskopie») mit anschliessender Polypenresektion angestrebt.
Indirekte Tests (Stuhlbluttests)
Die guajakbasierten Stuhlbluttests (Guaiac-based fecal occult blood testing, gFOBT; z.B. Haemoccult®) sind aufgrund unzureichender Sensitivität und Spezifität durch quantitative immunchemische Stuhlbluttests (immunochemical fecal occult blood testing (iFOBT) oder fecal immunochemical test (FIT); z.B. OC Sensor®) ersetzt worden. Die Testmethode basiert auf einer Latex-Agglutinationsreaktion und erfordert klinisch etablierte Labortechnologie (Photometrie). Die Sensitivität für kolorektale Karzinome liegt bei 73–88%, d.h. rund 1/5 der asymptomatischen Karzinome werden auch mit dieser Methode nicht erkannt (10). Die Spezifität ist mit 90–96% hoch, durch gastrointestinale Blutungen, unter Antikoagulation oder ASS-Therapie sind aber falsch positive Befunde möglich. Der Test ist einfach, relativ günstig, verursacht keinen Arbeitsausfall und wird gut akzeptiert, muss aber in regelmässigen Abständen (alle 2 Jahre) wiederholt werden. Bei pos. Testergebnis ist eine Koloskopie erforderlich.
Direkte (strukturelle) Tests zur Visualisierung von Polypen / Karzinomen
CT-Kolonographie
Mit der nicht-invasiven, aber mit einer Strahlenbelastung einhergehenden CT-Kolonographie («virtuelle Koloskopie») können nach entsprechender Darmvorbereitung wie für eine Koloskopie Polypen ab 6 mm Grösse bei asymptomatischen Personen mit einer Sensitivität von 73–98% bei einer Spezifität von 90% sowie extrakolische Befunde dargestellt werden (10). Kleinere Polypen können aber übersehen werden. Bei positivem Befund muss zur Polypenresektion eine komplette Koloskopie erfolgen.
Koloskopie
Seit 2013 ist die Koloskopie zum Polypenscreening bei asymptomatischen Personen vom 50. bis 69. Lebensjahr auch in der Schweiz kassenpflichtig. Kohortenstudien zufolge kann die Polypenresektion während der Koloskopie etwa 80% der kolorektalen Karzinome verhindern (3). In einer schweizerischen Kohortenstudie stellte die Koloskopie (entgegen der Einschätzung der Ärzte) aus Sicht der Patienten die gegenüber anderen Verfahren bevorzugte Screeninguntersuchung dar (11). Zur Prognoseverbesserung muss aber die Akzeptanz der Vorsorgeuntersuchungen weiter verbessert werden, da trotz ausführlicher Informationskampagne in dieser Studie nur 12% der Patienten, für die eine Untersuchung in Betracht gekommen wäre, diese auch tatsächlich wahrnahmen.
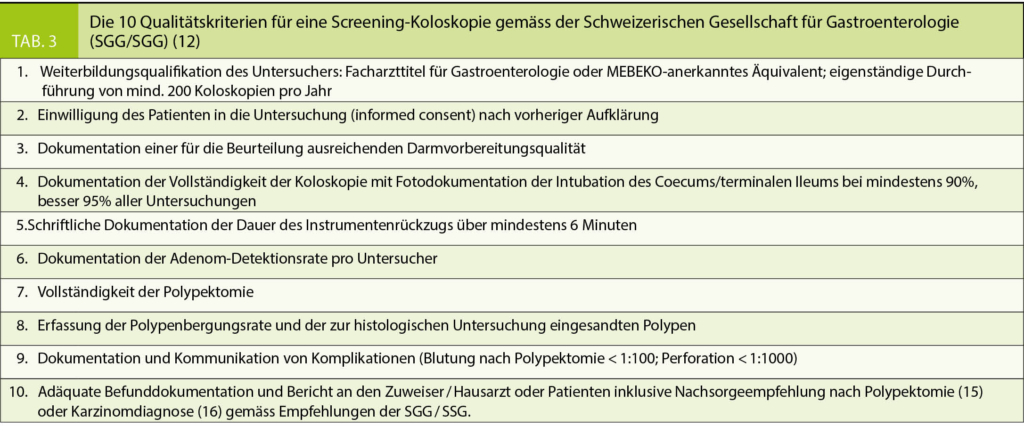
Die Screeningkoloskopie muss bestimmten Qualitätsstandards genügen, wie sie von der Schweizerischen Gesellschaft für Gastroenterologie (SGG / SGG) im Mai 2017 in Anlehnung an internationale Empfehlungen definiert worden sind (Tab. 3 (12)). Eine hohe Adenom-Detektionsrate (ADR) ist dabei der beste prospektive Parameter für eine geringe Rate an Intervallkarzinomen. Diese ist das erklärte Mass für eine gute Qualität in der Vorsorgekoloskopie und wird durch die gründliche Mukosainspektion während des langsamen Instrumentenrückzugs über mindestens 6 Minuten wesentlich mitbedingt.
Interaktive Entscheidungshilfe bei der Darmkrebsvorsorge
Die «Darm Check – App»
Die kostenlose Smartphone-Applikation «Darm Check – App» (App Store: https://itunes.apple.com/ch/app/id1273680828; Google Play: http://play.google.com/store/apps/details?id=com.fabware.darmcheck; Abb. 1) wurde auf Initiative des Dachverbands der Schweizerischen Patientenstellen (DVSP) nach evidenzbasierten Kriterien erarbeitet. Sie ermöglicht Patienten und Ärzten, unter Berücksichtigung der modernen Prinzipien der partizpativen Entscheidungsfindung (shared decision making), die Wahl des Screeningverfahrens unter Abwägung des Nutzens sowie möglicher Komplikationen unter Einbezug des individuellen Risikos aktiv mitzugestalten. Die auf diese Weise gemeinsam von Patienten und ihrem behandelnden Arzt erarbeitete Handlungsempfehlung basiert auf den Werten, Präferenzen und der Lebensqualität des über die medizinische Datenlage gut informierten Patienten. Dies ermöglicht Betroffenen, besser zu verstehen, was Ärzte mit Vorsorgeuntersuchungen zu erreichen versuchen. Damit verbunden ist die Hoffnung, die generelle Akzeptanz für die Teilnahme an Vorsorgeuntersuchungen zu erhöhen und Ängste abzubauen. Die kostenlose App informiert auch über Darmgesundheit und zeigt die Darmuntersuchungsmethoden zur Krebsvorsorge auf.
Therapieoptimierung und Verbesserung der Prozess- und Ergebnisqualität durch zertifizierte Tumorzentren
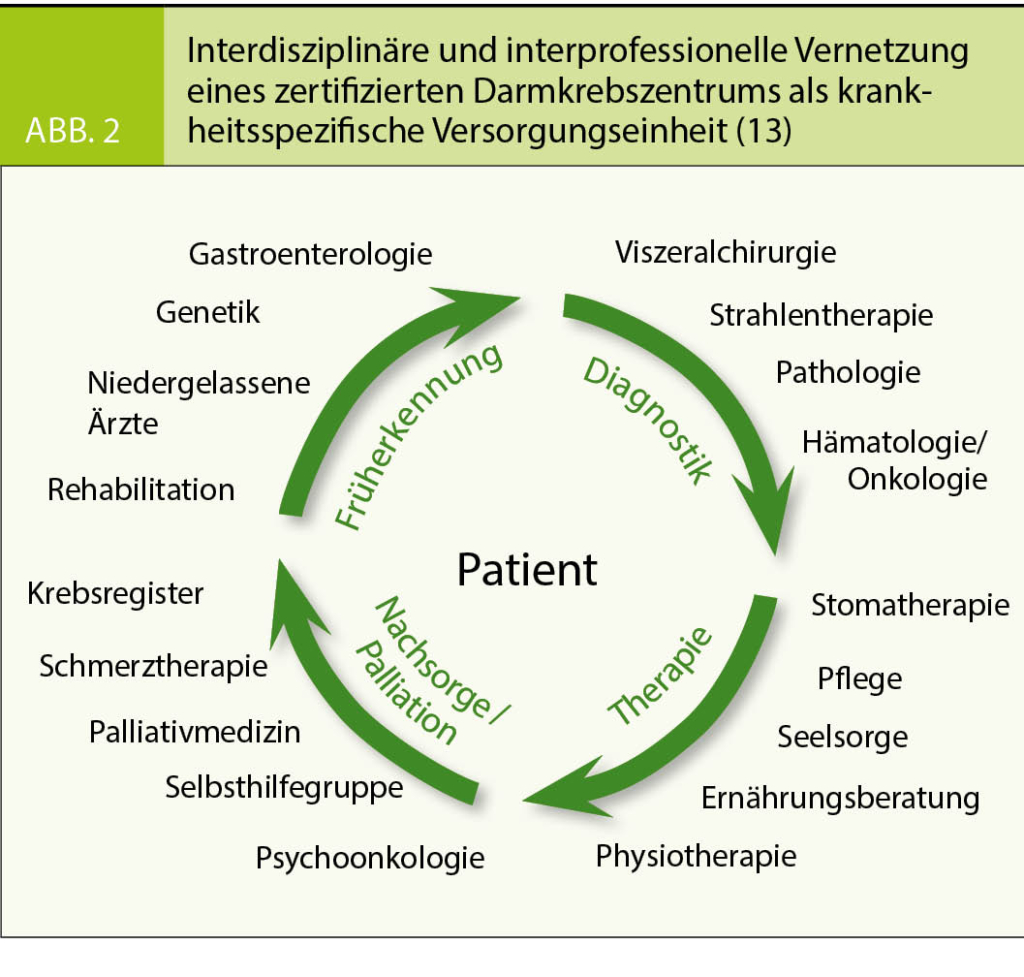
Eine Verbesserung der Prognose des kolorektalen Karzinoms kann nicht zuletzt durch den stadiengerechten Einsatz evidenzbasierter moderner chirurgischer und onkologischer Therapieverfahren erreicht werden. Um die Behandlungsergebnisse objektivierbar zu optimieren, setzen moderne Strategien zur flächendeckenden Steigerung der Versorgungsqualität auf das Konzept der Gründung von Darmkrebszentren. In diesen krankheitsspezifischen Netzwerken von qualifizierten und gemeinsam zertifizierten, multi- und interdisziplinären und ggf. standortübergreifenden Einrichtungen (Krankenhäuser, vertragsärztliche Versorgung, Rehabilitationseinrichtungen) werden transsektoral wirkende Struktureinheiten geschaffen. Sie umfassen die gesamte Versorgungskette für den Patienten mit Darmkrebs und erlauben, die aktuellen Erkenntnisse der evidenzbasierten Medizin umfassend in den klinischen Alltag zu implementieren. Zudem lassen sie die Überprüfung der korrekten Anwendung der Leitlinieninhalte durch externe Fachexperten in Form von Audits zu (Abb. 2).
Das steuernde Korrigieren bei analysierten Defiziten im Behandlungsprozess im Sinne eines «Plan-Do-Check-React»-Zyklus garantiert dabei die kontinuierliche fachliche und qualitative Weiterentwicklung (13). Die Qualität der Chirurgie wird als entscheidender Prognosefaktor angesehen, der mehr als 80% der Kurzzeitergebnisqualität garantiert und damit die Voraussetzung für eine entsprechende onkologische Langzeitergebnisqualität schafft. Die Qualität der multimodalen Chemo- und Strahlentherapie ist hingegen der wesentliche Faktor für die Beeinflussung der Langzeitprognose (13).
Einen wichtigen Aspekt zur Verbesserung der Behandlungsqualität mit konsekutiver Prognoseverbesserung stellt die Ergebnisdokumentation anhand von Kennzahlen dar. So zeigte eine Analyse von 31 055 operierten Patienten mit Kolonkarzinom aus 346 Kliniken in Deutschland, dass im Stadium UICC 3, in dem laut Leitlinien eine adjuvante Chemotherapie erforderlich ist, diese nur bei 72,4% der Patienten auch tatsächlich geplant wurde. In einer Auswertung der Krebsregister deutscher Tumorzentren an rund 100 000 Patienten erhielten sogar nur 61,2% der Patienten eine adjuvante Chemotherapie, die eine Verbesserung der 5-Jahres-Überlebensrate um 16% ermöglicht (13, 14). Sieht man die Divergenz in der Versorgungssituation zu den geforderten 80% geplanten Chemotherapien im Stadium UICC 3 der Deutschen Krebsgesellschaft, die übrigens auch die schweizerischen Tumorzentren zertifiziert, erkennt man die prognostische Bedeutung der Bildung zertifizierter Tumorzentren für die Behandlung des kolorektalen Karzinoms.
Zentrum für Gastroenterologie und Hepatologie
Vulkanplatz 8
8048 Zürich
fruehauf@zgh.ch
Der Autor war an der Entwicklung der Darm Check-App ohne finanzielle Interessen beteiligt, ansonsten hat er in
Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
- Mit der Screeningkoloskopie steht heute nicht nur eine Früherkennungs-, sondern eine echte Vorsorgeuntersuchung zur Verfügung, welche durch die Resektion von Polypen die Entwicklung und die Mortalität eines Karzinoms um bis zu 80% reduziert
- Patienten mit einem niedrigen Risiko für fortgeschrittene Polypen oder ein Karzinom können mit einem immunologischen Stuhltest untersucht werden, der allerdings alle 2 Jahre wiederholt werden muss und der bei positivem Befund eine Koloskopie erforderlich macht
- Durch Reduktion beeinflussbarer Risikofaktoren (z.B. Rauchstopp, Bewegung, Diät) kann das Risiko für die Entwicklung eines KRK um 11–23% gesenkt werden
- Mit Hilfe der neu verfügbaren Darm Check - App steht eine einfache Methode zur Verfügung, das individuelle KRK-Risiko auf Basis des Imperiale-Scores zu berechnen und im Sinne einer partizipativen Entscheidungsfindung (shared decision making) adäquate Massnahmen daraus abzuleiten
- Ein wichtiger Aspekt zur Verbesserung der chirurgischen und multimodalen Behandlungsqualität stellt die Zertifizierung von interdisziplinären Darmkrebszentren dar, welche die gesamte Versorgungskette für den Patienten mit Darmkrebs bereitstellen
1. Pendergrass CJ, Edelstein DL, Hylind LM, Phillips BT, Iacobuzio-Donahue C, Romans K, Griffin CA, Cruz-Correa M, Tersmette AC, Offerhaus GJ, Giardiello FM. Occurrence of Colorectal Adenomas in Younger Adults: An Epidemiologic Necropsy Study. Clin Gastroenterol Hepatol. 2008; 6(9):1011-5
2. Manser CN, Bachmann LM, Brunner J, Hunold F, Bauerfeind P, Marbet UA. Colonoscopy screening markedly reduces the occurrence of colon carcinomas and carcinoma-related death: a closed cohort study. Gastrointest Endosc. 2012; 76(1):110-7
3. Quintero E, Castells A, Bujanda L, Cubiella J, Salas D, Lanas Á, Andreu M, Carballo F, Morillas JD, Hernández C, Jover R, Montalvo I, Arenas J, Laredo E, Hernández V, Iglesias F, Cid E, Zubizarreta R, Sala T, Ponce M, Andrés M, Teruel G, Peris A, Roncales MP, Polo-Tomás M, Bessa X, Ferrer-Armengou O, Grau J, Serradesanferm A, Ono A, Cruzado J, Pérez-Riquelme F, Alonso-Abreu I, de la Vega-Prieto M, Reyes-Melian JM, Cacho G, Díaz-Tasende J, Herreros-de-Tejada A, Poves C, Santander C, González-Navarro A; COLONPREV Study Investigators. Colonoscopy versus fecal immunochemical testing in colorectal-cancer screening. N Engl J Med. 2012; 366(8):697-706
4. Meyerhardt JA, Mayer RJ. Systemic therapy for colorectal cancer. N Engl J Med. 2005; 352(5):476-87
5. Kirkegaard H, Johnsen NF, Christensen J, Frederiksen K, Overvad K, Tjønneland A. Association of adherence to lifestyle recommendations and risk of colorectal cancer: a prospective Danish cohort study. BMJ. 2010; 341:c5504
6. Friis S, Riis AH, Erichsen R, Baron JA, Sørensen HT. Low-Dose Aspirin or Nonsteroidal Anti-inflammatory Drug Use and Colorectal Cancer Risk: A Population-Based, Case-Control Study. Ann Intern Med. 2015; 163(5):347-55
7. Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA Jr, Kinzler KW. Cancer genome landscapes. Science. 2013; 339(6127):1546-58
8. Vogelstein B, Fearon ER, Hamilton SR, Kern SE, Preisinger AC, Leppert M, Nakamura Y, White R, Smits AM, Bos JL. Genetic alterations during colorectal-tumor development. N Engl J Med. 1988; 319(9):525-32
9. Imperiale TF, Monahan PO, Stump TE, Glowinski EA, Ransohoff DF. Derivation and Validation of a Scoring System to Stratify Risk for Advanced Colorectal Neoplasia in Asymptomatic Adults: A Cross-sectional Study. Ann Intern Med. 2015; 163(5):339-46
10. Lin JS, Piper MA, Perdue LA, Rutter CM, Webber EM, O’Connor E, Smith N, Whitlock EP. Screening for Colorectal Cancer: Updated Evidence Report and Systematic Review for the US Preventive Services Task Force. JAMA. 2016; 315(23):2576-94
11. Marbet UA, Bauerfeind P, Brunner J, Dorta G, Valloton JJ, Delcò F. Colonoscopy is the preferred colorectal cancer screening method in a population-based program. Endoscopy. 2008; 40(8):650-5
12. http://www.sggssg.ch/fileadmin/user_upload/Appendix_Screening_Koloskopie_2017_1.DE.pdf
13. Sahm M, Wesselmann S, Kube R, Schöffel N, Pross M, Lippert H, Kahl S. Der Prozess der Entwicklung von Zentren am Beispiel des Darmkrebszentrums Zentralbl Chir. 2013; 138(1):33-7
14. Pox C, Aretz S, Bischoff SC, Graeven U, Hass M, Heußner P, Hohenberger W, Holstege A, Hübner J, Kolligs F, Kreis M, Lux P, Ockenga J, Porschen R, Post S, Rahner N, Reinacher-Schick A, Riemann JF, Sauer R, Sieg A, Scheppach W, Schmitt W, Schmoll HJ, Schulmann K, Tannapfel A, Schmiegel W; Leitlinienprogramm Onkologie der AWMF; Deutschen Krebsgesellschaft e. V; Deutschen Krebshilfe e. V. S3-Leitlinie Kolorektales Karzinom Version 1.0 – Juni 2013 AWMF-Registernummer: 021/007OL Gastroenterol. 2013; 51(8):753-854
15. http://www.sggssg.ch/fileadmin/_migrated/content_uploads/Polypen_SGG_September_2014_DE_neu.pdf
16. http://www.sggssg.ch/fileadmin/_migrated/content_uploads/CRC_SGG_September_2014_DE_01.pdf).
der informierte @rzt
- Vol. 8
- Ausgabe 1
- Januar 2018