- Welche Normwerte gelten für Eisen?
Um Therapieentscheidungen zu treffen, werden oft Laborwerte erhoben. Diese sollen helfen, gesund von krank resp. therapiebedürftig von nicht-therapiebedürftig zu unterscheiden. In diesem Artikel wird die Sinnhaftigkeit von Normalwerten diskutiert und der Einsatz von Referenzintervallen resp. Berechnung von Wahrscheinlichkeiten erläutert. Am Beispiel von üblichen Eisenstoffwechselparametern werden ein paar praktische, alltägliche Fragestellungen diskutiert.
Sinn und Unsinn von Referenzintervallen
Referenzintervalle werden in einem aufwändigen und standardisierten Verfahren erhoben (1). Sie hängen von verschiedenen Faktoren ab wie Geschlecht, Rasse, Alter, allenfalls der prävalenten Population (z.B. die Bevölkerung im Einzugsgebiet des Testers), Eigenschaften der Analysenmethode (Gerät, Reagenzien) und vielem mehr. Deshalb variieren diese Werte oft sehr. Eine Projektgruppe der International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) versucht nun, die Methoden und Werte zu standardisieren oder wenigstens zu «harmonisieren», damit sie vergleichbarer werden. Es kommt auch darauf an, was der Arzt, Patient, Beamte, Versicherer, Jurist oder sogar die Gesellschaft mit dem Wert will. Will man keinen Kranken verpassen, so resultiert daraus, dass man den Wert tief ansetzt, aber gleichzeitig viele falsch Positive (Kranke) generiert. Will man nur schwer Kranke erfassen, setzt man den Wert höher an, womit aber viele, weniger stark Betroffene verpasst werden. War es früher zu Buddenbrocks (2) Zeiten nobel, blass, synkopisch und gemiedert zu sein, dürften tiefe Eisenwerte durchaus gesellschaftsfähig gewesen sein. In den USA will man kein «Redneck» (Bauer, Arbeiter, der viel im Freien ist) sein. Die Oberschicht leidet lieber an Vitamin-D-Mangel und ist auch blass, anämisch, eisendefizient. Vielleicht brauchen wir auch solide Normwerte, um uns gegen unsinnige Therapiewünsche der Patientinnen zu wehren. Gerade in der Schweiz findet eine übermässige Eisensubstitution (3) statt – die moderne Frau will 150% aktiv sein, schlank aber natürlich auch vegan. Die resultierenden Beschwerden wie Stress, Müdigkeit, Konzentrationsmangel und Leistungseinbruch, Depression sind unspezifisch und können auf viele Ursachen zurückgeführt werden. Oft sind sie psychogener Natur (4). Es ist aber viel einfacher, sich etwas Eisen einzuverleiben, am liebsten mit einer kurzen Injektion, und schon ist alles wieder besser.
Bayes’ Theorem und Serum-Ferritin
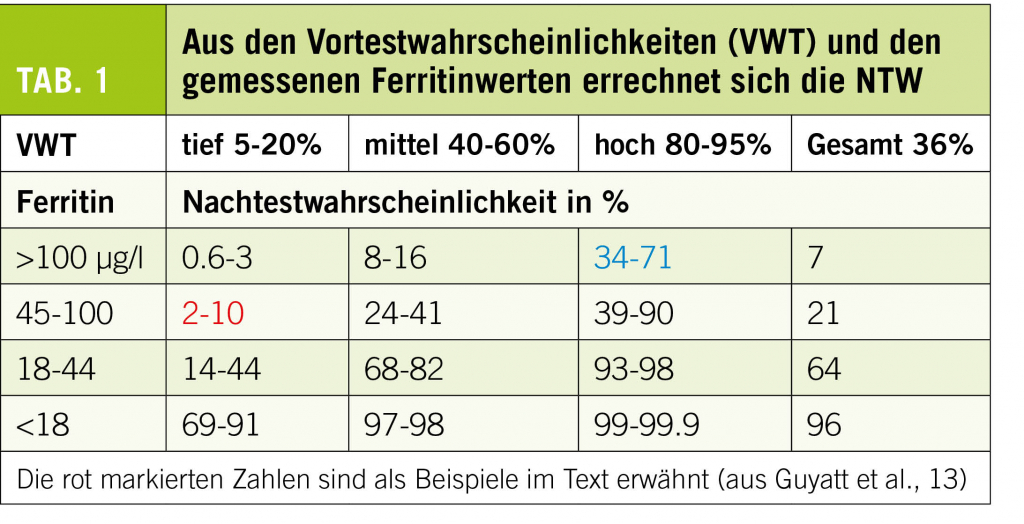
Spezifität und Sensitivität reichen für den klinischen Alltag nicht. Wollen wir unseren Patientinnen etwas Gutes tun, nehmen wir Vortestwahrscheinlichkeiten, machen einen Labortest auf einem guten Gerät und berechnen daraus die Nachtestwahrscheinlichkeit für das Vorliegen oder Fehlen einer Krankheit. Auf Neudeutsch PPV oder NPV (positive predictive value oder negative predictive value). Untenstehende Tabelle 1 eignet sich gut, das eben Gesagte am Eisenspeichermarker Ferritin zu demonstrieren. Je nach Vortestwahrscheinlichkeit (hier in % ausgedrückt) eines Patienten mit Verdachtssymptomen Eisenmangel und einem gemessenen Resultat lässt sich eine entsprechende Nachtestwahrscheinlichkeit berechnen, mit welcher dann auch ein Eisenmangel gefunden wird. Bei tiefer Vortestwahrscheinlichkeit ist selbst ein tiefes Ferritin seltener mit Eisenmangel (rot) assoziiert oder bei hoher Vortestwahrscheinlichkeit kann auch ein relativ hoher Ferritinwert noch mit einem Eisenmangel (blau) vergesellschaftet sein. Anstelle von % Wahrscheinlichkeit können auch Scores genommen werden.
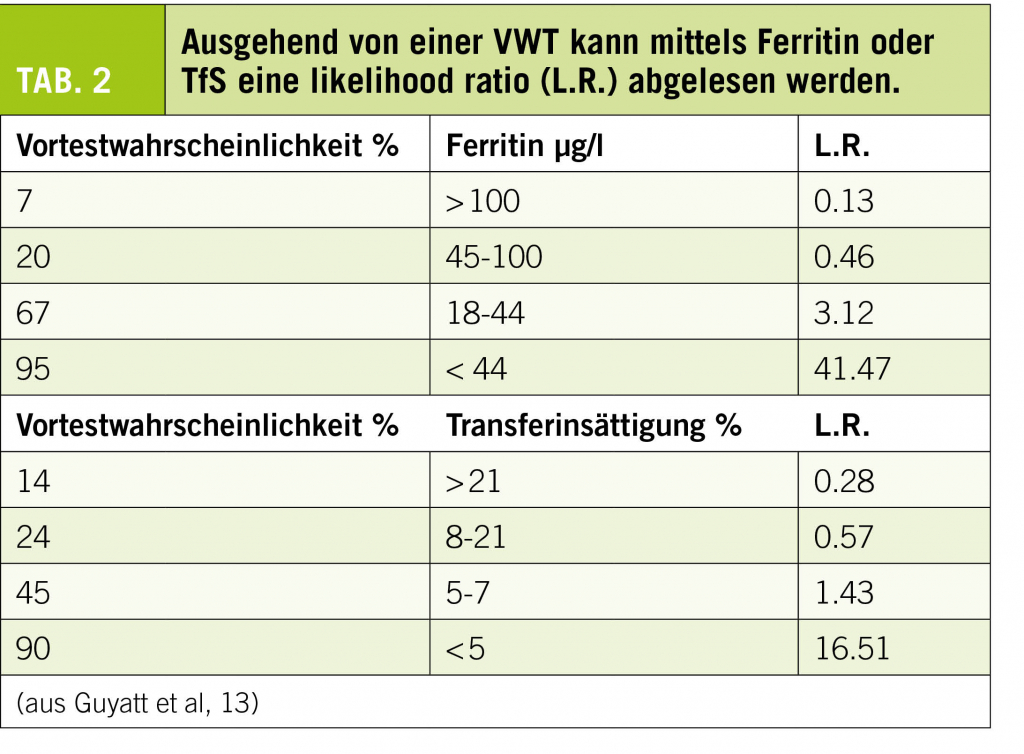
Hilfreich ist es, Wahrscheinlichkeiten als likelihood ratios (LR) auszudrücken. Tabelle 2 zeigt ein publiziertes Beispiel, in dem die LR eines Eisenmangels mittels Vortestwahrscheinlichkeit und Ferritinkonzentration oder Transferrinsättigung bestimmt wird. Als Faustregel gilt: LR-Werte über 5 (besser 10) oder unter 0.5 (lieber 0.1) sind als positiv respektive negativ zu betrachten (Tab. 2).
Wertigkeit von Eisenparametern
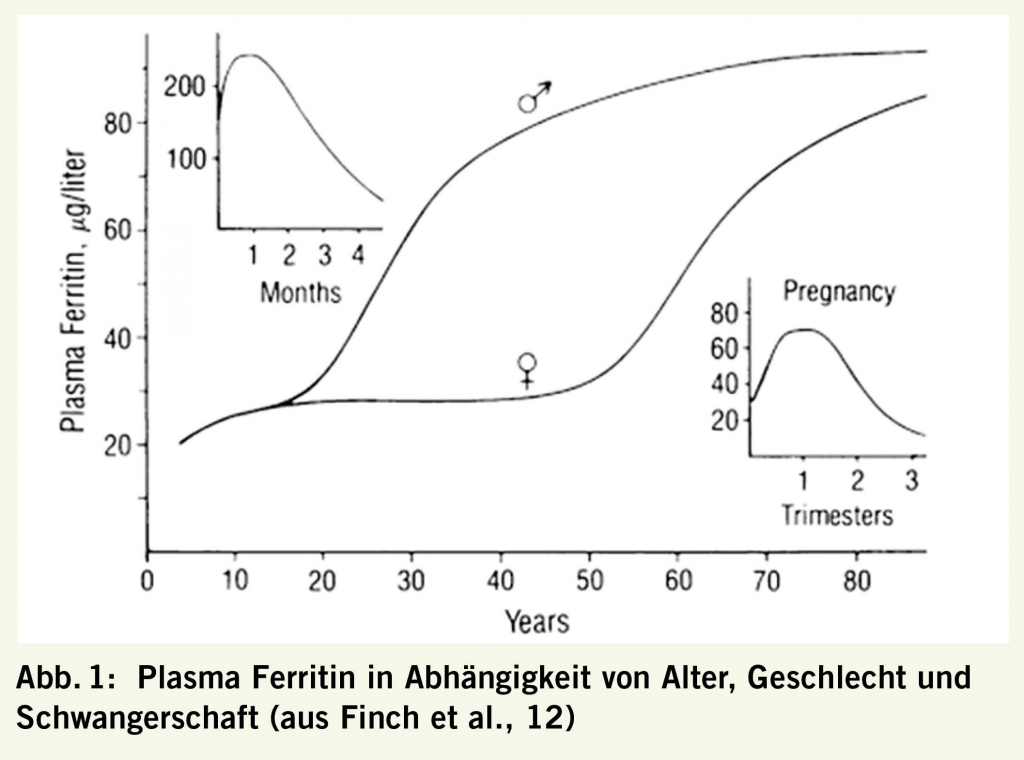
Es gibt eine Anzahl älterer und neuerer Eisenparameter, die gut validiert sind. Darunter zuvorderst Ferritin. Es ist ein Biomarker für das Speichereisen und nicht für funktionellen Eisenmangel und auch nicht ein Beweis für Eisenmangelanämie. Ferritin schwankt über Alter und Schwangerschaft sehr (Abb. 1).
Eine weitere Problematik besteht in der Tatsache, dass Ferritin ein positives Akutphasenprotein ist und bei Entzündungen ansteigt, was falsch negative Resultate gibt. Auch gibt es leichte Anstiege bei Leberschaden oder Erkrankungen des hämatopoietischen Systems, was ebenfalls zu falsch normalen Eisenspeicher-Resultaten führt. Man kann versuchen, mittels CRP eine Entzündung auszuschliessen. Thomas hat einen Plot publiziert (5) mit welchem diese Problematik gelöst werden soll. Es müssen aber weitere Parameter wie löslicher Transferrin Rezeptor (sTfR) gemessen werden. Anlehnend an eine Publikation von Fehr (6), weitere Studien und unsere Erfahrung sind bei Ferritin > 50 μg/l die Eisenspeicher ausreichend und bei Ferritin < 30 μg/l ungenügend gefüllt. Das gilt gleichermassen für Frauen und Männer, egal was die verschiedenen Labore als ihre Referenzwerte mitliefern. Dazwischen ist eine Grauzone. Für Kinder und Jugendliche haben wir in einem Konsensuspapier entsprechende Werte publiziert (7). Die Transferrin Sättigung (Transferrin und Fe2 +) hat auch ihren Platz in der Routinediagnostik. Die Präzision ist aber gering wegen der grossen zirkadianen und anderweitig bedingten Schwankung. Werte unter 20% sind mit leeren Eisenspeichern assoziiert (8). Zink-Protoporphyrin (ZnPP) ist ein guter Parameter, der aber bei uns wenig zum Einsatz kommt und wenig angeboten wird. ZnPP steigt bei Eisenmangel an, bleibt bei Thalassämien im Normalbereich und steigt bei Entzündungen nur wenig an. Es eignet sich deshalb zur Differenzierung mikrozytärer Anämien, wie Thalassämien und Anämien der chronischen Entzündung (ACD). Auch kann man ZnPP gut gebrauchen, um leere Eisenspeicher (Stadium 1 des Eisenmangels) vom funktionellen Eisenmangel ohne Anämie (Stadium 2) abzutrennen. ZnPP steigt erst im Stadium 2 über den Normwert an. Das volle Bild des Eisenmangels (Stadium 3) ist ja dann die Eisenmangelanämie (IDA) und die lässt sich bekanntlich ordentlich gut bestimmen (cave Pseudoanämie, Verdünnungsanämie bei Schwangerschaft, Herzinsuffizienz, Leistungssportlern, Infusionen, etc.). Der sTfR bringt in etwas dasselbe wie ZnPP, ist aber teuer und nicht standardisiert (verschiedene Werte je nach Hersteller). Neuer und allenfalls von Nutzen ist Hepcidin, ein Eisenregulator (9), der bei Eisenmangel sinkt und bei Entzündung ansteigt. Nützlich am ehesten bei der Differenzialdiagnose ACD vs. ACD plus IDA.
Laborseits sollte immer ein Hämatogramm bestimmt werden, am besten mit Retikulozytenzahl. So hat man eine gute Auskunft über die Hämatopoiese und kann Hämoglobin, MCV, RDW in die Eisenthematik mit einbeziehen.
Zusammenfassend gibt es leider nicht den Eisenparameter und den Normwert (das Referenzintervall), sondern klinische Einschätzung, Hantieren mit Wahrscheinlichkeiten und differenzialdiagnostische Überlegungen müssen konsequent angewendet werden. Es kommt letztlich immer darauf an, was man mit dem Wert erreichen will. Wir sprechen hier von Entscheidungswerten (decision values). Ab welchem Wert wird eine Massnahme ergriffen. Weiter hilfreich ist es auch, über die Zeit vom gleichen Patienten repetitiv denselben Parameter zu erheben. So muss eine Frau, die sich mit 15 μg/l Ferritin über Zeit absolut wohl fühlt nicht therapiert werden, selbst wenn dieser unter dem Referenzwert liegt. Erst bei einem noch tieferen Wert muss eine Therapie ins Auge gefasst werden. Wir sprechen bei dieser Methode von reference change value (10). Man legt so für jeden Patienten seine eigenen Referenzwerte fest. Es gibt dazu Berechnungsformeln, ab wann ein Unterschied zwischen 2 Messungen signifikant ist.
Der Therapie-Hype, Patienten mit Eisenmangel ohne Anämie (Stadium 2) zu behandeln, ist zweifelsohne ein Grund, sich mit den «Normwerten von Eisen» zu befassen. Es gibt zwar einige, teils auch neuere Studien (11), die das Vorkommen von funktionellem Eisenmangel (Stadium 2) aufzeigen und einen entsprechenden Nutzen durch Eisenzufuhr dokumentieren. Allerdings hat das in der Schweiz epidemische, kaum mehr rationale Formen angenommen, insbesondere die i.v.-Substitution. Gerade im Herbst liessen sich die Eisenspeicher ganz billig, angenehm und sehr effizient auffüllen. Man(n) und vor allem Frau esse doch dann und wann wieder eine Blutwurst. So kann dem Arzt (und der Patientin) der Normwert des Ferritins eigentlich Wurst sein.
LaboSalamin
Ave. du Rothorn 10, 3960 Sierre
s.brunner@labosalamin.ch
Private Universität im Fürstentum Liechtenstein
Dorfstrasse 24
FL-9495 Triesen
andreas.huber@ufl.li
Die Autoren haben im Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
- Referenzintervalle stellen aufwändig ermittelte Werte dar, die eine definierte Normal-Population beschreiben
- Hilfreich sind Entscheidungswerte, die Massnahmen unterstützen oder verhindern
- Mit dem Bayes-Theorem wird ausgehend von Vortestwahrscheinlichkeiten und dem aktuellen Messwert eine Nachtestwahrscheinlichkeit berechnet oder geschätzt
- Diverse Eisenparameter haben verschiedene Eigenschaften und erlauben unterschiedliche Aussagen
- Es gibt den Normwert und den Eisenparameter nicht
Literatur
1. Solberg HE, Stamm D. IFCC recommendation: The theory of reference values. Part 4. Control of analytical variation in the production, transfer and application of reference values. J Automat Chem 1991;13(5):231–4. doi: 10.1155/S146392469100038X.
2. Thomas Mann. Buddenbrooks; 1901.
3. Giger M, Achermann R. Ambulante Eisensubstitution in der Schweiz – Kostensteigerung infolge venöser Applikation. Z Evid Fortbild Qual Gesundhwes 2013;107(4-5):320–6. doi: 10.1016/j.zefq.2012.12.023.
4. Baumann K, Krayenbühl P. Müdigkeit. Praxis (Bern 1994) 2009; 98(9):465–71. doi: 10.1024/1661-8157.98.9.465.
5. Thomas C, Kirschbaum A, Boehm D, Thomas L. The diagnostic plot: a concept for identifying different states of iron deficiency and monitoring the response to epoetin therapy. Med Oncol 2006;23(1):23–36. doi: 10.1385/MO:23:1:23.
6. J. Fehr, B. Favrat, B. Schleiffenbaum, P. A. Krayenbühl, C. Kapanci, F. von Orelli. Diagnostic et traitement de la carence en fer sans anémie. Rev Med Suisse 2009;5:2229-34
7. Clénin G, Cordes M, Huber A, Schumacher YO, Noack P, Scales J et al. Iron deficiency in sports – definition, influence on performance and therapy. Swiss Med Wkly 2015;145:w14196. doi: 10.4414/smw.2015.14196.
8. Elsayed ME, Sharif MU, Stack AG. Transferrin Saturation: A Body Iron Biomarker. Adv Clin Chem 2016;75:71–97. doi: 10.1016/bs.acc.2016.03.002.
9. Rishi G, Wallace DF, Subramaniam VN. Hepcidin: regulation of the master iron regulator. Biosci Rep 2015;35(3). doi: 10.1042/BSR20150014.
10. O’Kane MJ, Lopez B. Explaining laboratory test results to patients: what the clinician needs to know. BMJ 2015;351:h5552. doi: 10.1136/bmj.h5552.
11. Drygalski A von, Adamson JW. Ironing out fatigue. Blood 2011;118(12):3191–2. doi: 10.1182/blood-2011-07-366120.
12. Finch CA, Bellotti V, Stray S, Lipschitz DA, Cook JD, Pippard MJ et al. Plasma ferritin determination as a diagnostic tool. West J Med 1986; 145(5):657–63.
13. Guyatt GH, Patterson C, Ali M, Singer J, Levine M, Turpie I et al. Diagnosis of iron-deficiency anemia in the elderly. Am J Med 1990; 88(3):205–9.
der informierte @rzt
- Vol. 9
- Ausgabe 1
- Januar 2019