- Aspirin in der Schwangerschaft
Niedrig dosiertes Aspirin wird zur Prävention von Schwangerschaftskomplikationen eingesetzt, welche mit einer Plazentainsuffizienz einhergehen. Aspirin wirkt vasodilatativ, antithrombotisch und antiinflammatorisch und somit den pathophysiologischen Prozessen der Plazentadysfunktion entgegen. Die am besten untersuchte Indikation ist die Prävention der Präeklampsie. In Kombination mit niedermolekularem Heparin wird Aspirin zudem zur Abortprophylaxe beim Antiphospholipidsyndrom eingesetzt.
Low dose aspirin is recommended for the prevention of adverse pregnancy outcomes related to placental dysfunction. Aspirin favours placentation by its vasodilating, anti-thrombotic and anti-inflammatory properties. Aspirin is well established for the prevention of preeclampsia. In combination with low molecular heparin, it is used for the prophylaxis of miscarriage in patients with antiphospholipid syndrome.
Key Words: Aspirin, Preeclampsia, Prevention, Screening
Die Präeklampsie (PE) ist eine plazenta-vermittelte hypertensive Schwangerschaftserkrankung mit Multisystembeteiligung. In Europa beträgt die Inzidenz 2%. Weltweit führt die PE jährlich zu ca. 70’000 maternalen Todesfällen. Zu den maternalen Langzeitfolgen zählt ein erhöhtes Risiko für kardiovaskuläre und zentralnervöse Erkrankungen (1). Auf der Seite des Neugeborenen sind die gesundheitlichen und ökonomischen Folgen der Frühgeburtlichkeit hervorzuheben. Hierzu gehören teils lebenslange Konsequenzen, wie eine verzögerte neurologische Entwicklung, arterielle Hypertonie, renale Erkrankungen oder metabolische Störungen (2). Eine kausale Therapie ist bis anhin nicht bekannt. Niedrig dosiertes Aspirin (low dose aspirin, LDA) wirkt vasodilatativ, antithrombotisch und anti-inflammatorisch und wird erfolgreich zur Prophylaxe bei erhöhtem PE-Risiko eingesetzt (1). LDA ist zudem zur Reduktion das Abortrisikos bei Frauen mit Antiphospholipidsyndrom (APLS) indiziert (3). Bislang gibt es keine klare Evidenz für einen positiven Effekt auf die Rate an Wachstumsrestriktion (IUWR), Frühgeburtlichkeit oder intrauterinem Fruchttod (IUFT).
ASPIRIN®: Acetylsalicylsäure (ASS)
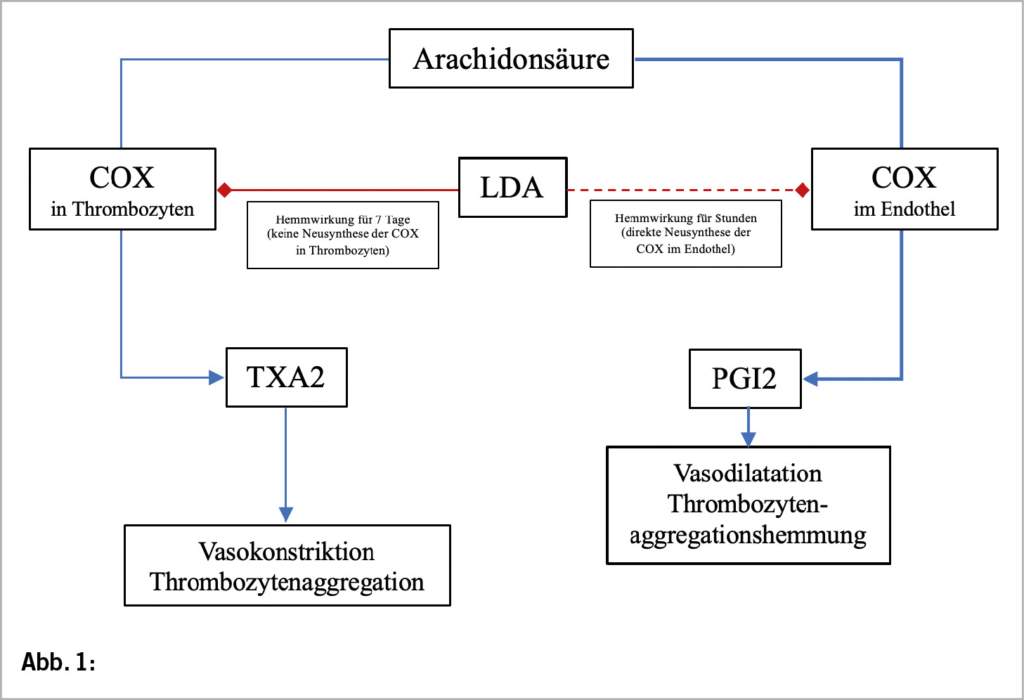
Die Salicylsäure ist ein Extrakt aus Weidenrinden und wurde bereits im 18. Jahrhundert als Arznei gegen Fieber oder Schmerzen verwendet. ASS hemmt irreversibel die Funktion des Enzyms Cyclooxygenase (COX), welches die Produktion von Prostazyklin (PGI2) im Endothel und Thromboxan (TXA2) in den Thrombozyten reguliert (4). PGI2 hat eine vasodilatative und antithrombotische Wirkung, TXA2 hat den gegenteiligen Effekt. Die Wirkung von ASS ist dosisabhängig. Eine Dosis bis 300mg/Tag führt zu einer anhaltenden Hemmung der TXA2-Synthese, ohne nennenswerten Einfluss auf PGI2, mit dem Nettoeffekt einer Vasodilatation und Thrombozytenaggregationshemmung (Abb. 1). Höhere Dosen führen zu einer Blockade der Prostaglandinproduktion und einer analgetischen und antipyretischen Wirkung (5).
Wirkung in der Schwangerschaft
Der Plazentainsuffizienz liegen eine abnormale Vaskularisation und Trophoblastinvasion und dadurch gestörte Umwandlung der plazentaren Spiralarterien zugrunde. Es kommt zu einer verminderten uteroplazentaren Perfusion und folglich zu einer chronischen Hypoxie und oxidativem Stress. Dies führt zur Ausschüttung von proinflammatorischen und anti-angiogenetischen Faktoren in den maternalen Kreislauf mit einer systemischen Entzündungsreaktion und Endotheldysfunktion (6). Das TXA2/PGI2-Gleichgewicht wird gestört (7). Niedrig dosiertes Aspirin (≤150mg/Tag) wirkt dieser Imbalance entgegen (2), hat diverse antiinflammatorische Effekte (5) und einen regulatorischen Einfluss auf (anti-)angiogenetische Faktoren (8).
Indikationen in der Schwangerschaft
Präeklampsie
Erkenntnisse aus randomisierten Studien zeigen, dass die Gabe von LDA das Risiko einer PE reduziert. Abhängig von Dosierung, Startzeitpunkt, untersuchtem Risikokollektiv und Studienendpunkten, variieren die Angaben zur Risikoreduktion zwischen 15-90%.
Ein Cochrane-Review fand eine Risikoreduktion von 17% bei LDA-Dosierungen von 50-150mg täglich, Therapiestart bis zur 32. SSW und sehr heterogenem Risikokollektiv (9). Gemäss dem ASPRE-Trial beträgt die Risikoreduktion der frühen PE (≤37. SSW) ca. 60% bei einer Dosierung von 150mg täglich, Therapiestart vor der 16. SSW, für Schwangere mit hohem PE-Risiko gemäss Screening-Algorithmus. Das Risiko einer PE ≤34. SSW liess sich um bis zu 90% reduzieren, bei einer Compliance ≥90% und fehlender vorbestehender Hypertonie (10). Ein signifikanter Einfluss auf die späte PE (>37. SSW) liess sich nicht nachweisen (11).
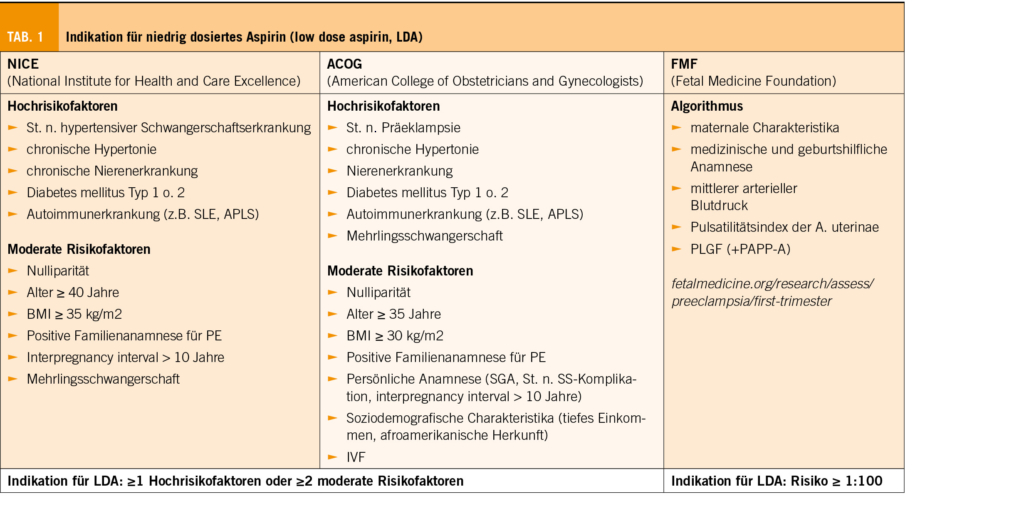
Die Pathophysiologie der frühen PE scheint auf der fehlerhaften Invasion der Spiralarterien zu beruhen. Bei der späten Form steht ein mangelndes Wachstum, der bis anhin normal entwickelten Plazenta, in Relation zu der vom Feten benötigten Blutzufuhr im Vordergrund (12). Internationale Guidelines empfehlen, die Gabe von LDA vor der 16. SSW und somit vor Abschluss der Plazentation zu initiieren (1, 14, 15). LDA scheint durch seine vasodilatativen und antiinflammatorischen Effekte auch nach abgeschlossener Plazentation wirksam zu sein und zu einer moderaten Reduktion der PE-Rate zu führen (13). Als Zeitpunkt zur Beendigung der Therapie hat sich die 36. SSW etabliert (1). LDA soll aufgrund chronobiologischer Faktoren abends eingenommen werden (16). Zur Identifikation des Risikokollektivs empfehlen ACOG und NICE ein auf anamnestischen Risikofaktoren basierendes PE-Screening (14, 15). Die Fetal Medicine Foundation (FMF) hat ein Screening mittels Algorithmus erarbeitet, welcher zusätzlich den mittleren arteriellen Blutdruck, den Pulsatilitätsindex der Uterinarterien und den placental growth factor (PlGF) berücksichtigt. Die Einnahme von LDA ist bei einem PE-Risiko ≥1:100 empfohlen (17) (Tab. 1). Diese Risikokalkulation ermöglicht eine Detektionsrate der frühen PE von ca. 75% im Vergleich zu ca. 40% bei einer Risikoerfassung mittels Anamnese (gemäss NICE-Guidelines) allein. Dies bei einer Falsch-positiv-Rate von jeweils 10%. Mittels dem von der ACOG empfohlenen anamnesebasierten Screening werden 94% der Präeklampsien vor der 32. SSW entdeckt, jedoch mit einer Falsch-positiv-Rate von knapp 65% (18). Gemäss dem Expertenbrief der SGGG ist die Durchführung des Screenings mittels FMF-Algorithmus empfohlen (19).
Wachstumsretardierung und Frühgeburt
Der Grossteil der vorhandenen Literatur zum Thema Prävention der IUWR und der Frühgeburt bezieht sich auf Schwangere mit hohem PE-Risiko. Die Definitionen von SGA und IUWR variieren erheblich und nicht alle Studien unterscheiden zwischen spontaner und iatrogener Frühgeburt. In Anbetracht der gemeinsamen pathophysiologischen Grundlagen der PE und der IUWR scheint eine protektive Wirkung von LDA plausibel. Bei Schwangerschaften mit vorzeitigem Blasensprung oder vorzeitigen Kontraktionen zeigt sich eine abnormale Plazentation mit pathophysiologisch ähnlichem Muster wie bei der PE (20). Die AWMF empfiehlt aktuell die Gabe von LDA bei erhöhtem Risiko für eine IUWR aufgrund einer Plazentainsuffizienz (21). Ob LDA die Rate an spontanen, nicht PE-assoziierten Frühgeburten reduzieren kann, ist bis anhin nicht geklärt.
Antiphospholipidsyndrom (APLS) und Aborte
LDA ist in Kombination mit niedermolekularem Heparin bei Frauen mit APLS zur Abort- und PE-Prophylaxe wirksam und empfohlen, erfolgt ab positivem SS-Test und führt zu einer Erhöhung der Lebendgeburtenrate (3). Bei Frauen mit idiopathischen wiederholten Spontanaborten konnte ein solcher Effekt nicht nachgewiesen werden (22). Gemäss dem Cochrane Review 2016 gibt es keine Evidenz für den Einsatz von LDA zur Verbesserung des Outcomes durch Reproduktionsmedizin (IVF) entstandener Schwangerschaften (23).
Mehrlingsschwangerschaften
Frauen mit Mehrlings-SS sind im Vergleich zu Einlings-SS einem höheren PE-Risiko ausgesetzt (RR 3.0) (1). Der FMF-Screening-Algorithmus kann auch bei Mehrlings-SS angewendet werden. Die Detektionsrate beträgt 97-100%, bei jedoch sehr hoher «Screen Positive Rate» von 75% (17). Der Nutzen von LDA zur PE-Prävention in Mehrlings-SS ist bisher nicht eindeutig belegt (2).
Sicherheit in der Schwangerschaft
Ein teratogener Effekt von Aspirin wird erst ab einer täglichen Dosis von 650mg beschrieben. Ein vorzeitiger Verschluss des Ductus arteriosus, eine fetale Nierenfunktionseinschränkung, fetale intrakranielle Blutungen oder andere fetale Komplikationen wurden unter LDA nicht beobachtet (5, 9, 11, 24, 25). Präpartale oder postpartale Blutungen >500ml sind je nach Literaturquelle nicht (11) oder mit nur gering erhöhter Inzidenz (9) zu erwarten. Es gibt Hinweise für eine nicht statistisch signifikant erhöhte Rate an vorzeitigen Plazentalösungen, vor allem bei LDA-Beginn nach der 16. SSW (2, 24).
Als Kontraindikation für eine LDA-Gabe gelten gemäss Arzneimittelkompendium eine Überempfindlichkeit auf Salicylate oder andere Entzündungshemmer, Gerinnungsstörungen mit erhöhter Blutungsneigung sowie eine schwere Leberfunktionsstörung, Niereninsuffizienz oder dekompensierte Herzinsuffizienz.
Copyright bei Aerzteverlag medinfo AG
Frauenklinik Kantonsspital Aarau
Tellstrasse 25
5001 Aarau
Chefärztin Geburtshilfe und Perinatalmedizin Kantonsspital Aarau
Tellstrasse 10
5000 Aarau
monya.todesco@ksa.ch
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ LDA unterstützt durch seine vasodilatative, antithrombotische und antiinflammatorische Wirkung eine physiologische Plazentaentwicklung und -funktion.
◆ LDA hat eine präventive Wirkung auf die Entwicklung der Präeklampsie, insbesondere der frühen Form.
◆ Die effektivste PE-Prophylaxe besteht in einer abendlichen Einnahme von 100-150mg LDA mit Beginn vor der 16. SSW bei Einlingsschwangerschaften mit einem PE-Risiko ≥1:100 gemäss FMF-Algorithmus.
◆ Beim APLS wird LDA in Kombination mit Heparin zur Abort und PE-Prophylaxe eingesetzt.
◆ Ob und in welcher Form LDA das PE-Risiko bei Mehrlingsschwangerschaften und die Rate an IUFT, Frühgeburten und IUWR senken kann, benötigt weiterer Forschung.
1. AWMF, Hypertensive Schwangerschaftserkrankungen: Diagnostik und Therapie, Version 1.1, 2019, https://register.awmf.org/de/leitlinien/detail/015-018
2. Rolnik DL, Nicolaides KH, Poon LC. Prevention of preeclampsia with aspirin. Am J Obstet Gynecol. 2022 Feb;226(2S):S1108-S1119. doi: 10.1016/j.ajog.2020.08.045. Epub 2020 Aug 21. PMID: 32835720.
3. Erkan D., Ortel T. (2023). Management of antiphospholipid syndrome. UpToDate. https://www.uptodate.com/contents/management-of-antiphospholipid-syndrome
4. Abramson S. B. (2023). Aspirin: Machanism of action, major toxicities, and use in rheumatic disease. UpTpDate. https://www.uptodate.com/contents/aspirin-mechanism-of-action-major-toxicities-and-use-in-rheumatic-diseases
5. Atallah, A., Lecarpentier, E., Goffinet, F. et al. Aspirin for Prevention of Preeclampsia. Drugs 77, 1819–1831 (2017). https://doi.org/10.1007/s40265-017-0823-0 US Preventive Services Task Force. Aspirin Use to Prevent Preeclampsia and Related Morbidity and Mortality: US Preventive Services Task Force Recommendation Statement. JAMA. 2021;326(12):1186–1191. doi:10.1001/jama.2021.14781
6. Cadavid Angela P. The Mechanism of Action Revisited in the Context of Pregnancy Complications. Frontiers in Immunology 8 (2017). DOI=10.3389/fimmu.2017.00261
7. Walsh SW, Strauss JF 3rd. The Road to Low-Dose Aspirin Therapy for the Prevention of Preeclampsia Began with the Placenta. Int J Mol Sci. 2021 Jun 29;22(13):6985. doi: 10.3390/ijms22136985. PMID: 34209594; PMCID: PMC8268135.
8. Loussert L, Vidal F, Parant O, Hamdi SM, Vayssiere C, Guerby P. Aspirin for prevention of preeclampsia and fetal growth restriction. Prenat Diagn. 2020 Apr;40(5):519-527. doi: 10.1002/pd.5645. Epub 2020 Feb 3. PMID: 31955436
9. Duley L, Meher S, Hunter KE, Seidler AL, Askie LM. Antiplatelet agents for preventing pre-eclampsia and its complications. Cochrane Database Syst Rev. 2019 Oct 30;2019(10):CD004659. doi: 10.1002/14651858.CD004659.pub3. PMID: 31684684; PMCID: PMC6820858.
10. Wright D, Poon LC, Rolnik DL, Syngelaki A, Delgado JL, Vojtassakova D, de Alvarado M, Kapeti E, Rehal A, Pazos A, Carbone IF, Dutemeyer V, Plasencia W, Papantoniou N, Nicolaides KH. Aspirin for Evidence-Based Preeclampsia Prevention trial: influence of compliance on beneficial effect of aspirin in prevention of preterm preeclampsia. Am J Obstet Gynecol. 2017 Dec;217(6):685.e1-685.e5. doi: 10.1016/j.ajog.2017.08.110. Epub 2017 Sep 6. PMID: 28888591.
11. Rolnik DL, Wright D, Poon LC, et al. Aspirin versus placebo in pregnancies at high risk for preterm preeclampsia. N Engl J Med 2017;377: 613–22.
12. Uzan J, Carbonnel M, Piconne O, Asmar R, Ayoubi JM. Pre-eclampsia: pathophysiology, diagnosis, and management. Vasc Health Risk Manag. 2011;7:467-74. doi: 10.2147/VHRM.S20181. Epub 2011 Jul 19. PMID: 21822394; PMCID: PMC3148420.
13. Roberge S, Nicolaides K, Demers S, Hyett J, Chaillet N, Bujold E. The role of aspirin dose on the prevention of preeclampsia and fetal growth restriction: systematic review and meta-analysis. Am J Obstet Gynecol 2017;216:110-120.e6
14. Hypertension in pregnancy: diagnosis and management. London: National Institute for Health and Care Excellence (NICE); 2019 Jun 25. PMID: 31498578.
15. Low-dose aspirin use for the prevention of preeclampsia and related morbidity and mortality. ACOG Practice Advisory. 2022. https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2021/12/low-dose-aspirin-use-for-the-prevention-of-preeclampsia-and-related-morbidity-and-mortality
16. Diana E. Ayala, Rafael Ucieda & Ramón C. Hermida (2013) Chronotherapy With Low-Dose Aspirin for Prevention of Complications in Pregnancy, Chronobiology International, 30:1-2, 260-279, DOI: 10.3109/07420528.2012.717455
17. Francisco C, Wright D, Benkő Z, Syngelaki A, Nicolaides KH. Competing-risks model in screening for pre-eclampsia in twin pregnancy according to maternal factors and biomarkers at 11-13 weeks’ gestation. Ultrasound Obstet Gynecol. 2017 Nov;50(5):589-595. doi: 10.1002/uog.17531. Epub 2017 Sep 25. PMID: 28556556.
18. O’Gorman N, Wright D, Poon LC, Rolnik DL, Syngelaki A, de Alvarado M, Carbone IF, Dutemeyer V, Fiolna M, Frick A, Karagiotis N, Mastrodima S, de Paco Matallana C, Papaioannou G, Pazos A, Plasencia W, Nicolaides KH. Multicenter screening for pre-eclampsia by maternal factors and biomarkers at 11-13 weeks’ gestation: comparison with NICE guidelines and ACOG recommendations. Ultrasound Obstet Gynecol. 2017 Jun;49(6):756-760. doi: 10.1002/uog.17455. Erratum in: Ultrasound Obstet Gynecol. 2017 Dec;50(6):807. PMID: 28295782.
19. SGGG, Risikospezifizierung Präeklampsie, No57, 02/2019
20. Berger R, Kyvernitakis I, Maul H. Spontaneous Preterm Birth: Is Prevention with Aspirin Possible? Geburtshilfe Frauenheilkd. 2021 Mar;81(3):304-310. doi: 10.1055/a-1226-6599. Epub 2021 Jan 28. PMID: 33692591; PMCID: PMC7938936.
21. AWMF, S2k-Leitlinie Intrauterine Wachstumsrestriktion, Version 1.0, 2016, https://register.awmf.org/de/leitlinien/detail/015-080
22. de Jong PG, Kaandorp S, Di Nisio M, Goddijn M, Middeldorp S. Aspirin and/or heparin for women with unexplained recurrent miscarriage with or without inherited thrombophilia. Cochrane Database Syst Rev. 2014 Jul 4;2014(7):CD004734. doi: 10.1002/14651858.CD004734.pub4. PMID: 24995856; PMCID: PMC6769058.
23. Siristatidis CS, Basios G, Pergialiotis V, Vogiatzi P. Aspirin for in vitro fertilisation. Cochrane Database of Systematic Reviews 2016, Issue 11. Art. No.: CD004832. DOI: 10.1002/14651858.CD004832.pub4
24. US Preventive Services Task Force. Aspirin Use to Prevent Preeclampsia and Related Morbidity and Mortality: US Preventive Services Task Force Recommendation Statement. JAMA. 2021;326(12):1186–1191. doi:10.1001/jama.2021.14781
25. August P., Jeyabalan A. (2023). Preeclampsia: Prevention. UpToDate. https://www.uptodate.com/contents/preeclampsia-prevention
info@gynäkologie
- Vol. 13
- Ausgabe 5
- Oktober 2023