- Der sonographisch kleine Fetus
Im klinischen Alltag stellt der sonographisch kleine Fetus eine Herausforderung dar. Es ist wichtig zu unterscheiden, ob es sich um einen konstitutionell kleinen Fetus (small for gestational age, SGA) oder um eine fetale Wachstumsrestriktion (fetal growth restriction, FGR) handelt, die eine potenzielle Gefährdung darstellt. Die Definitionen der FGR variieren zwischen verschiedenen Leitlinien und Autoren. Die Diagnose wird im klinischen Alltag oft erst nach der Geburt festgestellt. Insbesondere die Unterscheidung zwischen früher und später FGR ist in den Fokus aktueller Studien gerückt. Diese beiden Formen werden heute fast als unterschiedliche Entitäten betrachtet, da sie sich in ihren klinischen Merkmalen, den Diagnosekriterien, dem Schweregrad und dem Management unterscheiden. Der Artikel gibt einen Überblick über die aktuellen evidenzbasierten Empfehlungen zum FGR, zur Diagnostik, zum Management und zum optimalen Entbindungszeitpunktes. Die wichtigsten Forschungsschritte zum Thema FGR der letzten zwei Jahrzehnte werden dargestellt. Der retardierte Fetus mit v.a. genetische und/oder kongenitale Fehlbildung stellt eine eigenständige Gruppe dar und ist nicht Teil dieses Artikels.
In clinical practice, the small sonographic fetus presents a common challenge. It is of great importance to distinguish between a simply small fetus (small for gestational age, SGA) and a fetal growth restriction (FGR), which poses a potential risk. Definitions of FGR vary between different guidelines and authors. In different clinical settings the diagnosis is often made only postnatally. Especially the differentiation between early and late FGR has become the focus of many recent studies. These two forms are almost considered different entities due to the variation in clinical presentation, diagnostic criteria, severity, and management. This article aims to provide an overview of the current evidence-based recommendations in FGR, the diagnosis, management, and optimal time of delivery. We present the most important research in the field FGR over the last 20 years. The growth retarded fetus with suspected genetic disease or congenital malformation is an extra group and not part of this article.
Keywords: SGA Small for gestational age, FGR Fetal growth retardation, early and late FGR, Doppler
Hintergrund
Die Inzidenz des fetalen Wachstumsrestriktion (fetal growth restriction, FGR) liegt bei ca. 5–8 % aller Schwangerschaften und kann zu einer erheblichen perinatalen Morbidität und Mortalität führen (1–8). Die frühe intrauterine Prägung führt zu einem Risiko für kardiovaskulären Erkrankungen im Erwachsenenalter wie arterielle Hypertonie, koronare Herzerkrankung, metabolisches Syndrom, Insulinresistenz und Diabetes mellitus (9, 10).
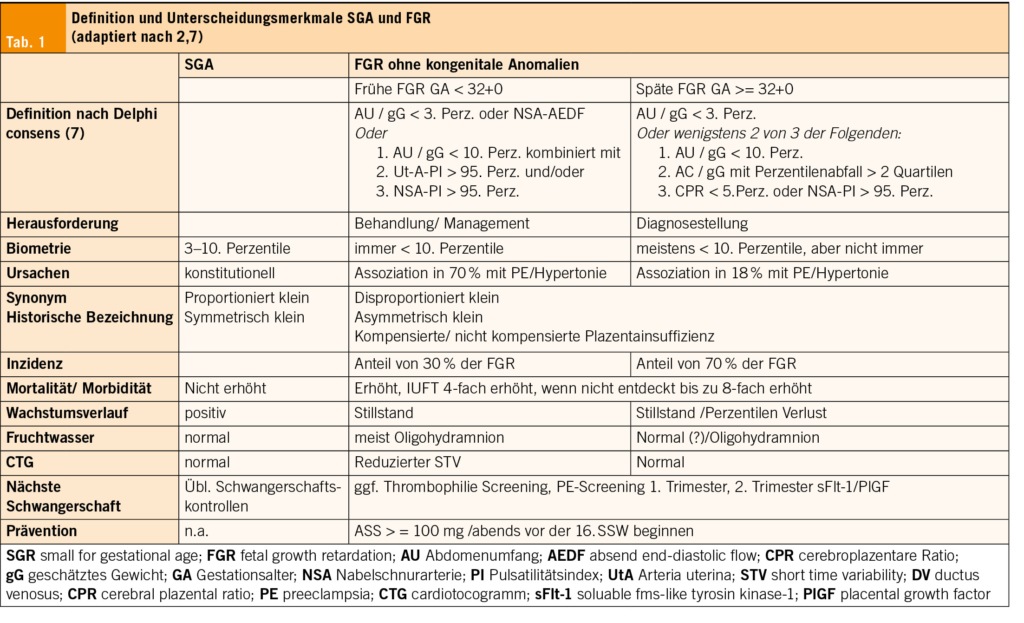
Die Herausforderung der FGR besteht in der pränatalen Erkennung des Wachstumsrückstandes. Ein Fetus gilt als wachstumsretardiert, wenn er sein genetisches Wachstumspotenzial nicht erreicht. Der «small for gestational age» (SGA) Fetus wächst auf seiner Perzentilenkurve und ist konstitutionell (d. h. anlagebedingt) klein. Der FGR-Fetus gilt als eine pathologische Variante, erreicht dieses Potenzial nicht und hat im Vergleich zum SGA eine erhöhte perinatale Morbidität, Mortalität und Langzeitfolgen. Besonders die späten fetalen Wachstumsretardierungen werden nur in der Hälfte der Fälle erkannt. Eine frühzeitige Diagnose einer FGR und das richtige Management können die perinatale Morbidität und Mortalität deutlich reduzieren (11-13). Etwa 30 % der intrauterinen Fruchttode sind mit FGR assoziiert und könnten unter Umständen verhindert werden (14) (Tab. 1).
Die Definition einer FGR ist je nach Autor und in internationalen Leitlinien verschieden. Die Empfehlungen zum Monitoring und zum Festlegen des Entbindungszeitpunktes bei FGR variieren erheblich.
Ziel dieses Artikels ist es durch eine Verbesserung der pränatalen Diagnose der FGR das Management und die Therapie entsprechend anzupassen und so die durch die FGR bedingte Morbidität und Mortalität zu senken.
Definition
Die häufigst verwendete Definition der fetalen Wachstumsrestriktion (FGR) stammt aus einem Delphi Verfahren von 2016 (Tab. 1) und wird in vielen Leitlinien zur Diagnostik und Management von SGA und FGR, angewendet (2, 7). Sie basiert auf einer Kombination aus fetalem Schätzgewicht und abnormen Dopplern der Arteria uterina und Arteria umbilicalis (NSA) sowie der Arteria cerebri media (MCA). Es wird zwischen früher (< 32. Schwangerschaftswoche (SSW)) und später FGR (>32. SSW) unterschieden, da sich diese in Schweregrad, Ursachen, diagnostischen Kriterien und Management deutlich unterscheiden (7).
Die Unterscheidung zwischen SGA und FGR ist wichtig, aber klinisch oft schwierig. Um einen Wachstumsverlauf zu beurteilen, ist eine Intervallbeurteilung zur Diagnose einer FGR notwendig. Sie wird ergänzt durch biophysikalische Parameter wie Doppler-Untersuchungen und Biomarker (8).
Feten unterhalb der 3. Perzentile haben sowohl als FGR und als SGA das höchste Risiko für einen intrauterinen Fruchttod und eine per se hohe perinatale Morbidität (15). Die ISUOG-Guideline klassifiziert Feten unterhalb der 3. Perzentile immer als wachstumsretardiert (2).
Pathophysiologie
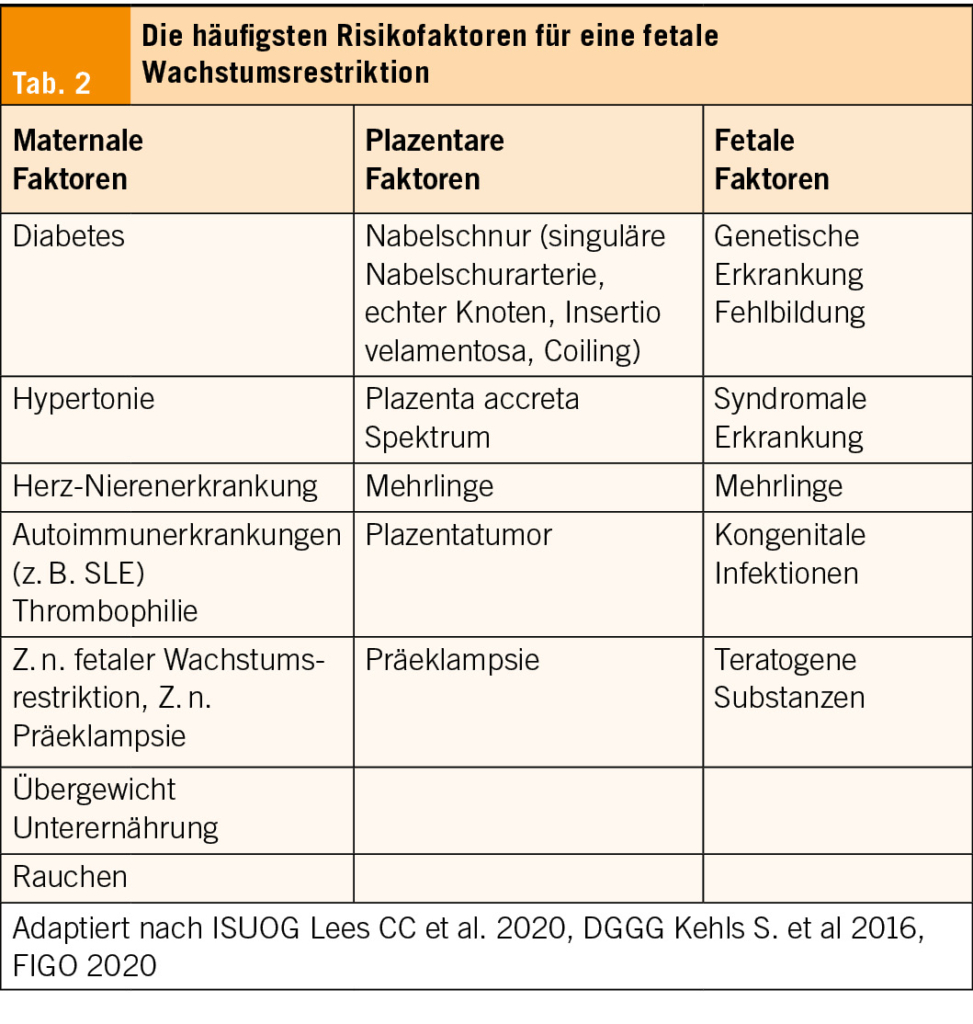
Die fetale Wachstumsrestriktion (FGR) kann durch maternale, plazentare oder fetale Erkrankungen verursacht werden (Tab. 2). Chromosomale Störungen und intrauterine Infektionen, wie z.B. Cytomegalie, verursachen jeweils etwa 5 % aller FGR-Fälle. Bei isolierter fetaler Retardierung wurde in 19 % der Fälle ein auffälliger Karyotyp festgestellt. Es konnten vor der 26. SSW am häufigsten Triploidien und nach der 26. SSW die Trisomie 18 als häufigste Auffälligkeiten festgestellt werden (16). Eine Metaanalyse von 14 Studien und 874 Fällen zur isolierten FGR ergab insgesamt eine chromosomale Aberrationsrate von 6.4 % (17).
Die Plazentainsuffizienz im Rahmen einer Präeklampsie (PE) ist in 70 % die häufigste Ursache für das frühe FGR (< 32. SSW). Als Ursache wird eine fehlende oder suboptimale Änderung der Plazentation (Remodelling der Spiralarterien) angenommen und mit angiogenen (PlGF) und antiangiogenen Faktoren (sFlt-1). Die fehlerhafte Plazentation führt zu lokalen Entzündungen, Endothelschäden, thrombotischen Folgen und Plazentainfarkten, die zu einer fetalen Unterversorgung mit Wachstumsstillstand führen können.
Die Reduktion des villösen Gefässbettes ist pathognomonisch für FGR und äussert sich in einer im Verlauf der Schwangerschaft zunehmenden Reduktion des enddiastolischen umbilikalen Flusses. Dies führt zu einem Anstieg der dopplersonographischen Widerstandsindizes (RI/PI) in der NSA und kann sich bis zum Fehlen (AEDV) und sogar zu einer umgekehrten enddiastolischen Geschwindigkeit (REDV) entwickeln (18, 19). Die verminderte Sauerstoffaufnahme über das beeinträchtigte villöse Gefässbett reduziert weiter den fetalen arteriellen Sauerstoffpartialdruck, was zu einer Weitstellung im cerebralen Gefässbett führt. Der messbare Widerstand in der A. cerebri media (ACM) senkt sich als Zeichen der Weitstellung des Gefässes. Beim frühen FGR ist die Doppleruntersuchung des DV nützlich, die a-Welle wird als Zeichen der cardialen Dekompensation flacher und analog zur NSA sogar negativ. Zum besseren Verständnis des späten FGR und der Überwachung kann die zerebroplazentare Ratio (CPR) als Entscheidungshilfe für die Geburtsplanung genutzt werden (20–22). Aktuell wird die Nutzung der CPR in Terminnähe bei unauffälligen Schwangerschaften untersucht; erste Daten zeigen dass die Nutzung der CPR zur Geburtsplanung die Morbidität günstig beeinflusst (23).
Screening und Prävention
Ein spezifisches Screening für fetale Wachstumsrestriktion (FGR) existiert nicht. Wichtig ist die Identifizierung anamnestischer Risikofaktoren, die eine FGR prädisponieren (Tab. 2). Die Veränderung der angiogenen und antiangiogenen Biomarker kann zu einem auffälligen Screeningsergebnis im 1. Trimester im PE-Screening und im 2. bis 3. Trimester zur erhöhten sFlt-1/PlGF Ratio führen. Das Präeklampsie-Screening im ersten Trimester, basierend auf mütterlichen Faktoren sowie biophysikalischen (UtA-PI) und biochemischen (PlGF) Markern, ist effektiv zur Vorhersage von SGA (Geburtsgewicht < 3. Perzentile) bei Frauen mit PE (23). Bei SGA/IUGR ohne PE ist die Vorhersagekraft moderat (25).
Aspirin kann bei auffälliger Anamnese und/oder Screeningergebnis zur Prävention gegeben werden. Es kann die Plazentation durch Hemmung der Cyclooxygenase-1 und Thromboxanbildung positiv beeinflussen (25-28). Metaanalysen zeigen, dass Aspirin bei Risikoschwangerschaften wirksam ist und das Risiko für FGR moderat reduziert (RR 0.90, 95 % CI 0.81–1). Die Dosis sollte ≥ 100 mg betragen und vor der 16. SSW begonnen werden. Low-molecular-weight Heparin zeigt in einer Metaanalyse keinen präventiven Effekt auf FGR (18 % vs 18 %; absolute risk difference, 0.6 %; 95 % CI 10.4–9.2) (26).
Diagnostik
• Ausführliche Anamneseerhebung
• Detaillierte Sonographie, Fehlbildungsausschluss
• Dopplerverlaufskontrolle
• Additive Tests (Biomarker (sFlt-1, PlGF), Ausschluss Infektionen (TORCH Serologie) Thrombophilieausschluss etc.)
Die Diagnosekriterien zur Detektion einer FGR und Unterscheidungsmerkmale der beiden Formen (frühe FGR und späte FGR) zum SGA sind wichtig (Tab. 1). Vor der Diagnose einer FGR ist es wichtig zu überprüfen, dass das korrekte Schwangerschaftsalter verwendet wird. Dies wird anhand der Schädelsteisslänge (SSL) im ersten Trimester erhoben. Bei Verdacht auf FGR werden neben der Biometrie auch die sonographische Fruchtwasserbestimmung und fetale und maternale Doppleruntersuchungen durchgeführt. Zudem ist additiv ein Kardiotokogramm (CTG), insbesondere bis zur 32. SSW ein computerisiertes CTG (cCTG) durchzuführen.
Allein durch die Durchführung der fetalen Biometrie nach der 36. SSW kann die Detektionsrate des späten FGR um das Dreifache erhöht werden (29, 30). Die ebenfalls durchgeführte Doppleruntersuchung mit auffällige CPR Ratio kann in 15 % insbesondere das späten FGR mit ungünstiger perinataler Morbidität entdecken (31, 32). Dies zeigt das Potential des dritten Screenings und weiterer Wachstums- und Dopplerkontrollen im 3. Trimester für allen Schwangerschaften, insbesondere natürlich für die identifizierten Risikogruppe.
Je früher und je ausgeprägter die beschriebenen Dopplerveränderungen sind, desto schwerwiegender ist die plazentare Dysfunktion mit konsekutiver Minderversorgung des Fetus. Beim frühen FGR ist der Fokus der Doppleruntersuchung die Aa. uterinae, der nachfolgenden Gefässe der NSA und des Ductus venosus. Beim späten FGR ist zusätzlich die Nutzung der CPR (Ratio aus der Messung der NSA und der ACM) von Bedeutung.
Ein Zusammenhang zwischen PE und FGR ist bekannt: Beide Zustände sind durch niedrige PlGF-Werte und dadurch eine erhöhte sFlt-1/PlGF-Ratio gekennzeichnet. Eine Studie, die 47 biochemische Marker bei Patientinnen mit PE zwischen der 20+0 und 34+6 SSW untersuchte, fand, dass niedrige maternale PlGF-Spiegel den besten Vorhersagewert für die Geburt eines FGR-Fetus hatten. PlGF-Konzentrationen < 100 pg/mL zeigten eine Sensitivität von 93.2 % und einen negativen prädiktiven Wert von 89.7 % für die Vorhersage eines FGR-Fetus. Dieser biochemische Marker übertraf die Ultraschallvorhersage, die eine Sensitivität von 71.2 % und einen negativen prädiktiven Wert von 78.5 % ergab (33).
Management und Therapie des FGR
Aktuell gibt es keine anerkannte Therapie bei FGR. Zunächst erfolgreiche theoretische Konstrukte zur Verbesserung der Plazentafunktion unter der Nutzung von Sildenafil oder Pentaerythritol tetranitrate (PETN) haben sich nicht durchsetzen können (34, 35).
Bei vorliegenden Risikofaktoren für ein FGR (Tab. 2) sollte im 3. Trimester (ab der 28. SSW) eine intensivierte Schwangerschaftskontrolle durchgeführt werden. Auch die Diagnose SGA sollte zu einem engmaschigen Monitoring führen. Dies beinhaltet in der Regel 10 bis 14-tägige Wachstums- und Dopplerkontrollen (Tab 3). Die Überwachungshäufigkeit bei diagnostizierter FGR wurde bisher in keiner explizierten Studie evaluiert und führt zu unterschiedlichen Empfehlungen.
Frühe FGR
Bei Diagnose einer frühen FGR wird eine Betreuung in einem Perinatalzentrum empfohlen. Die Überwachungsintensität sollte sich nach dem Schweregrad der FGR richten. Oft ist eine stationäre Überwachung mit häufigeren Kontrollen notwendig. Bei drohender Entbindungsindikation mit Frühgeburtlichkeit ist die Lungenreifungsinduktion (LRI) vor der 34+0 SSW und vor der 32. SSW die Gabe von Magnesium zur Neuroprotektion zu diskutieren.
Bei erhöhtem FGR-Risiko sollten engmaschige Dopplerkontrollen erfolgen. Bei erhöhtem Widerstand in der NSA werden auch die ACM und der DV gemessen. Veränderungen im Doppler der NSA und der MCA können frühe Anzeichen einer FGR sein, sind jedoch nicht unbedingt mit einem schlechten perinatalen Outcome assoziiert. Der Grad der Veränderungen im Nabelschnurdoppler mit AEDF oder REDV in der Diastole bestimmt den Grad der fetalen Verschlechterung. In diesem Fall ist ein intensives Monitoring mit Dopplerverlaufskontrollen alle 2 bis 3 Tage sowie täglichem CTG erforderlich.
Je weiter fortgeschritten die SSW, desto eher ist eine Entbindung bei FGR indiziert. Eine Entbindung bei extremer Frühgeburtlichkeit (< 28 SSW) muss sorgfältig abgewogen werden, da sie mit hoher Morbidität verbunden ist. Eine verzögerte Entbindung kann zu hypoxischen Schäden führen, während Frühgeburtlichkeit ebenfalls erhebliche Morbidität verursachen kann.
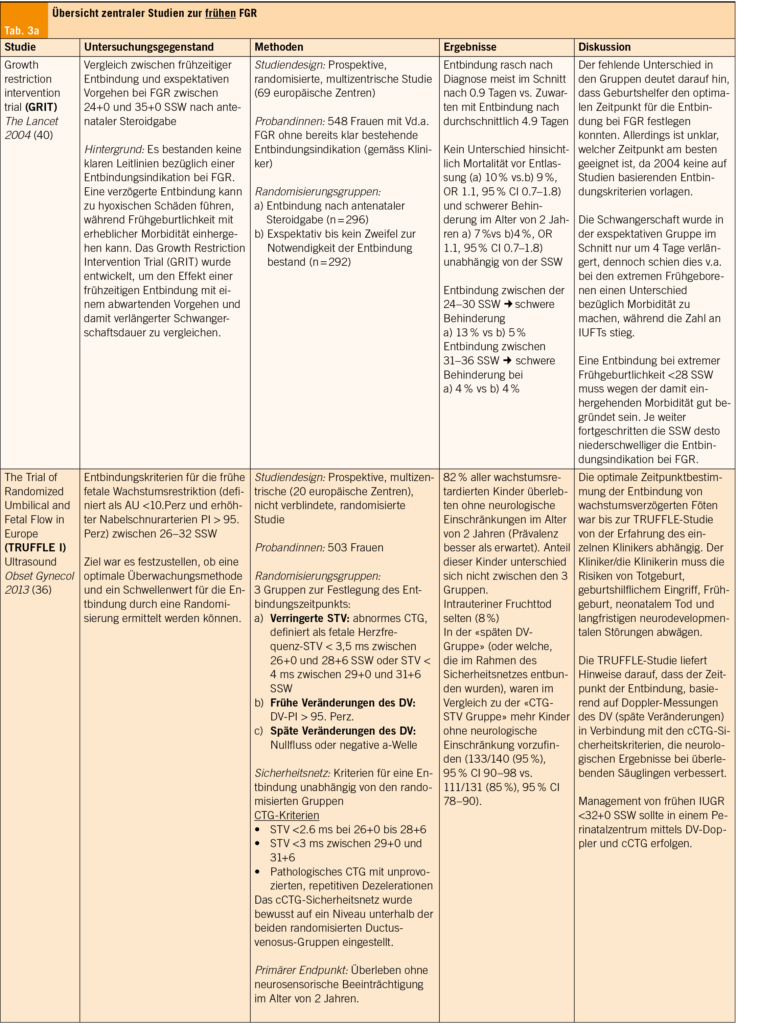
Die optimale Bestimmung des Entbindungszeitpunkts bei wachstumsverzögerten Föten war bis zur TRUFFLE-Studie (2013) von der Erfahrung einzelner Kliniker abhängig. Der Kliniker muss die Risiken von einer Totgeburt, geburtshilflichem Eingriff, Frühgeburt, neonatalem Tod und langfristigen Störungen der neurologischen Entwicklung abwägen. Die TRUFFLE-Studie zeigt, dass der Entbindungszeitpunkt < 32. SSW basierend auf Doppler-Messungen des DV unter Hinzuziehung der definierten cCTG-Sicherheitskriterien die besten neurologischen Ergebnisse bei überlebenden Säuglingen zeigte (Tab. 3) (36-42).
Die Fruchtwassermessung spielt im Monitoring beim frühen FGR eine wichtige Rolle, so konnte gezeigt werden, dass insbesondere bei schwerer FGR < 3.Perzentile und bestehenden Oligohydramion das perinatale Outcome sich verschlechtert (43).
Späte FGR
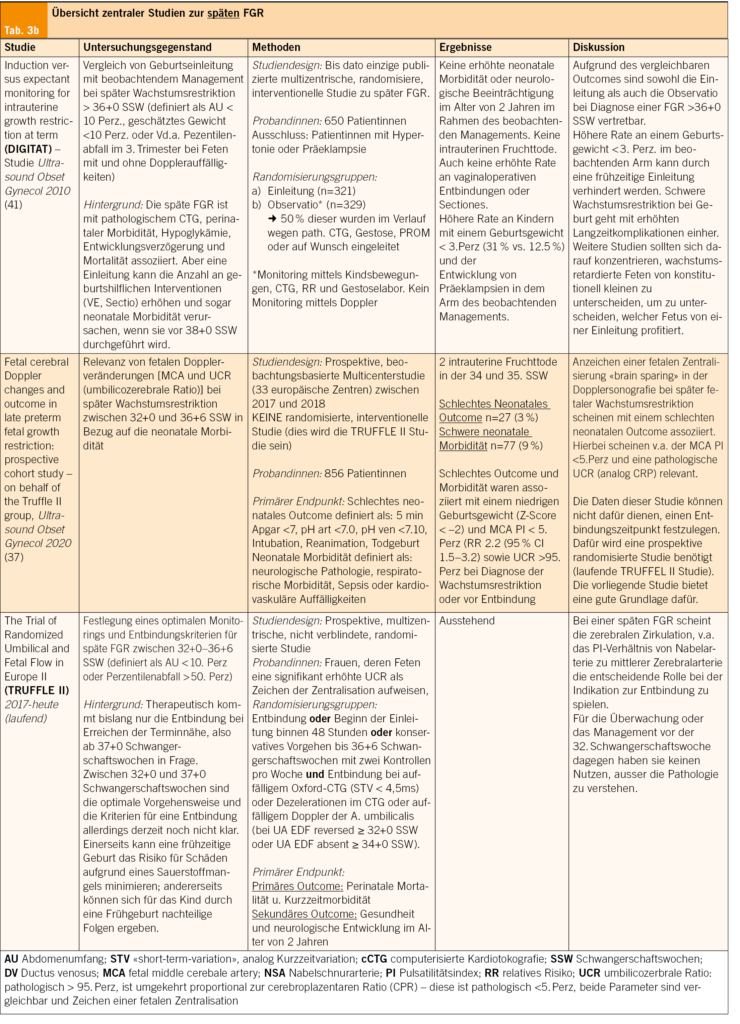
Aktuell besteht die therapeutische Option beim späten FGR primär in der Entbindung ab 37+0 SSW. Zwischen 32+0 und 37+0 SSW sind die optimale Vorgehensweise und Entbindungskriterien jedoch weitgehend unklar. Insbesondere die Anwendung der Dopplersonographie bei späten FGR variiert in den Empfehlungen, die bislang nicht durch randomisierte Studien belegt sind.
Die noch laufende TRUFFLE II-Studie untersucht deshalb als prospektive, multizentrische, nicht verblindete, randomisierte Studie das optimale Monitoring und die Entbindungskriterien für späte FGR zwischen 32+0 und 36+6 SSW.
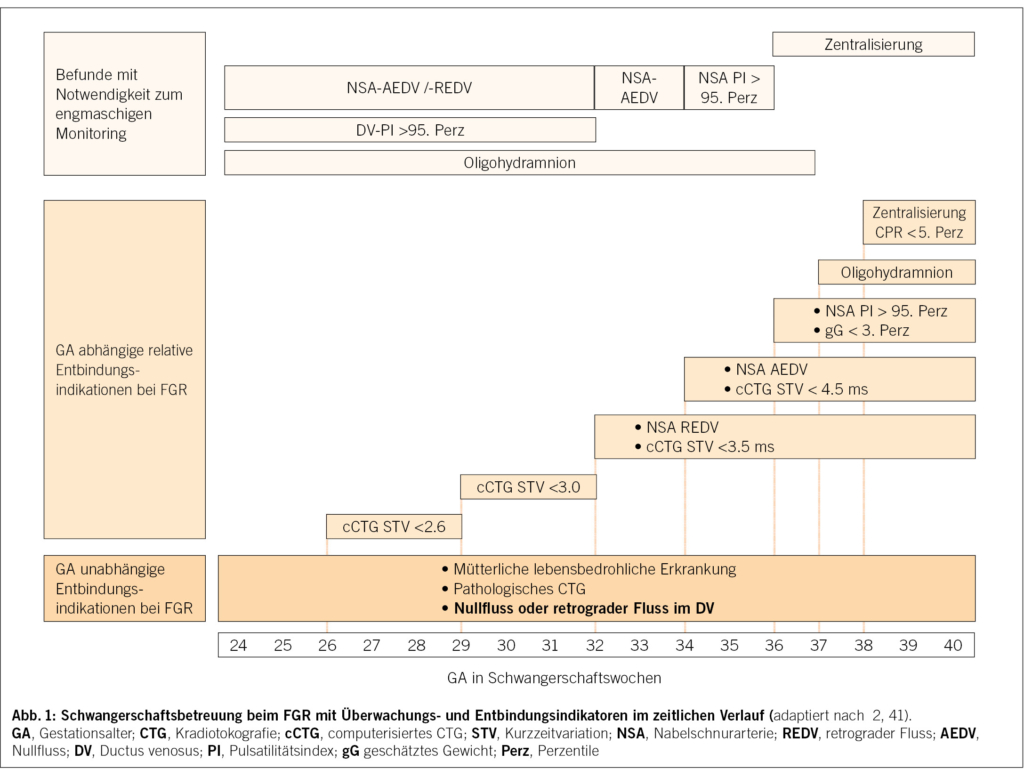
Im Allgemeinen besteht derzeit die Empfehlung zur Entbindung zwischen 32+0 bis 34+0 bei einem retrograden Flussmuster in der NSA und > 34+0 SSW bei einem Nullfluss der NSA sowie jederzeit bei einem pathologischen CTG (2, 4). Eine Subanalyse der TRUFFLE-Gruppe zeigte, dass Anzeichen einer fetalen Zentralisierung («brain sparing») in der Dopplersonographie bei späten FGR mit einem schlechten neonatalen Outcome assoziiert sind, insbesondere bei einem MCA PI < 5. Perzentile und pathologischer CPR (39).
Die aktuelle ISUOG-Guideline empfiehlt die Entbindung zwischen der 36+0 bis 37+6 SSW bei einem erhöhten NSA-PI > 95. Perz oder einem geschätzten Gewicht < 3. Perz. Zwischen der 38+0 bis 39+0 SSW sollte die Entbindung angestrebt werden, sobald der FGR-Fetus eine Zentralisierung aufweist (2, 4).
Bei einem SGA wird die Geburt in der Regel bei unauffälligen Kontrollen ab der 38. SSW, spätestens am errechneten Entbindungstermin terminiert (Abb. 1).
Entbindungsmodus
Eine FGR ist keine absolute Indikation für einen Kaiserschnitt. Bei schwerer maternaler Erkrankung und Frühgeburtlichkeit wird die Sectio caesarea jedoch häufig durchgeführt. Bei einem pathologischen Doppler mit Nullfluss oder retrograden Fluss in der NSA sollte dieser ebenfalls bevorzugt werden. Die Geburtseinleitung kann nach Abwägung der klinischen Situation durchgeführt werden (5,6). Allerdings sollte diese unter engmaschiger CTG-Überwachung erfolgen; die Rate an sekundären Sectiones ist erhöht (41).
Beratung für weitere Schwangerschaften
Für Folgeschwangerschaften sollte bei einem Zustand nach FGR, PE und Verdacht auf vaskuläre Erkrankungen ein Thrombophilie-Screening erfolgen (Lupus Antikoagulans, MTHFR Mutation, Antiphospholipidantikörper, Protein C, Protein S, APC-Resistenz etc.). Allen Frauen mit Z. n. FGR und oder PE vor der 34. SSW sollten in Folgeschwangerschaften ASS 100–160 mg am Abend bis zur 36+0 SSW einnehmen (Beginn vor der 16. SSW) (2,5,6, 24, 44).
Copyright Aerzteverlag medinfo AG
Spital Zollikerberg
Frauenklinik
Trichtenhauserstrasse 20
8125 Zollikerberg
Spital Zollikerberg
Frauenklinik
Trichtenhauserstrasse 20
8125 Zollikerberg
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Die fetale Wachstumsrestriktion ist häufig unerkannt. Anamnestische Risiken und auffällige Screening-Ergebnisse (erniedrigtes PlGF) müssen konsequent zur intensivierten Schwangerschaftskontrolle spätestens im dritten Trimester führen.
- Es wird heute zwischen dem frühen und späten FGR unterschieden. In den letzten Jahren erhärtet sich der Verdacht, dass das späte FGR nahezu eine eigene Entität darstellt und schwer zu erkennen ist.
- Durch eine intensivierte Schwangerschaftskontrolle beim FGR und die Planung der Geburt kann die Morbidität und Mortalität deutlich reduziert werden.
- Neben der einfachen Biometrie zur Feststellung des FGR steht die Doppleruntersuchung im Mittelpunkt. Die korrekte Durchführung und Interpretation der Doppleruntersuchung sind hier entscheidend wichtig.
1. Lees CC, Romero R, Stampalija T, Dall’Asta A, DeVore GA, Prefumo F, Frusca T, Visser GHA, Hobbins JC, Baschat AA, Bilardo CM, Galan HL, Campbell S, Maulik D, Figueras F, Lee W, Unterscheider J, Valensise H, Da Silva Costa F, Salomon LJ, Poon LC, Ferrazzi E, Mari G, Rizzo G, Kingdom JC, Kiserud T, Hecher K. Clinical Opinion: The diagnosis and management of suspected fetal growth restriction: an evidence-based approach. Am J Obstet Gynecol. 2022 Mar;226(3):366-378.
2. Salomon LJ, Alfirevic Z, Da Silva Costa F, Deter RL, Figueras F, Ghi T, Glanc P, Khalil A, Lee W, Napolitano R, Papageorghiou A, Sotiriadis A, Stirnemann J, Toi A, Yeo G. ISUOG Practice Guidelines: ultrasound assessment of fetal biometry and growth. Ultrasound Obstet Gynecol 2019; 53: 715–723.
3. Lees CC, Stampalija T, Baschat AA, da Silva Costa F, Ferrazzi E, Figueras F, Hecher K, Kingdom J, Poon LC, Salomon LJ, Unterscheider J. ISUOG Practice Guidelines: diagnosis and management of small-for-gestational-age fetus and fetal growth restriction. Ultrasound Obstet Gynecol 2020;56:298-312
4. https://www.isuog.org/static/b2aa3fb4-031e-4d84-b7246d613a466884/ISUOG-Practice-Guidelines-diagnosis-and-management-of-small-for-gestational-age-fetus-and-fetal-growth-restriction.pdf
5. Kehl S. Dötsch J. Hecher K. et al. Intrauterine Growth Restricition. Guideline oft he German Society of Gynecology and Obstetrics (S2k-Level, AWMF Registry No 015/080, October 2016
6. https://register.awmf.org/assets/guidelines/015/0801_S2k_Intrauterine_Wachstumsrestriktion_2017_06-verlaengert.pdf access 01.08.2024
7. Gordijn SJ, Beune IM, Thilaganathan B, et al. Consensus definition of fetal growth restriction: a Delphi procedure. Ultrasound Obstet Gynecol 2016;48:333–9.
8. Melamed N, Baschat A, Yinon Y, Athanasiadis A, Mecacci F, Figueras F, Berghella V, Nazareth A, Tahlak M, McIntyre HD, Da Silva Costa F, Kihara AB, Hadar E, McAuliffe F, Hanson M, Ma RC, Gooden R, Sheiner E, Kapur A, Divakar H, Ayres-de-Campos D, Hiersch L, Poon LC, Kingdom J, Romero R, Hod M. FIGO (international Federation of Gynecology and obstetrics) initiative on fetal growth: best practice advice for screening, diagnosis, and management of fetal growth restriction. Int J Gynaecol Obstet. 2021 Mar;152 Suppl 1(Suppl 1):3-57.
9. Vasak B, Koenen SV, Koster MP, et al. Human fetal growth is constrained below optimal for perinatal survival. Ultrasound Obstet Gynecol 2015;45:162–7.
10. Barker D J. Adult consequences of fetal growth restriction. Clin Obstet Gynecol. 2006;49:270–283.
11. Gardosi J, Madurasinghe V, Williams M, Malik A, Francis A. Maternal and fetal risk factors for stillbirth: population based study. BMJ. 2013 Jan 24;346:f108.
12. Roex A, Nikpoor P, van Eerd E, Hodyl N, Dekker G. Serial plotting on customised fundal height charts results in doubling of the antenatal detection of small for gestational age fetuses in nulliparous women. Aust N Z J Obstet Gynaecol 2012;52:78-82.
13. Poon LC, Tan MY, Yerlikaya G, Syngelaki A, Nicolaides KH. Birth weight in live births and stillbirths. Ultrasound Obstet Gynecol 2016; 48: 602–606.
14. Flenady V, Wojcieszek AM, Ellwood D, Leisher SH, Erwich JJHM, Draper ES, McClure EM, Reinebrant HE, Oats J, McCowan L, Kent AL, Gardener G, Gordon A, Tudehope D, Siassakos D, Storey C, Zuccollo J, Dahlstrom JE, Gold KJ, Gordijn S, Pettersson K, Masson V, Pattinson R, Gardosi J, Khong TY, Frøen JF, Silver RM. International Stillbirth Alliance Collaborative for Improving Classification of Perinatal Deaths; Classification of causes and associated conditions for stillbirths and neonatal deaths. Semin Fetal Neonatal Med. 2017 Jun;22(3):176-185.
15. Moraitis AA, Wood AM, Fleming M, Smith GCS. Birth weight percentile and the risk of term perinatal death. Obstet Gynecol. 2014 Aug;124(2 Pt 1):274-283.
16. Snijders RJ, Sherrod C, Gosden CM, Nicolaides KH. Fetal growth retardation: associated malformations and chromosomal abnormalities. Am J Obstet Gynecol. 1993 Feb;168(2):547-55.
17. Sagi-Dain L, Peleg A, Sagi S. Risk for chromosomal aberrations in apparently isolated intrauterine growth restriction: A systematic review. Prenat Diagn. 2017 Nov;37(11):1061-1066.
18. Baschat AA, Gembruch U, Harman CR. The sequence of changes in Doppler and biophysical parameters as severe fetal growth restriction worsens. Ultrasound Obstet Gynecol 2001; 18: 571–577.
19. Baschat AA, Gembruch U. The cerebroplacental Doppler ratio revisited. Ultrasound Obstet Gynecol. 2003;21:124–7.
20. Cruz-Martinez R, Savchev S, Cruz-Lemini M, Mendez A, Gratacos E, Figueras F. Clinical utility of third-trimester uterine artery Doppler in the prediction of brain hemodynamic deterioration and adverse perinatal outcome in small-for-gestational-age fetuses. Ultrasound Obstet Gynecol. 2015;45:273–8.
21. Vollgraff Heidweiller-Schreurs C A, De Boer M A, Heymans M W. Prognostic accuracy of cerebroplacental ratio and middle cerebral artery Doppler for adverse perinatal outcome: systematic review and meta-analysis. Ultrasound Obstet Gynecol. 2018;51:313–322.
22. Conde-Agudelo A, Villar J, Kennedy SH, Papageorghiou AT. Predictive accuracy of cerebroplacental ratio for adverse perinatal and neurodevelopmental outcomes in suspected fetal growth restriction: systematic review and meta-analysis. Ultrasound Obstet Gynecol. 2018 Oct;52(4):430-441.
23. Rial-Crestelo M, Lubusky M, Parra-Cordero M, Krofta L, Kajdy A, Zohav E, Ferriols-Perez E, Cruz-Martinez R, Kacerovsky M, Scazzocchio E, Roubalova L, Socias P, Hašlík L, Modzelewski J, Ashwal E, Castellá-Cesari J, Cruz-Lemini M, Gratacos E, Figueras F; RATIO37 Study Group. Term planned delivery based on fetal growth assessment with or without the cerebroplacental ratio in low-risk pregnancies (RATIO37): an international, multicentre, open-label, randomised controlled trial. Lancet. 2024 Feb 10;403(10426):545-553.
24. Papastefanou I, Wright D, Syngelaki A, Souretis K, Chrysanthopoulou E, Nicolaides KH. Competing-risks model for prediction of small-for-gestational-age neonate from biophysical and biochemical markers at 11-13 weeks’ gestation. Ultrasound Obstet Gynecol. 2021 Jan;57(1):52-61.
25. Rolnik DL Nicolaides KH, Poon LC. Prevention of preeclampsia with aspirin. Am J Obstet Gynecol. 2022 Feb;226(2S):S1108-S1119
26. Cruz-Lemini M, Vázquez JC, Ullmo J, Llurba E. Low-molecular-weight heparin for prevention of preeclampsia and other placenta-mediated complications: a systematic review and meta-analysis. Am J Obstet Gynecol. 2022 Feb;226(2S):S1126-S1144.e17.
27. Levine RJ, Lam C, Qian C, Yu KF, Maynard SE, Sachs BP, Sibai BM, Epstein FH, Romero R, Thadhani R, Karumanchi SA; CPEP Study Group. Soluble endoglin and other circulating antiangiogenic factors in preeclampsia. N Engl J Med 2006; 355: 992–1005.
28. Tan M Y, Poon L C, Rolnik D L. Prediction and prevention of small-for-gestational-age neonates: evidence from SPREE and ASPRE. Ultrasound Obstet Gynecol. 2018;52:52–59.
29. Sovio U, White IR, Dacey A, Pasupathy D, Smith GCS. Screening for fetal growth restriction with universal third trimester ultrasonography in nulliparous women in the Pregnancy Outcome Prediction (POP) study: a prospective cohort study. Lancet. 2015 Nov 21;386(10008):2089-2097.
30. Caradeux J, Martinez-Portilla RJ, Peguero A, Sotiriadis A, Figueras F. Diagnostic performance of third-trimester ultrasound for the prediction of late-onset fetal growth restriction: a systematic review and meta-analysis. Am J Obstet Gynecol. 2019 May;220(5):449-459.e19.
31. Grüttner B, Ratiu J, Ratiu D, Gottschalk I, Morgenstern B, Abel JS, Eichler C, Pahmeyer C, Ludwig S, Mallmann P, Thangarajah F. Correlation of Cerebroplacental Ratio (CPR) With Adverse Perinatal Outcome in Singleton Pregnancies. In Vivo. 2019 Sep-Oct;33(5):1703-1706.
32. Kalafat E, Khalil A. Clinical significance of cerebroplacental ratio. Curr Opin Obstet Gynecol. 2018 Dec;30(6):344-354.
33. Griffin M, Seed PT, Duckworth S, North R, Myers J, Mackillop L, Simpson N, Waugh J, Anumba D, Kenny LC, Redman CWG, Shennan AH, Chappell LC. Predicting delivery of a small-for-gestational-age infant and adverse perinatal outcome in women with suspected pre-eclampsia. Ultrasound Obstet Gynecol. 2018 Mar;51(3):387-395.
34. Sharp A, Cornforth C, Jackson R, Harrold J, Turner MA, Kenny LC, Baker PN, Johnstone ED, Khalil A, von Dadelszen P, Papageorghiou AT, Alfirevic Z; STRIDER group. Maternal sildenafil for severe fetal growth restriction (STRIDER): a multicentre, randomised, placebo-controlled, double-blind trial. Lancet Child Adolesc Health 2018; 2: 93–102.
35. Groten T, Lehmann T, Städtler M, Komar M, Winkler JL, Condic M, Strizek B, Seeger S, Jäger Y, Pecks U, Eckmann-Scholz C, Kagan KO, Hoopmann M, von Kaisenberg CS, Brodowski L, Tauscher A, Schrey-Petersen S, Friebe-Hoffmann U, Lato K, Hübener C, Delius M, Verlohren S, Sroka D, Schlembach D, de Vries L, Kraft K, Seliger G, Schleußner E; PETN Study Group. Effect of pentaerythritol tetranitrate (PETN) on the development of fetal growth restriction in pregnancies with impaired uteroplacental perfusion at midgestation-a randomized trial. Am J Obstet Gynecol. 2023 Jan;228(1):84.e1-84.e12.
36. Lees C, Marlow N, Arabin B, Bilardo CM, Brezinka C, Derks JB, Duvekot J, Frusca T, Diemert A, Ferrazzi E, Ganzevoort W, Hecher K, Martinelli P, Ostermayer E, Papageorghiou AT, Schlembach D, Schneider KT, Thilaganathan B, Todros T, van Wassenaer-Leemhuis A, Valcamonico A, Visser GH, Wolf H; TRUFFLE Group. Perinatal morbidity and mortality in early-onset fetal growth restriction: cohort outcomes of the trial of randomized umbilical and fetal flow in Europe (TRUFFLE). Ultrasound Obstet Gynecol 2013; 42: 400–408.
37. Lees CC, Marlow N, van Wassenaer-Leemhuis A, Arabin B, Bilardo CM, Brezinka C, Calvert S, Derks JB, Diemert A, Duvekot JJ, Ferrazzi E, Frusca T, Ganzevoort W, Hecher K, Martinelli P, Ostermayer E, Papageorghiou AT, Schlembach D, Schneider KT, Thilaganathan B, Todros T, Valcamonico A, Visser GH, Wolf H; TRUFFLE study group. 2 year neurodevelopmental and intermediate perinatal outcomes in infants with very preterm fetal growth restriction (TRUFFLE): a randomised trial. Lancet 2015; 385: 2162–2172.
38. Bilardo C M, Hecher K, Visser G HA. Severe fetal growth restriction at 26–32 weeks: key messages from the TRUFFLE study. Ultrasound Obstet Gynecol. 2017;50:285–290.
39. Stampalija T, et al TRUFFLE-2 Group. Fetal cerebral Doppler changes and outcome in late preterm fetal growth restriction: prospective cohort study. Ultrasound Obstet Gynecol. 2020 Aug;56(2):173-181.
40. Thornton JG, Hornbuckle J, Vail A, Spiegelhalter DJ, Levene M; GRIT study group. Infant wellbeing at 2 years of age in the Growth Restriction Intervention Trial (GRIT): multicentred randomised controlled trial. Lancet 2004; 364: 513–520.
41. Boers KE, Vijgen SM, Bijlenga D, van der Post JA, Bekedam DJ, Kwee A, van der Salm PC, van Pampus MG, Spaanderman ME, de Boer K, Duvekot JJ, Bremer HA, Hasaart TH, Delemarre FM, Bloemenkamp KW, van Meir CA, Willekes C, Wijnen EJ, Rijken M, le Cessie S, Roumen FJ, Thornton JG, van Lith JM, Mol BW, Scherjon SA; DIGITAT study group. Induction versus expectant monitoring for intrauterine growth restriction at term: randomised equivalence trial (DIGITAT). BMJ. 2010 Dec 21;341:c7087. doi: 10.1136/bmj.c7087. PMID: 21177352; PMCID: PMC3005565.
42. Baschat AA. Considering evidence in the management of fetal growth restriction. Ultrasound Obstet Gynecol. 2021 Jan;57(1):25-28.
43. Unterscheider J, Daly S, Geary MP, Kennelly MM, McAuliffe FM, O’Donoghue K, Hunter A, Morrison JJ, Burke G, Dicker P, Tully EC, Malone FD. Optimizing the definition of intrauterine growth restriction: the multicenter prospective PORTO Study. Am J Obstet Gynecol. 2013 Apr;208(4):290.e1-6
44. Vayssière C, Sentilhes L, Ego A, Bernard C, Cambourieu D, Flamant C, Gascoin G, Gaudineau A, Grangé G, Houfflin-Debarge V, Langer B, Malan V, Marcorelles P, Nizard J, Perrotin F, Salomon L, Senat MV, Serry A, Tessier V, Truffert P, Tsatsaris V, Arnaud C, Carbonne B. Fetal growth restriction and intra-uterine growth restriction: guidelines for clinical practice from the French College of Gynaecologists and Obstetricians. Eur J Obstet Gynecol Reprod Biol. 2015 Oct;193:10-8.
info@gynäkologie
- Vol. 14
- Ausgabe 5
- Oktober 2024