- Diagnose und Therapie uteriner Nischen
Uterine Sectionarbendefekte, sogenannte Nischen, werden häufig im Rahmen der gynäkologischen Vorsorge diagnostiziert und stellen aufgrund der limitierten Datenlage eine Herausforderung für den betreuenden Arzt dar. Typische Symptome umfassen Blutungsstörungen, chronische Unterleibsschmerzen oder Subfertilität mit negativen Auswirkungen auf die Lebensqualität der Betroffenen. In einer Folgeschwangerschaft besteht ein erhöhtes Risiko für lebensbedrohliche Komplikationen wie eine Implantation in der Sectionarbe, Plazenta accreta Spektrum Störungen, Dehiszenz und Uterusruptur. Die Diagnosestellung erfolgt mittels Transvaginalultraschall. Relevant ist dabei v.a. die verbleibende Myometriumsdicke über dem Defekt als prognostischer Faktor für Folgeschwangerschaften sowie zur Wahl der Operationsmethode. Operationsindikationen sind v.a. grössere Defekte bei Kinderwunsch oder therapierefraktäre Blutungsstörungen. Die operative Sanierung kann hysteroskopisch, (roboter-unterstützt) laparoskopisch, kombiniert oder vaginal erfolgen. Jedoch ist nicht jede Nische therapiebedürftig.
Cesarean scar defects, called niches, are frequently diagnosed during routine gynecological examination and are challenging for physicians due to limited data. Typical symptoms include bleeding disturbance, chronic pain or subfertility with negative impact on quality of life. A following pregnancy is at higher risk of life-threatening complications as ectopic scar pregnancy, placenta accreta spectrum disorder and uterine dehiscence or rupture. Transvaginal ultrasound is the diagnostic method of choice. The residual myometrial thickness is especially of interest as it is a prognostic relevant factor for subsequent pregnancies and determines which surgical method to use for a niche repair. Surgery is recommended in cases of severe scar defects and a wish to conceive or with persistent abnormal bleeding patterns. The repair can be performed by hysteroscopy, (robotic-assisted) laparoscopy, combined or with a vaginal approach. But not every niche needs to be treated.
Key Words: robotic, hysteroscopy, laparoscopy, niche repair, cesarean scar defect
32,6% aller Kinder wurden 2020 in der Schweiz per Kaiserschnitt entbunden (1). Weltweit sind es über 1,5 Millionen Sectiones pro Jahr (2). Zunehmend rücken uterine Narbendefekte, sogenannte Nischen und deren Komplikationen in den Fokus der Wissenschaft. Erstmalig wurde ein solcher, kleiner, keilförmiger Narbendefekt 1961 mittels Hysterosalpingographie beschrieben (3).
Definition
In verschiedenen Studien wird die Prävalenz aufgrund unterschiedlicher Definitionen zwischen 7-69% angegeben (3-4). Grundsätzlich wird ein uteriner Sectionarbendefekt als Auftreten eines hypoechogenen Bereiches im Myometrium des unteren Uterinsegmentes an der Inzisionsstelle definiert (3).
Risikofaktoren
Als Ursachen für die Entstehung dieser Nischen werden verschiedene Faktoren diskutiert und in 5 Kategorien unterteilt (5):
a) Nahttechnik der Uterotomie (5-6)
b) Einflussfaktoren auf das untere Uterinsegment, z.B. multiple Sectiones (7-9), Wehentätigkeit (10-13)
c) Höhe der Inzisionsstelle der Uterotomie (5)
d) Die Wundheilung beeinflussende Faktoren, z.B. Retroflexion uteri (7-10) oder Adhäsionsbildung (6)
e) Andere Faktoren, z.B. Alter der Patientin (10)
Narbendefekte befinden sich häufig distaler im unteren Uterinsegment als intakte Narben (8, 10, 13), da ein Einbezug von Zervikaldrüsen in den Wundbereich nach sekundären Sectiones und konsekutiver Ansammlung von Mukus (sog. Mukozele) eine Nischenbildung begünstigen kann (6).
Die Datenlage zum Einfluss der Nahttechnik der Uterotomie ist kontrovers. Während Bujold et al. (14-17) einen klaren Vorteil im zweischichtigen Verschluss sehen, fanden andere Autoren keine negativen Auswirkungen bei Anwendung des einschichtigen, nicht überwendlichen Verschlusses (18-20). Im multizentrischen CORONIS-Follow-up Trial liessen sich hingegen keine Unterschiede der Nahttechnik auf das Risiko einer Uterusruptur in einer Folgeschwangerschaft nachweisen (21).
Als protektiver Faktor für die Nischenentstehung wurde die Expression bestimmter Wachstumsfaktoren als mögliche Ursache für individuell verschiedene Wundheilung identifiziert (22).
Problematik
Nicht alle Nischen sind behandlungsbedürftig. Häufig werden sie als Zufallsbefund im Rahmen eines Vaginalultraschalls (TVUS) erhoben und können zu Verunsicherung der Patientin und aufgrund fehlender Leitlinien auch zu Ratlosigkeit beim Behandelnden führen. Mit dieser Übersichtsarbeit wollen wir eine praktische Handlungsanweisung geben.
Symptome
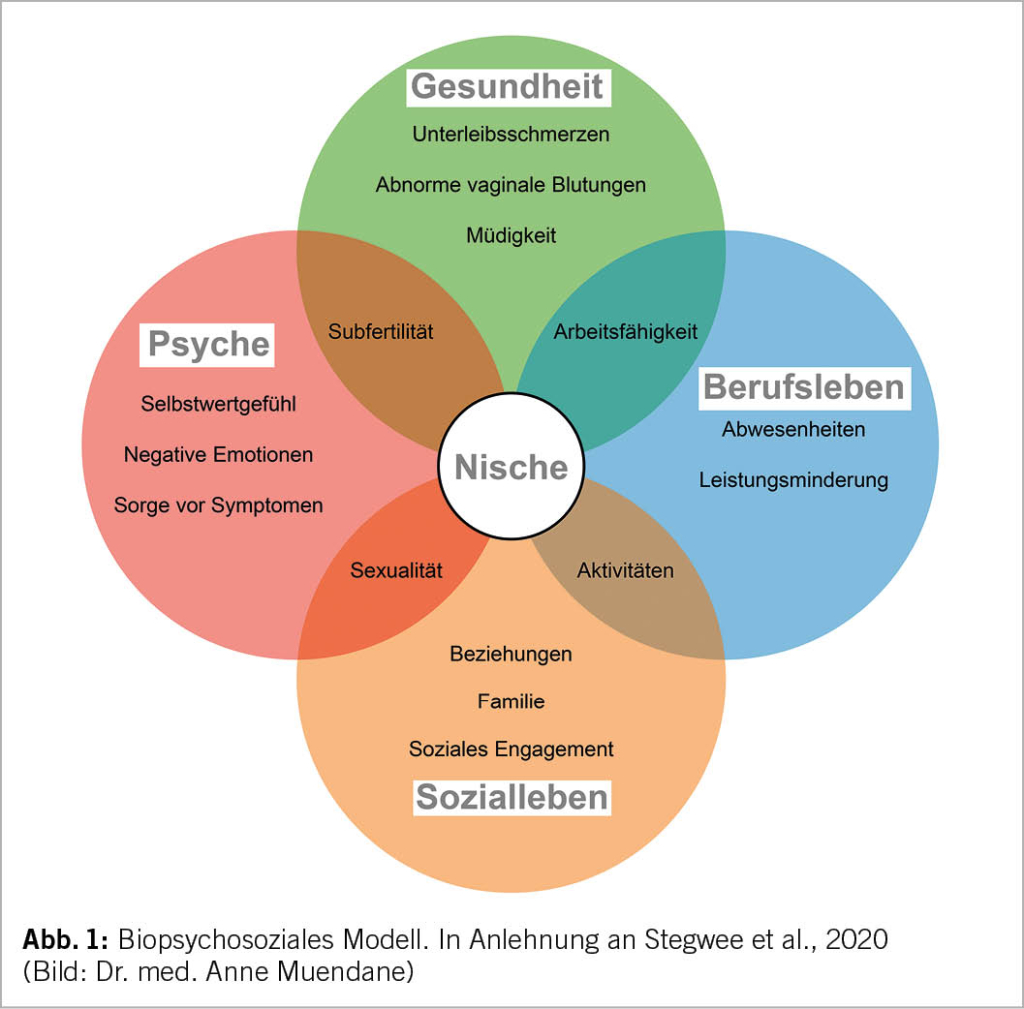
Als erstes stellt sich die Frage: hat die Patientin Beschwerden? Als typische Nischen-Symptome werden Blutungsstörungen (3-5, 7, 23), chronische Unterleibsschmerzen (7, 24), welche nicht selten durch Adhäsionen entstehen, und eine Subfertilität (3, 24) beschrieben. Diese können die Lebensqualität der Betroffenen massiv beeinträchtigen mit Auswirkungen auf die psychische Gesundheit, das Sozial- und Berufsleben sowie die Sexualität (25) (Abb. 1). Besonders gefürchtet sind lebensbedrohliche Komplikationen in einer Folgeschwangerschaft wie Plazentationstörungen (3, 8-9), Sectionarbenschwangerschaften (3, 8-9, 24) oder eine Uterusruptur (3, 8).
Diagnostik
Ein uteriner Narbendefekt kann mittels TVUS (8-9, 11, 26-27), Sonohysterographie (26-28) und MRI (29) diagnostiziert werden. Aufgrund der Zuverlässigkeit hat sich der TVUS als Diagnostikum der Wahl durchgesetzt (7-8, 30), wobei sich Nischen am häufigsten (83%) triangulär darstellen (8, 23). Die Untersuchung ist ab 6 Wochen postpartal sinnvoll (4, 29, 31). In Studien wird v.a. nach 6-9 Monaten postpartal untersucht (8-9, 11, 26-27), da zu diesem Zeitpunkt die zonale Anatomie des unteren Uterinsegmentes vollständig wiederhergestellt ist (32). Die Messungen im nicht-schwangeren Zustand sind vergleichbar mit denen in der 11.-14. SSW (33), sodass bereits eine präkonzeptionelle Beratung erfolgen kann.
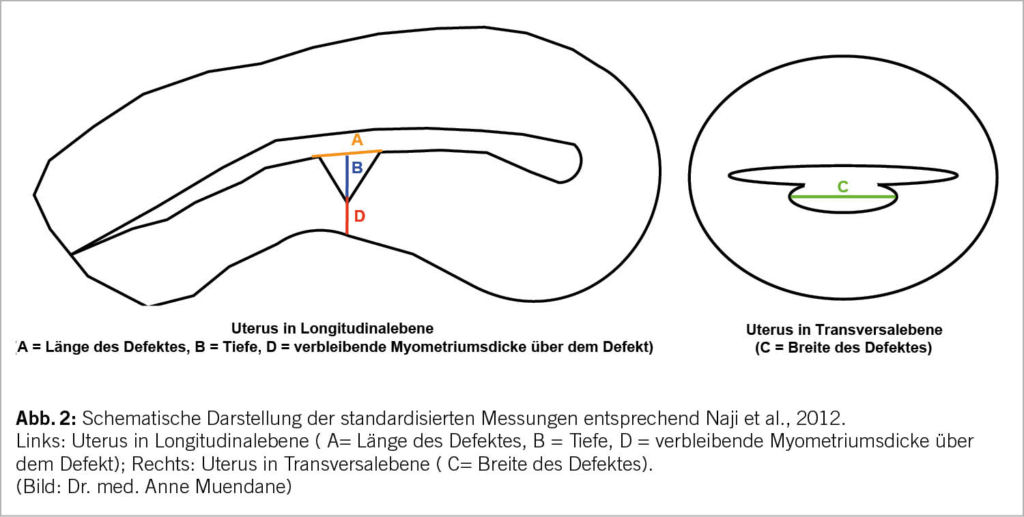
Seit 2012 wurde von Naji et al. eine standardisierte Messtechnik eingeführt (3). Dabei wird der Uterus zuerst im Longitudinalschnitt dargestellt und die Länge und Tiefe des dreieckigen Narbendefektes sowie die Dicke des verbleibenden Myometriums über dem Defekt, die sog. RMT (residual myometrial thickness), bestimmt (Abb. 2). Abschliessend wird in der Transversalebene die Breite des Defektes gemessen (Abb. 2). Während die Narbendimension mit der Häufigkeit von Blutungsstörungen zusammenhängt (4, 23), ist für Folgeschwangerschaften die RMT prognoserelevant (34). Als grosser Narbendefekt wird daher eine RMT von < 2,2 mm bei St.n. Sectio und <1,9mm bei St.n. Re-Sectio definiert (26) bzw. eine RMT von < 50% im Verhältnis zur Myometriumsdicke an dieser Stelle (4). In einer kleineren prospektiven Studie wurde bei grossem Narbendefekt eine Odds ratio von 11,8 für Uterusdehiszenz oder -ruptur in einer Folgeschwangerschaft festgestellt (34).
OP-Techniken
Verschiedene OP-Verfahren werden erfolgreich angewandt: therapeutische Hysteroskopie (35-39), vaginal operativ (37,39), Laparoskopie, (roboter-unterstützt) (37-39) oder kombinierte Laparoskopie und Hysteroskopie in rendez-vous Technik (37).
Behandlungsalgorithmen
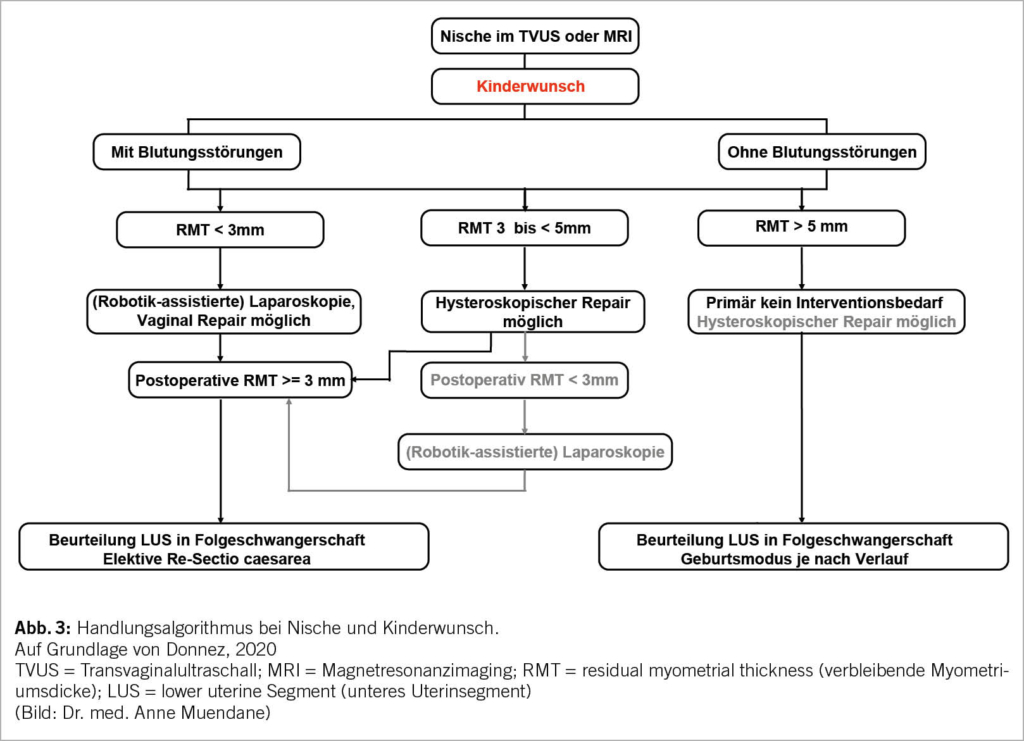
Kriterien für eine Operation sind v.a. Blutungsstörungen sowie Kinderwunsch. Donnez empfiehlt ein situations-adaptiertes Vorgehen (40). Bei Kinderwunsch und RMT < 3 mm soll zur Vermeidung einer Ausdünnung des Restmyometriums keine hysteroskopische Versorgung erfolgen (40). Hier bietet sich die laparoskopische oder roboter-unterstützte Operation an, um eine suffiziente anteriore Myometriumsschicht wiederherzustellen. Im eigenen Kollektiv bevorzugen wir aufgrund der feinen Nahttechniken die roboterunterstützte 3-schichtige Korrektur: innere sowie äussere Myometriumschicht und Serosaadaptation. Bei den laparoskopischen Verfahren ist auf die Nahtplatzierung zur spannungsfreien Uterotomieabheilung zu achten, die den Uterus in einer anteflektierten Position abheilen lässt. Entsprechende Daten hierzu werden aktuell ausgewertet und demnächst publiziert.
Grundsätzlich kann bei ausreichender RMT und Blutungsstörungen auch ein hysteroskopisches oder vaginal-operatives Vorgehen Anwendung finden. Das Prinzip der Hysteroskopie ist die Resektion der oberen und unteren Nischenkanten zur Optimierung des Mensabflusses (Verminderung Spotting), sowie Resektion von dysfunktionellem Endometrium im Nischengrund.
Wenn unabhängig von der OP-Methode postoperativ eine RMT von mindestens 3 mm besteht, wird ein regelmässiges Follow up in einer Folgeschwangerschaft mit elektiver Re-Sectio bei 39 SSW empfohlen (40).
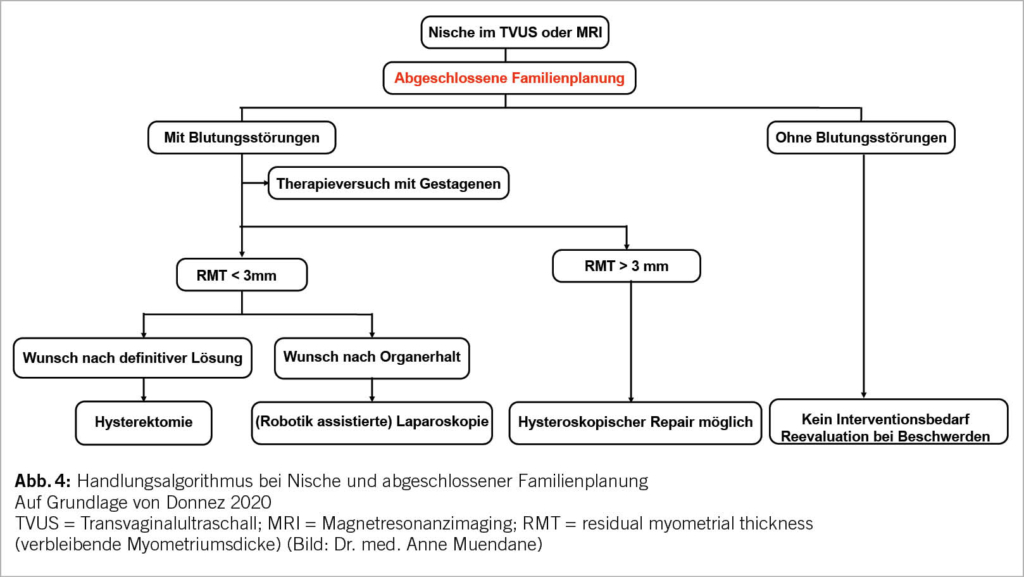
Ein angepasster Handlungsalgorithmus wird in Abbildung 3 und 4 vorgestellt.
Ausblick
Die Prävention von Nischen hat ein hohes Entwicklungspotential, welches in Studien präklinisch und klinisch begleitet werden sollte. Eine Studiengruppe am USZ untersucht, wie sich die Expression von Wachstumsfaktoren in den Nischen gegenüber gesundem Myometrium unterscheidet, da es in der Prävalenz grössere ungeklärte Unterschiede gibt.
Copyright bei Aerzteverlag medinfo AG
Klinik für Gynäkologie, USZ
Frauenklinikstrasse 10
8006 Zürich
Stellvertretende Klinikdirektorin
Klinik für Gynäkologie, USZ
Frauenklinikstrasse 10
8006 Zürich
cornelia.betschart@usz.ch
Anne Muendane hat keinen Interessenskonflikt.Cornelia Betschart ist Mitentwicklerin eines Medizinproduktes zur operativen Nischenkorrektur (Innosuisse Grant).
◆ Uterine Nischen sind ein häufiges Phänomen und sollten bei
Schmerzen, Blutungen oder Subfertilität bei St.n. Sectio als Differen-tialdiagnose in Betracht gezogen werden.
◆ Die Diagnostik sollte mittels TVUS erfolgen und standardisiert beurteilt werden. Ein MRI ist nur bei unklaren Befunden indiziert.
◆ Die verbleibende RMT ist für Folgeschwangerschaften prognostisch relevant und hat Einfluss auf die Wahl der Operationsmethode.
◆ Es stehen verschiedene OP-Methoden zur Nischensanierung zur
Verfügung, wobei bei Kinderwunsch eine Laparoskopietechnik
bevorzugt wird.
1. Bundesamt für Statistik, Tabelle Reproduktive Gesundheit, https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/reproduktive.html, zuletzt abgerufen am 17.03.2023, 00:31 Uhr.
2. Guise JM, Eden K, Emeis C, Denman MA, Marshall N, Fu RR, Janik R, Nygren P, Walker M, McDonagh. M Vaginal birth after cesarean: new insights. Evid Rep Technol Assess (Full Rep) 2010 Mar;(191):1-397.
3. Naji O, Abdallah Y, Bij de Vaate AJ, Smith A, Pexsters A, Stalder C, McIndoe A, Ghaem-Maghami S, Lees C, Brölmann HAM, Huirne JAF, Timmerman D, Bourne T. Standardized approach for imaging and measuring Cesarean section scars using ultrasonography. Ultrasound Obstet Gynecol 2012; 39: 252–259.
4. Van der Voet LF, Bij de Vaate AM, Veersema S, Brölmann HAM, Huirne JAF. Long-term complications of caesarean section. The niche in the scar: a prospective cohort study on niche prevalence and its relation to abnormal uterine bleeding. BJOG 2014;121:236–244.
5. Bij de Vaate AJM, Van der Voet LF, Naji O, Witmer M, Veersema S, Brölmann HAM, Bourne T, Huirne JAF. Prevalence, potential risk factors for development and symptoms related to the presence of uterine niches following Cesarean section: systematic review. Ultrasound Obstet Gynecol 2014; 43: 372–382.
6. Vervoort AJMW, Uittenbogaard LB, Hehenkamp WJK, Brölmann HAM, Mol BWJ, Huirne JAF. Why do niches develop in Caesarean uterine scars? Hypotheses on the aetiology of niche development. Human Repro- duction, Vol.30, No.12 pp. 2695–2702, 2015.
7. Wang CB, Chiu WWC, Lee CY, Sun YL, Lin YH, Tseng CJ. Cesarean scar defect: correlation between Cesarean section number, defect size, clinical symptoms and uterine position. Ultrasound Obstet Gynecol 2009; 34: 85–89.
8. Vikhareva Osser O, Jokubkiene L, Valentin L. High prevalence of defects in Cesarean section scars at transvaginal ultrasound examination. Ultrasound Obstet Gynecol 2009; 34: 90–97.
9. Ofili-Yebovi D, Ben-Nagi J, Sawyer E, Yazbek J, Lee C, Gonzalez J, Jurkovic D. Deficient lower-segment Cesarean section scars: prevalence and risk factors. Ultrasound Obstet Gynecol 2008; 31: 72–77.
10. Pomorski M, Fuchs T, Rosner-Tenerowicz A, Zimmer M. Morphology of the cesarean section scar in the non-pregnant uterus after one elective cesarean section. Ginekol Pol. 2017;88(4):174-179.
11. Vikhareva Osser O, Valentin L. Risk factors for incomplete healing of the uterine incision after caesarean section. BJOG 2010;117:1119–1126.
12. Jastrow N, Gauthier RJ, Gagnon G, Leroux N, Beaudoin F, Bujold E. Impact of labor at prior cesarean on lower uterine segment thickness in subsequent pregnancy. Am J Obstet Gynecol. 2010 Jun;202(6):563.e1-7.
13. Zimmer EZ, Bardin R, Tamir A, Bronshtein M. Sonographic imaging of cervical scars after Cesarean section. Ultrasound Obstet Gynecol 2004; 23: 594–598.
14. Roberge S, Demers S, Berghella V, Chaillet N, Moore L, Bujold E. Impact of single- vs double-layer closure on adverse outcomes and uterine scar defect: a systematic review and metaanalysis. Am J Obstet Gynecol 2014;211:453 – 460.
15. Roberge S, Chaillet N, Boutin A, Moore L, Jastrow N, Brassard N, Gau- thier RJ, Hudic I, Shipp TD, Weimar CH et al. Single- versus double- layer closure of the hysterotomy incision during cesarean delivery and risk of uterine rupture. Int J Gynaecol Obstet 2011;115:5-10.
16. Bujold E, Bujold C, Hamilton EF, Harel F, Gauthier RJ. The impact of a single-layer or double-layer closure on uterine rupture. Am J Obstet Gynecol 2002;186:1326–1330.
17. Bujold E, Goyet M, Marcoux S, Brassard N, Cormier B, Hamilton E, Abdous B, Sidi EA, Kinch R, Miner L et al.The role of uterine closure in the risk of uterine rupture. Obstet Gynecol 2010;116:43-50.
18. Durnwald C, Mercer B. Uterine rupture, perioperative and perinatal morbidity after single-layer and double-layer closure at cesarean delivery. Am J Obstet Gynecol 2003;189:925-929.
19. Roberge S, Chaillet N, Boutin A, Moore L, Jastrow N, Brassard N, Gau- thier RJ, Hudic I, Shipp TD, Weimar CH et al. Single- versus double- layer closure of the hysterotomy incision during cesarean delivery and risk of uterine rupture. Int J Gynaecol Obstet 2011;115:5-10.
20. Bennich G, Rudnicki M, Wilken-Jensen C, Lousen T, Lassen PD, Wo- jdemann K. Impact of adding a second layer to a single unlocked closure of a Cesarean uterine incision: randomized controlled trial. Ultra- sound Obstet Gynecol 2016; 47: 417–422.
21. CORONIS collaborative group, Abalos E, Addo V, Brocklehurst P, El Sheikh M, Farrell B, Gray S, Hardy P, Juszczak E, Mathews JE, Naz Masood S, Oyarzun E, Oyieke J, Sharma JB, Spark P. Caesarean section surgical techniques: 3 year follow-up of the CORONIS fractional, factorial, unmasked, randomised controlled trial. Lancet. 2016 Jul 2;388(10039):62-72.
22. Lofrumento DD, Di Nardo MA, De Falco M, Di Lieto A. Uterine Wound Healing: A Complex Process Mediated by Proteins and Peptides. Curr Protein Pept Sci. 2017;18(2):125-128.
23. Bij de Vaate AJM, Brölmann HAM, Van der Voet LF, Van der Slikke JW, Veersema S, Huirne JAF. Ultrasound evaluation of the Cesa- rean scar: relation between a niche and postmenstrual spotting. Ultrasound Obstet Gynecol 2011; 37: 93–99.
24. Tower AM, Frishman GN. Cesarean scar defects: an underrecognized cause of abnormal uterine bleeding and other gynecologic complications. J Minim Invasive Gynecol. 2013 Sep-Oct;20(5):562-72.
25. Stegwee S, Beij A, de Leeuw R, Mokkink L, van der Voet L, Huirne J. Niche-related outcomes after caesarean section and quality of life: a focus group study and review of literature, Qual Life Res. 2020 Apr;29(1):1013-1025.
26. Vikhareva Osser O, Jokubkiene L, Valentin L. Cesarean section scar defects: agreement between transvaginal sonographic findings with and without saline contrast enhancement. Ultrasound Obstet Gynecol 2010; 35: 75–83.
27. Baranov A, Gunnarsson G, Salvesen KA, Isberg PE, Vikhareva O. Assessment of Cesarean hysterotomy scar in non-pregnant women: reliability of transvaginal sonography with and without contrast enhancement. Ultrasound Obstet Gynecol 2016; 47: 499–505.
28. Regnard C, Nosbusch M, Fellemans C, Benali N, Van Rysselberghe M, Barlow P, Rozenberg S. Cesarean section scar evaluation by saline contrast sonohysterography. Ultrasound Obstet Gynecol 2004; 23: 289–292.
29. Bolten K, Fischer T, Bender YY, Diederichs G, Thomas A. Pilot study of MRI/ultrasound fusion imaging in postpartum assessment of Cesarean section scar. Ultrasound Obstet Gynecol. 2017 Oct;50(4):520-526.
30. Naji O, Daemen A, Smith A, Abdallah Y, Saso S, Stalder C, Sayasneh A, McIndoe A, Ghaem-Maghami S, Timmerman D, Bourne T. Visibility and measurement of cesarean section scars in pregnancy: a reproducibility study. Ultrasound Obstet Gynecol. 2012 Nov;40(5):549-56.
31. Pomorski M, Fuchs T, Zimmer M. Prediction of uterine dehiscence using ultrasonographic parameters of cesarean section scar in the non- pregnant uterus: a prospective observational study. BMC Pregnancy and Childbirth 2014, 14:365.
32. Dicle O, Küçükler C, Pirnar T, Erata Y, Posaci C. Magnetic reso- nance imaging evaluation of inscision healing after cesarean sections. Eur Radiol. 1997;7(1):31-4.
33. Baranov A, Salvesen KA, Vikhareva O. Assessment of Cesarean hysterotomy scar before pregnancy and at 11–14weeks of gestation: a prospective cohort study.Ultrasound Obstet Gynecol 2017; 50: 105–109.
34. Vikhareva Osser O, Valentin L. Clinical Importance of Appearance of Cesarean Hysterotomy Scar at Transvaginal Ultrasonography in Non- pregnant Women.Obstet Gynecol 2011;117:525–32.
35. Abacjew-Chmylko A, Wydra DG, Olszewska H. Hysteroscopy in the treatment of uterine cesarean section scar diverticulum: A systematic review. Adv Med Sci. 2017 Sep;62(2):230-239.
36. Al Mutairi BH und Alrumaih I. Hysteroscopy in the Treatment of Myometrial Scar Defect (Diverticulum) Following Cesarean Section Delivery: A Systematic Review and Meta- Analysis. Cureus 12(11): e11317.
37. He Y, Zhong J, Zhou W, Zeng S, Li H, Yang H, Shan N. Four Surgical Strategies for the Treatment of Cesarean Scar Defect: A Systematic Review and Network Meta-analysis. J Minim Invasive Gynecol. Mar-Apr 2020;27(3):593-602.
38. Mashiach R und Burke YZ. Optimal Isthmocele Management: Hysteroscopic, Laparoscopic, or Combination. J Minim Invasive Gynecol. 2021 Mar;28(3):565-574.
39. Vitale SG, Ludwin A, Vilos GA, Török P, Tesarik J, Vitagliano A, Lasmar RB, Chiofalo B. From hysteroscopy to laparoendoscopic surgery: what is the best surgical approach for symptomatic isthmocele? A systematic review and meta-analysis. Arch Gynecol Obstet. 2020 Jan;301(1):33-52.
40. Donnez O. Cesarean scar defects: management of an iatrogenic pathology whose prevalence has dramatically increased. Fertil Steril. 2020 Apr;113(4):704-716.
info@gynäkologie
- Vol. 13
- Ausgabe 2
- April 2023