- Duktales Carcinoma in situ der Brust: ein Update
Das duktale Carcinoma in situ (DCIS) ist weltweit auf dem Vormarsch. Bei circa 20% aller im Mammographiescreening detektierten Neoplasien handelt es sich um ein DCIS. In diesem Artikel fassen wir die aktuellen Empfehlungen zur Therapie des DCIS zusammen. Dabei wird auch auf die 10-Jahres-Follow-up-Daten der TAM-01 Studie eingegangen, die den adjuvanten Einsatz von «Baby-TAM» nach verschiedenen prämalignen Läsionen untersucht hat.
Ductal carcinoma in situ (DCIS) is on the rise worldwide. Approximately 20% of all neoplasms detected in mammography screening are DCIS. In this article, we summarize the current recommendations for the treatment of DCIS. The 10-year follow-up data from the TAM-01 trial, which investigated the adjuvant use of “Baby-TAM” after various premalignant lesions, is also discussed.
Key Words: Ductal carcinoma in situ, TAM-01 trial, Baby-TAM, premalignant lesions
Einleitung
Bei ca. 20% der mittels Mammographie diagnostizierten Neoplasien handelt es sich um ein duktales Carcinoma in situ (DICS), welches zumeist durch radiologisch suspekt angeordnete Mikroverkalkungen entdeckt wird. In den letzten Jahren kam es durch die Einführung von Screeningprogrammen zu einem deutlichen Anstieg der diagnostizierten DCIS-Fälle von etwa 3% vor Einführung des Screenings auf über 25%. Diese deutliche Zunahme der Inzidenz des DCIS birgt auch eine gewisse Gefahr der Überdiagnose und Übertherapie dieser Erkrankung.
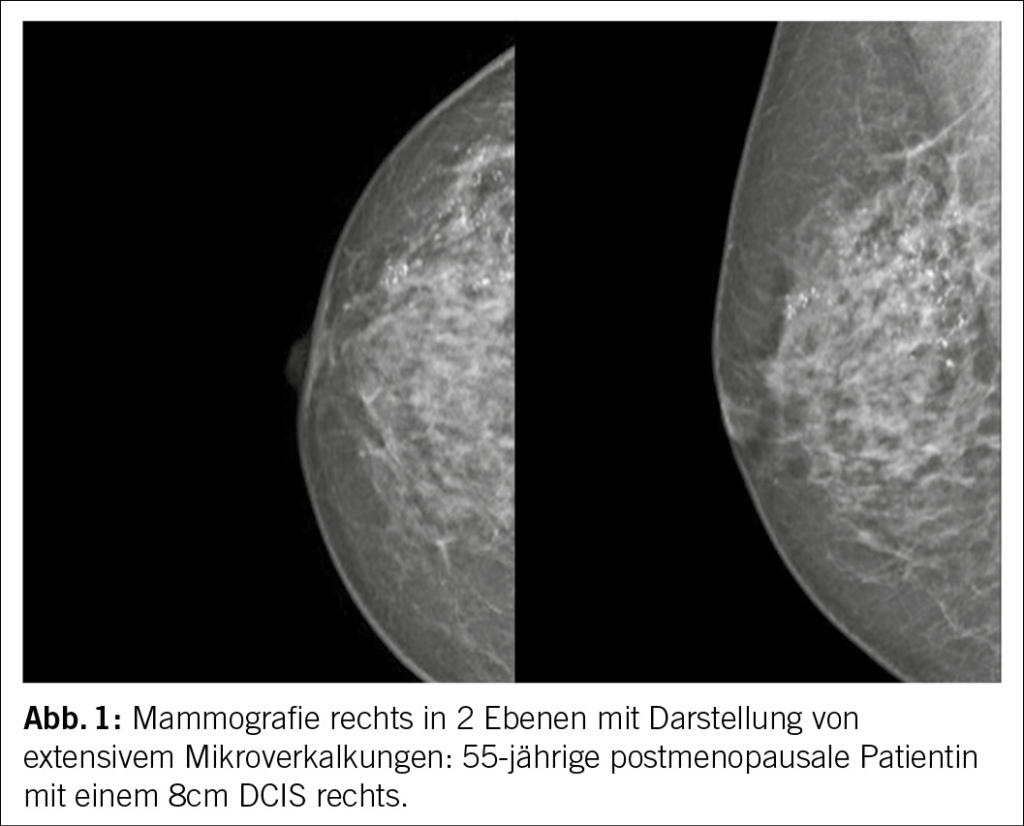
Das Krankheitsbild des DCIS ist sehr häufig assoziiert mit Mikroverkalkungen im Gewebe (Abb. 1). DCIS bilden nur selten einen Knoten und sind deshalb praktisch nicht durch eine Tastuntersuchung zu entdecken. In den meisten Fällen handelt es sich hierbei um eine Zufallsdiagnose im Rahmen der Vorsorge. In den letzten Jahren wird über alle Fachbereiche hinweg sehr intensiv diskutiert, inwiefern welche Therapien sinnvoll sind, um unnötige Interventionen zu vermeiden. Dieser Artikel soll einen Überblick über die aktuellen Behandlungsempfehlungen geben und einen kritischen Blick darauf werfen, was wirklich mit einem Nutzen für die Patientin einhergeht.
Histopathologie und natürlicher Verlauf
Das duktale Carcinoma in situ gehört pathomorphologisch zu einer sehr heterogenen Gruppe von präinvasiven Läsionen mit unterschiedlichem malignen Potential. Das Spektrum erstreckt sich von kleinen low-grade Befunden bis hin zu ausgedehnten high-grade Läsionen. Das Hauptmerkmal des DCIS ist die fehlende Stromainvasion. In manchen Ländern wird auch von einem intraduktalen Karzinom als non-invasivem Brustkrebs gesprochen, welcher durch eine Proliferation von abnormen Zellen innerhalb der Basalmembran erklärt wird.
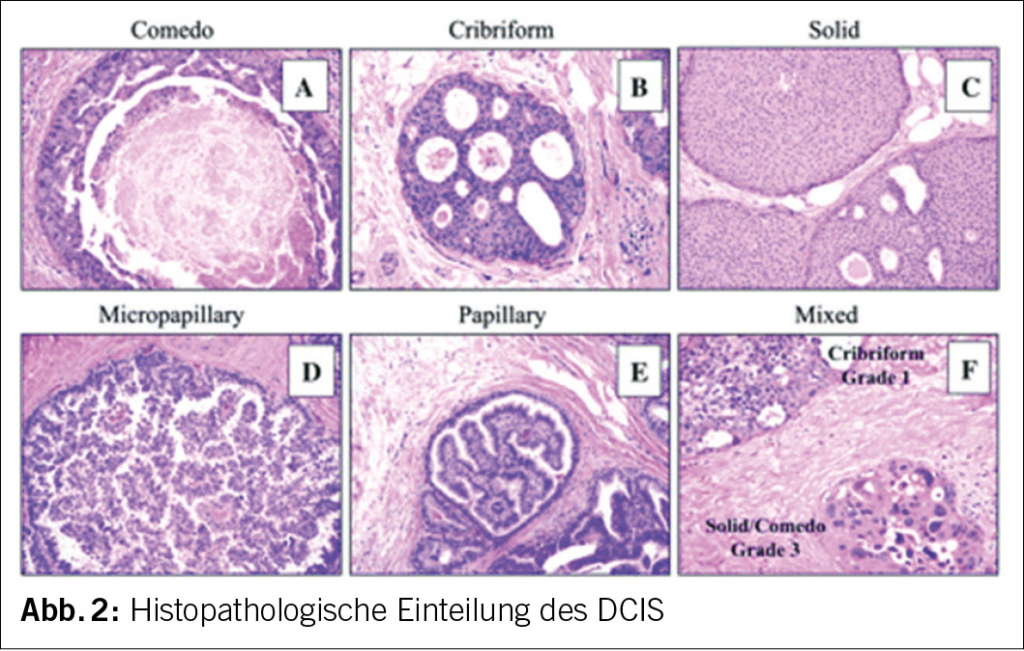
Eine Einteilung nach Pathologie und Wachstumsmuster zum besseren Verständnis dieser Krankheit ist sinnvoll (Abb. 2). Es werden die Komedo-Typen und Nicht-Komedo Typen unterschieden. Bei dem häufigsten Typ, dem DCIS vom Komedo Typ, zeigen die zentralen Zellen eine Nekrose mit Kalzifikationen. Sie sind deutlich aggressiver im Wachstum als die Nicht-Komedo Typen und gehen in circa 40% der Fälle in ein invasives Karzinom über. Bei den Nicht-Komedo Typen werden solide, kribriforme, papilläre, mikropapilläre und gemischte Typen unterschieden. Trotz der ausgeprägten Heterogenität der DCIS-Typen und der damit verbundenen unterschiedlichen klinischen Verläufe, wird heutzutage noch jedes DCIS praktisch gleichbehandelt. Ansätze, die verschiedenen DCIS- Entitäten besser charakterisieren zu können und dementsprechend auch zielgerechter behandeln zu können, liegen beispielsweise in der Nutzung von Multigen-Panel-Testungen (wie z.B. Oncotype DX Breast DCIS Score). Das Ziel dieser Testung ist es, die jeweiligen biologischen Eigenschaften des DCIS zu berücksichtigen und über Risiko-Scores Patientengruppen zu identifizieren, die weniger Therapie benötigen (1). Diese Testungen sind allerdings heutzutage noch wenig im Einsatz.
Leider fehlen noch immer Prädiktoren zur Abschätzung des Progressionsrisikos eines DCIS, die darüber Auskunft geben, wann das DCIS in ein invasives Karzinom übergeht. Aus den wenigen vorhandenen Publikationen zum natürlichen Verlauf des DCIS wird ersichtlich, dass ein unbehandeltes high-grade DCIS in mehr als 50% der Fälle innerhalb von 5 Jahren in ein invasives Karzinom übergehen kann. Auch ca. 35-50% der low-grade DCIS gehen in ein invasives Karzinom über, allerdings über einen Zeitraum von > 40 Jahren (2).
Operative Therapie des DCIS
Der Stellenwert der Operation des DCIS ist weiterhin unbestritten und ist nach den aktuellen Leitlinien der AGO-Mamma die wichtigste Therapiesäule. Gemäss diesen Empfehlungen sollte bei einem histologisch gesicherten DCIS eine Exzision des Befundes erfolgen. Inwiefern eine brusterhaltende Therapie oder eine Mastektomie durchgeführt werden kann, hängt natürlich von verschiedenen Faktoren, wie insbesondere Grösse von Läsion und Brust, ab und muss interdisziplinär und mit der Patientin diskutiert werden. Die ausreichende chirurgische Resektion des DCIS ist ein wichtiger Pfeiler der operativen Therapie. Da eine Korrelation zwischen freien Resektionsrändern und der lokalen Kontrolle besteht (3), sollte der Sicherheitsabstand zu den Resektionsrändern ≥ 2 mm betragen (4). Jedoch wird das Outcome der Patientinnen nachweislich nicht verbessert, wenn die Schnittränder grösser sind. Daher wird auch in einem Konsensus der SSO-ASTRO-ASCO – basierend auf einer Metaanalyse aus 20 Studien mit insgesamt 8651 Patientinnen – ein Resektatrand von 2 mm beim DCIS als ausreichend erachtet (5,6).
Eine Intervention in der Axilla mittels Sentinellymphonodektomie ist nur bei einer Mastektomie indiziert.
Strahlentherapie
Eine weitere Säule der Behandlung des DCIS ist die Bestrahlung. In den aktuellen AGO – Guidelines werden die konventionelle fraktionierte Radiotherapie (50 Gy in 25 Fraktionen) und die hypofraktionierte Radiotherapie (40-42,5 Gy in 15-16 Fraktionen) weiterhin als Standard formuliert (7). Dieses wird empfohlen nach einer brusterhaltenden Therapie und nicht nach einer Mastektomie.
Die adjuvante Radiotherapie muss jedoch mit der Patientin auf der Basis einer Risiko-Nutzen-Bewertung individuell erörtert werden, da sie keinen Einfluss auf das Gesamtüberleben hat.
In der NSABP-B17 und dem EORTC 10853-Trial wurde gezeigt, dass die meisten Lokalrezidive bei high-grade DCIS mit positiven oder unbekannten Resektionsrändern auftraten. Die Radiotherapie führte zur Reduktion, aber nicht zur Eliminierung der Lokalrezidivrate mit einer ca. 50%igen Risikoreduktion in allen Subgruppen. Insgesamt konnte kein Einfluss auf das Gesamtüberleben der Patientinnen festgestellt werden. Die Nebenwirkungen und Nachteile der Radiotherapie müssen gegenüber der erreichbaren Risikoreduktion abgewogen werden. Falls man auf eine Bestrahlung nach einer brusterhaltenden Therapie verzichtet, erhöht sich das lokale Rezidivrisiko ohne Einfluss auf das Überleben der Patientin. In einzelnen Fällen (z.B. hohes Alter der Patientin, kleine low risk-DCIS mit ausreichenden Resektaträndern) sollte über einen Verzicht der Bestrahlung diskutiert werden. Laufende Studien, wie der LORIS Trial (Low Risk DCIS Trial) aus England oder die LORD (Low Risk DCIS) Study der EORTC sollen die Frage klären, bei welchen Frauen vielleicht auch ein aktives Monitoring ausreicht.
Endokrine Therapie
Tamoxifen kann das Risiko für ein ipsilaterales DCIS-Rezidiv um 25% und das Auftreten eines kontralateralen DCIS-Rezidivs um 50% senken (8). Die Cochrane-Analyse zeigte aber auch, dass invasive ipsilaterale Rezidive nicht signifikant reduziert wurden, es jedoch zu einer signifikanten Reduktion der kontralateralen invasiven Karzinome kam. Insgesamt liegt die «Number needed to treat» bei 15 Patientinnen für alle In-Brust Events. Die «Number needed to treat» um ein invasives Mammakarzinom zu verhindern, liegt bei 59. Es zeigte sich kein Benefit für das Gesamtüberleben. Diesem geringen Benefit für die Reduktion lokaler Events steht ein nicht zu vernachlässigendes Nebenwirkungsprofil gegenüber: Lebensqualitätseinschränkungen, ein erhöhtes Thrombose-/Embolie-Risiko und ein erhöhtes Risiko für Endometriumkarzinome müssen sorgfältig abgewogen werden.
Die Aromataseinhibitoren wie z.B. das Anastrozol zeigen in der adjuvanten Anwendung hier vergleichbare Effekte wie das Tamoxifen. In der IBIS-II DCIS Studie (9) konnte kein Unterschied in der Rezidivrate zwischen Anastrozol und Tamoxifen festgestellt werden. Aber auch hier ist das Nebenwirkungsspektrum zu beachten, wie z.B. die Reduktion der Knochendichte, Gelenkschmerzen und Wechseljahresbeschwerden. Es ist ebenfalls zu beachten, dass sich alle Studien bezüglich adjuvanter endokriner Therapien auf postmenopausale Patientinnen beziehen, die eine brusterhaltende Therapie erhalten haben. Somit kann aktuell aufgrund der Nebenwirkungen und der aber unveränderten Gesamtmortalität die endokrine Therapie bei einem DCIS nicht generell empfohlen werden. Sicherlich kann man aber auch in Einzelfällen die endokrine Therapie als Option für die Rezidivprophylaxe anbieten.
Low-dose Tamoxifen (Baby-TAM)
In der Phase-III-TAM-01-Studie wurden 500 Frauen mit prämalignen bzw. Hochrisikoläsionen eingeschlossen: 20% mit atypischer duktaler Hyperplasie, 11% mit LCIS und 69% mit DCIS. Diese Frauen wurden randomisiert und erhielten für 3 Jahre entweder 5 mg Tamoxifen oder Placebo täglich. Nach einem medianen Follow-up von 9,7 Jahren wurden 15 in situ und 51 invasive Mammakarzinome diagnostiziert: 25 in der low-dose-Tamoxifengruppe und 41 in der Placebogruppe (Hazard ratio [HR], 0.58; 95% CI, 0.35 to 0.95; log-rank P = .03). Die meisten Rezidive waren invasiv (77%) und traten ipsilateral auf (59%). Bei den kontralateralen Rezidiven traten sechs im Tamoxifenarm auf und 16 im Placeboarm (HR, 0.36; 95% CI, 0.14 to 0.92; P = .025). Um einen Brustevent in der Tamoxifengruppe zu verhindern, mussten – bezogen auf einen Zeitraum von 10 Jahren – 14 Frauen behandelt werden. Dieser Benefit konnte in allen Subgruppen gesehen werden. Es zeigte sich eine signifikante 50-prozentige Rezidivreduktion in der DCIS-Kohorte, die 70% der Gesamtpopulation in der TAM-01-Studie repräsentierte (HR, 0.50; 95% CI, 0.28 to 0.91; P = .02). Zwischen der Placebogruppe und der low-dose Tamoxifengruppe zeigten sich auch im verlängerten Follow-up keine Unterschiede bezüglich der Inzidenz von Nebenwirkungen.
Mit den nun vorliegenden 10 Jahres-Follow-Up-Daten stellt low-dose Tamoxifen eine echte Alternative zur adjuvanten endokrinen Therapie beim DCIS dar, insbesondere bei Frauen mit einem höheren Risikoprofil.
Copyright bei Aerzteverlag medinfo AG
Interdisziplinäres Brustzentrum Kantonsspital Baden
5404 Baden
Interdisziplinäres Brustzentrum
Kantonsspital Baden AG
Im Ergel 1
5404 Baden
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Der Goldstandard der Therapie des DCIS bleibt weiterhin die operative Therapie mit ausreichendem Sicherheitsabstand ≥ 2 mm.
◆ In den meisten Fällen ist die Durchführung einer brusterhaltenden Therapie möglich und sollte hier auch bevorzugt werden.
◆ Im Anschluss an die operative Entfernung sollte, insbesondere beim high-grade DCIS, eine adjuvante Radiatio der betroffenen Brust erfolgen. Diese muss jedoch mit der Patientin auf der Basis einer Risiko-Nutzen-Bewertung individuell erörtert werden.
◆ Nach einer Mastektomie ist keine postoperative Bestrahlung indiziert.
◆ Aufgrund des hohen Nebenwirkungsspektrum der endokrinen Therapie ohne positiven Einfluss auf das Gesamtüberleben wird eine adjuvante endokrine Therapie bei einem DCIS nicht generell empfohlen.
◆ Eine endokrine Deeskalation mit Tamoxifen 5mg, dem sogenannten «Baby-TAM», kann erwogen werden.
1. Solin LJ, Gray R, Baehner FL, et al.: A multigene expression assay to predict local recurrence risk for ductal carcinoma in situ. J Natl Cancer Inst 2013; 105: 701–10
2. Sanders ME et al., ModernPathology 2015 ; 28,662–669
3. Lebeau A, Kühn T: Updates in the treatment of ductal carcinoma in situ of the breast. Curr Opin Obstet Gynecol 2016; 28; 49–58
4. Dunne C, Burke JP, Morrow M, Kell MR: Effect of margin status on local recurrence after breast conservation and radiation therapy for ductal carcinoma in situ. J Clin Oncol 2009; 27: 1615–20
5. Morrow M et al. J Clin Oncol. 2016;34:4040-4046.
6. Marinovich ML et al. JAMA Surg. 2020;155(10):e203025
7. www.ago-online.de/fileadmin/ago-online/downloads/_leitlinien/kommission_mamma/2023/Einzeldateien_Literatur/AGO_2023D_07_DCIS_REF.pdf
8. Staley H, et al.: Postoperative Tamoxifen for ductal carcinoma in situ: Cochrane systematic review and meta-analysis. Breast 2014; 23: 546–51
9. Forbes JF et al. Lancet 2016; 387: 866–73
10. DeCensi A. et al: J Clin Oncol 2019, 37:1629-1637.
11. Lazzeroni M. et al. J Clin Oncol. 2023 Jun 10;41(17):3116-3121.
info@gynäkologie
- Vol. 13
- Ausgabe 6
- Dezember 2023