- Hormonanalytik in der gynäkologischen Sprechstunde
Zyklusstörungen sind häufige Anliegen in der gynäkologischen Praxis und können auf hormonelle Dysregulationen wie das polyzystische Ovarialsyndrom hinweisen. Die Hormonanalyse dient dazu, verschiedene Hormone wie die Gonadotropine (FSH, LH) Östradiol, Testosteron, Sexualhormon-bindende Globuline (SHBG), Dihydroepiandrosteron (DHEAS), Thyroidea-stimulierendes Hormon (TSH), Prolaktin und das Anti-Müller-Hormon (AMH) zu bewerten. Diese Parameter ermöglichen Einblicke in die ovarielle Funktion, den Menstruationszyklus und das endokrine Gleichgewicht der Patientin. Insbesondere bei Hinweisen auf Androgenisierung oder Hyperandrogenismus ist eine differenzierte Hormonanalyse von grosser Bedeutung. Die Identifizierung von Zyklusstörungen und Hormonungleichgewichten eröffnet die Möglichkeit zur gezielten Therapie, die von der hormonellen Regulation bis zur Behandlung spezifischer Symptome reichen kann. Ein umfassendes Verständnis der zugrunde liegenden Pathophysiologie und eine individualisierte Herangehensweise sind entscheidend, um die Gesundheit und das Wohlbefinden von Frauen mit Zyklusstörungen und Androgenisierung effektiv zu managen.
Menstrual disorders are common concerns in gynecological practice and can signal hormonal dysregulations such as polycystic ovary syndrome. Hormone analysis serves to assess various hormones including gonadotropins (FSH, LH), estradiol, testosterone, sex-hormone-binding globuline (SHBG), dehydroepiandrosteron (DHEAS), prolactine, thyroidea stimulating hormone (TSH) and anti-mullerian hormne (AMH). These parameters offer insights into ovarian function, the menstrual cycle, and the patient’s endocrine balance. A detailed hormone analysis is particularly crucial when there are indications of androgenization or hyperandrogenism. Identifying menstrual disorders and hormonal imbalances provides the opportunity for targeted therapy, ranging from hormonal regulation to treating specific symptoms. A comprehensive understanding of the underlying pathophysiology and an individualized approach are essential for effectively managing the health and well-being of women experiencing menstrual disorders and androgenization.
Key words: Menstrual disorders, hormonal dysregulations, hormonal analysis
Hormonanalytik in der Praxis
Die Hormonanalytik spielt während der reproduktiven Phase einer Frau in der Diagnosestellung eine entscheidende Rolle. Sie ist unverzichtbar sowohl für das Monitoring des Menstruationszyklus als auch für die differenzierte Diagnose von Zyklusstörungen. Weitere häufige Anliegen wie Androgenisierungserscheinungen können oft nur durch endokrinologische Diagnostik geklärt werden.
Der vorliegende Artikel vermittelt die grundlegenden Prinzipien der Hormonanalytik, die in der täglichen Arbeit der gynäkologischen Praxis Anwendung finden.
Der weibliche Hormonhaushalt ist komplex und sollte nicht einseitig betrachtet werden. Daher sollten auch die Lebensumstände, Ernährungsgewohnheiten und die Einnahme von Medikamenten in die Diagnose miteinbezogen werden (1).
Physiologie
Die übergeordnete Funktionseinheit zur Steuerung des weiblichen Zyklus besteht aus dem Hypothalamus und der Hypophyse. Das Ovar fungiert als Zielorgan und bewirkt unter anderem durch die Produktion weiblicher Geschlechtshormone die charakteristischen Effekte des weiblichen Zyklus. Die Gonadotropine LH (Luteinisierendes Hormon) und FSH (Follikelstimulierendes Hormon) erfüllen bei beiden Geschlechtern eine zweifache Funktion: Sowohl die Produktion der Keimzellen als auch die Bildung und Ausschüttung von Sexualhormonen aus den Eierstöcken und Hoden werden durch die beiden Gonadotropine gesteuert.
Die Voraussetzung für einen normalen ovulatorischen Zyklus ist die pulsatile Sekretion von LH, die unter anderem durch die Ausschüttung von GnRH (Gonadotropin Releasing Hormone) und die Rückkopplung des Östradiols beeinflusst wird. FSH vermittelt die Umwandlung zu Östrogenen in den Granulosazellen. Gonadotropine werden ihrerseits durch positive und negative Feedback-Mechanismen der Steroide reguliert (2).
Vor dem Einsetzen einer regulären Menstruation und dem Beginn eines neuen Menstruationszyklus, falls keine Schwangerschaft eingetreten ist, erfolgt die Luteolyse des Gelbkörpers, gefolgt von einem darauffolgenden Abfall der Östradiol- und Progesteronspiegel.
Das Anti-Müller-Hormon und die Ovarreserve
Die Bedeutung des Anti-Müller-Hormons (AMH) im Zusammenhang mit der ovariellen Reserve nimmt eine besondere Stellung ein. Der Höchstwert im Lebensverlauf wird etwa im 25. Lebensjahr erreicht. AMH verringert die Anfälligkeit der Granulosazellen für FSH und blockiert somit die Rekrutierung von Follikeln aus dem Pool der primordialen Follikel sowie die Sekretion des dominierenden Follikels. AMH bestimmt in erheblichem Masse somit den Verbrauch von Follikeln (2).
Die AMH-Konzentration sinkt mit abnehmendem Follikelpool und somit mit einer altersbedingten Reduktion der Gesamtmasse an Granulosazellen. Eine AMH-Bestimmung ist daher sinnvoll, wenn Zyklusstörungen auftreten und das FSH auffällig hoch ist oder wenn eine Stimulation mit FSH-Medikamenten im Rahmen einer Kinderwunschbehandlung geplant ist.
Basierend auf den Erkenntnissen lässt sich feststellen, dass die AMH-Werte nur dann eine valide Einschätzung der ovariellen Reserve und der Fertilität ermöglichen, wenn eine Subfertilität vorliegt, also wenn über einen Zeitraum von mindestens 12 Monaten aktiv eine Schwangerschaft angestrebt wurde. Die Messung von AMH bei Frauen ohne Kinderwunsch liefert keinen verlässlichen Hinweis darauf, ob der spätere Zeitpunkt für eine Schwangerschaft eher unter-, überdurchschnittlich oder altersgemäss sein wird (3,4).
Zur Beurteilung der ovariellen Reserve sind FSH, Östradiol (in der frühen Follikelphase) und das AMH geeignet. AMH wird als der aussagekräftigste Parameter für die Einschätzung der ovariellen Reserve betrachtet. Mit zunehmendem Alter nimmt der Follikelvorrat ab, was zu einem Rückgang des AMH-Werts führt. Ein AMH-Wert unterhalb der Nachweisgrenze bedeutet jedoch nicht zwangsläufig, dass bereits die Wechseljahre eingetreten sind.
Selbst bei AMH-Werten unter-halb der Nachweisgrenze können noch ovulatorische Zyklen auftreten. Untersuchungen haben gezeigt, dass im Durchschnitt 5–6 Jahre nach dem Verlust der Nachweisbarkeit das Einsetzen der Menopause beobachtet wurde (3).
Zyklusdiagnostik
Für die Basisdiagnostik kann man mit hoher Wahrscheinlichkeit davon ausgehen, dass ein ovulatorischer Zyklus vorliegt, wenn die Patientin einen regelmässigen Menstruationszyklus angibt.
Eine Hormonanalyse kann dennoch im Rahmen des Zyklusmonitorings durchgeführt werden. Hierbei erfolgt die Basisbestimmung zur Erfassung der ovariellen Funktion zu Beginn des Menstruationszyklus in der Follikelphase (2.–5. Zyklustag). In dieser Phase sind üblicher-weise niedrige Östradiol- und Gonadotropinspiegel festzustellen.
Ein erhöhter FSH-Serumspiegel im Frühfollikelstadium (>12 U/l) deutet auf eine ovarielle Störung hin, deren Gründe weiter untersucht werden sollten.
Die Detektion eines LH-Peaks, der der Ovulation 18-24h vorausgeht, ist möglich, jedoch sind möglicherweise mehrere LH-Messungen erforderlich (5).
Klinisch hat sich die Einzelmessung von LH und Östradiol in der Zyklusmitte sowie die gleichzeitige sonographische Beurteilung der Endometriumdicke mit Grösse und Anzahl der Follikel als gängige Vorgehensweise etabliert. Als Alternative besteht die Möglichkeit, den LH-Peak durch den Gebrauch handelsüblicher, urinbasierter Ovulationstests mit akzeptabler Genauigkeit zu erfassen (6).
Die Lutealphase setzt nach der Ovulation ein, die durch den mitt-zyklischen Anstieg von LH ausgelöst wird. Durch die Freisetzung der Oozyte aus dem dominierenden Follikel entsteht das Corpus luteum. Neben Östrogenen, weiteren Hormonen und Wachstumsfaktoren sezerniert es vor allem Progesteron, das als Schlüsselhormon der zweiten Hälfte des Menstruationszyklus fungiert.
Etwa 4-6 Tage nach der Ovulation wird im weiblichen Zyklus als der optimale Zeitpunkt für die Rezeptivität des Endometriums und eine erfolgreiche Implantation angesehen.
Gegen Ende der zweiten Zyklushälfte ist die Sekretion von Progesteron verstärkt mit der LH-Pulsatilität verbunden, was zu einer zunehmenden Schwankungsbreite der gemessenen Serumwerte für Progesteron führen kann. Aufgrund der variablen Ausschüttung von Progesteron im pulsierenden Rhythmus scheint ein einzelner, zu niedrig bestimmter Wert nicht geeignet zu sein, um eine Lutealphaseninsuffizienz zu dokumentieren.
Ein grundlegendes Problem in Bezug auf die Definition einer Lutealphaseninsuffizienz liegt daher in der fehlenden verlässlichen und validen diagnostischen Methode zur Beurteilung der Sekretionsleistung des Corpus luteum. Rein klinisch kann eine verkürzte zweite Zyklushälfte oder das Auftreten prämenstrueller Schmierblutungen sowie Spotting auf die Lutealphaseninsuffizienz hinweisen (2).
Hormonanalyse bei Zyklusstörungen
Die Beschreibung einer normalen Menstruation umfasst eine moderate Blutung von 3 bis 7 Tagen Dauer mit einem Blutverlust von unter 80 ml. Die Eumenorrhoe geht in der Regel mit minimalen Beschwerden einher und folgt einem Zyklus von 24 bis 35 Tagen.
Die Ursachen für Zyklusstörungen sind vielfältig. Hormonelle als auch organische Ursachen, (Stress, Polypen, Myome, Asherman-Syndrom, Essstörungen und Leistungssport) können unregelmässige Zyklen verursachen.
Eine eindeutige Indikation für eine umfassendere hormonelle Diagnostik liegt vor, wenn Zyklusstörungen auftreten, die sich als Unregelmässigkeiten im Menstruationsrhythmus oder im Menstruationstypus manifestieren können.
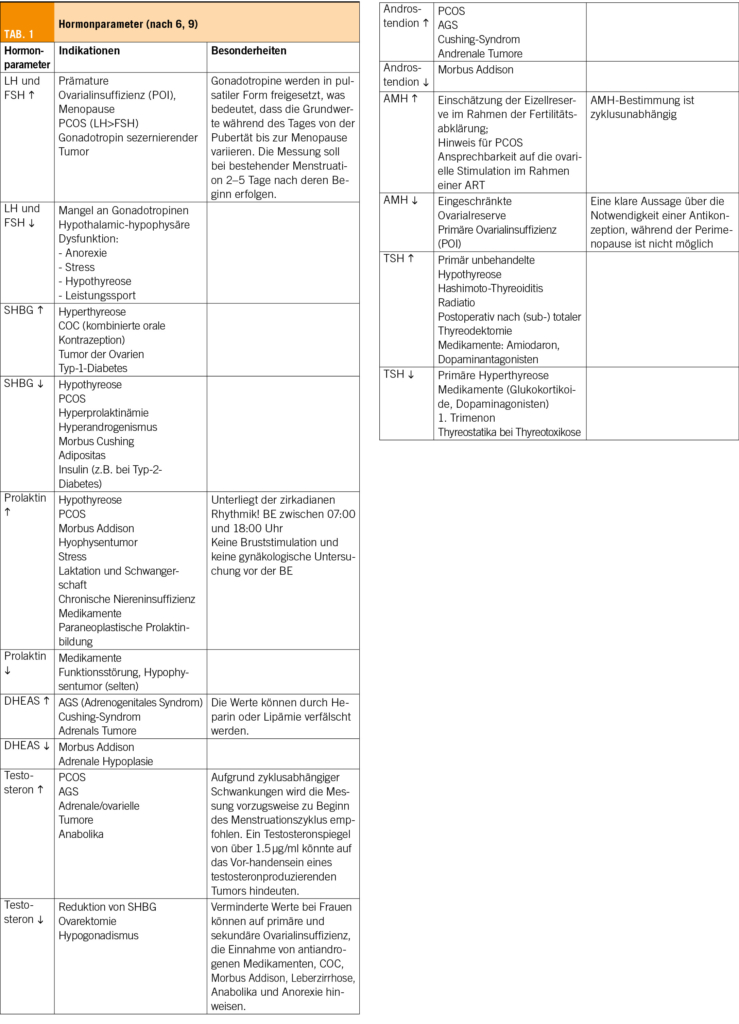
Diese Diagnostik sollte idealerweise zwischen dem 2. und 5. Zyklustag oder während der ovariellen Funktionsruhe (Amenorrhoe) durchgeführt werden. Relevante Parameter zur Untersuchung von Zyklusstörungen umfassen LH, FSH, Östradiol, Gesamttestosteron, Sexualhormon-bindendes-Globulin (SHBG), Dehydroepiandrosteron-Sulfat (DHEAS), Prolaktin und (Thyroidea stimulierendes Hormon) TSH, sowie den Ausschluss einer Schwangerschaft (6).
Präanalytik
Die Verwendung hormoneller Kontrazeptiva führte in verschiedenen Studien zu einer Senkung der AMH-Werte im Vergleich zu Frauen, die keine solchen Präparate einnehmen (bis zu 30 % niedrigere Werte) (7). Die Dosierung von Ethinylestradiol in den Präparaten hatte dabei keine Auswirkung. Nach dem Absetzen der hormonellen Kontrazeptiva wurde jedoch eine signifikante Zunahme der AMH-Spiegel festgestellt (8).
Auch andere Medikamente können einen Einfluss auf die Hormondiagnostik haben. Prolaktin ist ein typisches Beispiel eines hormonellen Parameters, der durch Medikamenteneinnahme beeinflusst wird. Insbesondere die Einnahme von Neuroleptika, Antidepressiva, Gastroprokinetika, aber auch einige Antihypertensiva führen zu erhöhten Prolaktinwerten im Serum und können so auch klinische Symptome (z. B. Galaktorrhö, Oligo-/Amenorrhö) bewirken (9) (siehe Tab. 1).
Diagnostik der Androgenisierung
Der Ausdruck Androgenisierung bezeichnet die serologischen oder phänotypischen Veränderungen einer Frau, die typischerweise zu männlich orientierten Merkmalen führen.
Zeichen der Androgenisierung, wie zum Beispiel vermehrter Haarwuchs im männlichen Muster (Hirsutismus), Akne, und androgenetische Alopezie (männlicher Haarausfall), mit oder ohne Zyklusstörungen gehören zu den häufigsten Gründen für eine gynäkologische Konsultation. Differenzialdiagnotisch müssen die funktionelle Androgenisierung (polyzystisches Ovarialsyndrom PCOS, Adrenogenitales Syndrom AGS), androgen produzierende Tumore und die pharmakologisch bedingte Androgeniserung (z.B. Anabolika) in Betracht gezogen werden.
Um eine Hyperandrogenämie oder einen Hyperandrogenismus differenzialdiagnostisch zu untersuchen, werden insbesondere folgende Hormone bestimmt:
– Gesamt-Testosteron
– DHEAS
– Androstendion
– SHBG
Testosteron ist ein lipophiles Steroidhormon, das im Blutplasma zu etwa 60 % an SHBG und zu etwa 30–40 % an Albumin gebunden wird. Obwohl bisher kein guter Assay für die direkte Messung des freien Testosterons verfügbar ist, wird empfohlen, neben der Bestimmung des Gesamttestosterons auch den SHBG-Spiegel zu messen. Dies ermöglicht die Ableitung des Anteils des freien, also wirksamen Testosterons. Der freie Androgenindex (FAI) kann auf diese Weise ermittelt werden. Bei einem Anstieg der adrenalen Androgene wie DHEAS und Androstendion wird im Rahmen der differenzialdiagnostischen Untersuchung, insbesondere bei entsprechender klinischer Symptomatik, ein Cushing-Syndrom als mögliche Ursache für die Hyper-androgenämie ausgeschlossen. Hierfür erfolgt die Bestimmung von Cortisol. Bei nachgewiesener Erhöhung des Cortisols wird ein Dexamethason-Kurztest durchgeführt.
Auch sollte bei einem Anstieg der adrenalen Androgene ein möglicher Enzymdefekt in der Nebenniere durch eine frühzyklische Überprüfung von 17-Hydroxyprogesteron (17-OHP) ausgeschlossen werden. Bei erhöhten 17-OHP-Spiegeln (>2 ng/ml) wird ein ACTH-Stimulationstest durchgeführt. Bei auffälligem ACTH-Test erfolgt eine anschliessende molekulargenetische Diagnostik zur Präzisierung des Enzymdefektes.
Ein Testosteronspiegel von >1,5–2 ng/ml oder ein DHEAS-Spiegel von >7 μg/ml, zusammen mit schnell fortschreitenden Androgenisierungssymptomen, können auf das Vorliegen eines androgenbildenden Tumors hinweisen.
Wenn die Hyperandrogenämie oder der Hyperandrogenismus auf das polyzystische Ovarialsyndrom (PCOS) zurückzuführen ist, wird in der Grunddiagnostik zusätzlich ein oraler Glukosetoleranztest (oGTT) empfohlen. Dies dient dazu, eine Insulinresistenz auszuschliessen, die bei mehr als 30% der Betroffenen nachgewiesen werden kann (6).
Zyklusstörungen spielen eine führende Rolle bei unerfülltem Kinderwunsch.
Ein unregelmässiger Zyklus oder eine Amenorrhoe deuten auf mögliche Störung der Follikelreifung oder Ovulation hin. Hormonveränderungen können auch die Lutealphase beinträchtigen.
Etwa 15% der Frauen mit einer Paarsterilität haben ihre Ursache in Anovulation oder einer Störung der Follikulogenese. Klinisch kann dies als primäre oder sekundäre Amenorrhoe auftreten.
Normogonadotrope Anovulationen werden sehr häufig durch PCOS verursacht.
Hypogonadotrope Anovulationen werden häufig durch eine hypothalamisch-hypophysäre Dysfunktion verursacht, die zum Beispiel auf einen niedrigen Body-Mass-Index (BMI) oder starke körperliche oder psychische Belastungen zurückzuführen sein kann.
Hypergonadotrope Anovulationen sind häufig ein Merkmal der prämaturen Ovarialinsuffizienz (9). Häufig gehen Zyklusstörungen mit Störungen des Prolaktinhaushalts einher. Ein erhöhter Prolaktinspiegel hemmt die Progesteronsekretion, was letztlich zu Zyklusstörungen und dem Ausbleiben der Ovulation führen kann.
Frauen mit PCOS haben ein erhöhtes Risiko für Endometriumhyperplasie aufgrund unregelmässiger oder fehlender Menstruationszyklen. Unbehandelte Zyklusstörungen bei PCOS können zu verschiedenen Komplikationen führen, darunter Sterilität, metabolische Störungen wie Insulinresistenz und Diabetes, Herz-Kreislauf-Erkrankungen und das Endometriumkarzinom.
In der Regel strebt man an, mindestens alle drei Monate eine Menstruation zu haben, um das Risiko einer Endometriumhyperplasie zu reduzieren. Dies kann durch Lebensstiländerungen, Medikamente zur Regulation des Menstruationszyklus und andere therapeutische Ansätze erreicht werden.
Auch bei postmenopausalen Frauen besteht eine Verbindung zwischen hohen Androgenspiegeln, Insulinresistenz und Typ-2-Diabetes mellitus (10).
Das nicht-klassische adrenogenitale Syndrom (AGS) mit einer Minderung der Enzymaktivität von CYP21A2 manifestiert sich nicht mit offensichtlichen Genitalauffälligkeiten, Kortisol- oder Aldosteronmangel, wie es bei der klassischen Form des AGS der Fall ist. Stattdessen treten die Symptome des Androgenüberschusses normalerweise erst im späteren Alter auf.
Bei Frauen mit geringen Anzeichen von Androgenisierung können die Verwendung von oral kombinierten Kontrazeptiva gewählt werden. Als erste Wahl können Ethinylestradiol (EE)/Levonorgestrel (LNG) und als zweite Wahl antiandrogene Gestagene in Betracht gezogen werden.
Aufgrund der Zeit, die bis zum sichtbaren Therapieerfolg benötigt wird, empfiehlt es sich bei ausgeprägtem Hirsutismus, neben einer hochdosierten antiandrogenen Therapie auch eine gleichzeitige mechanische Haarentfernung wie Laserbehandlungen in Betracht zu ziehen.
Nach einer mechanischen Haarentfernung im Gesichtsbereich kann die Anwendung von Efflornithin (Vaniqua 11,5 % Creme) dazu beitragen, das Nachwachsen der Haare zu verlangsamen (11). Insgesamt unterstreicht die gezielte Hormondiagnostik die Bedeutung einer umfassenden und differenzierten Herangehensweise an die Untersuchung und Behandlung von Zyklusstörungen, insbesondere im Zusammenhang mit Androgenisierung und PCOS. Dies ermöglicht eine verbesserte Betreuung und optimale Gesundheitsergebnisse für betroffene Frauen.
Copyright Aerzteverlag medinfo AG
Abteilung für Reproduktionsmedizin und
gynäkologische Endokrinologie
Frauenklinik Luzerner Kantonsspital
Spitalstrasse
6000 Luzern 16
Frauenklinik Luzerner Kantonsspital
Spitalstrasse
6000 Luzern 16
alexandra.kohlschwartz@luks.ch
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Die Hormondiagnostik sollte idealerweise zwischen dem 2. und 5. Zyklustag durchgeführt werden oder während der ovariellen Ruhephase (Amenorrhoe).
◆ Zu den bedeutenden Parametern für die Abklärung von Zyklusstörungen gehören TSH, LH, FSH, Östradiol, Testosteron, DHEAS, SHBG, Prolaktin und DHEAS.
◆ Die Messung des AMH bei Frauen ohne aktuellen Kinderwunsch gibt keine verlässliche Auskunft darüber, ob der spätere Zeitpunkt für eine Schwangerschaft eher unter-, über- oder altersgemäss sein wird.
◆ AMH ist ein anschauliches Beispiel dafür, dass die Bestimmung eines Hormonspiegels nur dann sinnvoll ist, wenn das Ergebnis direkte Konsequenzen für die folgende Diagnostik oder Therapie hat.
◆ Frauen mit PCOS (Ausschlussdiagnose ) haben aufgrund unregelmässiger oder ausbleibender Menstruationszyklen ein erhöhtes Risiko für Endometriumhyperplasie. Es wird generell angestrebt, alle drei Monate mindestens eine Menstruation zu haben.
1. Sonntag B. Zyklusstörungen. Gynäkologe 49, 357–372 (2016).
https://doi.org/10.1007/s00129-016-3878-1
2. Diedrich K., Ludwig M. Griesinger, Georg. Reproduktionsmedizin, 2. Auflage
3. Hagen CP, Aksglaede L, Sorensen K, Mouritsen A, Andersson AM, Petersen JH, Main KM, & Juul A (2012). Individual serum levels of anti-Mullerian hormone in healthy girls persist through childhood and adolescence: a longitudinale cohort study. Hum Reprod 27, 861-866.
4. Hagen CP, Vestergaard S, Juul A, Skakkebaek NE, Andersson AM, Petersen JH, Main KM, Hjollund NH, Ernst E, Bonde JP, Anderson RA, & Jensen TK (2012). Low concentration of circulating antimullerian hormone is not predictive of reduced fecundability in young healthy women: aprospective cohort study.
Fertil Steril.
5. Von Wolff M. Natural Cycle and minimal Stimulation IVF, Springer Nature Switzerland AG 2022
6. Segerer S., Sonntag B., Gutensohn K., Keck C. Hormonanalytik-was der Frauenarzt wissen muss. Gynäkologe 2018. Springer Medizin
7. Bentzen JG, Forman JL, Pinborg A, Lidegaard O, Larsen EC, Friis- Hansen L et al (2012). Ovarian reserve paramters: a comparison between users and non-users of hormonal contraception. Reprod Biomed Online 25(6):612-619
8. Van den Berg MH, van Dulmen-den Broeder E, Overbeek A, Twisk JW, Schats R, van Leeuwen FE et al (2010). Comparison of ovarian function markers in users of hormonal contraceptives during the hormone free interval and subsequent natural early follicular wphases. Hum Reprod 25(6): 150-1527
9. Von Wolff M., Stute P. Gynäkologische Endokrinologie und Reproduktionsmedizin, das Praxisbuch, Schattauer 2013.
10. Lerchbaum, E. Androgene und kardiovaskuläres Risiko/Androgens and cardiovascular risk, LaboratoriumsMedizin, vol. 36, no. 4, 2012, pp. 217-225. https://doi.org/10.1515/labmed-2011-0028
11. Ludwig M. Gynäkologische Endokrinologie, 3. Auflage, 2019
info@gynäkologie
- Vol. 14
- Ausgabe 3
- Juni 2024