- Nausea und Erbrechen in der Schwangerschaft
Nausea und Erbrechen sind sehr häufige Symptome (50-80%), die typischerweise im ersten Trimenon der Schwangerschaft auftreten. Davon erleiden 0,3-3% eine Hyperemesis gravidarum (HG), die schwerste klinische Form von anhaltendem Erbrechen in der Schwangerschaft (1). Die Ätiologie von Nausea mit und ohne Erbrechen in der Schwangerschaft (nausea and vomiting in pregnancy – NVP) ist höchst wahrscheinlich multifaktoriell. Hormonelle, mechanische, psychologische und genetische Faktoren spielen dabei eine Rolle (2-5). Im folgenden Beitrag soll die Wichtigkeit der systematischen Erhebung der Symptome, der weiteren Abklärungen sowie der Stufentherapie erläutert werden. Die Grundlage bietet dabei der Expertenbrief No. 76 der Schweizerischen Gesellschaft für Gynäkologie und Geburtshilfe (SGGG) (6).
Nausea and vomiting are very common symptoms (50-80%), typically occurring in the first trimester of pregnancy. Of these, 0.3-3% experience hyperemesis gravidarum (HG), the most severe clinical form of persistent vomiting in pregnancy (1). The etiology of nausea with and without vomiting in pregnancy (NVP) is most likely multifactorial. Hormonal, mechanical, psychological, and genetic factors all play a role (2-5). In the following article, the importance of a systematic assessment of symptoms, further investigations and stepwise therapy will be explained. The basis for this is provided by Expert Letter No. 76 of the Swiss Society of Gynecology and Obstetrics (SGGG) (6).
Key-Words: Nausea, vomiting, hyperemesis gravidarum
Definition und Diagnose
Der Übergang zwischen einer leichten NVP und einer HG ist oft schleichend. Das typische Krankheitsbild der HG ist anhaltendes Erbrechen, akute Dehydrierung, Hungern (Ketonurie) und Gewichtsverlust >5% im Vergleich zum Gewicht von vor der Schwangerschaft. Es handelt sich hierbei um eine Ausschlussdiagnose, die sich mit diesem typischen Krankheitsbild präsentiert, andere Ursachen aber ausgeschlossen werden müssen (6).
Der Schweregrad des Krankheitsbildes der NVP und insbesondere der HG wird oft unterschätzt (7). In einigen Ländern wurde in diesem Rahmen gar eine Zunahme von Notfallkonsultationen und schweren Formen der HG beobachtet, zudem beklagen Patientinnen in einer Umfrage ein suboptimales Management im Rahmen dieses Krankheitsbildes (7, 8). Es empfiehlt sich daher, ab der ersten Schwangerschaftskontrolle alle Schwangeren nach Symptomen der NVP zu fragen und dabei HG favorisierende Komorbiditäten und Differenzialdiagnosen mit in die Anamnese einzubeziehen (Tab. 1).
Um den Schweregrad und insbesondere auch die Indikation zur Hospitalisation bei HG richtig einzuschätzen, bietet sich die Benutzung von standardisierten Scores wie dem Pregnancy-Unique quantification of Emesis (PUQE-24) -Score (9) (Abb. 1) und dem etwas aufwändigerem HELP-Score (iOS HG Care App © gratis, The HER Foundation) an (10).
Komplikationen
Die HG ist nicht nur der Hauptgrund für eine Hospitalisation im ersten Trimenon, sondern auch mit schlechterem mütterlichem und kindlichem Outcome assoziiert (7). Zu den mütterlichen Komplikationen gehören kurzfristig häufig der übermässige Gewichtsverlust (>15%), eine Erschöpfung, welche nicht selten bis hin zu Suizidgedanken (32%) führen kann, ein durch die Dehydratation erhöhtes Thromboembolierisiko und Elektrolytverschiebung. In äusserst seltenen und schweren Fällen der HG wird aufgrund der Mangelernährung sogar von Wernicke Enzephalopathien berichtet (Vitamin-B-Mangel) (11). Längerfristig ist auch das Risiko einer mit einem posttraumtischen Stresssyndrom assoziierten Depression erhöht (18%) (12).
Bei einer leichten NVP-Symptomatik scheint die Versorgung des Ungeborenen gewährleistet. Feten von Frauen mit HG hingegen, haben eine leicht erhöhte Inzidenz an intrauterinen Wachstumsrestriktionen (IUWR), niedrigerem Geburtsgewicht und Frühgeburtsraten (12). Diese Komplikationen scheinen mit dem Schweregrad und der Dauer der HG zu korrelieren. In extremen Fällen mit Gewichtsverlust von >15% wurde letztlich eine Assoziation mit einem kleineren Kopfumfang, einem signifikant reduziertem kortikalen Hirnvolumen und einem erhöhten Risiko für neurologische Entwicklungsstörung und Autismus beschrieben (13, 14).
Abklärungen
Jede gewöhnliche Schwangerschaftskontrolle umfasst die Erhebung der Vitalparameter. Eine leichte Nausea und gelegentliches morgendliches Erbrechen (leichte NVP, PUQE-Score <6) im ersten Trimenon bedarf, bei sonst unauffälliger Anamnese, keiner weiteren Abklärungen. Bei mittelschwerer NVP (PUQE-Score 7-12) und HG (PUQE-Score >12) sollen aber weitere Abklärungen zur Abschätzung des Schweregrades und insbesondere auch zum Ausschluss von Differentialdiagnosen erfolgen. Der Expertenbrief No. 76 empfiehlt hierzu, falls nicht bereits erfolgt, die Erhebung eines Urinstix, des maternalen Gewichtes, eine Ultraschalluntersuchung (Ausschluss einer Mehrlingsschwangerschaft oder Blasenmole) sowie eine Blutuntersuchung (Infektlabor, Elektrolyten, Nieren-, Leber und Schilddrüsenfunktionstest). In schweren Fällen folgen weitere Blutanalysen wie Blutgasanalyse und Vitaminstatus (insb. Vitamin B1) sowie weitere, klinisch orientierte Untersuchungen zum Ausschluss einer zugrunde liegender Pathologie (6).
Stufenschema Therapie
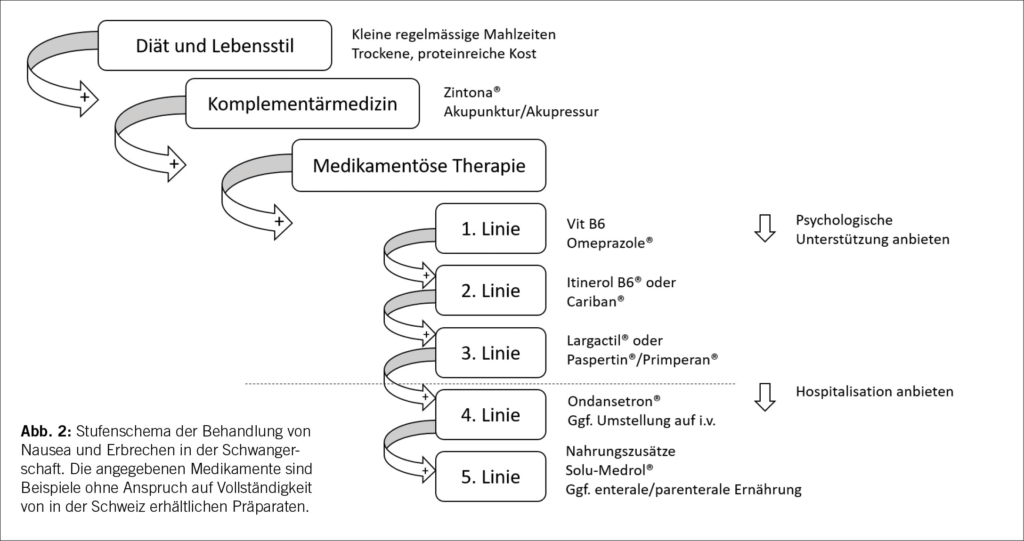
NVP und HG sollen mit einem symptomadaptierten Stufenschema behandelt werden (Tab. 2). Ziele dabei sind die Symptomreduktion, die Verbesserung der Lebensqualität und das Vorbeugen schwerer Komplikationen bei den betroffenen Frauen und Feten/Kindern. Die Behandlung soll zudem nach dem Prinzip «so viel wie nötig, so wenig wie möglich» erfolgen, um die potentiellen fetalen Auswirkungen der pharmakologischen Therapie möglichst kleinzuhalten (6).
1. Diät und Lebensstilveränderungen
Kleine Anpassungen in der Diät und im Lebensstil können bei leichter NVP bereits sehr entlastend wirken. Hierzu gehört das Vermeiden von einem ganz leeren oder einem zu vollen Magen. Dies lässt sich mit regelmässigen, kleinen Malzeiten erreichen (15, 16).
Zwischensnacks mit trockenen und proteinhaltigen Nahrungsmitteln (z.B. Knäckebrot) und auch das Verzehren derselben bereits vor dem Aufstehen, können helfen (17, 18). Zudem kann der Verzicht von Eisenpräparaten und grossen Mulitvitamintabletten Linderung der NVP Symptomatik bringen (24). Folsäure Monopräparate sollten, wenn irgendwie möglich, beibehalten und weiter eingenommen werden.
2. Komplementärtherapie
Es konnte gezeigt werden, dass Ingwer und Ingwerpräparate (z.B. Zintona® p.o.) Nausea reduzieren können, nicht aber die Anzahl von Erbrechen (1, 19). Bei Akupunktur und Akupressur gibt es keine klare Evidenz in der Behandlung von NVP (19, 20). Der Placebo-Effekt kann sich für einige Patientinnen aber durchaus positiv auswirken.
3. Pharmakologische Stufentherapie
Die erste Linie der medikamentösen Therapie besteht aus der Substitution von Pyridoxin (Vitamin B) per p.o. (6). Auch hierzu gibt es gute Evidenz für einen positiven Effekt auf die Nausea, nicht aber aufs Erbrechen (1). Bei Sodbrennen kann es Sinn machen zusätzlich einen Protonen-Pumpen-Inibitor zum Beispiel Esomeprazole (Omeprazol® p.o.) zu verordnen.
Als Zweitlinientherapie wird zusätzlich ein Antihistaminikum, entweder ein Kombinationspräparat mit Meclozin/Pyridoxin/Koffein (Itinerol B6® p.o) oder mit dem etwas neuere Präparat mit Doxylamin/Pyridoxin (Cariban® p.o), erfolgreich angewandt. Beide diese Medikamente gelten als Mittel der Wahl bei NVP Symptomatik (6, 21).
Als Linie 3 wird die Therapie zusätzlich mit einem Dopaminantagonist ausgebaut (Largagtil® p.o oder Primperan/Paspertin® p.o)(6). Spätestens hier sollte auch eine psychologische Unterstützung angeboten werden.
In 4. Linie wird die Zugabe von einem Serotoninantagonisten (Ondansetron®/Zofran®) empfohlen. Der Erfahrungswert der Anwendung dieses Präparates in der Schwangerschaft ist sehr hoch (Embryotox). Da ein geringes Risiko an Teratogenizität – es wurden Fälle von Lippen-Kiefer-Gaumenspalte, Ventrikelseptumdefekt und Nierenagenesie beschrieben, jedoch mit geringer Evidenz (17, 18) – nicht ausgeschlossen werden kann, sollte es nur bei ausgeprägter Symptomatik und Versagen der primär empfohlenen Antiemetika eingesetzt werden (6, 21). Ab Linie 4 der medikamentösen Therapie sollte zusätzlich die Notwendigkeit einer Hospitalisation und die Umstellung der per os Medikation auf eine intravenöse Gabe der Präparate evaluiert werden.
In Linie 5 der pharmakologischen Therapie wird zusätzlich Methylprednisolon (Zolu-Medrol®) angewandt. Je nach Ansprechen der Therapie muss auch der Bedarf an Nahrungszusätzen (weitere Vitamine i.v.) sowie die Umstellung auf eine enterale oder sogar parenterale Ernährung in Erwägung gezogen werden (6).
Prävention
Leider gibt es keine gute Evidenz für die Vermeidung von Nausea und Erbrechen in der Schwangerschaft. Eine präkonzeptionelle Beratung mit gemeinsamen Planen eines frühzeitigen Managements, sollte es zu Symptomen von NVP kommen, trägt sicherlich zu einer gewissen psychologischen Sicherheit bei.
Copyright bei Aerzteverlag medinfo AG
Klinik für Geburtshilfe
UniversitätsSpital Zürich
Frauenklinikstrasse 10
8091 Zürich
ladina.vonzun@usz.ch
Faculté de Médecine, Université de Genève, Suisse.
Département de pédiatrie, gynécologie et obstétrique
Hôpitaux Universitaires de Genève (HUG)
30 Boulevard de la Cluse
1205 Genève, Suisse
bamt@hcuge.ch
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Beitrag deklariert.
◆ NVP sind sehr häufige (50-80%) Schwangerschaft assoziierte Symptome, welche häufig unterschätzt werden.
◆ Die schwere Form der HG (0.3-3%) geht mit einem erhöhten Risiko für mütterliche und fetale Morbidität und Mortalität einher.
◆ Das Erfragen von NVP Symptomatik soll ab der ersten Schwangerschaftskontrolle in die Anamnese integriert werden.
◆ Die Therapie der NVP soll nach einem Stufenschema erfolgen, welches mit diätetischen Massnahmen, Komplementärmedizin und Vitamingabe beginnt und mit einer pharmakologischen Therapie eskaliert wird.
1. Matthews A, Haas DM, O’Mathuna DP, Dowswell T. Interventions for nausea and vomiting in early pregnancy. Cochrane Database Syst Rev. 2015(9):CD007575.
2. Simpson SW, Goodwin TM, Robins SB, Rizzo AA, Howes RA, Buckwalter DK, et al. Psychological factors and hyperemesis gravidarum. J Womens Health Gend Based Med. 2001;10(5):471-7.
3. Flaxman SM, Sherman PW. Morning sickness: a mechanism for protecting mother and embryo. Q Rev Biol. 2000;75(2):113-48.
4. Fejzo MS, Sazonova OV, Sathirapongsasuti JF, Hallgrimsdottir IB, Vacic V, MacGibbon KW, et al. Placenta and appetite genes GDF15 and IGFBP7 are associated with hyperemesis gravidarum. Nat Commun. 2018;9(1):1178.
5. Fejzo MS, Myhre R, Colodro-Conde L, MacGibbon KW, Sinsheimer JS, Reddy M, et al. Genetic analysis of hyperemesis gravidarum reveals association with intracellular calcium release channel (RYR2). Mol Cell Endocrinol. 2017;439:308-16.
6. Martinez de Tejada B VL, Von Mandach U, Burch A, Yaron M, Hodel M, Surbek D, Hoesli I. Nausea and Vomiting of Pregnancy, Hyperemesis gravidarum. Expert Letter No 76. 2022.
7. Fejzo MS, Trovik J, Grooten IJ, Sridharan K, Roseboom TJ, Vikanes A, et al. Nausea and vomiting of pregnancy and hyperemesis gravidarum. Nat Rev Dis Primers. 2019;5(1):62.
8. Havnen GC, Truong MB, Do MH, Heitmann K, Holst L, Nordeng H. Women’s perspectives on the management and consequences of hyperemesis gravidarum – a descriptive interview study. Scand J Prim Health Care. 2019;37(1):30-40.
9. Ebrahimi N, Maltepe C, Bournissen FG, Koren G. Nausea and vomiting of pregnancy: using the 24-hour Pregnancy-Unique Quantification of Emesis (PUQE-24) scale. J Obstet Gynaecol Can. 2009;31(9):803-7.
10. MacGibbon KW, Kim S, Mullin PM, Fejzo MS. HyperEmesis Level Prediction (HELP Score) Identifies Patients with Indicators of Severe Disease: a Validation Study. Geburtshilfe Frauenheilkd. 2021;81(1):90-8.
11. Spruill SC, Kuller JA. Hyperemesis gravidarum complicated by Wernicke’s encephalopathy. Obstet Gynecol. 2002;99(5 Pt 2):875-7.
12. Veenendaal MV, van Abeelen AF, Painter RC, van der Post JA, Roseboom TJ. Consequences of hyperemesis gravidarum for offspring: a systematic review and meta-analysis. BJOG. 2011;118(11):1302-13.
13. Fejzo M, Kam A, Laguna A, MacGibbon K, Mullin P. Analysis of neurodevelopmental delay in children exposed in utero to hyperemesis gravidarum reveals increased reporting of autism spectrum disorder. Reprod Toxicol. 2019;84:59-64.
14. Fejzo MS, Magtira A, Schoenberg FP, Macgibbon K, Mullin PM. Neurodevelopmental delay in children exposed in utero to hyperemesis gravidarum. Eur J Obstet Gynecol Reprod Biol. 2015;189:79-84.
15. Bischoff SC, Renzer C. Nausea and nutrition. Auton Neurosci. 2006;129(1-2):22-7.
16. Erick M, Cox JT, Mogensen KM. ACOG Practice Bulletin 189: Nausea and Vomiting of Pregnancy. Obstet Gynecol. 2018;131(5):935.
17. Power ML, Holzman GB, Schulkin J. A survey on the management of nausea and vomiting in pregnancy by obstetrician/gynecologists. Prim Care Update Ob Gyns. 2001;8(2):69-72.
18. Jednak MA, Shadigian EM, Kim MS, Woods ML, Hooper FG, Owyang C, et al. Protein meals reduce nausea and gastric slow wave dysrhythmic activity in first trimester pregnancy. Am J Physiol. 1999;277(4):G855-61.
19. McParlin C, O’Donnell A, Robson SC, Beyer F, Moloney E, Bryant A, et al. Treatments for Hyperemesis Gravidarum and Nausea and Vomiting in Pregnancy: A Systematic Review. JAMA. 2016;316(13):1392-401.
20. Roscoe JA, Matteson SE. Acupressure and acustimulation bands for control of nausea: a brief review. Am J Obstet Gynecol. 2002;186(5 Suppl Understanding):S244-7.
21. www.embryotox.de.
info@gynäkologie
- Vol. 13
- Ausgabe 5
- Oktober 2023