- Neue Therapiestandards beim Zervixkarzinom
Die randomisierte SHAPE Studie zeigte, dass beim IA2 und IB1 Zervixkarzinom mit < 10mm Stromainvasion keine Exzision des parazervikalen Gewebes nötig ist. Dies hat auch Konsequenzen für fertilitätserhaltende Operationsmethoden. Beim lokal fortgeschrittenen Zervixkarzinom verbessert eine kurze Induktionschemotherapie über 6 Wochen vor Standard Chemo-Radiotherapie das Überleben, wie die INTERLACE Studie belegt. Beim lokal fortgeschrittenen Zervixkarzinom bringt die Zugabe des immun Checkpoint Inhibitors Pembrolizumab zur Standard Chemo-Radiotherapie (Cisplatin wöchentlich) eine Verbesserung des progressionsfreien und Gesamtüberlebens. Auch bei der Primärtherapie des metastasierten Zervixkarzinom verlängern immun Checkpoint Inhibitoren (Pembrolizumab oder Atezolizumab) in Kombination mit Chemotherapie und Angiogenesehemmer das mediane Gesamtüberleben um ca. 10 Monate.
The randomized SHAPE study could show that simple hysterectomy has the same recurrence rate as radical hysterectomy but less complications in early stage cervical cancer IA2 and IB1 with less than 10mm stromal invasion. This study will change practice also in fertility sparing surgery. In locally advanced cervical cancer a short induction chemotherapy over 6 weeks before standard chemo-radiotherapy does increase survival as shown in the INTERLACE study. Also the addition of the checkpoint inhibitor Pebrolizumab to chemo-radiotherapy was able to prolong survival. In metastasized cervical cancer the addition of a checkpoint inhibitor to standard chemotherapy including bevacizumab was able to prolong survival by about 10 months.
Keywords: cervical cancer, checkpoint inhibitor, induction chemotherapy, radical hysterectomy
Die Schweiz ist mit einer Inzidenz von 5 pro 100 000 Frauen pro Jahr ein Niedrigrisiko-Land betreffend Zervixkarzinom. Über 99 % aller Zervixkarzinome werden durch onkogene humane Papilloma Viren (HPV) verursacht, einzelne Zervixkarzinome des oberen Zervikalkanals sind offenbar HPV negativ. Mit der HPV-Impfung wird die niedrige Inzidenz in der Schweiz hoffentlich auch so bleiben oder sogar weiter sinken, wie Populations-basierte Studien aus Schweden und England vermuten lassen. Dort zeigte sich, dass Mädchen, welche sich vor dem 17 Lebensjahr impfen liessen, beinahe vollständig vor Zervixkarzinomen geschützt sind (1).
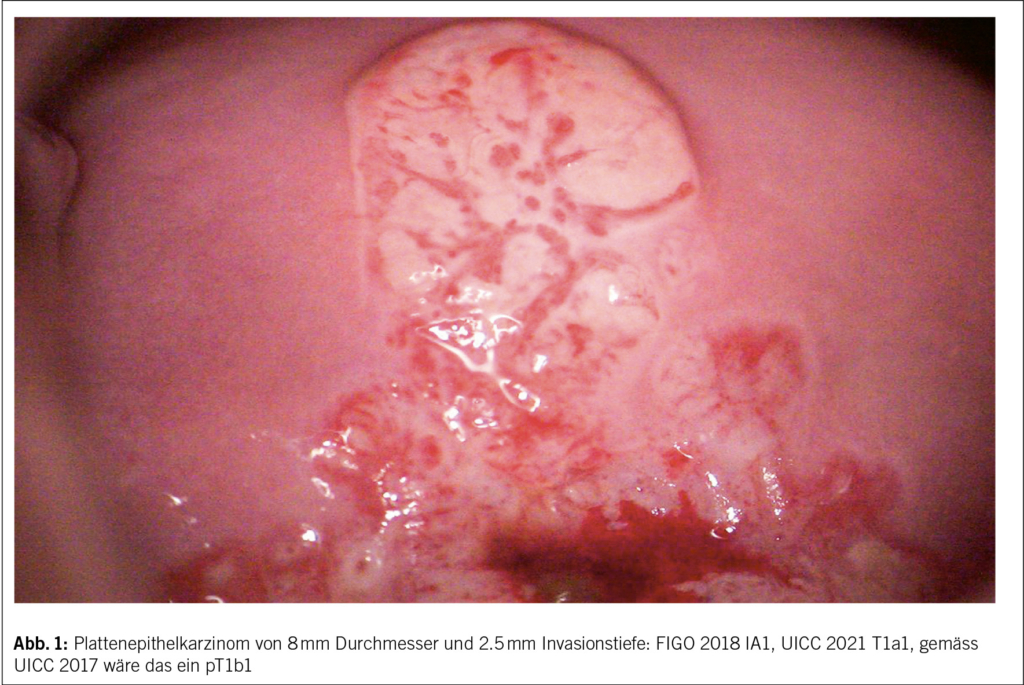
Die FIGO 2018 und UICC 2021 Klassifikation berücksichtigt die oberflächliche Ausdehnung eines frühen Karzinoms nicht mehr und klassifiziert allein aufgrund der Invasionstiefe: IA1 mit < 3 mm Invasionstiefe, IA2 mit 3.1– < 5 mm, IB1 > 5 mm Invasionstiefe und unter 2 cm Tumordurchmesser etc.
Konservativere chirurgische Therapie und Konsequenzen für die Fertilitätserhaltung
Schon lange ist bekannt, dass Metastasen im parazervikalen Gewebe beim frühen Zervixkarzinom sehr selten sind, selbst bei befallenen Lymphknoten. Die SHAPE Studie mit 700 Patientinnen mit Zervixkarzinom IA2 und IB1 (d. h. < 2 cm Durchmesser und < 10 mm Invasion im Konus oder im MRI < 50 % Stromainvasion unabhängig von Lymphangiose oder Grading und klinisch N0) wies die gleiche pelvine Rezidivrate bei einfacher Hysterektomie auf wie bei radikaler Hysterektomie jedoch mit deutlich weniger Komplikationen bei einer Nachkontrollzeit von 4.5 Jahren (2).
Somit können diese frühen Stadien schonender mit Sentinel Lymphknotenexzision (plus pelviner Lymphadenektomie bei IB1) und einfacher Hysterektomie behandelt werden. Diese Studie hat auch Konsequenzen für die fertilitätserhaltende Operation indem in diesen Stadien keine radikale Trachelektomie mehr durchgeführt werden muss und eine einfache Trachelektomie mit Sentinel Lymphknotenexzision (mit pelviner Lymphadenektomie bei IB1) genügt.
Lokal forgeschrittenes Zervixkarzinom:
Fortschritte mit Induktions Chemotherapie und Check-point Inhibitoren
Stadium IIB bis IVA gelten als lokal fortgeschrittene Zervixkarzinome, das heisst ohne Fernmetastasen. Die EORTC-55994 Studie verglich die neoadjuvante Chemotherapie gefolgt von radikaler Chirurgie mit der Standard Chemo-Radiotherapie bei 626 Patientinnen im Stadium IB3-IIB (3). Das 5-Jahresüberleben unterschied sich nicht in den zwei randomisierten Gruppen, sodass die Chemo-Radiotherapie (Radiotherapie mit Cisplatin wöchentlich) Standard bleibt, auch weil mehr schwere > Grad 3 Nebenwirkungen in der Gruppe mit neoadjuvanter Chemotherapie und Operation auftraten.
Auch die zusätzliche Gabe von 4 Zyklen Carboplatin/Paclitaxel Chemotherapie nach Standard Chemo-Radiotherapie mit Cisplatin brachten keine Verlängerung des 5-Jahresüberleben bei 919 randomisierten Patientinnen in der OUTBACK Studie (4).
Hingegen zeigte die Induktionschemotherapie über 6 Wochen mit wöchentlichem Paclitaxel 80 mg/m2 + Carbo AUC2 gefolgt von Cisplatin-Radiotherapie gegenüber der Standard Chemo-Radiotherapie in der randomisierten INTERLACE Studie einen Überlebensvorteil der Gruppe mit Induktionschemotherapie nach 5 Jahren von 80 % versus 72 % (5). Eine 6 wöchige wöchentliche Chemotherapie vor Chemo-Radiotherapie muss somit beim Stadium IB N1 bis IVA in Betracht gezogen werden.
Auch die Zugabe des Check-point Inhibitors Pembrolizumab während der Chemo-Radiotherapie (gefolgt von 15 Zyklen Pembrolizumab) konnte in der ENGOT Cx11/Keynote A-18 Phase III Studie (n = 1060) das progressionsfreie Überleben nach 2 Jahren um 10 % verbessern (67.8 % versus 57.3 %) (6). Ob die Prognoseverbesserung additiv zum Benefit der Induktions-Chemotherapie ist, müssen zukünftige Studien klären.
Metastasiertes Zervixkarzinom:
Prognoseverbesserung durch Immuntherapie
Vor sieben Jahren konnte erstmals wieder eine Prognoseverbesserung des metastasierten Zervixkarzinom durch die Zugabe des Angiogenesehemmers Bevacizumab zur Standard-Chemotherapie mit Platin/Paclitaxel erreicht werden (7). Der Benefit war allerdings überschaubar. Nun konnte die KEYNOTE-826 Studie einen Überlebensvorteil durch die Zugabe des Check-point Inhibitors Pembrolizumab nachweisen. 617 Patientinnen mit persistierendem, rezidivierendem oder primär metastasiertem Zervixkarzinom ohne vorhergehende Systemtherapie wurden in die randomisierte Studie eingeschlossen. Die Zugabe von Pembrolizumab zu Platin/Paclitaxel Chemotherapie (+/– Bevacizumab) führte bei PD-L1 positivem Zervixkarzinomen zu einer Verlängerung des progressionsfreien Überlebens von 8.2 auf 10.4 Monate (HR 0.58, CI 0.47–0.71, p < 0.001). Auch das Gesamtüberleben nach 24 Monaten wurde signifikant von 41.7 % auf 53 % erhöht.
Interessanterweise waren die Resultate ähnlich, wenn auch die kleine Gruppe PD-L1 negativer Zervixkarzinome in die Analyse miteingeschlossen wurde. Hingegen war die Gruppe der PD-L1 negativen Karzinome zu klein um einen Benefit in dieser Gruppe nachzuwiesen. Die Subgruppenanalyse zeigte, dass der Benefit unabhängig von der Verabreichung von Bevacizumab eintrat (8).
Auch die BEATcc Studie mit dem Check-point Inhibitor Atezolizumab zusätzlich zur Chemotherapie +/– Bevacizumab konnte eine signifikante Verlängerung des progressionsfreien- und Gesamtüberlebens nachweisen (9). Das mediane progressionsfreie Überleben wurde von 10.4 auf 13.7 Monate verlängert, und das mediane Gesamtüberleben von 22.8 Monate auf 32.1. Somit gehören diese Check-point Inhibitoren zur Standard-Primärtherapie beim metastasierten Zervixkarzinom.
Copyright Aerzteverlag medinfo AG
Chefarzt Gynäkologische Onkologie
Frauenklinik STGAG
Kantonsspital,
8501 Frauenfeld
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Beim IA2 und IB1 Zervixkarzinom mit < 10 mm Stromainvasion ist keine Exzision des parazervikalen Gewebes nötig.
- Beim lokal fortgeschrittenen Zervixkarzinom verbessert eine
kurze Induktionschemotherapie über 6 Wochen vor Standard Chemo- Radiotherapie das Überleben. - Beim metastasierten Zervixkarzinom verlängern immun Checkpoint Inhibitoren in Kombination mit Chemotherapie und Angiogenesehemmer das mediane Gesamtüberleben um ca. 10 Monate.
- Auch beim lokal fortgeschrittenen Zervixkarzinom bringt die Zugabe eines immun Checkpoint Inhibitors zur Standard Chemo-Radiotherapie (Cisplatin wöchentlich) eine Verbesserung des progressionsfreien und Gesamtüberlebens.
1. Lei J et al. N Engl J Med 2020;383:1340-1348
2. Plante M et al. N Engl J Med 2024;390:819-829
3. Kenter GG et al. J Clin Oncol 2023;41:5035-5043
4. Mileshkin LR et al. Lancet Oncol 2023;24:468-482
5. McCormack M et al. ESMO 2023
6. Lorusso D et al Lancet 2024;403:1341-1350
7. Tewari KS et al. Lancet 2017;390:1654-1663
8. Colombo N et al. N Engl J Med 2021;385:1856-1867
9. Oaknin A et al. Lancet 2024;403:31-43
info@gynäkologie
- Vol. 14
- Ausgabe 4
- August 2024