- Perioperatives Management von gynäkologischen Patientinnen
Dieser Artikel soll den Leserinnen und Lesern eine optimale Planung der perioperativen Phase ihrer Patientinnen unter Vermeidung unnötiger Massnahmen ermöglichen. Das Outcome unserer Patientinnen soll hierdurch verbessert und idealerweise sollen die Kosten reduziert werden. In den vergangenen Jahren konnten in der perioperativen Phase etliche alte Zöpfe abgeschnitten werden. Hervorzuheben sind hier die Richtlinien (1, 2) der europäischen Gesellschaft für Anästhesie, ESAIC sowie die britischen NICE-Guidelines. Bestanden Anästhesisten früher praktisch bei allen Patientinnen auf EKG, Labor und nicht selten auch auf ein Thorax-Röntgenbild, werden diese Untersuchungen heute nur noch ganz gezielt verordnet. Stattdessen sind heute Anämie-Therapie und das korrekte Management der Patientenmedikation ganz oben in der Prioritätsliste, um unsere Patientinnen optimal für die perioperative Phase vorzubereiten.
This article is intended to enable readers to plan the perioperative phase of their patients in the best possible way, avoiding unnecessary interventions. This will improve the outcome of our patients and ultimately reduce costs. In recent years, several old habits have been cut out of the perioperative phase. The guidelines (1, 2) of the European Society of Anesthesiology, ESAIC, and the British NICE guidelines should be emphasized here. Whereas anesthetists used to insist on an ECG, laboratory and often also a chest X-ray for practically all patients, these examinations are now only prescribed very specifically. Instead, anemia therapy and the correct management of patient medication are now at the top of the priority list to guarantee optimal preparation for the perioperative period.
Keywords: perioperative management, Anesthesiology guidelines
Welche Befunde sind für die Anästhesisten am wichtigsten?
Für eine sichere Patientenbetreuung sind aktuelle Befunde zu kardiologischen Abklärungen oder stattgefundenen kardialen Interventionen sowie die aktuelle Medikationsliste besonders wichtig. Falls vorhanden, können auch frühere Narkoseprotokolle hilfreich sein. Wenn bei der Patientin ein OSAS (Obstruktive Schlafapnoe) (3) bekannt ist, ist eine entscheidende Frage, ob diese behandelt wird und wenn ja, per CPAP (oder ähnlichem) oder per Schiene. Ganz wichtig ist, dass die Patientin dieses Gerät auch am Operationstag mitbringt (4, 5). Andernfalls ist unter Umständen eine intensive Überwachung in der ersten postoperativen Nacht notwendig. Dies verursacht unnötige Kosten und Aufwand. Für eine suffiziente Aufklärung benötigen Anästhesisten auch eine genaue Angabe über die Operationstechnik und Umfang der geplanten Operation. Nur wenn diese Angaben vorliegen, kann zum Beispiel das Analgesie-Konzept den Anforderungen entsprechend geplant werden. Auch für das Patient Blood Management (PBM) und für die Entscheidung, welche präoperativen Abklärungen notwendig sind, sind diese Angaben unumgänglich.
Präoperative Abklärungen
Der Fokus der präoperativen Phase für die Anästhesie liegt auf einer ausführlichen Anamnese, wenigen gezielten Untersuchungen und der Wegleitung zu relevanten Abklärungen durch andere Disziplinen wie zum Beispiel Kardiologie.
Wichtig für eine sichere Anästhesie sind Fragen nach eingeschränkter Leistungsfähigkeit, Angina pectoris sowie Belastungs- oder Ruhedyspnoe und weiteren «red flags». Auch eine orientierende Anamnese über die restlichen Organsysteme kann daher schon richtungsweisend sein.
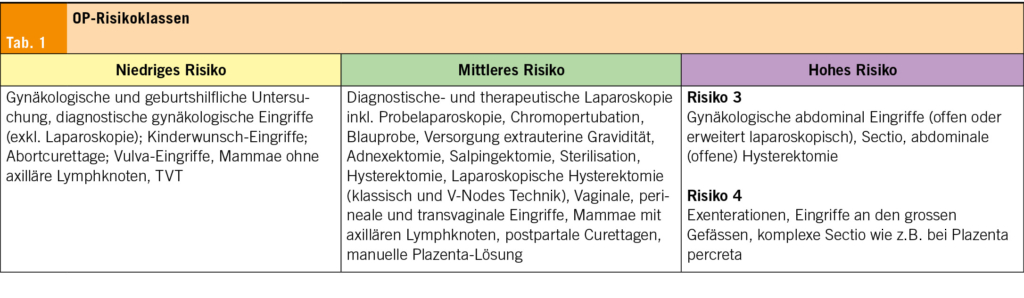
Entsprechend den britischen NICE-Guidelines (6) macht es Sinn, sich anhand der Vorerkrankungen der Patientin sowie der OP-Risikoklasse in einem nächsten Schritt ein Bild über die präoperativen Abklärungen zu machen (Tab. 1).
ASA-Klassifizierung
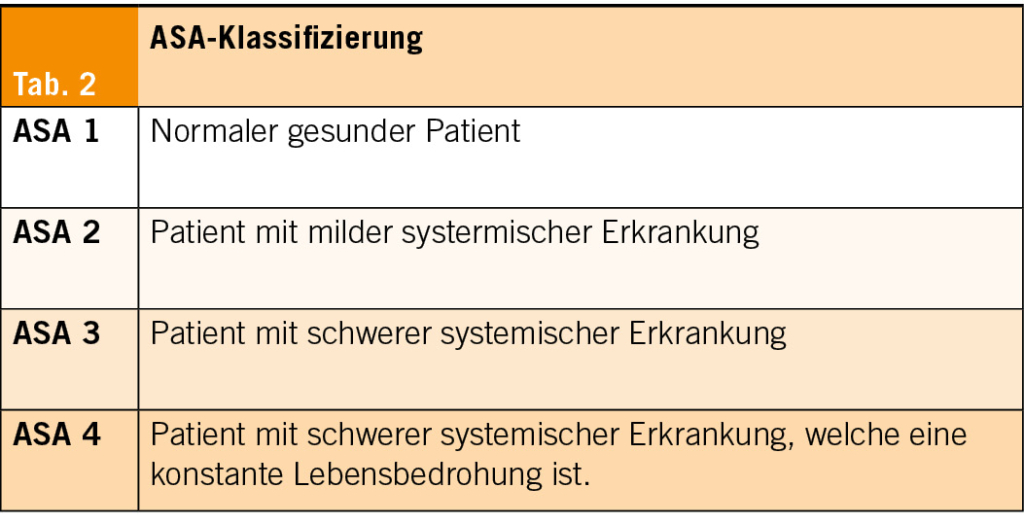
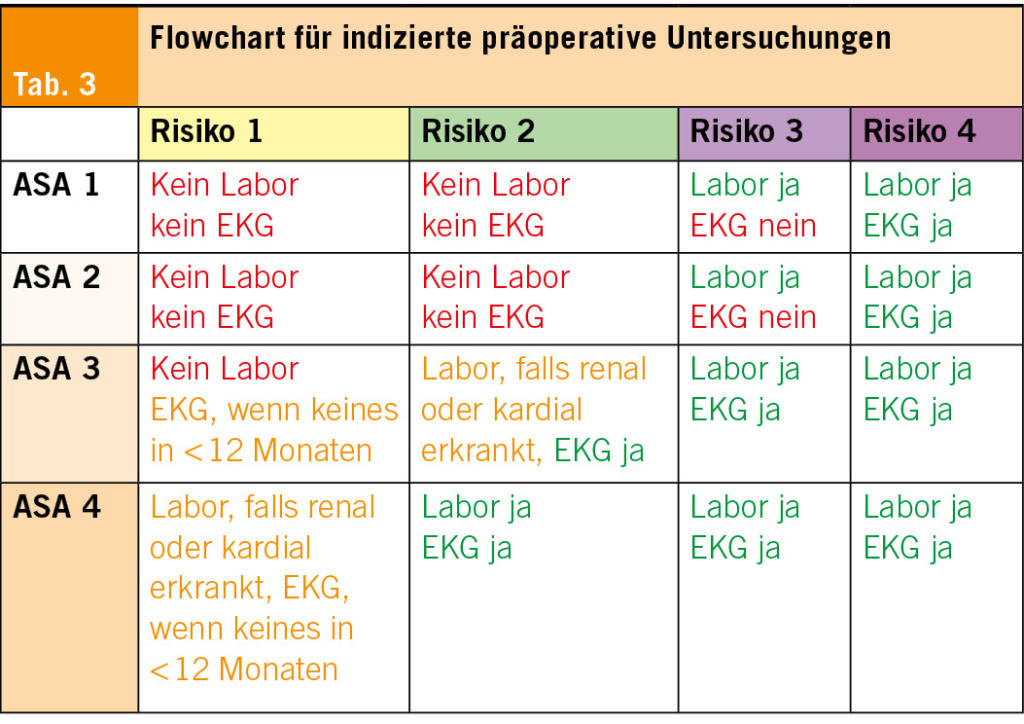
Anästhesisten klassifizieren den Gesundheitszustand und damit einhergehend das perioperative Risiko nach den sogenannten ASA-Klassen, diese wurden von der American Society of Anesthesiologists erstellt und kürzlich aktualisiert (Tab. 2, Tab. 3).
Wichtig: kein Routine-Thorax-Röntgen, auch keine Lungenfunktionsuntersuchungen ohne konkrete Indikation und Fragestellung. Speziell die Spirometrie (7) hat sich nicht als geeignet erwiesen, postoperative pulmonale Komplikationen zu prädiktieren. Eine Spirometrie ist lediglich bei schwerem OSAS oder bei chronischen Lungenerkrankungen nach Konsultation des behandelnden Spezialisten zu erwägen (15).
Labor
Falls entsprechend dem Flowchart eine Laboruntersuchung indiziert ist, werden folgende Parameter standardmässig abgenommen: Elektrolyte, Nieren- und Leberwerte, CRP, Ferritin, Transferrin-Sättigung, Hämatologie, Gerinnung.
Bei unklarer kardialer Situation zusätzlich NTproBNP (8, 1, 9)
Bei erhöhtem Blutungsrisiko auch Faktor XIII.
Allergologische Abklärungen
Sollte bei der Patientin der Verdacht auf eine Allergie auf ein perioperativ relevantes Medikament bestehen, so kann es sinnvoll sein, die Phase der gynäkologischen Abklärung auch für eine möglichst frühzeitige allergologische Stellungnahme oder Testung zu nutzen. Im Zweifelsfall ist es zu empfehlen, bei den Kollegen der Anästhesie nachzufragen, ob eine Allergietestung bei dieser Patientin notwendig ist. Der Vortag der OP bei der anästhesiologischen Aufklärung ist auf jeden Fall zu spät, um allergologische Fragen noch suffizient abklären zu können. Dies gilt besonders auch bei einer geplanten Sectio caesarea.
Patient Blood Management (PBM)
In den letzten Jahren wurde vielerorts das PBM fest etabliert (7). Hierbei geht es darum, eine Anämie präoperativ zu behandeln (10), intraoperativ möglichst blutungsarm unter optimalen Gerinnungsbedingungen zu operieren und so Transfusionen zu vermeiden. Dies, um zum einen das Outcome unserer Patientinnen zu verbessern, aber zum anderen auch um Kosten zu sparen. Patientinnen mit einer bekannten Anämie oder Operationen mit einem möglichen Blutverlust grösser 500ml bzw. einer Transfusionswahrscheinlichkeit > 10 % werden in das perioperative PBM eingeschlossen. Durch Bestimmung von Hb, Hämatokrit, Ferritin und Transferrin-Sättigung wird geklärt, ob die Anämie Therapie mit Vitamin B12, Folsäure, Eisen intravenös (nicht per os) und bei kurzfristig geplanten OPs auch Erythropoetin indiziert wird. Ziel ist, dass alle Patienten (Frauen und Männer) mit einem Hb ≥ 130 g/l und ohne Eisenmangel (Ferritin ≥ 100 µg/l und TSAT ≥ 20 %) zur Operation kommen (11). Auch wenn die WHO bei Frauen eine Anämie bei Frauen erst bei einem Hb < 120g/l definiert, macht es mindestens perioperativ Sinn, auch bei Patientinnen die Grenze bei 130g/l zu setzen. Frauen haben aufgrund der kleineren Körpergrösse ein geringeres Gesamt-Blutvolumen. So dass ein in Millilitern identischer Blutverlust bei einer Frau im Vergleich zu einem Mann einen grösseren prozentualen Blutverlust bedingt.
Intraoperativ kommt der Cell Saver, wann immer möglich und sinnvoll, zum Einsatz. Die Bestrahlung des gefilterten Blutes ist inzwischen so schnell und unkompliziert möglich, dass ein Karzinom keine Kontraindikation für diese blutsparende Technik ist. Auch hier empfiehlt sich eine enge Interaktion mit den lokalen Anästhesisten bzw. wenn vorhanden mit dem PBM-Team.
Management der vorbestehenden Patientenmedikation
Dieser Abschnitt ist von hoher Relevanz, denn es hat sich gezeigt, dass gerade hier noch Unklarheiten verbreitet sind. Eine gute Faustregel ist, Ihrem Anästhesie-Team das Stoppen, Pausieren oder Fortführen der Medikation zu überlassen oder zumindest die Expertise der Kolleginnen und Kollegen zu nutzen. Bei den Antihypertensiva zum Beispiel hängt es von der Klasse ab, ob sie beibehalten werden (z.B. Betablocker) oder gestoppt werden (z.B. ACE-Hemmer). Individuelle Entscheide hängen aber von der Patientin, der Operation sowie der geplanten Narkoseform ab.
Bei den direkten oralen Antikoagulanzien, kurz DOAK, vielerorts auch als NOAK (neue orale Antikoagulanzien) bezeichnet, wird aus zeitlichen Gründen oft schon vor der anästhesiologischen Visite das Management durch die Operateure festgelegt. DOACs müssen generell nie mit niedermolekularem Heparin gebridged werden (12, 5), sondern in der Regel nur für 24 bzw. 48 Stunden pausiert werden.
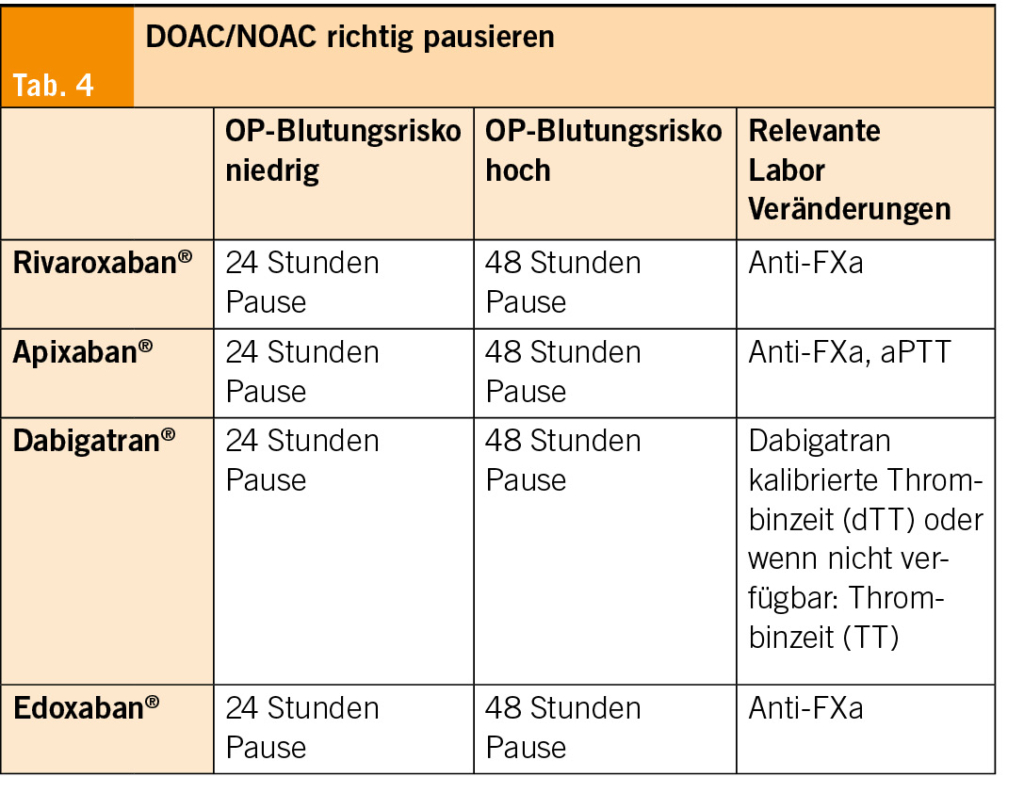
Orientierend gelten für die meisten Situationen die Daten in Tabelle 4. Im Zweifelsfall empfehle ich die Konsultation der Kollegen der Anästhesie und den entsprechenden stets aktuellen Guidelines wie z.B. in Up-To-Date (Tab. 4).
Bei Patientinnen mit starker Niereninsuffizienz, insbesondere bei einer Therapie mit Dabigatran (wird renal eliminiert), muss das DOAC für 72 Stunden präoperativ pausiert werden und bei Spital-Eintritt der Spiegel bestimmt werden.
Wenn möglich, wird dieses am ersten postoperativen Tag wieder gestartet. Bei Operationen mit hohem Risiko für eine Nachblutung bzw. bei insuffizienter Gerinnung muss bis zu 72 Stunden pausiert werden. Wenn das DOAC postoperativ länger pausiert werden muss (zum Beispiel wie beschrieben für 72 Stunden), kann bis zum Wiederbeginn die Indikation für ein Bridging mit Heparin gegeben sein.
Es ist ein Fehler, und dies soll klar so ausgedrückt werden, eine Patientin präoperativ von ihrem DOAC auf ein niedermolekulares Heparin umzustellen. Sollte Unsicherheit bestehen, ob das Medikament tatsächlich für den verordneten Zeitraum pausiert worden ist oder bei Niereninsuffizienz, kann am Operationstag unkompliziert das spezifische Anti-Faktor Xa für das jeweilige DOAC bestimmt werden. Die Kollegen der Anästhesie können hier und auch bei anderen Koagulanzien bei Bedarf unterstützen. Ein hämatologisches Konsil ist bei Patientinnen unter DOAC nicht notwendig.
Bei Patientinnen, die aufgrund einer Stentimplantation Aspirin® oder andere Thrombozytenaggregationshemmer verordnet bekommen haben, dürfen diese besonders in den ersten Monaten unter keinen Umständen pausiert werden. Das Risiko einer In-Stent-Thrombose ist in dieser Phase sehr hoch. Im Zweifelsfall bitte mit dem behandelnden Interventionalisten Kontakt aufnehmen.
Noch relativ neu auf dem Markt sind die sogenannten «Abnehm-Spritzen». Diese Produkte, am bekanntesten ist Ozempic® (Semaglutid) (13), führen nicht nur zu Gewichtsabnahme und zu einer Reduzierung des Risikos für kardiovaskuläre Ereignisse, sondern sie bewirken auch eine stark verlangsamte Magenentleerung (14). Es gibt noch keine befriedigende Evidenz, wie lange diese Präparate präoperativ idealerweise pausiert werden sollten, manche Konsensus-Statements sprechen von minimal 14 Tagen, andere Experten sogar von bis zu vier Wochen. Wenn dies nicht möglich ist, werden die Kollegen der Anästhesie eine Ileus-Einleitung durchführen, um das Aspirationsrisiko zu reduzieren. Bitte teilen Sie den Anästhesisten daher eine entsprechende Medikation mit und/oder instruieren Sie die Patientin zur rechtzeitigen Pausierung.
In der Regel wird das Pausieren oder Fortführen der restlichen Medikation während der anästhesiologischen Konsultation festgelegt. Lokale Unterschiede in der Regelung, ob Chirurgen oder Anästhesisten die entsprechenden Verordnungen vornehmen, sind zu beachten.
Interaktion der Teams
Auch wenn Chirurgen und Anästhesisten unbestritten immer das gemeinsame Ziel der besten Patientenversorgung anstreben, gibt es im Alltag gelegentlich unnötige Differenzen. Hier hat es sich bewährt, regelmässige Check-Ins zu vereinbaren. Zum Beispiel zwischen Chefärztin/Chefarzt Gynäkologie und Bereichsleiter/Bereichsleiterin Anästhesie, der für den betreffenden OP-Bereich zuständig ist. So vermeidet man, dass man sich nur in Krisensituationen trifft und kann sich zum Beispiel monatlich in entspannter Atmosphäre austauschen. Mit dieser Grundlage des gegenseitigen Vertrauens kann man dann seinem ganzen Team eine respektvolle, kollegiale und freundschaftliche Interaktion vorleben. Und am Ende ist man dann auf beiden Seiten glücklich, mit dem besten Team zusammenarbeiten zu dürfen. So geht es zumindest dem Autor mit «seinen» Gynäkologen.
Copyright Aerzteverlag medinfo AG
Bereichsleiter Anästhesie für Gynäkologie
Urologie und Materno-Fetale-Anästhesie USZ
Universitätsspital Zürich
Frauenklinikstrasse 10
8091 Zürich
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
- Ihr Anästhesie Team muss wissen, was und wie sie genau operieren. Teilen Sie auch alle anderen wichtigen medizinischen Informationen, die Ihnen vorliegen, inkl. einer potenziellen Medikation mit Ozempic®, mit Ihren Anästhesisten.
- DOACs müssen nie gebridget werden und Aspirin, falls nicht als reine Primärprophylaxe verordnet, sollte in der Regel nicht gestoppt werden.
- Patient Blood-Management schafft für Operateure und ihre Patientinnen optimale Bedingungen; lassen Sie daher die potenziellen Patientinnen möglichst frühzeitig entsprechend abklären und ggf. auch behandeln.
1. Longrois, Dan; Hoeft, Andreas; Hert, Stefan de (2014): 2014 European Society of Cardiology/European Society of Anaesthesiology guidelines on non-cardiac surgery: cardiovascular assessment and management: A short explanatory statement from the European Society of Anaesthesiology members who participated in the European Task Force. In: European journal of anaesthesiology 31 (10), S. 513–516. DOI: 10.1097/EJA.0000000000000155.
2. Hert, Stefan de; Staender, Sven; Fritsch, Gerhard; Hinkelbein, Jochen; Afshari, Arash; Bettelli, Gabriella et al. (2018): Pre-operative evaluation of adults undergoing elective noncardiac surgery: Updated guideline from the European Society of Anaesthesiology. In: European journal of anaesthesiology 35 (6), S. 407–465. DOI: 10.1097/EJA.0000000000000817.
3. Memtsoudis, Stavros; Liu, Spencer S.; Ma, Yan; Chiu, Ya Lin; Walz, J. Matthias; Gaber-Baylis, Licia K.; Mazumdar, Madhu (2011): Perioperative pulmonary outcomes in patients with sleep apnea after noncardiac surgery. In: Anesthesia and analgesia 112 (1), S. 113–121. DOI: 10.1213/ANE.0b013e3182009abf.
4. Practice guidelines for the perioperative management of patients with obstructive sleep apnea: an updated report by the American Society of Anesthesiologists Task Force on Perioperative Management of patients with obstructive sleep apnea (2014). In: Anesthesiology 120 (2), S. 268–286.
5. Siyam, Mohammad A.; Benhamou, Dan (2002): Difficult endotracheal intubation in patients with sleep apnea syndrome. In: Anesthesia and analgesia 95 (4), 1098-102, table of contents. DOI: 10.1097/00000539-200210000-00058.
6. Routine preoperative tests for elective surgery: © NICE (2016) Routine preoperative tests for elective surgery (2018). In: BJU international 121 (1), S. 12–16.
7. Spahn, Donat R.; Goodnough, Lawrence T. (2013): Alternatives to blood transfusion. In: Lancet (London, England) 381 (9880), S. 1855–1865. DOI: 10.1016/S0140-6736(13)60808-9.
8. Lurati Buse, Giovanna; Bollen Pinto, Bernardo; Abelha, Fernando; Abbott, Tom E. F.; Ackland, Gareth; Afshari, Arash et al. (2023): ESAIC focused guideline for the use of cardiac biomarkers in perioperative risk evaluation. In: European journal of anaesthesiology 40 (12), S. 888–927. DOI: 10.1097/EJA.0000000000001865.
9. Katsanos, Spyridon; Babalis, Dimitrios; Kafkas, Nikolaos; Mavrogenis, Andreas; Leong, Darryl; Parissis, John et al. (2015): B-type natriuretic peptide vs. cardiac risk scores for prediction of outcome following major orthopedic surgery. In: Journal of cardiovascular medicine (Hagerstown, Md.) 16 (6), S. 465–471. DOI: 10.2459/JCM.0000000000000210.
10. Cappellini, Maria Domenica; Comin-Colet, Josep; Francisco, Angel de; Dignass, Axel; Doehner, Wolfram; Lam, Carolyn S. et al. (2017): Iron deficiency across chronic inflammatory conditions: International expert opinion on definition, diagnosis, and management. In: American journal of hematology 92 (10), S. 1068–1078. DOI: 10.1002/ajh.24820.
11. Spahn, Donat R.; Beer, Jürg-Hans; Borgeat, Alain; Chassot, Pierre-Guy; Kern, Christian; Mach, François et al. (2019): NOACs in Anesthesiology. In: Transfusion medicine and hemotherapy : offizielles Organ der Deutschen Gesellschaft fur Transfusionsmedizin und Immunhamatologie 46 (4), S. 282–293. DOI: 10.1159/000491400.
12. Kim, Kwang-Sub; Song, Jong Wook; Soh, Sarah; Kwak, Young-Lan; Shim, Jae-Kwang (2020): Perioperative management of patients receiving non-vitamin K antagonist oral anticoagulants: up-to-date recommendations. In: Anesthesia and pain medicine 15 (2), S. 133–142. DOI: 10.17085/apm.2020.15.2.133.
13. Sherwin, Marc; Hamburger, Joshua; Katz, Daniel; DeMaria, Samuel (2023): Influence de l’utilisation du sémaglutide sur la présence de solides gastriques résiduels à l’échographie gastrique : une étude observationnelle prospective auprès de volontaires sans obésité ayant récemment commencé à prendre du sémaglutide. In: Canadian journal of anaesthesia = Journal canadien d’anesthesie 70 (8), S. 1300–1306. DOI: 10.1007/s12630-023-02549-5.
14. Silveira, Saullo Queiroz; da Silva, Leopoldo Muniz; Campos Vieira Abib, Arthur de; Moura, Diogo Turiani Hourneaux de; Moura, Eduardo Guimarães Hourneaux de; Santos, Leonardo Barbosa et al. (2023): Relationship between perioperative semaglutide use and residual gastric content: A retrospective analysis of patients undergoing elective upper endoscopy. In: Journal of clinical anesthesia 87, S. 111091. DOI: 10.1016/j.jclinane.2023.111091.
15. van Huisstede, Astrid; Biter, Laser Ulas; Luitwieler, Ronald; Castro Cabezas, Manuel; Mannaerts, Guido; Birnie, Erwin et al. (2013): Pulmonary function testing and complications of laparoscopic bariatric surgery. In: Obesity surgery 23 (10), S. 1596–1603. DOI: 10.1007/s11695-013-0928-9.
info@gynäkologie
- Vol. 14
- Ausgabe 5
- Oktober 2024