- Sonographische Beurteilung der Fertilität
Zur Beurteilung der Fertilität stehen verschiedene Instrumente zur Verfügung. Anamnese und Klinik in Kombination mit einer strukturierten Ultraschalluntersuchung sind meist ausreichend, um der Patientin weitreichende Auskünfte über ihre Fruchtbarkeit zu geben. Dieser Artikel soll die Möglichkeiten der sonographischen Fertilitätsdiagnostik darstellen, um diese bei Bedarf in der eigenen Praxis anzuwenden.
Different tools are available to evaluate female fertility. Medical history and clinical examination in combination with structured ultrasonography can deliver detailed insights regarding the fertility status of a patient. This article aims to provide an overview on the possibilities of ultrasonography in the evaluation of female fertility.
Key Words: Fertilität, Ultraschall, Zyklusmonitoring
In der klinischen Praxis hat die Fertilitätsdiagnostik zunehmend an Bedeutung gewonnen. Kommt es bei einem gesunden Paar nach zwölf Monaten ungeschützten und regelmässigen Geschlechtsverkehrs zu keiner Spontankonzeption, so spricht man von «Infertilität». Immer mehr Menschen sind hiervon betroffen, laut jüngsten Schätzungen der World Health Organization (WHO) aktuell ca. 17,5% der Bevölkerung weltweit (1). Es ist erwiesen, dass Paare die Familienplanung zunehmend ins höhere Alter verlagern. Dies kann zu erheblichen Problemen bei der Erfüllung des Kinderwunsches führen, da sowohl die Quantität als auch die Qualität der Keimzellen mit steigendem Alter abnimmt und die Rate an Schwangerschaftskomplikationen steigt (2–5). Eine sorgfältige Aufklärung durch die behandelnde Ärztin bzw. den behandelnden Arzt kann zu einer wunschgerechten Realisierung der Familienplanung und zu einer Senkung dieser Komplikationen führen (6).
Um Patientinnen optimal beraten zu können, sollte eine objektive Einschätzung der aktuellen Fertilität erfolgen. Essenziell wichtig ist hierbei eine fundierte Kenntnis der physiologischen Abläufe und Mechanismen in der menschlichen Reproduktion. Diese ist die Grundlage für ein genaues Verständnis potenzieller Störfaktoren. Ein äusserst hilfreiches und heute unverzichtbares
Instrument zur Untersuchung der individuellen Fertilität ist der Ultraschall.
Das «Zyklusmonitoring»
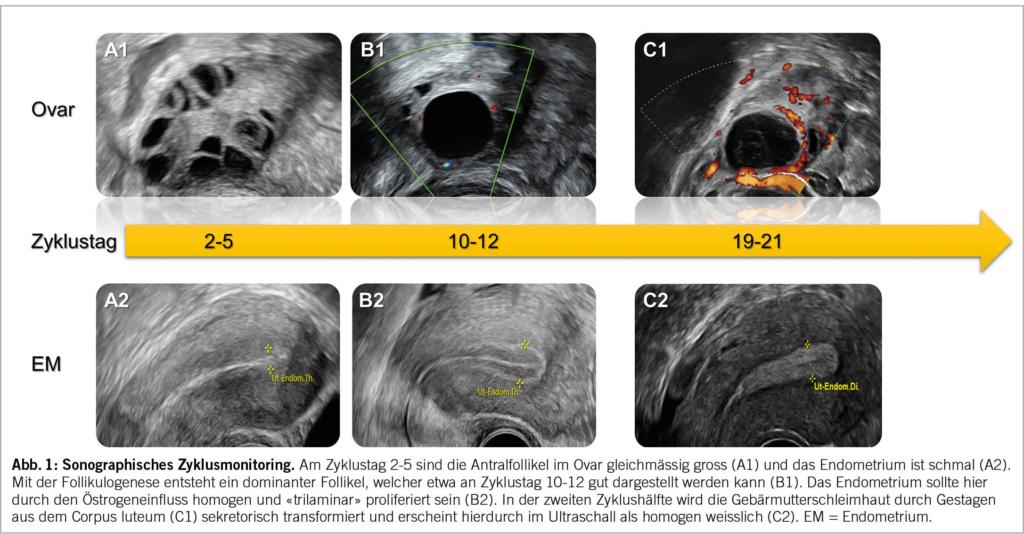
Bei einer Patientin mit Kinderwunsch bzw. Wunsch nach Fertilitätsdiagnostik sollte nach erfolgter Erstkonsultation mit Anamnese und klinischer Untersuchung ein sogenanntes sonographisches Zyklusmonitoring (Abb. 1) durchgeführt werden.
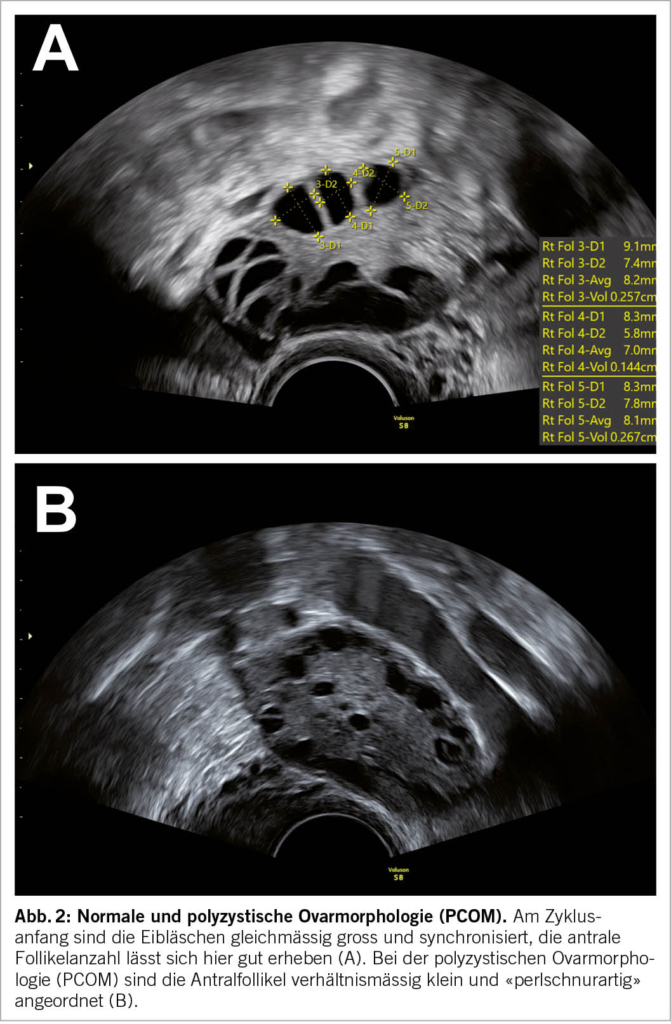
Die Patientin wird gebeten, sich bei Menstruationsbeginn zu melden, um zwischen Zyklustag 2-5 einen Untersuchungstermin zu erhalten. Bei dieser Untersuchung am Zyklusanfang sollten die Antralfollikel im Ovar gleichmässig gross (ca. 2-8 mm) und das Endometrium schmal sein (Abb. 1A1 & Abb. 1A2). Durch das einfache Zählen der vorhandenen Eibläschen in den Ovarien lässt sich der sogenannte «antral follicle count (AFC)» (Abb. 2A) erheben, der nachgewiesenermassen gut mit dem Anti-Müller-Hormon (AMH) korreliert und so eine verlässliche Aussage über die vorhandene Eizellreserve der Patientin zulässt (7). Je nach Alter existieren unterschiedliche Normalwerte für den AFC, die an Perzentilenkurven in der Literatur abgelesen werden können (8). Frauen mit polyzystischem Ovarsyndrom (PCOS) haben in der Regel eine ausserordentlich hohe Eizellreserve, die sich typischerweise in einer polyzystischen Ovarmorphologie (PCOM) manifestiert. Die zahlreichen und verhältnismässig kleinen Antralfollikel können hier in den Ovarien «perlschnurartig» angeordnet sein (Abb. 2B) (9). An dieser Stelle ist es wichtig zu erwähnen, dass die perlschnurartige Anordnung nach den Rotterdam-Kriterien kein sonographisches Diagnosekriterium für das PCOS ist. Massgeblich ist die Anzahl der frühzyklisch bestimmten Antralfollikel (mind. 20 pro Ovar) und/oder des Ovarvolumens (mind. 10 ml) (10).
Bei der Untersuchung am Zyklusanfang lassen sich neben der Bestimmung der Eizellreserve weitere potenziell fertilitätsrelevante Aspekte abklären. Hierzu gehören Raumforderungen in den Adnexbereichen (z.B. Ovarialzysten) sowie bestimmte Uterusauffälligkeiten (z.B. Myome, ausgeprägte Retroversio/Retroflexio uteri). Auch die Mobilität von Uterus und Adnexen sollte untersucht werden («sliding sign» und «kissing ovaries»). Ist diese eingeschränkt und liegt bei der Patientin ein sonopalpatorisch leicht auslösbarer Portioschiebeschmerz vor, so können sich daraus Hinweise auf potenziell vorhandene Pathologien (z.B. Endometriose, Adhäsionen, Adnexitis) ergeben (11).
Die zweite Untersuchung sollte am Zyklustag 10-12 bzw. zur Zyklusmitte hin erfolgen. Durch die Follikulogenese sollte ein dominanter Follikel entstanden sein (Abb. 1B1), welcher je nach Durchmesser (ca. 12-20 mm) eine zeitliche Aussage über die anstehende Ovulation zulässt (der Leitfollikel vergrössert sich im Durchschnitt um etwa 2 mm in zwei Tagen, wobei sein mittlerer Ovulationsdurchmesser bei ca. 22-24 mm liegt). Das Endometrium sollte durch den zunehmenden Östrogeneinfluss homogen «trilaminar» proliferiert sein und keine Unebenheiten aufweisen (Abb. 1B2). Die trilaminare Struktur hat nach aktueller Datenlage einen relevanten Einfluss auf die Fruchtbarkeit einer Frau, während die Endometriumdicke entgegen verbreiteter Annahmen eine eher untergeordnete Rolle spielt (12–15).
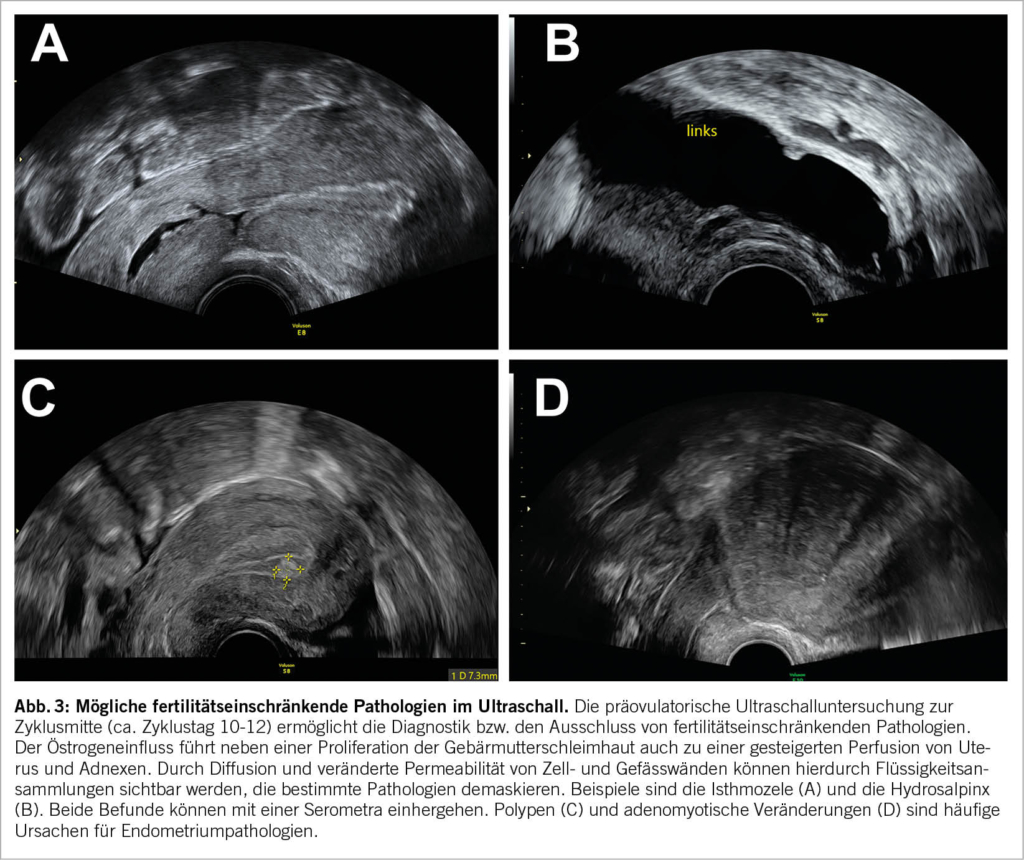
Die direkt präovulatorische Untersuchung bietet eine ausgezeichnete Gelegenheit, um möglicherweise fertilitätseinschränkende Pathologien von Uterus und Adnexen festzustellen. Die mittzyklisch erhöhten Serum-Östrogenspiegel führen zu einer gesteigerten Diffusion und Perfusion im Gewebe. Hierdurch lassen sich durch Flüssigkeit gefüllte und damit sonographisch echoleere Strukturen besser abgrenzen und beurteilen. Beispiele sind die Isthmozele (Abb. 3A) und die Hydrosalpinx (Abb. 3B). Beide Befunde können mit einer Serometra einhergehen.
Da das Endometrium durch den Östrogeneinfluss gleichmässig proliferiert sein sollte, lassen sich hier auch bestimmte Strukturveränderungen gut untersuchen. Diese beinhalten z.B. Polypen (Abb. 3C), submuköse Myome, Restmaterial einer vorangegangenen Schwangerschaft oder Konturveränderungen durch eine Adenomyose (Abb. 3D). Letztere hat in der jüngeren Vergangenheit in der Ultraschalldiagnostik und im Hinblick auf die Fertilität zunehmend an Bedeutung gewonnen. Typische sonographische Zeichen sind: Unscharf begrenzte Junktionalzone, inhomogen aufgelockertes und ggf. zystisch verändertes Myometrium, Wandasymmetrien der Gebärmutter sowie das sogenannte «fan sign» (Abb. 3D) (16).
Ein Sonderfall der Endometriumpathologien ist das Asherman-Syndrom, das sich durch folgende Auffälligkeiten im Ultraschall erkennen lässt: Mittzyklisch schmales Endometrium mit unterbrochener Junktionalzone und hyperechogenen Inseln sowie Synechien und Flüssigkeitsansammlungen (17). Besteht der Verdacht auf das Vorliegen eines Asherman-Syndroms, so kann als nächster Schritt eine Hydrosonographie sinnvoll sein (siehe Abschnitt «Weiterführende Untersuchungen»).
Zum Zeitpunkt der mittzyklischen Untersuchung sollte je nach Zykluslänge noch keine Ovulation stattgefunden haben. Ein sprungreifer Leitfollikel zeigt sich im Ultraschall rund und echoleer sowie glatt begrenzt (Abb. 1B1). Sonographische Zeichen des Eisprungs können sein: Entrundung, freie Flüssigkeit im Douglas sowie intrafollikulär gleichmässig-echogene Areale, sogenannte «Ovulationsschleier».
Das Zyklusmonitoring kann bei Bedarf durch eine Ultraschalluntersuchung in der Lutealphase ergänzt werden. Diese sollte etwa an Zyklustag 19-21 erfolgen. Ist bei dieser Untersuchung ein Gelbkörper durch den sogenannten «ring of fire» nachweisbar (Abb. 1C1) und die Schleimhaut durch den Gestageneinfluss sekretorisch transformiert bzw. homogen weisslich, so entspricht dies dem sonographischen Normalbefund (Abb. 1C2).
Weiterführende Untersuchungen
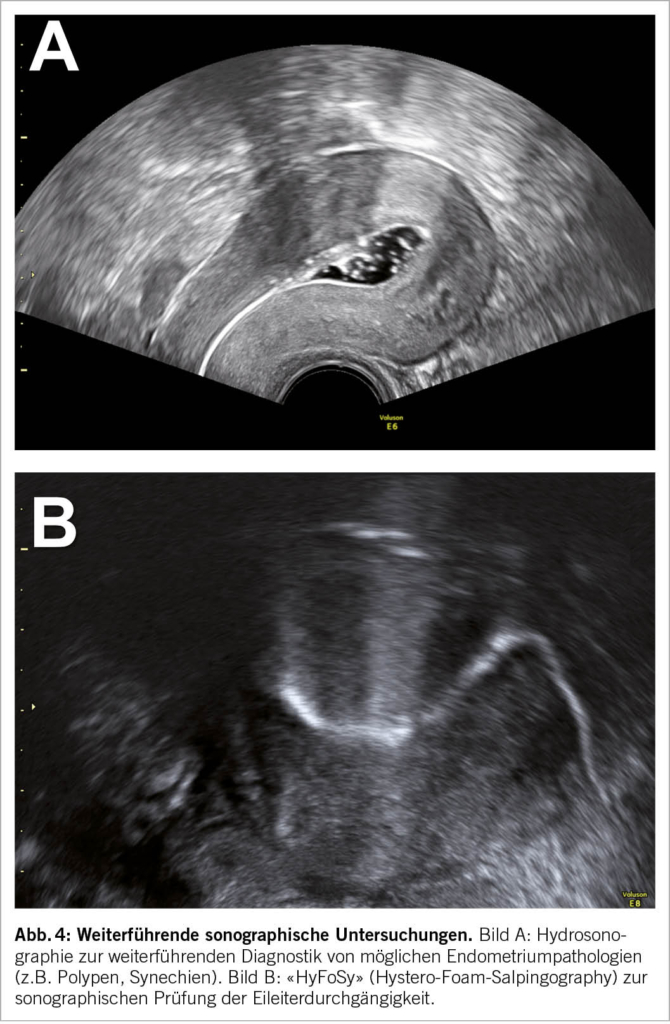
Zusätzlich zum Zyklusmonitoring lassen sich weitere sonographische Untersuchungen durchführen, um die individuelle Fertilität einschätzen zu können: Bei der «Hydrosonographie» (Abb. 4A) wird simultan zur Ultraschalluntersuchung sterile Kochsalzlösung über einen in den Zervikalkanal eingebrachten Katheter in die Gebärmutterhöhle gespült. Das Cavum uteri dehnt sich hierdurch echoleer auf, wodurch bestimmte schleimhautverändernde Pathologien besser zu erkennen sind (z.B. kleinste Polypen, Synechien, submuköse Myome). Bei der «Hystero-Foam-Salpingography (HyFoSy)» (Abb. 4B) wird ebenfalls ein Katheter in die Zervix eingebracht. Über diesen wird während der Ultraschalluntersuchung eine schaumartige, kolloidhaltige Lösung in Gebärmutterhöhle und konsekutiv Eileiter eingespritzt. Der Fluss dieser sonographisch echoreichen Lösung kann dynamisch nachverfolgt werden, um eine Eileiterdurchgängigkeitsdiagnostik zu ermöglichen. Die Hydrosonographie und die HyFoSy sollten präovulatorisch durchgeführt werden. Vor Durchführung sollten mikrobiologische und zytologische Abklärungen bei der Patientin erfolgt sein, um ein mögliches Verschleppen von Keimen und dysplastischen Zellen zu vermeiden. Bei Bedarf ist eine Kombination der beiden Untersuchungen möglich.
Ein weiteres, wichtiges Instrument zur sonographischen Fertilitätsdiagnostik ist der «3D-Ultraschall». Dieser kann in der zweiten Zyklushälfte zur Diagnose von Uterusanomalien oder – pathologien hilfreich sein. Studien konnten zeigen, dass der 3D-Ultraschall im Hinblick auf diese Fragestellungen gleichwertig mit der Magnetresonanztomographie (MRT) ist (18).
Copyright bei Aerzteverlag medinfo AG
Universitätsspital Basel
Spitalstrasse 21
4031 Basel
Universitätsspital Basel
Reproduktionsmedizin und gynäkologische Endokrinologie (RME)
Vogesenstrasse 134
4031 Basel
Die Autoren haben keinen Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
◆ Die Sonographie ist ein unverzichtbares Hilfsmittel bei der fertilitätsbezogenen Diagnostik und Therapie.
◆ Basis der sonographischen Beurteilung der Fruchtbarkeit ist der Menstruationszyklus.
◆ Das «Zyklusmonitoring» kann weitreichende Informationen über die Fruchtbarkeit der Frau liefern.
◆ In der Praxis ist eine ultraschallbasierte Diagnostik meist ausreichend, um der Patientin eine zuverlässige Aussage hinsichtlich ihrer Fruchtbarkeit geben zu können.
1. World Health Organization (WHO). Infertility Prevalence Estimates, 1990–2021.
2. Te Velde ER, Pearson PL. The variability of female reproductive ageing. Hum Reprod Update. 2002;8(2):141–54.
3. Wallace WHB, Kelsey TW. Human ovarian reserve from conception to the menopause. PLoS One. 2010;5(1):e8772.
4. Schmidt L, Sobotka T, Bentzen JG, Andersen AN. Demographic and medical consequences of the postponement of parenthood. Hum Reprod Update. 2012;18(1):29–43.
5. Balasch J, Gratacós E. Delayed childbearing: effects on fertility and the outcome of pregnancy. Curr Opin Obstet Gynecol. 2012;24(3):187–93.
6. Wyndham N, Marin Figueira PG, Patrizio P. A persistent misperception: Assisted reproductive technology can reverse the “aged biological clock. Fertil Steril. 2012;97(5):1044–7.
7. Birch Petersen K, Hvidman HW, Forman JL, Pinborg A, Larsen EC, Macklon KT, et al. Ovarian reserve assessment in users of oral contraception seeking fertility advice on their reproductive lifespan. Hum Reprod. 2015;30(10):2364–75.
8 Neu La Marca A, Spada E, Sighinolfi G, Argento C, Tirelli A, Giulini S, et al. Age-specific nomogram for the decline in antral follicle count throughout the reproductive period. Fertil Steril. 2011;95(2):684-8.
9. Reid SP, Kao C-N, Pasch L, Shinkai K, Cedars MI, Huddleston HG. Ovarian morphology is associated with insulin resistance in women with polycystic ovary syndrome: a cross sectional study. Fertil Res Pract. 2017;3(1).
10. Teede HJ, Misso ML, Costello MF, Dokras A, Laven J, Moran L, et al. International PCOS Network. Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome. Fertil Steril. 2018;110(3):364-379.
11. Guerriero S, Ajossa S, Pascual MA, Rodriguez I, Piras A, Perniciano M, et al. Ultrasonographic soft markers for detection of rectosigmoid deep endometriosis. Ultrasound Obstet Gynecol. 2020;55(2):269–73.
12. Quaas AM, Gavrizi SZ, Peck JD, Diamond MP, Legro RS, Robinson RD, et al. Endometrial thickness after ovarian stimulation with gonadotropin, clomiphene, or letrozole for unexplained infertility, and association with treatment outcomes. Fertil Steril. 2021;115(1):213–20.
13. Gingold JA, Lee JA, Rodriguez-Purata J, Whitehouse MC, Sandler B, Grunfeld L, et al. Endometrial pattern, but not endometrial thickness, affects implantation rates in euploid embryo transfers. Fertil Steril. 2015;104(3):620-628.e5.
14. Kasius A, Smit JG, Torrance HL, Eijkemans MJC, Mol BW, Opmeer BC, et al. Endometrial thickness and pregnancy rates after IVF: a systematic review and meta-analysis. Hum Reprod Update. 2014;20(4):530–41.
15. Weiss NS, Van Vliet MN, Limpens J, Hompes PGA, Lambalk CB, Mochtar MH, et al. Endometrial thickness in women undergoing IUI with ovarian stimulation. How thick is too thin? a systematic review and meta-analysis. Vol. 72, Obstetrical and Gynecological Survey. 2017. p. 484–5.
16. Butenschön A, Manegold-Brauer G. Differenzierte gynäkologische Sonografie: Adenomyose. Gynäkologie & Geburtshilfe, Universimed, Medizin im Fokus. 2021.
17. Amin TN, Saridogan E, Jurkovic D. Ultrasound and intrauterine adhesions: A novel structured approach to diagnosis and management. Vol. 46, Ultrasound in Obstetrics and Gynecology. 2015. p. 131–9.
18. Bermejo C, Martínez Ten P, Cantarero R, Diaz D, Pérez Pedregosa J, Barrón E, et al. Three-dimensional ultrasound in the diagnosis of Müllerian duct anomalies and concordance with magnetic resonance imaging. Ultrasound Obstet Gynecol. 2010;35(5):593–601.
info@gynäkologie
- Vol. 13
- Ausgabe 3
- Juni 2023