- Update PCOS Diagnostik und Therapie 2023
Das polyzystische Ovarialsyndrom (PCOS) ist die häufigste Hormonerkrankung bei Frauen im reproduktiven Alter. Schätzungen zufolge sind 10-13% betroffen (1). Die Dunkelziffer ist womöglich deutlich höher, da ein Teil der Erkrankten weiterhin nicht adäquat diagnostiziert und therapiert ist. Dieser Artikel soll als Leitfaden für die Diagnostik, Beratung und Therapie bei PCOS dienen. Grundlage bildet die neuste ESHRE Guideline 2023 (1).
Polycystic ovary syndrome (PCOS) is the most common hormonal disorder in women of reproductive age. About 10-13% are affected (1). The number of unreported cases may be higher, as some of those affected are still not diagnosed and treated. This article is intended to serve as a guide for the diagnosis, counseling and treatment of PCOS. It is based on the latest ESHRE Guideline 2023 (1).
Key words: PCOS, Health relevance, Rotterdam criteria, individualised therapy
Einfluss auf die Gesundheit
Das PCOS kann mit erheblichen gesundheitlichen Folgen einhergehen und die Lebensqualität einschränken. Psychische Komorbiditäten wie Depressionen, Angst- und Essstörungen werden oft unterschätzt. Unabhängig vom BMI besteht ein erhöhtes Risiko für eine arterielle Hypertonie. 95% der adipösen, aber auch 75% der schlanken Betroffenen zeigen eine Glukosestoffwechselstörung. Eine Dyslipidämie ist ebenso mit einem PCOS assoziiert (2). Durch die chronische Anovulation und hormonelle Dysbalance, oft kombiniert mit einem metabolischen Syndrom, steigt das Risiko für ein Endometriumkarzinom. Auch scheint das Risiko für Ovarialkarzinome erhöht zu sein (3, 4). PCOS ist eine häufige Sterilitätsursache und wird mit einer erhöhten Abortrate assoziiert, wobei insbesondere metabolische Faktoren ursächlich zu sein scheinen (5). Studien zeigen, dass Betroffene verglichen mit gesunden Frauen kumulativ eine ähnlich hohe Wahrscheinlichkeit haben, ein Kind zu gebären. Sie brauchen tendenziell länger für die Geburt ihres ersten Kindes und haben gesamthaft weniger Kinder. Eine frühe Diagnosestellung und Aufklärung scheinen die Chancen auf ein Kind zu erhöhen (6). Das PCOS Zentrum USZ verfolgt das Ziel, die Sensibilität für das Krankheitsbild zu steigern und eine ganzheitliche Betreuung anzubieten.
Diagnostik
Das PCOS wird anhand der Rotterdam-Kriterien diagnostiziert (7). Vorausgesetzt andere Ursachen sind ausgeschlossen, darf beim Vorliegen von mindestens 2 der folgenden 3 Kriterien die PCOS-Diagnose gestellt werden:
1. Zyklusstörungen
Unregelmässige Menstruationszyklen gelten als klinisches Leitsymptom beim PCOS. Sind mindestens 3 Jahre nach der Menarche vergangen und liegt eine Poly- (< 21 Tage), Oligo- (> 35 Tage oder < 8 Zyklen/Jahr) oder Amenorrhoe (> 90 Tage) vor, ist das Rotterdam-Kriterium erfüllt. Die diagnostisch schwierigste Phase stellt die Pubertät dar. 95% der Adoleszentinnen haben innerhalb von 3 Jahren nach der Menarche regelmässige Zyklen, die restlichen 5% erst innerhalb von 5 Jahren (8). Die Guideline beschreibt Zyklusstörungen im ersten Jahr nach der Menarche als normal im Rahmen der Pubertätsentwicklung. Sofern die Menarche ≥ 1 und ≤ 3 Jahre zurückliegt, ist das Rotterdam-Kriterium der Zyklusstörungen beim Vorliegen einer Poly- (< 21 Tage), Oligo- (> 45 Tage) oder primären Amenorrhoe (keine Menarche bis zum 15. Lebensjahr oder > 3 Jahre nach der Thelarche) erfüllt.
2. Polyzystische Ovarien, Anti-Müller-Hormon (AMH)
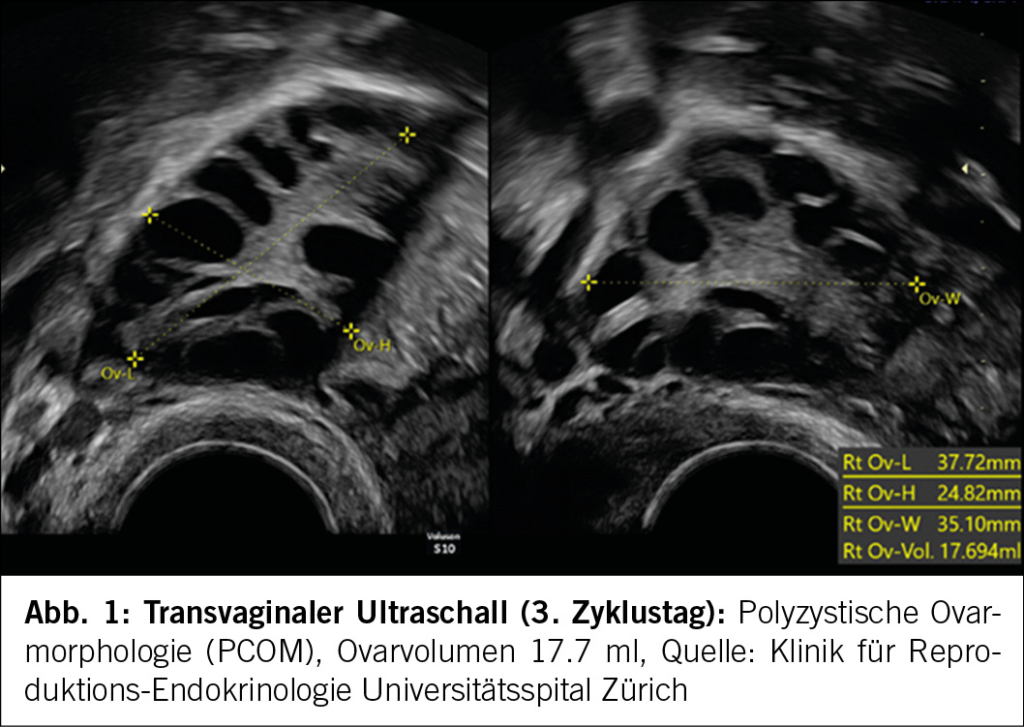
Namensgebend für das PCOS ist eine polyzystische Ovarmorphologie (PCOM) (Abb. 1). Die Ovarienbeurteilung sollte frühzyklisch (2.-5. Zyklustag) und ohne Nachweis eines dominanten Follikels, Corpus luteums oder einer Zyste erfolgen. Es muss zwischen dem transvaginalen und transabdominalen Ultraschall unterschieden werden (Tab. 1). Eine PCOM kommt bei Adoleszentinnen sehr häufig vor (9), sodass polyzystische Ovarien frühestens 8 Jahre nach der Menarche diagnostiziert werden dürfen. Bei Adoleszentinnen mit Zyklusstörungen und Hyperandrogenismus darf ohne Ultraschall und nach Ausschluss anderer Ursachen ein PCOS diagnostiziert werden.
Neu gilt auch ein hoher Serum AMH-Wert als Diagnosekriterium für eine PCOM (1). Die Guideline nennt keinen Grenzwert. Folgende Faktoren haben einen Einfluss auf den AMH Wert und sollten bei der Interpretation beachtet werden: Ein hoher BMI kann den Wert erniedrigen, ebenso eine Messung unter hormonellen Kontrazeptiva oder periovulatorisch. Ein hoher AMH Wert ist bei Adoleszentinnen und jungen Erwachsenen zu erwarten (Peak: 20.-25. Lebensjahr) (10). Das Kriterium sollte nur bei Erwachsenen angewendet werden und dient nicht als «Single-Test». Vielmehr sollte der Wert in der Gesamtschau der Befunde bewertet werden.
3. Hyperandrogenismus (klinisch oder laborchemisch)
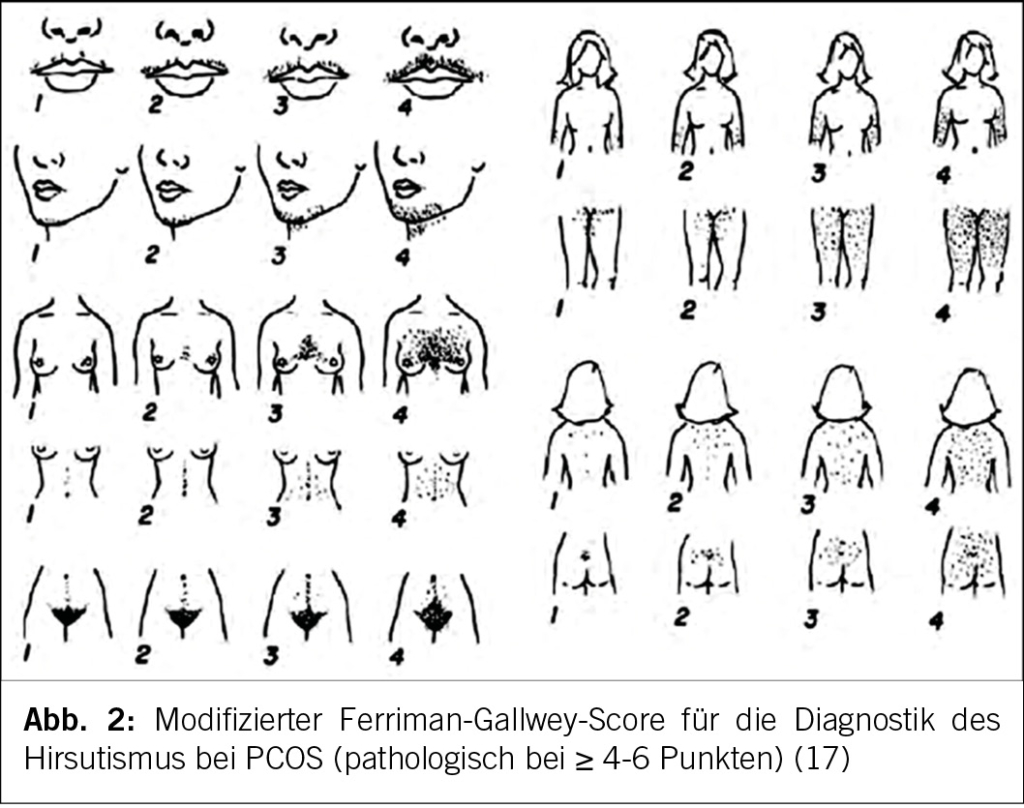
Es kann entweder ein klinischer oder ein biochemischer Hyper-androgenismus vorliegen. Bei PCOS-Verdacht sollte eine körperliche Untersuchung mit Augenmerk auf einen Hirsutismus, Akne und Alopezie erfolgen. Klinische Androgenisierungszeichen können die Lebensqualität betroffener Frauen deutlich reduzieren (11). Oft erfolgten bereits kosmetische Interventionen (Laser, Rasur, etc.), die die Aussagekraft der körperlichen Untersuchung einschränken. Da Akne bei Adoleszentinnen häufig vorkommt, zählt nur eine schwere Akne oder ein Hirsutismus. Zur Hirsutismusdiagnostik soll der modifizierte Ferriman-Gallwey-Score (mFG) (Abb. 2) angewendet werden. Nur terminales, pigmentiertes Haar mit einem unbehandelten Wachstum > 5 mm zählt. Ein Hirsutismus liegt bei einem mFG ≥ 4-6 Punkten vor. Die Ethnizität der Patientin ist bei der Interpretation zu berücksichtigen.
Eine Hyperandrogenämie kann durch eine frühzyklische Blutentnahme (2.-5. Zyklustag) diagnostiziert werden. Das Gesamttestosteron und Sexualhormon-bindende Globulin (SHBG) sollten bestimmt werden. Hieraus kann der freie Androgenindex (FAI) berechnet werden. Auch eine Bestimmung von Androstendion, DHEA-S und insbesondere 17-OH-Progesteron zum Ausschluss eines late-onset AGS sollten erfolgen. Da unter hormonalen Kontrazeptiva die Androgen-spiegel durch eine Erhöhung des SHBG falsch zu niedrig gemessen werden können, sollten diese mindestens 3 Monate vor der Hormondiagnostik abgesetzt werden.
Weitere Diagnostik
Bei allen Betroffenen sollten jährliche Gewichts- und Blutdruckkon-trollen erfolgen. Auch ist unabhängig vom Alter und BMI eine Lipidkontrolle (Cholesterin gesamt, LDL- und HDL-Cholesterin, Triglyzeride) sowie eine Abklärung auf Glukosestoffwechselstörungen bei Diagnosestellung indiziert. Das Diabetesscreening sollte alle 1 bis 3 Jahre wiederholt werden, falls möglich immer mittels 75g oGTT. Alternativ kann im Wissen einer reduzierten Aussagekraft die Nüchternglukose und/oder der HbA1c Wert bestimmt werden. Auch präkonzeptionell sollte ein oGTT erfolgen. Der Lipidstatus wird abhängig vom Resultat sowie anderer kardiovaskulärer Risikofaktoren verlaufskontrolliert.
Therapie
So unterschiedlich die Symptome der Betroffenen sind, so individuell sollte das Therapiekonzept sein. Ein Ziel des PCOS Zentrums USZ ist es, mit einem interdisziplinären Team aus Reproduktions-Endokrinologen, Adipositasspezialisten, Dermatologen, Sportmedizinern und Psychiatern/Psychologen einen auf jede Patientin abgestimmten Behandlungspfad zu definieren.
Lifestyle-Management
Die Basis der Therapie bildet eine gesunde Lebensführung mit körperlicher Bewegung und ausgewogener Ernährung. Es werden keine Empfehlungen hinsichtlich eines speziellen Diättypen oder Sportart ausgesprochen. Vor allem bei adipösen Betroffenen kann eine Gewichtsreduktion sich positiv auf den Zyklus, die Fertilität und erhöhte Androgenspiegel auswirken. Der Insulinspiegel und das kardiovaskuläre Risiko sinken signifikant (2).
Kombinierte orale Kontrazeptiva (COC)
Bei Hyperandrogenismus und/oder Zyklusstörungen ohne Kinderwunsch stellen COC nach Ausschluss von Risikofaktoren ein Mittel der Wahl dar. Hierbei werden keine spezifischen Präparate empfohlen. Aufgrund des erhöhten Thromboembolierisikos sollten antiandrogene Pillen mit Cyproteronacetat/Ethinylestradiol (z.B. Diane 35®) nicht als Erstlinientherapie eingesetzt werden (12). Positive Effekte auf Androgenisierungszeichen (u.a. Hirsutismus) sind meist frühestens nach 6 Monaten zu erwarten.
Metformin
Das orale Antidiabetikum kann die Zykluslängen, die Häufigkeit von Ovulationen als auch die klinische Schwangerschaftsrate verbessern (13). Betroffene mit einem BMI > 25 kg/m2 scheinen besonders zu profitieren. Es handelt sich um einen off-label use. Um häufige zu Beginn der Therapie und oft im Verlauf selbstlimitierende gastrointestinale Nebenwirkungen vorzubeugen, sollte die Dosierung langsam gesteigert werden. Die Startdosis beträgt 500mg/Tag und sollte wöchentlich bis 2.5g/Tag (Erwachsene) bzw. 2g/Tag (Jugendliche) gesteigert werden. Eine Metformintherapie kann mit einem erniedrigten Vitamin B12 Spiegel einhergehen, sodass bei langfristiger Einnahme entsprechende Kontrollen indiziert sind.
Inositol
Inositol wirkt als natürlicher Insulinsensitizer und ist an der Regulation der Androgensynthese im Ovar beteiligt. Die Studienlage ist spärlich, sodass eine Gabe auf individueller Präferenz erfolgen sollte. Metformin sollte bevorzugt eingesetzt werden.
Gestagene
Um Risiken wie Endometriumhyperplasien/-karzinome zu minimieren, sollte bei einer Oligo-/Amenorrhoe spätestens nach 3 Monaten eine Periodeninduktion erfolgen (14). Ist eine kombinierte Pille nicht gewünscht oder führten Metformin bzw. Inositol nicht zur Zyklusregulation, können Gestagenpräparate eingesetzt werden. Bei Wunsch der Patientin nach einem regelmässigen Zyklus, können diese auch monatlich verabreicht werden.
Antiandrogene
Führten kosmetische Therapien (z.B. Laser) und/oder COC für mindestens 6 Monate nicht zu einer Reduktion kutaner Androgenisierungszeichen (v.a. Hirsutismus), können in Kombination mit einer sicheren Verhütung Antiandrogene in Betracht gezogen werden. Die Studienlage ist allerdings eingeschränkt. Therapieoptionen sind Spironolacton (25-100mg/Tag) oder Cyproteronacetat (≥10mg). Bei Finasterid, Flutamid und Bicalutamid muss das Risiko einer Lebertoxizität beachtet werden.
Therapien bei Kinderwunsch
Aromatase-Inhibitoren
Letrozol gilt als first-line Therapie zur Ovulationsinduktion bei infertilen Frauen mit PCOS, sofern keine weiteren Sterilitätsursachen des Paares vorliegen. Mehrere Studien haben gegenüber Clomiphenzitrat die höhere Wirksamkeit und bessere Lebendgeburtenraten gezeigt; insbesondere bei übergewichtigen Frauen (15). Es handelt sich um eine off-label Anwendung. Die Dosierung beträgt 2,5-7,5mg/Tag vom 5.-9. Zyklustag. Regelmässige Ultraschallkontrollen sind indiziert und die Ovulation muss bei einem Leitfollikel (≥ 18 mm) und gutem Endometrium (≥ 7 mm, Bilayer) induziert werden. Die Anwendung von Letrozol gilt als sicher und es bestehen keine Unterschiede hinsichtlich Teratogenität verglichen mit Clomiphenzitrat oder natürlicher Konzeption.
Gonadotropine
Diese gelten als second-line Therapie zur Ovulationsinduktion bei Frauen mit PCOS ohne weitere Sterilitätsursachen des Paares und wo Aromataseinhibitoren nicht zum Erfolg führten. Es sollte ein low-dose step up Protokoll gewählt werden, sprich der Beginn mit einer möglichst niedrigen Dosierung. Die Effektivität verschiedener Präparate scheint sich nicht zu unterscheiden. Die Behandlung erfordert ein hohes Mass an fachlicher Expertise. Es müssen regelmässige Follikulometrien stattfinden. Die Präparate sind teuer und werden nach entsprechender Kostengutsprache von den Krankenkassen übernommen.
Assistierte Reproduktionsmedizin
Eine IVF/ICSI sollte nur durchgeführt werden, sofern die first- und second line Therapien nicht zum Ziel führten. Das erhöhte Risiko für ein ovarielles Überstimulationssyndrom (OHSS) kann durch die Anwendung eines Antagonistenprotokolls sowie einem «freeze all» reduziert werden. Hierbei werden alle Embryonen nach der Befruchtung zunächst eingefroren und zu einem späteren Zeitpunkt transferiert.
«Ovarian drilling»
Bei dieser «Ovarstichelung» wird meist laparoskopisch die Kapsel der Ovarien entweder mit Strom oder Laser «durchlöchert». Betroffene zeigen postoperativ häufig regelmässigere Menstruationszyklen, niedrigere Androgenspiegel, weniger Akne und Hirsutismus sowie bessere Schwangerschaftschancen (16). Die Methode wird als second-line Therapie bei anovulatorischen Frauen mit PCOS und Kinderwunsch, sofern eine monofollikuläre Stimulation missglückte und keine weiteren Sterilitätsfaktoren vorliegen, empfohlen. Aufgrund der Invasivität und fehlenden Standardisierung des operativen Eingriffes sowie Risiken einer sekundären Ovarialinsuffizienz bzw. Adhäsionen wird die Indikation zurückhaltend gestellt.
Copyright Aerzteverlag medinfo AG
Leitung PCOS Zentrum USZ, Universitätsspital Zürich
Klinik für Reproduktions-Endokrinologie
Frauenklinikstrasse 10
8091 Zürich
Die Autorin hat deklariert, keine potentiellen
Interessenskonflikte zu haben.
◆ Die PCOS-Diagnose wird anhand der Rotterdam-Kriterien (1. Zyklusstörungen,
2. PCOM oder hoher AMH-Wert, 3. klinischer oder laborchemischer
Hyperandrogenismus; ≥ 2 von 3 Kriterien zutreffend) nach Ausschluss anderer Ursachen gestellt.
◆ Das kardiovaskuläre Risiko (Diabetes mellitus, Hypertonie, Adipositas,
Dyslipidämie) sowie das Risiko für gynäkologische Karzinome (Endometrium,
Ovar) sind erhöht. Es sollten entsprechend regelmässige
Kontrollen von Blutdruck, Gewicht, Blutzucker und Lipidstatus erfolgen.
◆ Die Therapie muss individuell und bedürfnisorientiert sein.
◆ Lifestyle-Massnahmen mit Gewichtsreduktion und gesunder Ernährung
bilden den Grundstein der PCOS-Therapie.
1. Teede HJ, Tay CT, Laven J, Dokras A, Moran LJ, Piltonen TT, et al. Recommendations from the 2023 International Evidence-based Guideline for the Assessment and Management of Polycystic Ovary Syndrome†. Human Reproduction. 2023;38(9):1655-79.
2. Guan C, Zahid S, Minhas AS, Ouyang P, Vaught A, Baker VL, et al. Polycystic
ovary syndrome: a “risk-enhancing” factor for cardiovascular disease. Fertil Steril. 2022;117(5):924-35.
3. Fearnley EJ, Marquart L, Spurdle AB, Weinstein P, Webb PM. Polycystic ovary syndrome increases the risk of endometrial cancer in women aged less than 50 years: an Australian case-control study. Cancer Causes Control. 2010;21(12):2303-8.
4. Ding DC, Chen W, Wang JH, Lin SZ. Association between polycystic ovarian syndrome and endometrial, ovarian, and breast cancer: A population-based cohort study in Taiwan. Medicine (Baltimore). 2018;97(39):e12608.
5. online A. S2k-Leitlinie Diagnostik und Therapie von Frauen mit wiederholten
Spontanaborten 2022 [Available from: https://register.awmf.org/de/leitlinien/
detail/015-050.
6. Persson S, Elenis E, Turkmen S, Kramer MS, Yong EL, Sundström-Poromaa I.
Fecundity among women with polycystic ovary syndrome (PCOS)-a populationbased study. Hum Reprod. 2019;34(10):2052-60.
7. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome (PCOS). Hum Reprod. 2004;19(1):41-7.
8. Metcalf MG, Skidmore DS, Lowry GF, Mackenzie JA. Incidence of ovulation in the years after the menarche. J Endocrinol. 1983;97(2):213-9.
9. Kristensen SL, Ramlau-Hansen CH, Ernst E, Olsen SF, Bonde JP, Vested A, et al. A very large proportion of young Danish women have polycystic ovaries: is a revision of the Rotterdam criteria needed? Hum Reprod. 2010;25(12):3117-22.
10. Kelsey TW, Wright P, Nelson SM, Anderson RA, Wallace WH. A validated model of serum anti-müllerian hormone from conception to menopause. PLoS One. 2011;6(7):e22024.
11. Ekbäck MP, Lindberg M, Benzein E, Årestedt K. Health-related quality of life,
depression and anxiety correlate with the degree of hirsutism. Dermatology.
2013;227(3):278-84.
12. Combined hormonal contraception and the risk of venous thromboembolism: a guideline. Fertil Steril. 2017;107(1):43-51.
13. Sharpe A, Morley LC, Tang T, Norman RJ, Balen AH. Metformin for ovulation
induction (excluding gonadotrophins) in women with polycystic ovary syndrome. Cochrane Database Syst Rev. 2019;12(12):Cd013505.
14. Teede HJ, Misso ML, Costello MF, Dokras A, Laven J, Moran L, et al. Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome. Hum Reprod. 2018;33(9):1602-18.
15. Legro RS, Brzyski RG, Diamond MP, Coutifaris C, Schlaff WD, Casson P, et al. Letrozole versus clomiphene for infertility in the polycystic ovary syndrome. N Engl J Med. 2014;371(2):119-29.
16. Debras E, Fernandez H, Neveu ME, Deffieux X, Capmas P. Ovarian drilling in polycystic ovary syndrome: Long term pregnancy rate. Eur J Obstet Gynecol Reprod Biol X. 2019;4:100093. 17. Khan A, Karim N, Ainuddin JA, Fahim MF. Polycystic Ovarian Syndrome: Correlation between clinical hyperandrogenism, anthropometric, metabolic and endocrine parameters. Pak J Med Sci. 2019;35(5):1227-32.
info@gynäkologie
- Vol. 14
- Ausgabe 1
- Februar 2024